Активация сигнального пути интерферона-альфа ресвератролом, генистеином и кверцетином
Автор: Власова Ольга Александровна, Борунова Анна Анатольевна, Сафина Альфия, Сметанина Инна Васильевна, Лесовая Екатерина Андреевна, Белицкий Геннадий Альтерович, Заботина Татьяна Николаевна, Гурова Катерина, Кирсанов Кирилл Игоревич, Якубовская Марианна Геннадиевна
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1 т.18, 2019 года.
Бесплатный доступ
Ресвератрол, кверцетин и генистеин, относящиеся к полифенолам вторичных метаболитов растений, обладают антиканцерогенным и противовирусным эффектами, реализуемыми в результате их плейо-тропного действия на различные макромолекулы клетки. Эти соединения могут взаимодействовать с ДНК, не образуя ковалентные связи. При этом может происходить изменение пространственных, физико-химических и структурных характеристик ДНК, что может приводить к нарушению функциони-рования белков метаболизма ДНК и вызывать дестабилизацию хроматина. Такие эффекты были опи-саны для нового противоопухолевого препарата Кураксина CBL0137, причем индуцированная данным соединением дестабилизация хроматина приводила к активации сигнального пути интерферона-α. Используя клеточную линию HeLa с трансгенным флуоресцентным белком mCherry, содержащим в промоторной области консенсусный сайт связывания интерферона-α (ISRE), мы продемонстрировали дозозависимый стимулирующий эффект ресвератрола, кверцетина и генистеина на активность сигналь-ного пути интерферона-α. Использование прижизненной флуоресцентной микроскопии на клеточной линии HT1080 c трансгенным флуоресцентно-меченным гистоном H1.5 позволило продемонстриро-вать, что данные полифенолы вызывают перераспределение данного линкерного гистона в ядрах клеток. Полученные нами данные свидетельствуют о возможности существования ДНК-зависимого механизма реализации противоопухолевого действия растительных полифенолов и необходимости дальнейшего изучения влияния полифенолов на структуру хроматина и связанного с этим изменения функционирования генома, в частности регуляции сигнального пути интерферона-α.
Растительные полифенолы, ресвератрол, генистеин, кверцетин, интерферон-α, гистон н1, макромолекулы клетки, флуоресцентная микроскопия, ферменты метаболизма, histone н1
Короткий адрес: https://sciup.org/140254241
IDR: 140254241 | УДК: 577.3: | DOI: 10.21294/1814-4861-2019-18-1-50-55
Activation of interferon- signaling by resveratrol, genistein and quercetin
Resveratrol, genistein and quercetin from the group of polyphenols from secondary plant metabolites reveal cancer preventive and antivirus effects realized via their pleiotropic influence on the different macromolecules in cells. These compounds can interact with DNA without the formation of covalent bonds. This process is usually followed by changes in spatial, physical-chemical and structural DNA characteristics that can result in disfunction of DNA metabolism enzymes and chromatin destabilization. Similar effects were described for anticancer drug Curaxine CBL0137 in association with activation of interferon-α signaling. We demonstrated dose-dependent stimulating effects of resveratrol, genistein and quercetin on interferon-α signaling using HeLa cells expressed mCherry protein with interferon-stimulated response elements (ISRE) in promoter. Furthermore, it was shown by live-cell fluorescent microscopy in HT1080 cells with mCherry-labeled histone H1.5 that described polyphenols induced the redistribution of this linker histone in cell nuclei. The data obtained suggest an existence of DNA-dependent mechanism of anticancer effects of plant polyphenols and a need for further study of crosslinks between the polyphenols’ influence on chromatin structure and the changes in genome function, in particular, induction of interferon- interferon-α signaling.
Текст научной статьи Активация сигнального пути интерферона-альфа ресвератролом, генистеином и кверцетином
Анализу биологических эффектов ресвератрола, кверцетина и генистеина, вторичных метаболитов растений из группы полифенолов, посвящены мно‑ гочисленные исследования [1–3]. В экспериментах на грызунах эти соединения эффективно снижа‑ ют частоту возникновения и множественность опухолей толстой кишки, индуцированных 1,2‑ диметилгидразином или азоксиметаном, опухолей яичников, индуцированных 7,12‑диметилбенз(а) антраценом, и опухолей молочных желез, ин‑ дуцированных 7,12‑диметилбенз(а)антраценом и N‑метил‑N‑нитрозомочевиной, и др. [4–7]. Ресвератрол, кверцетин и генистеин обладают антипролиферативным, проапоптотическим, противовоспалительным и иммуномодулирующим эффектами [1, 2, 8, 9]. При этом для их действия в клетках млекопитающих характерна плейотроп‑ ность. В частности, ресвератрол имеет более 20 молекулярных мишеней, включая клеточные рецепторы, ферменты метаболизма гидрофобных ксенобиотиков, компоненты ряда сигнальных путей, транскрипционные факторы, ферменты метаболизма ДНК и системы эпигенетической регуляции транскрипции [1, 4, 10]. Аналогичные данные о существовании целого ряда молеку‑ лярных мишеней были продемонстрированы для генистеина и кверцетина [11, 12]. Плейотропность эффектов изучаемых полифенолов делает исклю‑ чительно сложной интерпретацию интегрального результата их воздействия на клетку, которая становится невозможной без использования соот‑ ветствующих баз данных [1]. Кроме того, ресвера‑ трол, кверцетин и генистеин представляют собой ДНК‑тропные соединения, способность которых к интеркаляции показана тушением флуоресценции в системе ДНК‑EtBr [13–15].
Эти данные, в сопоставлении с результатами исследований по влиянию интеркаляторов ДНК и УБЛ на структуру и свойства дуплекса [16], позволяют считать, что изучаемые нами поли‑ фенолы, взаимодействуя с ДНК, могут влиять на геометрические характеристики и термоди‑ намическую стабильность дуплекса, гибкость и физико‑химические свойства биополимера, а также вероятность формирования и стабилизации раз‑ личных альтернативных структур ДНК, таких как G‑квадруплексы, Н‑ДНК и круциформы. Кроме того, эти соединения могут экранировать опреде‑ ленные позиции по малой и большой бороздкам ДНК, конкурентно ингибируя работу ферментов «домашнего хозяйства». Всё это может влиять на процессы компактизации ДНК и трехмерную организацию эукариотического генома.
В настоящее время эффекты дестабилизации хроматина ДНК‑тропными агентами были описаны лишь для нового противоопухолевого препарата CBL0137 [17, 18] и ряда узкобороздочных лигандов (УБЛ) [19]. Причем при действии как CBL0137, так и УБЛ наблюдалось повышение уровня экспрес‑ сии ретротранспозонов и других повторяющихся последовательностей ДНК. Это, в свою очередь, должно приводить к активации сигнального пути интерферона‑α, как это было показано для CBL0137 [17]. Для изучения этих эффектов CBL0137 были получены модельные системы, позволяющие оценить запуск сигнального пути интерферона‑α с помощью репортерного анализа и изменения локализации гистона Н1 методом прижизненной флуоресцентной микроскопии. При изучении эффектов CBL0137 активность сигнального пути интерферона‑α оценивали в клетках HeLa по уров‑ ню экспрессии трансгенного флуоресцентного белка mCherry, имеющего в промоторной области консенсусный сайт связывания интерферона‑α (ISRE). Анализ локализации гистона H1 в ядрах обработанных клеток проводили на линии HT1080 с трансгенным гистоном Н1.5, флуоресцентно меченным mCherry [17, 18]. При этом активация сигнального пути интерферона‑α наблюдалась при тех же концентрациях CBL0137, которые вы‑ зывали изменение локализации гистона H1 в ядрах обработанных клеток. Эти данные согласуются с результатами исследования функций гистона Н1, демонстрирующими, что снижение содержания ряда изоформ Н1 в хроматин‑связанной фракции приводит к запуску экспрессии ретротранспозонов, а затем интерферон‑зависимых генов [20]. Исполь‑ зуя модельные системы, разработанные для анализа эффектов CBL0137 на интерфероновый сигналинг I типа и локализацию гистона H1, можно оценить наличие и ассоциацию аналогичных эффектов рас‑ тительных полифенолов, выявление которых будет свидетельствовать о целесообразности изучения механизмов действия этих соединений, связанных с нарушениями процессов компактизации ДНК и пространственной структуры хроматина.
Цель исследования – анализ влияния рас‑ тительных полифенолов ресвератрола, кверце‑ тина и генистеина на запуск сигнального пути интерферона‑α и локализацию гистона Н1.
Материал и методы
Клеточные линии. В работе использованы следующие клеточные линии: HT1080 (ATCC), HT1080‑H1‑mCherry, HeLa‑TI‑ISRE‑mCherry. По‑ следние две линии были получены в лаборатории К. Гуровой, как это было описано ранее [17]. Клетки культивировали в стандартных условиях (+37 °C, 5 % CO2) в культуральной среде DMEM (Dulbecco’s modified Eagle’s medium, двойная модификация среды Игла) с добавлением эмбрио‑ нальной телячьей сыворотки (10 %), L‑глутамина и смеси антибиотиков пенициллина‑стрептомицина (откуда реактивы).
ДНК-тропные соединения
В работе использовались следующие раститель‑ ные полифенолы: ресвератрол (Selleck Chemical LLC), кверцетин (Sigma Aldrich), генистеин (Sigma Aldrich).
Прижизненная клеточная микроскопия
Для данного исследования была использована клеточная линия HT1080 H1‑mCherry. Клетки культивировали в 48‑луночных планшетах с про‑ зрачным дном (Mat‑Tek Corporation (Ashland, MA, USA). Оценку влияния растительных полифенолов на состав клеточной популяции в зависимости от локализации гистона Н1.5 в ядрах клеток прово‑ дили через 24 ч после обработки с помощью инвер‑ тированного микроскопа Zeiss Axio Observer A1 с иммерсионным объективом NAchroplan 100×/1.25 и камерой Zeiss MRC5 с программным обеспечени‑ ем AxioVision Rel.4.8. В некоторых случаях перед анализом флуоресценции клетки фиксировались в 4 % параформальдегиде в течение 10 мин.
Проточная цитофлуориметрия
Клетки линии HeLa TI ISRE‑mCherry инкуби‑ ровали с ДНК‑тропными соединениями в течение 48 ч в стандартных условиях, затем снимали с под‑ ложки с помощью растворов Версена и Трипсина, центрифугировали 4 мин при 1100 об/мин и про‑ мывали осадок в однократном буфере PBS. Анализ распределения клеточной популяции по уровню флуоресценции проводили на проточном цитоме‑ тре BD LSRII UV A Cytometers (BD Biosciences, San Jose, CA, USA). Полученные данные анализи‑ ровали с помощью программы WinList 3D (Verity Software House, Topsham, ME, USA).
Статистическая обработка данных
Все эксперименты выполнены в трех биоло‑ гических повторах с анализом триплета проб в каждом из них. Средние значения и среднеква‑ дратичные отклонения рассчитывали с помощью пакета программ Microsoft Excel. Для определения статистической значимости выявленных различий использовали парный двухвыборочный t‑тест Стьюдента для средних.
Результаты и обсуждение
На первом этапе исследования была определе‑ на цитотоксичность ресвератрола, генистеина и кверцетина на клетки линий HeLa c ISRE‑mCherry и Н1080 Н1.5‑mCherry с помощью МТТ‑теста. Максимальные нетоксичные дозы при обработке клеток HeLa c ISRE‑mCherry в течение 48 ч со‑ ставили для ресвератрола и кверцетина 100 мкМ и 61 мкМ соответственно, а для генистеина IC20 – 111 мкМ. В связи с этим в качестве максимальных
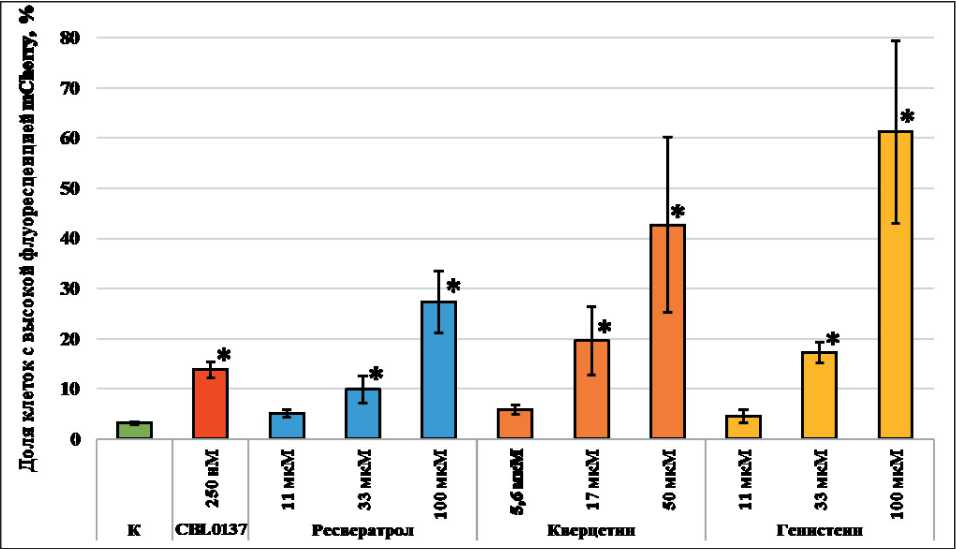
Рис. 1. Влияние ДНК-тропных фитонутриентов на экспрессию mCherry, находящегося под контролем ISRE.
Примечание: * – доля клеток с высокой флуоресценцией mCherry, статистически значимо превышающей контрольный уровень (p<0,05)
концентраций соединений при анализе их эффек‑ тов на активацию сигнального пути интерферона‑α использовали 100 мкМ для ресвератрола и гени‑ стеина и 50 мкМ для кверцетина.
Активацию сигнального пути интерферона‑α оценивали методом проточной цитофлуориметрии, учитывая экспрессию репортерного гена mCherry c ISRE в промоторной области через 48 ч после добав‑ ления в среду культивирования клеток анализируе‑ мого соединения. В качестве позитивного контроля использовали обработку клеток CBL0137 в дозе 0,25 мкМ. При обработке клеток HeLa‑ISRE‑mCher‑ ry ресвератролом в нетоксичных концентрациях 33 и 100 мкМ через 48 ч наблюдалось увеличение активности сигнального пути интерферона‑α в 3,3 и 9,0 раз соответственно (рис. 1).
При действии наименьшей концентрации ресве‑ ратрола (11 мкМ) увеличение доли клеток с флуо‑ ресценцией mCherry, превышающей контрольный уровень, составило 1,6 раза, однако это изменение не было статистически значимым.
Действие генистеина и кверцетина в концен‑ трациях 11 мкМ и 5,6 мкМ соответственно также не вызвало статистически значимого увеличения активности сигнального пути интерферона‑α, одна‑ ко имелась тенденция к увеличению доли клеток с высокой флуоресценцией mCherry (в 1,4 и 1,7 раза). При использовании генистеина в нетоксичных концентрациях (33 мкМ и 100 мкМ) наблюдалось увеличение доли клеток с высокой флуоресцен‑ цией mCherry – в 6,1 и 20,1 раза соответственно. Обработка клеток кверцетином в нетоксичной дозе 33 мкМ вызывала увеличение активности сигналь‑ ного пути интеферона‑α в 5,9 раза, а при действии 50 мкМ (IC20) – в 14,1 раза.
Таким образом, при обработке клеток HeLa‑ ISRE‑mCherry изучаемыми полифенолами расте‑ ний наблюдали дозозависимый эффект на уровень активности сигнального пути интерферона‑α.
Далее с помощью метода прижизненной флуоресцентной микроскопии оценивали влияние растительных полифенолов на состав клеточной популяции в зависимости от локализации гистона Н1.5 в ядрах клеток через 24 ч после обработки кле‑ ток соединениями в концентрациях, соответствую‑ щих IC50 при 48‑часовой обработке (рис. 2).
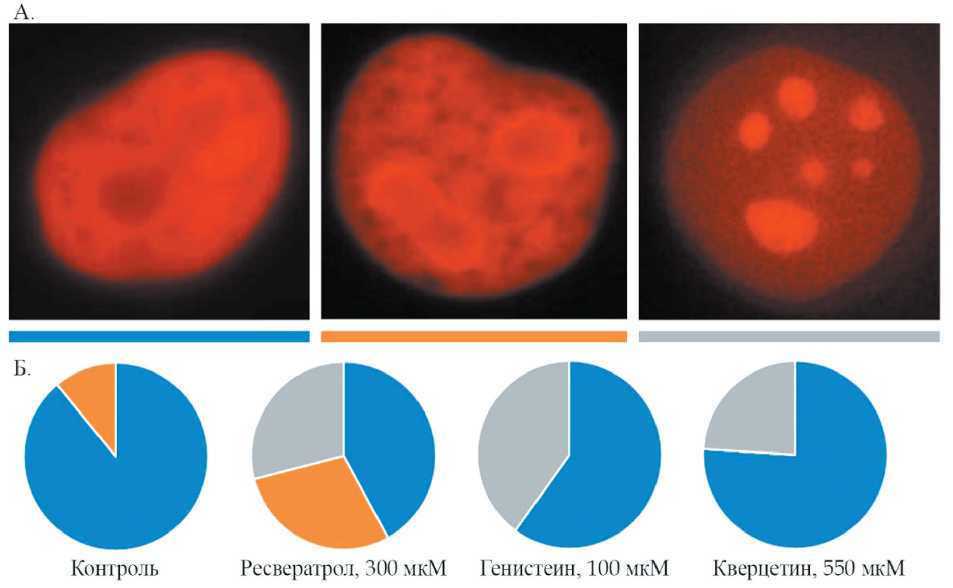
Рис. 2. Влияние ДНК-тропных соединений на локализацию гистона H1 через 24 ч после обработки клеток (синий – гистон H1.5 колокализован с хроматином, оранжевый – промежуточный тип, серый – гистон H1.5 преимущественно локализован в ядрышках):
А – метод прижизненной микроскопии клеток с флуоресцентно-меченным белком H1 (клеточная линия HT1080-H1-mCherry); Б – распределение ядер по типу локализации гистона H1.5
В образцах, не обработанных ДНК‑тропными соединениями, гистон H1.5 был колокализован с хроматином в 89 % ядер, промежуточный тип, при котором гистон частично находился в ядрышках, наблюдался в 11 % ядер, при этом ядер с ядрышко‑ вой локализацией гистонового белка H1 (3‑й тип) обнаружено не было. Наибольшие изменения в локализации гистона H1.5 вызвал ресвератрол в концентрации 333 мкМ: доля ядер с промежуточ‑ ным типом увеличилась до 29 %, при этом ещё в 29 % клеток наблюдалась ядрышковая локализация гистонового белка. При обработке клеток двумя другими агентами ядра с промежуточным типом локализации гистонового белка отсутствовали, в то же время доля клеток с интенсивным накоплением гистона Н1 в ядрышках для генистеина составила 40 %, для кверцетина – 24 %. Таким образом, изу‑ чаемые нами растительные полифенолы вызывали достаточно интенсивное изменение локализации гистона Н1.5 в ядрах клеток через 24 ч после начала обработки, что позволяет сделать вывод о наличии слабого хроматин‑дестабилизирующего эффекта у изученных соединений.
Наши данные об активации сигнального пути интерферона‑α ресвератролом и кверцетином согласуются с результатами исследований об активации этими соединениями экспрессии гена
Список литературы Активация сигнального пути интерферона-альфа ресвератролом, генистеином и кверцетином
- Pezzuto J.M. Resveratrol: Twenty Years of Growth, Development and Controversy. Biomol Ther (Seoul). 2018 Oct 11. DOI: 10.4062/biomolther.2018.176
- Russo M., Russo G.L., Daglia M., Kasi P.D., Ravi S., Nabavi S.F., Nabavi S.M. Understanding genistein in cancer: The «good» and the «bad» effects: A review. Food Chem. 2016 Apr 1; 196: 589-600. DOI: 10.1016/j.foodchem.2015.09.085
- Rauf A., Imran M., Khan I.A., Ur-Rehman M., Gilani S.A., Mehmood Z., Mubarak M.S. Anticancer potential of quercetin: A comprehensive review. Phytother Res. 2018 Nov; 32 (11): 2109-2130. DOI: 10.1002/ptr.6155
- Bishayee A. Cancer prevention and treatment with resveratrol: from rodent studies to clinical trials. Cancer Prev Res (Phila). 2009 May; 2 (5): 409-18. DOI: 10.1158/1940-6207.CAPR-08-0160
- Whitsett T.G.Jr., Lamartiniere C.A. Genistein and resveratrol: mammary cancer chemoprevention and mechanisms of action in the rat. Expert Rev Anticancer Ther. 2006; 6 (12): 1699-706. DOI: 10.1586/14737140.6.12.1699


