Активность лектинов проростков озимой пшеницы, выращеных на разнокачественом составе света в условиях засоления и действия тяжелых металлов
Автор: Якушенкова Татьяна Петровна, Тимофеева Ольга Арнольдовна, Зиатдинова Алина Александровна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Экология
Статья в выпуске: 3-5 т.15, 2013 года.
Бесплатный доступ
Показано,что свет различного спектрального состава регулирует активность лектинов корней проростков пшеницы под воздействием засоления и действия тяжелых металлов
Проростки пшеницы, спектральный состав света, тивность лектинов засоление, тяжелые металлы, активность лектинов, устойчивость растений
Короткий адрес: https://sciup.org/148202036
IDR: 148202036 | УДК: 57.042
Lectin activity prostki winter wheat grown on differint quailty part in the light of salinity and heavy metals
It is shown that light of different spectral composition regulates the activity of lectin wheat seedling roots under the influence of salinity and the effect of heavy metals
Текст научной статьи Активность лектинов проростков озимой пшеницы, выращеных на разнокачественом составе света в условиях засоления и действия тяжелых металлов
Одним из важнейших факторов окружающей среды, регулирующих процесс жизнедеятельности растений, является свет. Хорошо известно, что свет обеспечивает не только осуществление фотосинтеза, но и действует прямо или косвенно на все процессы обмена веществ и жизнедеятельность растительного организма, в частности устойчивость растений. Свет действует на растительный организм полифункционально: является субстратом для фотосинтеза и оказывает мощное регуляторное воздействие на растение.
Для оценки качества и количества падающего света у растений имеются разнообразные рецепторы: криптохромы, фитохромы, фототропины.
Поглощая свет определенного спектрального диапазона, фоторецепторы вступают в фотохимические реакции с образованием первичных фотопродуктов. Последние участвуют в биохимических процессах клеточной регуляции, что приводит к развитию конечных фотобиологических эффектов.
В последнее время из различных видов растений выделены углеводсвязывающие белки – лектины. Физиологическая роль лектинов многообразна, они участвуют в межклеточном узнавании растениями фитопатогенов [1], обратимо взаимодействуют с фитогормонами [14], вовлекаются в формирование неспецифического адаптационного синдрома при низкотемпературном воздействии [9], в формировании ответных реакций при гипертермии, засухе и осмотическом шоке [17], засолении среды [15]. Все эти данные, по мнению Ф.М. Шакировой [14], позволяют рассматривать лектины как маркеры и участники системы формирования устойчивости растений.
Несмотря на детальное исследование физикохимических и биологических свойств многих лектинов, их физиологическая значимость для растений носит предположительный характер [14]. Данных о регуляторном влиянии света различного качества на устойчивость растений в литературе име-
Якушенкова Татьяна Петровна, к.б.н., старший преподаватель, е- mail: tyakushe@ ksu.ru; Тимофеева Ольга Арнольдовна, д.б.н., проф., зав. кафедрой; Зиатдинова Алина Александровна, студент ется недостаточно, и они носят эпизодический характер [3, 8, 18]. В связи с этим приобретают исключительную актуальность исследования механизмов фоторегуляторного влияния света различного качества на активность лектинов при действии засоления и солей тяжелых металлов.
Целью работы явилось изучение активности лектинов клеточной стенки и растворимых лектинов у проростков озимой пшеницы сорта Казанская 560 при выращивании на свету различного качества в условиях засоления среды и действия солей тяжелых металлов.
Объектом исследования служили корни семидневных проростков озимой пшеницы ( Triticum aestivum L.) сорта Казанская 560.
Семена перед посевом стерилизовали 2%-ным перманганатом калия (15 мин), промывали дистиллированной водой, проращивали в кюветах на влажной фильтровальной бумаге. Растения выращивали в кюветах на водопроводной воде (контроль). В качестве фактора засоления использовали NaCl в концентрации 150 мМ, в качестве действия тяжелых металлов – CuSO 4 в концентрации 1 мМ и CdSO 4 в концентрации 1 мМ (опыт). Водопроводную воду заменяли на растворы солей и тяжелых металлов на 5-е сут.
Растения проращивали в растильне, разделенной на три светоизолированных блока: 1-й – белый свет (источник освещения – люминесцентные лампы ЛДС-40), 2-й – синий свет (источник – люминесцентные лампы ЛГ-40, область пропускания 420-460 нм), 3-й – красный свет (источник – люминесцентные лампы ЛК-40, область пропускания 620-640 нм) при 12-часовом световом периоде.
Для экстрагирования растворимых лектинов навеску растительного материала (0,5 г корней) гомогенизировали в 5 мл 0,05н. HCl при соотношении навеска:среда 1:10, постоянно перемешивая в течение одного часа при t=40C. Известно, что лектины экстрагируются больше в кислой среде (0,05н. HCl), чем в нейтральной (0,01М фосфатнобуферная смесь (ФБС) [6]. Затем экстракт центрифугировали при 8000 об/мин в течение 10 мин и промывали половинным от исходного объемом соляной кислоты (2,5 мл). Надосадочные жидкости собирали, нейтрализовали 10%-ным раствором КОН в соотношении щелочь:экстракт 1:2, супернатант повторно центрифугировали и использовали для определения лектиновой активности. Осадок использовали для выделения лектинов клеточной стенки. Остаток после экстрагирования растворимых лектинов гомогенизировали в среде, содержащей 5 мМ ацетатный буфер (рН 4,6), 0,4 М сахарозы и центрифугировали при 8000 об/мин в течение 10 мин. Надосадочные жидкости сливали, а осадок последовательно промывали в средах, содержащих 5 мМ ацетатного буфера (рН 4,6), 0,6 М сахарозы/ 1М сахарозы и центрифугировали при 8000 об/мин в течение 10 мин. Далее осадок промывали на нейлоновой ткани большим количеством 5 мМ ацетатного буфера (рН 4,6). Из оставшегося на ткани твердого осадка, содержащего клеточные стенки, лектины экстрагировали исходной средой с добавлением (в конечной концентрации) 0,05% тритона Х-100 и 0,9% NaCl. Так как тритон Х-100 состоит из неионных детергентов на основе полиэтиленгликоля, которые растворяют мембрану и защищают компоненты мембраны алифатическими или ароматическими цепями, то он способствует вытеснению прочно связанного белка. Настаивали 3 ч при 1=200С и постоянном перемешивании, затем центрифугировали 10 мин при 8000 об/мин. Осадок отбрасывали, а супернатант (фракция, обогащенная лектинами клеточных стенок) использовали для определения активности лектинов. Белок определяли по методу Лоури.
Для идентификации лектиновой активности исследовали агглютинацию трипсинизированных эритроцитов человека I группы крови. Лектиновую активность определяли методом микротитрования. Реакцию проводили в специальных планшетах для иммунологических реакций с U-образными лунками. Для этого готовили серию последовательных двукратных разведений белкового эктракта лектинов (10 разведений) по 0,05 мл, в каждую лунку добавляли 0,05 мл 2%-ной суспензии эритроцитов и смесь оставляли при комнатной температуре на 60-120 мин.
Учитывали агглютинацию эритроцитов по форме осадка. Титр лектина характеризовался максимальным разведением или минимальной концентрацией его в растворе, при которой наблюдалась агглютинация эритроцитов. Активность лектинов выражали величинах, обратных минимальной концентрации белка, при которой отмечали реакцию гемагглютинации (мкг/мл)-1.
Все эксперименты проводились в трехкратной биологической повторности. Повторность в пределах одного опыта трехкратная.
Статистическую обработку экспериментальных данных проводили путем определения средних арифметических и их стандартных ошибок.
Засоление относится к числу распространенных неблагоприятных условий окружающей среды, приводящих к снижению интенсивности интегральных физиологических процессов в растениях [2, 11, 25]. Безусловно, растительные организмы вырабатывают в ответ на это воздействие разнообразные защитные механизмы, среди которых важное место отводят сдвигу в белковом спектре: на фоне снижения тотального синтеза белка наблюдается новообразование ряда пептидов [23], а также усиление синтеза некоторых белков, характерных для нормы [13, 16, 20, 21, 23] было показано, что воздействие 2%-го NaCl вызывало уже через 2 ч двукратное накопление АЗП в корнях проростков пшеницы и к 7 ч наблюдалось 5-кратное возрастание содержания этого белка. Это четко демонстрирует факт довольно значительного изменения в содержании лектина при солевом стрессе, что свидетельствует о вовлечении его в формирование быстрых АБК-регулируемых ответных реакций проростков пшеницы на это воздействие [13].
Предполагают, что засоление среды вызывает быстрое накопление АБК, которое может приводить к существенному сдвигу в белковом спектре клеток растений, в частности балансе [1, 23, 24].
Отмечают, что количественные изменения лектина в вегетирующих растениях пшеницы при стрессовых воздействиях могут контролироваться не только на транскрипционном, но и посттранскрипционном и посттрансляционном уровнях. Такая ситуация вполне возможна, поскольку лектин пшеницы является присущим для растений на протяжении всего онтогенеза и, скорее всего, определенный резерв лектиновых мРНК и предшественников АЗП всегда присутствует в клетках. Спектральный состав света в условиях засоления увеличивал активность как растворимых, так и связанных с клеточной стенкой лектинов (рис. 1, 2).
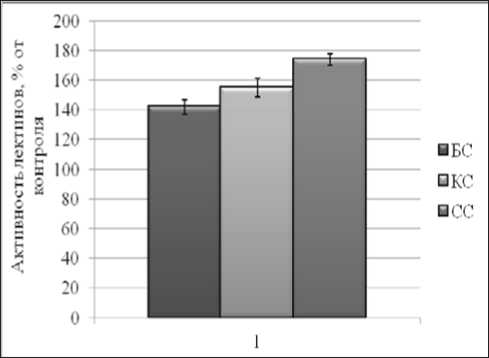
Рис. 1. Влияние 150 мМ NaCl [1] на активность растворимых лектинов в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
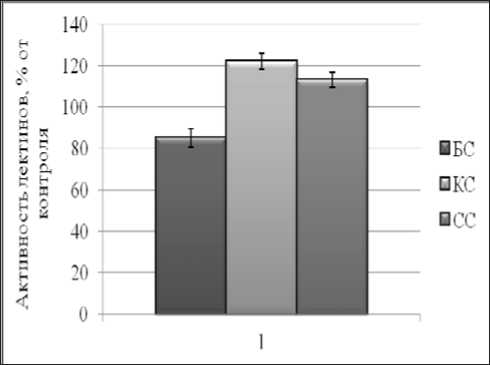
Рис. 2. Влияние 150 мМ NaCl [1] на активность лектинов клеточной стенки в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
На активность растворимых лектинов в условиях засоления наиболее сильный эффект оказывал синий свет: наблюдалось увеличение до 174%. Такое же действие на лектины клеточной стенки оказывал красный свет – активность повышалась и составила 122% от контрольного уровня.
Возможно, что увеличение лектиновой активности под действием различного спектрального состава в условиях засоления происходит как за счет регуляции накопления лектина (например АЗП), так и, в большей степени, за счет ускорения созревания его предшественников, т.е. на посттрансляционном уровне.
Известно, что в процессе эволюции растения выработали целый ряд приспособительных механизмов, защищающих клеточный метаболизм от присутствующих в окружающей среде тяжелых металлов. К ним относятся: уменьшение поступления металлов в клетку, активация систем их выведения, изоляция в метаболически малоактивных соединениях и компартментах, изменения метаболизма, направленные на снижение токсического действия металлов или ликвидацию его последствий [12].
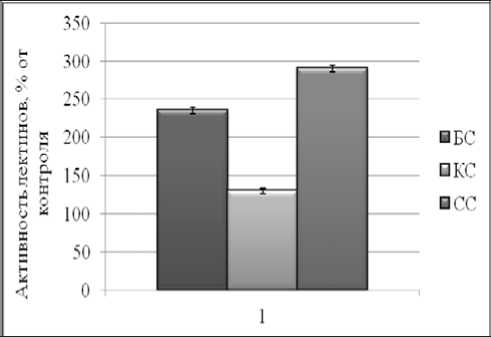
Рис. 3. Влияние 1 мМ CuSO4 [1] на активность растворимых лектинов в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
Первым барьером на пути поступления ионов тяжелых металлов являются клеточные стенки корня. Данные многих авторов свидетельствуют о значительном накоплении тяжелых металлов именно в клеточной стенке [7]. При этом прочность связи различных ионов металлов с компонентами клеточной оболочки неодинакова. Она коррелирует с величиной констант стабильности (log K) комплексов металлов с карбоксильными группами углеводов. Для Cd равен 4 [22].
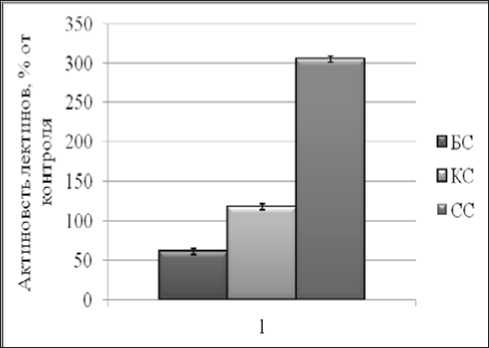
Рис. 4 . Влияние 1 мМ CuSO4 [1] на активность лектинов клеточной стенки в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
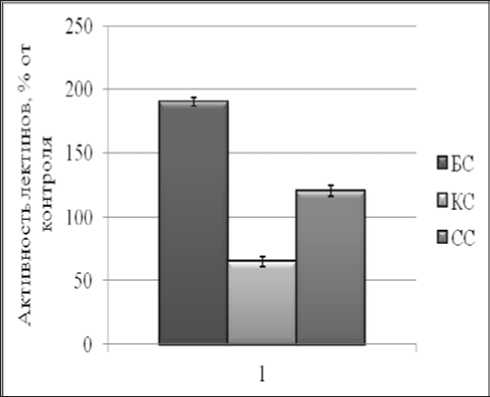
Рис. 5. Влияние 1 мМ CdSO 4 на активность растворимых лектинов в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
Сродство других тяжелых металлов к полига-лактуроновой кислоте уменьшается в ряду: Pb > Cr > Cu > Ca > Zn. Сравнение констант стабильности показывает, что тяжелые металлы могут успешно конкурировать с кальцием за места связывания в «замковых зонах» пектинов. Таким образом, вероятно, что тяжелые металлы способны прочно связываться с SH-группами лектиновых белков и карбоксильными группами углеводных компонентов лектинов. Образование таких связей может нарушать конформационную структуру лектинов кле- точной стенки, а также их физико-химические свойства и углеводную специфичность, результатом этих событий будет ингибирование активности лектиновых белков. Кроме того, возможно, что высокая концентрация тяжелых металлов в клеточной стенке и свободном пространстве приводит к изменению углеводного состава клетки, в результате чего может накапливаться ряд углеводов, являющихся или же, наоборот, не являющихся специфическими гаптенами для исследуемых лектинов.
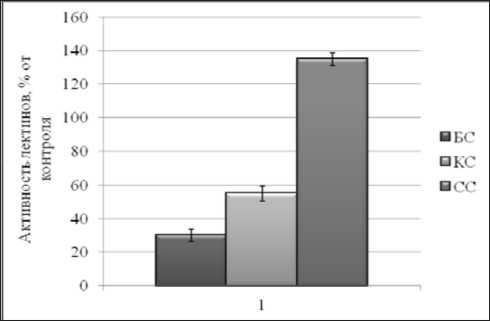
Рис. 6. Влияние 1 мМ CdSO 4 на активность лектинов клеточной стенки в корнях проростков озимой пшеницы Казанская 560, выращенных на разнокачественном свету
В таком случае увеличение или уменьшение связывания лектинов со специфичными для них сахарами также может изменять их активность.
Выращивание растений озимой пшеницы на среде с солями тяжелых металлов вызывало значительное возрастание активности растворимых лектинов, под которыми мы подразумеваем АЗП (Рис. 3,5). Вероятно, увеличение активности растворимых лектинов является транзитным и растет по мере развития повреждения растений от тяжелых металлов. В тоже время, известно, что АЗП является стрессовым белком, и увеличение его активности может свидетельствовать о вовлечении АЗП в защитные реакции к действию тяжелых металлов.
Изменение лектиновой активности, может быть следствием как трансляционных, так и посттрансляционных событий. Известно, что в ходе своего синтеза АЗП претерпевает сложный посттрансляционный процессинг, этапы которого были прослежены с использованием полученных к предшественникам АЗП антител, не преципитирующих зрелый белок [22]. В связи с этим, увеличение содержания лектинов может происходить за счет ранее синтезированных предшественников.
Попадая в клетку растения, часть ионов металлов связывается специфическими белками, названными металлотионеинами. Металлотионеины представляют собой низкомолекулярные белки (810 кД), в составе которых около 30% приходится на серосодержащую аминокислоту цистеин [19]. Механизм их действия заключается в связывании ионов тяжелых металлов сульфгидрильными группа- ми цистеина. Согласно сведениям литературы, в ответ на повышение концентрации тяжелых металлов в окружающей среде в растениях может синтезироваться довольно большое количество металло-тионеинов, что позволяет связывать до 60-100% металла [10]. Мы полагаем, что АЗП может участвовать в связывании тяжелых металлов и выведение их из клеток корней, что способствует уменьшению их концентрации на наружной поверхности клеток. В пользу этого предположения выступает способность АЗП в больших количествах выделяться в корневой чехлик/окружающую среду.
Под влиянием спектрального состава света увеличивалась активность лектинов корней проростков пшеницы, выращенных на СС, в условиях действия ТМ. Наибольшее увеличение в активности лектинов наблюдали под действием CuSO 4 (в 3 раза). Красный свет практически не влиял на активность лектинов при действии меди и уменьшал активность лектинов под воздействием кадмия. Возможно, что изменение активности лектинов под влиянием синего света обусловлено в первую очередь синтезом новых белков и их предшественников, обладающих агглютинирующей способностью, но не способных к прочному связыванию ТМ с SH-группами белков. В тоже время повышение активности лектинов может свидетельствовать об увеличении устойчивости растений к различным абиотическим стрессам [5]. Исходя из этого можно предположить, что синий свет положительно влиял на устойчивость проростков пшеницы при действии ионов меди и кадмия.
-
1. Антонюк Л.П., Игнатов В.В. О роли агглютинина зародыша пшеницы в растительно-бактериальном взаимодействии: гипотеза и экспериментальные данные в ее поддержку // Физиол. раст. 2001. Т. 48. № 3. С. 427-433.
-
2. Блехман Г.И. Синтез белка в условиях стресса // Успехи совр. биол. 1987. Т. 103. С. 340-353.
-
3. Креславский В.Д., Христин Н.И., Шабнова Н.И. ,Любимов В.Ю . Предоблучение отдельных листьев шпината красным светом повышает устойчивость фотосинтетического аппарата к УФ-радиации // Физиол. раст. 2012. Т. 59. № 6. С. 723-729.
-
4. Левчук А.Н., Войтович Е.Н., Лях В.А . // Физиол. раст. 2013. Т. 60. № 1. С. 75-81.
-
5. Луцик М.Д., Панасюк Е.Н., Луцик А.Д. Лектины. Львов: Высш. шк. Изд-во при Львов. ун-те, 1981. 156 с.
-
6. Серегин И.В., Иванов В.Б. Является ли барьерная функ- ция эндодермы единственной причиной устойчивости
ветвления корней к солям тяжелых металлов? // Физиол. раст. 1997. Т. 44. № 6. С. 922-925.
-
7. Сысоева М.И., Марковская Е.Ф., Шерудило Е.Г. Роль фитохрома в формировании холодоустойчивости растений огурца на свету и в темноте // Физиол. раст. 2013. Т. 60. № 3. С.386-392.
-
8. Тимофеева О.А. Лектины как активные компоненты адаптивных реакций озимой пшеницы к неблагоприятным условиям среды: Автореф. дис. … д-ра биол. наук. Уфа, 2009. 38 с.
-
9. Титов А.Ф., Таланова В.В., Казнина Н.М., Лайдинен Г.Ф. Устойчивость растений к тяжелым металлам / Под ред. Н.Н. Немова. Петрозаводск: КарНЦ РАН, 2007. 172 с.
-
10. Удовенко Г.В. Механизмы адаптации растений к стрессам // Физиол. и биохимия культ. раст. 1979. Т. 11. С. 99107.
-
11. Чиркова Т.В . Физиологические основы устойчивости растений. СПб.: Изд-во СПбГУ, 2002. 244 с.
-
12. Шакирова Ф.М . Неспецифическая устойчивость растений к стрессовым факторам и ее регуляция. Уфа: Гилем, 2001. 159 с.
-
13. Шакирова Ф.М . Современные представления о предполагаемых функциях лектинов растений // Журн. общ. биол. 2007. Т. 68. № 2. С. 98-114.
-
14. Шакирова Ф.М., Безрукова М.В., Хайруллин Р.М . Стимуляция увеличения уровня лектина в проростках пшеницы под влиянием солевого стресса // Изв. РАН Сер. биол. 1993. №. 1. С. 143-145.
-
15. Amitai-Zeigerson H., Scolnik C.A., Bar-Zvi D. Tomato Asr1 mRNA and protein are transiently expressed following salt stress, osmotic stress and abscisic acid // Plant Sci. 1995. V. 110. P. 205-213.
-
16. Cammue B.P.A., Broecaert W.F., Kellens T.S. Stress-indused accumulation of wheat germ agglutinin and abscisic acid in roots of wheat seedlings // Plant Physiol. 1989. V. 91. P. 1432-1435.
-
17. Foreman J., Johansson H., Hornitschek P., Josse E.M.,Fankhauser C., Halliday K.J. Light receptor action is
critical for maintaiming plant biomass at warm ambient temperatures // The Plant Journ. 2011. 65 (3). P. 444-452.
-
18. Gibson D.M., Sharon S.I., Hous K.J. A comparision of soy-been agglutinin in cultivars resistant and susceptible to Phy-tophtora megasperma var sojae // Plant Physiol. 1982. V. 70. P. 560-566.
-
19. Hurkman W., Tanaka C.K. The effects of salt on the pattern of protein synthesis in barley roots // Plant Physiol. 1987. V. 83. P. 517-524.
-
20. Hurkman W., Tanaka C.K . Effect of salt stress on germin gene expression in barley roots // Plant Physiol. 1996. V. 110. P. 971-977.
-
21. Mansfield M.A., Peumans W.J., Raikhel N.V . Wheat germ agglutinin is synthesized as a glycosylated precursor // Planta. 1988. V. 173. P. 482-489.
-
22. Ramagopal S. Salinity stress induced tissuespecific proteins in barley seedlings // Plant Physiol. 1987. V. 84. P. 324-331.
-
23. Singh P.S., Bhaglal P., Bhullar S.S. Wheat germ agglutinin (WGA) gene expression and ABA accumulation in the developing embryos of wheat ( Triticum aestivum ) in response to drought // Plant Growth Reg. 2000. Vol. 30. P. 145-150.
-
24. Sugino M., Hibino T., Tanako Y. et al . Overexpression of DnaK from a halotolerant cyanobacte-rium Aphanothece ha-lophytica acquires resistance to salt stress in transgenic tobacco plants // Plant Sci. 1999. V. 146. P. 81-88.
LECTIN ACTIVITY PROSTKI WINTER WHEAT GROWN ON DIFFERINT QUAILTY PART IN THE LIGHT OF SALINITY AND HEAVY METALS
Список литературы Активность лектинов проростков озимой пшеницы, выращеных на разнокачественом составе света в условиях засоления и действия тяжелых металлов
- Антонюк Л.П., Игнатов В.В. О роли агглютинина зародыша пшеницы в растительно-бактериальном взаимодействии: гипотеза и экспериментальные данные в ее поддержку//Физиол. раст. 2001. Т. 48. № 3. С. 427-433.
- Блехман Г.И. Синтез белка в условиях стресса//Успехи совр. биол. 1987. Т. 103. С. 340-353.
- Креславский В.Д., Христин Н.И., Шабнова Н.И.,Любимов В.Ю. Предоблучение отдельных листьев шпината красным светом повышает устойчивость фотосинтетического аппарата к УФ-радиации//Физиол. раст. 2012. Т. 59. № 6. С. 723-729.
- Левчук А.Н., Войтович Е.Н., Лях В.А.//Физиол. раст. 2013. Т. 60. № 1. С. 75-81.
- Луцик М.Д., Панасюк Е.Н., Луцик А.Д. Лектины. Львов: Высш. шк. Изд-во при Львов. ун-те, 1981. 156 с.
- Серегин И.В., Иванов В.Б. Является ли барьерная функция эндодермы единственной причиной устойчивости ветвления корней к солям тяжелых металлов?//Физиол. раст. 1997. Т. 44. № 6. С. 922-925.
- Сысоева М.И., Марковская Е.Ф., Шерудило Е.Г. Роль фитохрома в формировании холодоустойчивости растений огурца на свету и в темноте//Физиол. раст. 2013. Т. 60. № 3. С.386-392.
- Тимофеева О.А. Лектины как активные компоненты адаптивных реакций озимой пшеницы к неблагоприятным условиям среды: Автореф. дис. … д-ра биол. наук. Уфа, 2009. 38 с.
- Титов А.Ф., Таланова В.В., Казнина Н.М., Лайдинен Г.Ф. Устойчивость растений к тяжелым металлам/Под ред. Н.Н. Немова. Петрозаводск: КарНЦ РАН, 2007. 172 с.
- Удовенко Г.В. Механизмы адаптации растений к стрессам//Физиол. и биохимия культ. раст. 1979. Т. 11. С. 99-107.
- Чиркова Т.В. Физиологические основы устойчивости растений. СПб.: Изд-во СПбГУ, 2002. 244 с.
- Шакирова Ф.М. Неспецифическая устойчивость растений к стрессовым факторам и ее регуляция. Уфа: Гилем, 2001. 159 с.
- Шакирова Ф.М. Современные представления о предполагаемых функциях лектинов растений//Журн. общ. биол. 2007. Т. 68. № 2. С. 98-114.
- Шакирова Ф.М., Безрукова М.В., Хайруллин Р.М. Стимуляция увеличения уровня лектина в проростках пшеницы под влиянием солевого стресса//Изв. РАН Сер. биол. 1993. №. 1. С. 143-145.
- Amitai-Zeigerson H., Scolnik C.A., Bar-Zvi D. Tomato Asr1 mRNA and protein are transiently expressed following salt stress, osmotic stress and abscisic acid//Plant Sci. 1995. V. 110. P. 205-213.
- Cammue B.P.A., Broecaert W.F., Kellens T.S. Stressindused accumulation of wheat germ agglutinin and abscisic acid in roots of wheat seedlings//Plant Physiol. 1989. V. 91. P. 1432-1435.
- Foreman J., Johansson H., Hornitschek P., Josse E.M.,Fankhauser C., Halliday K.J. Light receptor action is critical for maintaiming plant biomass at warm ambient temperatures//The Plant Journ. 2011. 65 (3). P. 444-452.
- Gibson D.M., Sharon S.I., Hous K.J. A comparision of soybeen agglutinin in cultivars resistant and susceptible to Phytophtora megasperma var sojae//Plant Physiol. 1982. V. 70. P. 560-566.
- Hurkman W., Tanaka C.K. The effects of salt on the pattern of protein synthesis in barley roots//Plant Physiol. 1987. V. 83. P. 517-524.
- Hurkman W., Tanaka C.K. Effect of salt stress on germin gene expression in barley roots//Plant Physiol. 1996. V. 110. P. 971-977.
- Mansfield M.A., Peumans W.J., Raikhel N.V. Wheat germ agglutinin is synthesized as a glycosylated precursor//Plan-ta. 1988. V. 173. P. 482-489.
- Ramagopal S. Salinity stress induced tissuespecific proteins in barley seedlings//Plant Physiol. 1987. V. 84. P. 324-331.
- Singh P.S., Bhaglal P., Bhullar S.S. Wheat germ agglutinin (WGA) gene expression and ABA accumulation in the developing embryos of wheat (Triticum aestivum) in response to drought//Plant Growth Reg. 2000. Vol. 30. P. 145-150.
- Sugino M., Hibino T., Tanako Y. et al. Overexpression of DnaK from a halotolerant cyanobacterium Aphanothece halophytica acquires resistance to salt stress in transgenic tobacco plants//Plant Sci. 1999. V. 146. P. 81-88.


