Активность магнетита в шпинельном растворе системы Fe-Cu-O
Автор: Лыкасов A.A., Голлай A.B., Павловская М.С., Катков А.Э.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 3 (43), 2005 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/147156512
IDR: 147156512 | УДК: 541.123.3:
Текст статьи Активность магнетита в шпинельном растворе системы Fe-Cu-O
В системе Fe-Cu-О в широкой области парциальных давлений кислорода и состава системы существует фаза со структурой шпинели [1-10]. Примем за компоненты этой фазы магнетит (Fe3O4) и феррит меди (CuFe2O4) и выразим ее состав формулой Ре^СщОу. Степень окисленности шпинели в пределах ее области гомогенности изменяется незначительно, так что «у» можно считать равным 1,333.
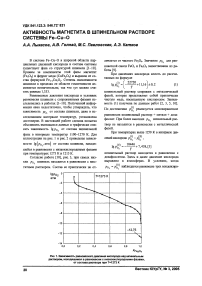
Равновесные давления кислорода в условиях равновесия шпинели с сопряженными фазами исследовались в работах [1-10]. Полученной информации явно недостаточно, чтобы утверждать, что зависимость р01 от состава шпинели, даже в исследованном интервале температур, установлена достоверно. В настоящей работе сделана попытка объединить имеющиеся данные и графически описать зависимость lgpo2от состава шпинельной фазы в интервале температур 1100-1270 К. Для иллюстрации на рис. 1 и рис. 2 приведены зависимости lg^p02,aTM) от состава шпинели, находящейся в равновесии с низкокислородными фазами при температурах 1273 К и 1213 К.
хРе3О4
Рис. 1. Зависимость равновесного давления кислорода над шпинельным раствором, находящимся в равновесии с низкокислородными фазами, от состава раствора при Т=1273 К
личается от чистого Fe3O4. Значения рОз для равновесной смеси FeOr и Fe3O4 заимствованы из работы [9].
При давлениях кислорода вплоть до рассчитанных по формуле
18^0? =(-^^ + 11’16)±0’2
шпинельный раствор сопряжен с металлической фазой, которая представляет собой практически чистую медь, насыщенную кислородом. Зависимость (1) получена по данным работ [2, 3, 5, 10]. По достижении р^ реализуется моновариантное равновесие шпинельный раствор + металл + делафоссит. При более высоких рОг шпинельный раствор не находится в равновесии с металлической фазой.
При температурах выше 1250 К в интервале давлении кислорода - р^’,
. (П) 10446
№2 =--—+7,438, [3]
шпинельный раствор находится в равновесии с
xFe3O4
Рис. 2. Зависимость равновесного давления кислорода над шпинельным раствором, находящимся в равновесии с низкокислородными фазами, от состава раствора при Т=1213 К
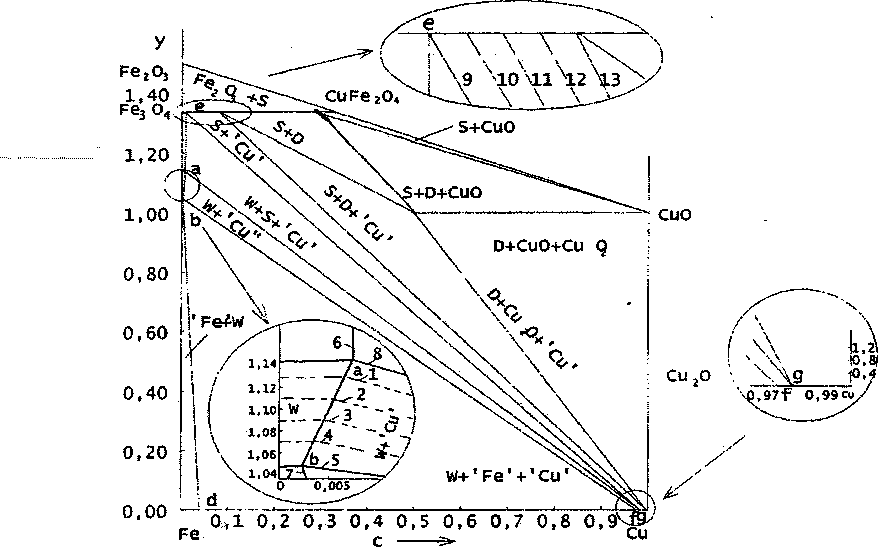
Рис. 3. Фазовая диаграмма системы Fe-Cu-О при 1273 К -lg pOi : 1 -13,03; 2 -13,49; 3 -13,95; 4 - 14,42; 5, 7 -14,88; 6, 8, 9 - 12,56; 10 - 10,02; 11 - 7,35; 12 - 7,02; 13 - 6,68
ванных фаз: шпинельный раствор + делафоссит + СпО. Состав шпинельной фазы в этих условиях мало изменяется с температурой. По данным работ [2, 8, 5, 6] зависимость состава шпинели от температуры в интервале 1000-1700 К может быть выражена уравнением хРезО4 = 1,137-2,167-Ю"4/-.
При Г<1250 К область гомогенности шпинельной фазы расслаивается на две области. Бога тая Fe3O4 область при заданной температуре стабильна до pOi = рх0 ', lg^=-^ + 18,46,[10]
а фаза на основе CuFeO, стабильна при ро а Pq
-1^-19,22 [10].
Т, К 1260
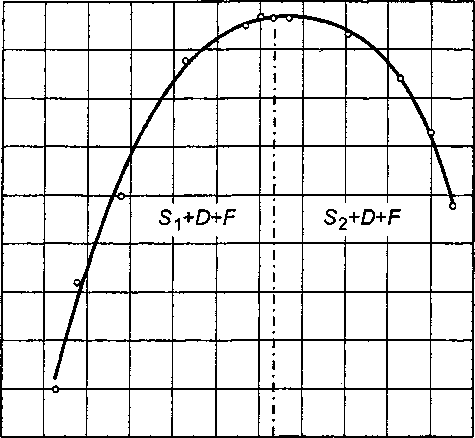
0,04 0,06 0,08 0,10 0,12 0,14 0,16 0,18 0,20 0,22 0,24 С
Рис. 4. Состав шпинельных фаз в условиях моновариантного равновесия с Fe2O3 и CuFeO2. Si - шпинельный раствор на основе магнетита, S2 - шпинельный раствор на основе феррита, D - делафоссит, F - гематит
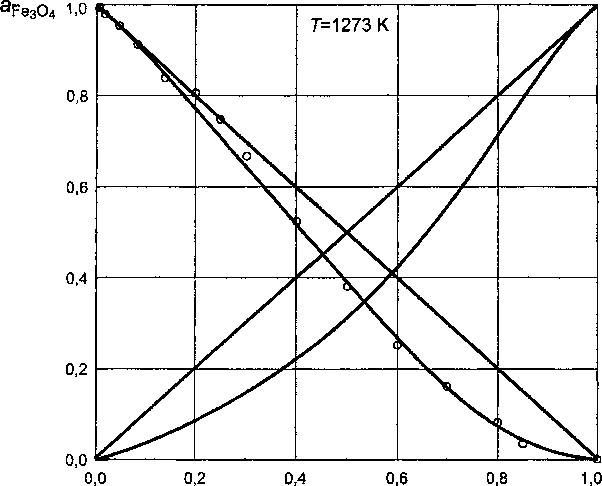
хСи РегОд
Рис. 5. Активность Fe2O2 и CuFeO2 в шпинельном растворе при Г = 1273 К
Растворы не сопряжены друг с другом. Равновесными фазами насыщенных растворов являются Fe2O3 и делафоссит (CuFeO2). Составы шпинельных фаз в условиях моновариантных равновесий с Fe2O3 и CuFeO2 приведены на рис. 4. Левая ветвь «купола» распада определяет предельной содержание Fe3O4 в фазе на основе магнетита, а правая -на основе феррита меди.
Полученные зависимости lgpO2 = /(хРезо4) позволили рассчитать активности Fe3O4 в шпи нельном растворе, используя условия равновесия и уравнение Гиббса-Дюгема:
« 2 « с
"F.,O.=
Концентрационные зависимости активности Fe3O4 в шпинельном растворе представлены на рис. 5 и рис. 6. При Т = 1273 К в условиях равновесия шпинели с металлом активность РеэО4 практически равна молярной доле Fe3O4. В дальнейшем наблюдаются отрицательные отклонения от закона

хСиРегО4
Рис. 6. Активность РегОз в шпинельном растворе при Т=1273 К
Рауля, возрастающие по мере уменьшения содержания Ре3О4 в растворе.
Для описания зависимости активности Ре3О4 от состава раствора и температуры при Т> 1250 К применили модель субрегулярного раствора Ре3О4 и СиРеО2:
°РезО4 =хРезО4 х хехр-
l~xFe3O4
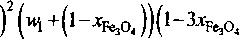
RT
М2)
где и^ = 21132 — 18,9927, w2 = -224304 +174,4097 (1253-1273 К). Расчеты по формуле (2) сопоставлены с опытными данными на рис. 5. Согласие достаточное, чтобы эту модель применить для описания зависимости активности делафоссита от состава раствора. Эта зависимость при Т=1273 К приведена на рис. 5.
С понижением температуры при равновесии с металлом проявляется тенденция к положительным отклонениям от закона Рауля, которая явно проявляется при 7=1250 К. Ниже 1250 К отклонения от закона Рауля знакопеременные для раствора на основе магнетита и отрицательные для раствора на основе феррита меди (рис. 6).
Список литературы Активность магнетита в шпинельном растворе системы Fe-Cu-O
- Третьяков Ю.Д. Термодинамика ферритов -Л.: Химия, 1967.
- Залазинский А.Г., Балакирев В.Ф., Чуфаров Г.И. Диаграмма «давление кислорода -состав» в системе Cu-Fe-O при 1000°С//ЖФХ. -1969. Т. 43. -№ 6-С. 1636 -1637.
- Schaefer S.C., Hundley G.L., Block F.E. and other. Phase Equilibria and X-Ray Diffraction Investigation of the System Cu-Fe-O//Metal. Trans. -1970, -V.1. -№ 9. -P. 2557-2561.
- Katsutoshi O., Yoshihiro I., Ario Y. and other. The Equilibrium Phase Diagram of Cu-Fe-О System//J. Japan Inst. Metals. -1972. -V. 36. -№ 7. -P. 701-704.
- Paulsson H., Rosen E., Terman R. Thermodynamic Studies of High Temperature Equilibria. Potentiometriс determination of the stability of CuFeО2 using a galvanic cell involving stabilized ZrО2 as solid electrolyte//Chem. Scr. -1975. -V. 8. -№ 5. -P. 193-196.
- Fredriksson M., Rosen E. Thermodynamic Stud ies of High Temperature Equilibria. On phase relations and equilibrium oxygen pressures in the system Cu-CuFeO2-Fe2O3-Fe3O4 at temperatures 1100-1300 K//Chem. Scr. -1976. -V. 9. -№ 3. -P. 118-121.
- Eriksson G., Tegman R. Thermodynamic Studies of High Temperature Equilibria. Determination of the stability of CuFe2O4 by оf measurements using stabilized ZrO2 as solid electrolyte//Chem. Scr. -1976. -V. 10. -№ 4. -P. 164-167.
- Jacob K.T., Fitzner K., Alcock C.B. Activities in the spinel Solid Solution. Phase Equilibria and Thermodynamic Properties of Ternary Phases in the System Cu-Fe-O//Metal. Trans. -1977. -V. 8B. -№ 3. -P. 451-460.
- Лыкасов A.A., Карел К., Мень А.Н., Варшавский М.Т., Михайлов Г.Г. Физико-химические свойства вюстита и его растворов. -Свердловск: УНЦ АН СССР, 1987.
- Катков А.Э., Лыкасов A.A. Фазовые равновесия твердых растворов со структурой шпинели в системе Fe3O4-CuFe2O4//Неорганические материалы. -2003. -Т. 39. -№ 2. -С. 223 -226.