Активность пероксидазы в органах и тканях деревьев березы повислой
Автор: Галибина Наталия Алексеевна, Целищева Юлия Леонидовна, Андреев Владимир Петрович, Софронова Ирина Николаевна, Никерова Михайловна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Биология
Статья в выпуске: 4 (133), 2013 года.
Бесплатный доступ
На деревьях березы повислой с разной степенью проявления узорчатости в структуре древесины в течение вегетационного сезона изучали активности кислых и основных пероксидаз во флоэмной и ксилемной частях камбиальной зоны. Для обеих форм березы повислой в тканях флоэмы активность пероксидазы была выше, чем в тканях ксилемы. Были выявлены отрицательные корреляции между активностью пероксидазы и интенсивностью камбиального роста. К июню, когда в стволовой части начинаются ростовые процессы, активность пероксидазы существенно снижалась по сравнению с маем, когда камбий еще неактивен. В конце июля продолжительные высокие температуры привели к существенному торможению камбиальной активности. При этом в ксилеме и во флоэме наблюдалось увеличение пероксидазной активности как для кислых, так и для основных форм фермента. Наличие высокой ферментативной активности обнаружено только в тканях ствола с узорчатым строением. У безузорчатых растений активность пероксидазы не изменялась. Обсуждаются возможные пути участия пероксидазы в процессах аномального морфогенеза древесных растений.
Карельская береза, пероксидазы, крахмал, пигменты
Короткий адрес: https://sciup.org/14750438
IDR: 14750438 | УДК: 581.1
Peroxidase activity in organs and tissues of silver birch trees
Silver birch trees with different degrees of manifestation of wood grain patterns were studied to reveal acid and alkaline peroxidase activity in the phloem and xylem parts of the cambial zone during the trees' growing season. Peroxidase activity in the phloem tissues of both types of silver birch was elevated in xylem tissues. Correlations between peroxidase activity and intensity of the cambial growth were negative. In June, when growth processes commenced in the trunk, peroxidase activity dropped significantly when compared to data obtained in May. At this time, cambium was not yet active. Later in July, a prolonged high temperature period resulted in substantial inhibition of cambial activity. Peroxidase activity in both acid and alkaline forms of the enzymes rose during this period both in xylem and in phloem tissues. High enzyme activity was found only in tissues of curly-grained trunks. Peroxidase activity in straight-grained plants did not change. Possible pathways of peroxidase involvement in the processes of abnormal morphogeny of woody plants are discussed.
Текст научной статьи Активность пероксидазы в органах и тканях деревьев березы повислой
Пероксидаза (1.11.1.7) – функционально очень лабильный фермент, способный выполнять многообразные функции в живых организмах. Основной функцией пероксидазы, наряду с супе-роксиддисмутазой и каталазой, является защита организма от вредного воздействия перекиси водорода и других активных форм кислорода, образующихся при окислительном стрессе [2], [24], [30]. Другой важной функцией этого фермента является непосредственное участие в процессах дифференциации тканей и органов высших наземных растений [17]. Поскольку субстратами пероксидазы могут быть фитогормоны (абсцизовая кислота, гибберелловая кислота, ауксин), фермент может регулировать состав физиологически активных веществ в тканях растения [14], [22].
Пероксидазе принадлежит ключевая роль в процессе лигнификации [3], [15], [16], [20], [21], который, в свою очередь, определяет некоторые различия между карельской березой ( Betula pendula var. carelica ) c аномальной узорчатой древесиной ствола и обычной березой повислой ( Betula pendula var. pendula ). Так, карельская береза отличается более высокой степенью жесткости структуры стенки ксилемных производных за счет увеличения лигнифика-ции [8].
У карельской березы при любом варианте скрещивания родительских форм в потомстве появляются особи как с узорчатой, так и без-узорчатой текстурой древесины. Для диагностики узорчатости в потомстве карельской березы был предложен метод определения активности пероксидазы лубяной ткани в одногодичных сеянцах в фазе глубокого покоя [13], но, несмотря на взаимосвязь данного фермента с ростовыми процессами в растительном организме и формированием аномальной структуры ствола, изучение активности пероксидазы в тканях и органах березы повислой ранее не проводилось. В связи с этим целью работы было изучить активность пероксидазы в тканях и органах у растений березы повислой с разной степенью узорчатости древесины.
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Объектами исследования были 41-43-летние деревья обычной березы повислой ( Betula pendula Roth var. pendula ) и карельской березы ( B. pendula var. carelica ). Все растения произрастали в одинаковых почвенно-климатических условиях на Агробиологической станции Карельского научного центра РАН в 2 км от Петрозаводска (61o45‘ с. ш., 34o20’ в. д.).
Отбор образцов вели в течение 2010-2011 годов: май - распускание листьев (активный ксилемный транспорт); июнь - интенсивный прирост ксилемы (активный флоэмный транспорт ассимилятов к камбиальной зоне и ксилеме); июль – период активного роста, формирование вторичной клеточной стенки, в связи с отсутствием дождей и высокими температурами в это время имело место преждевременное торможение камбиального роста [7]; февраль – период покоя (из-за отрицательных температур транспорт отсутствует).
Из ствола берез препарировали ткани флоэмы и ксилемы. На анализ брали по три растения каждой формы березы.
Растительный материал растирали с жидким азотом, затем для получения экстракта ткани ксилемы и флоэмы гомогенизировали при 4 оС в буфере следующего состава: 50 мМ Hepes (pH = 7,5), 1 мМ ЭДТА, 1 мМ ЭГТА, 3 мМ DTT, 5 мМ MgCl2, 0,5 мМ PMS, экстрагировали 20 минут при 4 оС и центрифугировали при 10 000 g в течение 20 минут (центрифуга Sigma 2-16PK, Германия). Осадок троекратно промывали буфером. Осадок и объединенный супернатант диализовали при 4 оС в течение 18–20 часов против буфера для гомогенизации, разбавленного в 10 раз. Активность пероксидазы определяли в полученных после диализа ферментативных препаратах.
В качестве донора водорода использовали бензидин и гваякол, в качестве субстрата - перекись водорода.
Для определения активности пероксидазы в реакции окисления бензидина использовали реакционную смесь следующего состава: 50 мМ K, Na-фосфатный буфер (рН = 7,8), 2,5– 5 мМ перекись водорода и 34 мкМ бензидина. О ферментативной активности пероксидазы судили по интенсивности уменьшения оптической плотности в области поглощения бензидина (λ = 282 нм) и выражали ее таким образом: израсходовано мкмоль бензидина / г сырой ткани за минуту.
Состав реакционной смеси для определения активности пероксидазы в реакции окисления гваякола был следующий: 50 мМ K, Na-фосфатный буфер (рН = 5), 2,5-5 мМ перекиси водорода, 21,5 мМ гваякола. Ферментативную активность пероксидазы определяли по скорости образования продукта реакции тетрагваякола (с учетом коэффициента экстинкции ε470нм = 0,0266 мкМ-1см-1) и выражали следующим образом: образовалось мкмоль тетрагваякола / г сырой ткани за минуту.
Изменения электронных спектров поглощения реакционной смеси, содержащей ферментативный препарат из тканей ксилемы карельской березы, перекись водорода и гваякол (21,5 mM) или бензидин (33,6 мкМ), приведены в работе [1].
В листьях определяли содержание хлорофиллов и каротиноидов. Для этого замороженные высечки листьев растирали на холоде в 80 % ацетоне. Содержание хлорофиллов a и b и сумму каротиноидов определяли спектрофотометрически (спектрофотометр СФ 2000, Россия) в ацетоновой вытяжке при длинах волн 663 и 646 нм (хлорофиллы) и 470 нм (каротиноиды) [5]. Долю хлорофиллов в светособирающем комплексе (ССК) рассчитывали исходя из того, что весь Хл b находится в ССК, а соотношение хлорофиллов а / b в этом комплексе составляет 1,2 [27].
Крахмал из листьев и тканей извлекали хлорной кислотой [29], его содержание определяли по количеству образованной в результате кислотного гидролиза глюкозы глюкозооксидаз-ным методом.
Данные на графиках представляют средние арифметические значения, полученные из трех биологических и четырех аналитических повторностей опыта.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Активность пероксидазы в тканях ствола деревь ев березы повислой
Индивидуальные пероксидазы различаются по субстратной специфичности, что связано с изменением заряда и конфигурации фермента и субстрата при разных значениях рН [6]. Инкубационная среда в реакции окисления гваякола по значению рН ближе к рН-оптимуму для ва-куолярных пероксидаз и пероксидаз клеточных стенок, в то время как в реакции окисления бензидина условия соответствуют рН-оптимуму цитоплазматических пероксидаз.
В мае во флоэме у растений обычной березы повислой были обнаружены высокие активности пероксидазы как в реакции окисления гваякола, так и бензидина. В тканях ксилемы в этот период активности пероксидаз не определялись совсем (рис. 1). Причиной высокой активности пероксидазы может быть повышение субстратов, в том числе соединений фенольной природы. В мае во флоэме активируется гидролиз полимерных компонентов, в результате мобилизации запасных веществ образуется большое количество сахаров, основная масса которых со ксилемным соком поднимается к главным акцепторам асси-милятов – распускающимся листьям, но часть сахаров используется в клетке на метаболические нужды, в том числе на образование фенольных соединений.
В июне – июле интенсивно фотосинтезирующие листья являются донорами ассимилятов, а основным местом потребления метаболитов становится камбиальная зона и формирующиеся клетки ксилемы и флоэмы. В этот период у растений березы повислой в ксилеме обнаружена самая высокая активность сахарозосинтазы [7], благодаря которой сахароза интенсивно оттекает из флоэмы в камбиальную зону, где в результате ее метаболизации по сахарозосинтазному пути появляется большое количество УДФ-глю-козы, идущей на синтез компонентов клеточных стенок ксилемы. При этом в июне во флоэме происходило снижение активности гваяколовой и бензидиновой пероксидазы, в то время как в ксилеме эти пероксидазы начинали проявлять незначительную активность (рис. 1а, б).
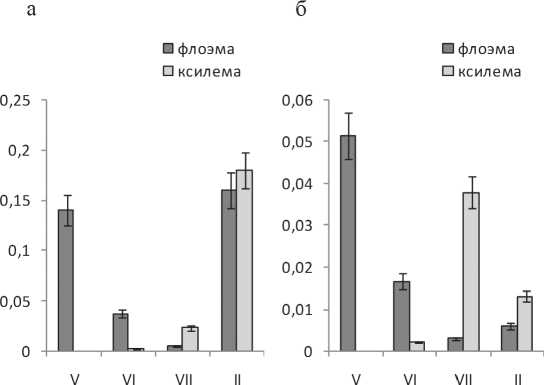
Рис. 1. Активность пероксидазы в тканях ствола растений B. pendula var. pendula в реакции окисления гваякола (а) и бензидина (б). По оси абсцисс – время взятия образцов (месяц), по оси ординат – активность фермента: а – мкмоль образовавшегося тетрагваякола на 1 г сырой ткани за минуту, б – мкмоль израсходованного бензидина на 1 г сырой ткани за минуту
Середина и конец июля в нашем исследовании – это период торможения деятельности камбия, вызванного погодными условиями. Так, отсутствие дождей в течение июля и высокие температуры привели к преждевременному торможению камбиального роста и снижению активности сахарозосинтазы в ксилеме [7].
В этот период у обычной березы повислой во флоэме происходило дальнейшее снижение активности пероксидазы, в то время как в ксилеме ее активность возрастала, особенно в реакции окисления бензидина. Так, активность бензидиновой пероксидазы в ксилеме в июле была самой высокой за весь сезон (рис. 1б). В феврале растения находились в состоянии вынужденного покоя, то есть все изменения в метаболических процессах были обусловлены в первую очередь влиянием внешних факторов, таких как свет и температура. Как во флоэме, так и в ксилеме в этот период активности пероксидаз в реакции окисления бензидина были невысоки (рис. 1б), в то время как активность гваяколовых пероксидаз в тканях ствола была довольно высокой (рис. 1б). Вероятно, у обычной березы повислой в период вынужденного покоя пероксидазы клеточных стенок и вакуолярные пероксидазы, в отличие от цитоплазматических, принимают активное участие в метаболических процессах.
Таким образом, получено, что активность пероксидазы находится в обратной корреляции с ростовыми процессами.
У растений карельской березы активности пероксидаз как в реакции окисления гваякола (рис. 2а), так и в реакции бензидина (рис. 2б) были примерно в 10 раз выше по сравнению с обычной березой повислой. Высокая активность пероксидазы может быть причиной увеличения у карельской березы жесткости структуры клеточной стенки по сравнению с обычной березой, как было показано нами ранее [8].
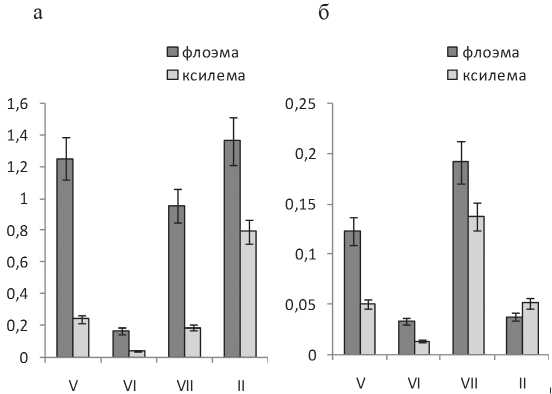
Рис. 2. Активность пероксидазы в тканях ствола растений B. pendula var. carelica в реакции окисления гваякола (а) и бензидина (б). Обозначения, как на рис. 1
Именно пероксидаза участвует в укреплении клеточной стенки растений путем катализа полимеризации фенольных соединений с образованием лигнина и суберина [19], [23], [25], [31] и их кросс-связывания с такими структурными белками, как экстенсин [18] и гидроксипролин-богатые белки [28].
Еще одна отличительная особенность карельской березы – это существенное возрастание в июле в тканях флоэмы активности всех форм пероксидаз (рис. 2а, б). Повышение пероксидазной активности при торможении камбиального роста у узорчатых растений может быть связано с возрастанием утилизации сахарозы на синтез соединений фенольной природы.
Тот факт, что у обычной березы повислой не происходило возрастания пероксидазной активности в период снижения камбиального роста во флоэме, может свидетельствовать о включении у нее избытка сахаров в другие метаболические процессы. Известно, что хорошим индикатором изменения условий среды является крахмал [11], который может временно депонироваться в растении при избытке метаболитов. Крахмал накапливается в виде слоистых зерен различного размера, и поскольку зерна не могут передвигаться из клетки в клетку, то крахмал обнаруживается именно там, где он синтезируется [10].
В мае – июне в тканях ствола у двух форм березы повислой не обнаруживалось большого количества крахмала (рис. 3). При снижении камбиальной активности у 40-летних растений его количество возрастало у карельской березы во флоэме (рис. 3а), а у обычной березы – во флоэме и ксилеме (рис. 3). Особенно существенное увеличение содержания крахмала происходило во флоэме у обычной березы повислой, его значения достигали 50 мг/г (рис. 3).
а б
□ var. carelica □ var. carelica
□ var.pendula Dvar.pendula
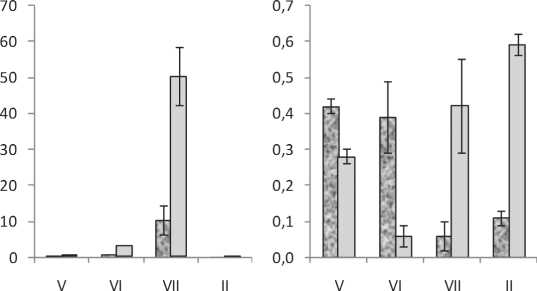
Рис. 3. Содержание крахмала (мг/г сухой ткани) во флоэме (а) и ксилеме (б) у растений березы повислой. По оси абсцисс – время взятия образцов (месяц)
Таким образом, временно образующийся во флоэме избыток метаболитов по причине торможения камбиального роста у обычной бере- зы повислой откладывается в виде крахмала, а у карельской березы, вероятно, идет синтез вторичных метаболитов, в котором пероксидаза принимает активное участие.
Динамика активности пероксидазы в листьях
У 40-летних деревьев березы повислой в июне в листьях, которые выступают в качестве донора вновь синтезированных органических веществ, активность пероксидазы (рис. 4) была значительно ниже, чем в тканях флоэмы и ксилемы (рис. 1а, 2а) в этот период.
Длительное действие высоких температур в июле и отсутствие дождей, приведшее к временному снижению камбиальной активности, не могли не сказаться и на метаболическом статусе листьев. Так, активность фермента в листьях B. pendula var. pendula снизилась в семь раз, в то время как у B. pendula var. carelica активность пероксидазы почти не изменилась (рис. 4).
-
□ var. pendula
-
□ var. carelica
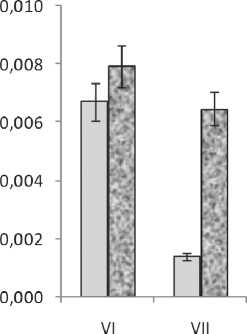
Рис. 4. Активность пероксидазы (образуется мкмоль тетрагваякола на 1 г сырой ткани за минуту) в листьях у растений березы повислой в период активного роста (VI – июнь, VII – июль)
Известно, что при действии неблагоприятных факторов [26], в том числе повышенной температуры [32], [33], в клетках растений развивается окислительный стресс, связанный с повышенной продукцией активных форм кислорода (АФК). Наряду с антиоксидантными ферментами, к которым относится пероксидаза, у растений к важным низкомолекулярным антиоксидантам относятся пигменты [12].
Изучение изменения содержания пигментов в листьях карельской березы показало, что длительное действие высоких температур приводило к снижению суммарного содержания хлорофиллов ( хл а + хл b ) (рис. 5а) и каротиноидов (рис. 5б) примерно в 1,5 раза. Следует отметить, что в листьях обычной березы повислой не происходило достоверных изменений в количестве фотосинтезирующих пигментов (рис. 5а, б).
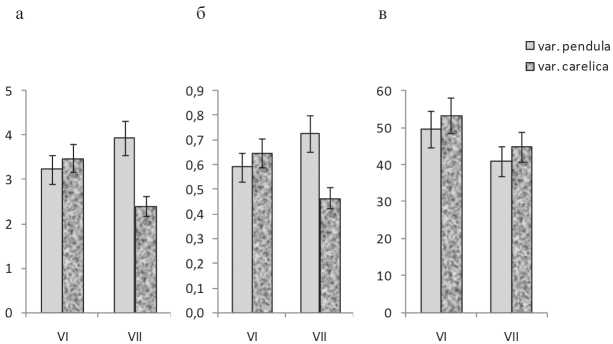
Рис. 5. Содержание хлорофиллов ( хл а + хл b ) (а), каротиноидов (б) (мг/г сухой ткани) и количество пигментов в светособирающем комплексе (%) (в) в листьях растений березы повислой в период активного роста (VI – июнь, VII – июль)
Устойчивость фотосинтетического аппарата растений формируется за счет изменения концентрации и перераспределения зеленых и желтых пигментов в ССК [4]. У обеих форм растений березы повислой к июлю наблюдалось снижение количества хлорофиллов примерно в 1,2 раза по сравнению с июнем в составе ССК (рис. 5в), что в условиях повышенных температур можно рассматривать как адаптивную реакцию, позволяющую избежать фотоингибирования путем уменьшения количества поглощаемого света [9].
Подводя итог, можно заключить, что в ответ на длительное влияние высоких температур на фоне отсутствия дождей, приведшее к торможению камбиального роста ствола, у двух форм березы повислой в листовом аппарате происходили разные изменения. У обычной березы повислой снижение доли хлорофиллов в ССК сопровождалось возрастанием суммы хлорофиллов и содержания каратиноидов при существенном снижении активности пероксидазы. У карельской березы снижение доли хлорофиллов в ССК, наоборот, происходило на фоне снижения содержания пигментов, при этом активность пероксидазы почти не изменялась.
Таким образом, в результате проведенного исследования было установлено, что в аномальных по строению тканях ствола карельской березы активность пероксидазы значительно превосходит таковую в тканях обычной березы повислой. Наблюдаемые изменения активности фермента на разных фазах развития указывают на его активное участие в метаболических процессах и свидетельствуют о перспективности выбранного направления исследований. Настоящую работу можно рассматривать как первое приближение к пониманию функциональной роли пероксидазы в процессах, предшествующих и сопровождающих нарушение морфогенеза у древесных растений.
Список литературы Активность пероксидазы в органах и тканях деревьев березы повислой
- Андреев В. П., Соболев П. С., Зайцев Д. О., Галибина Н. А., Зыкина Н. С., Плясунова Л. Ю., Романова М. И. Взаимодействие цинк-тетрафенилпорфина, бромистого пропаргила и пероксидазы хрена с анилинами//Ученые записки Петрозаводского государственного университета. Сер. «Естественные и технические науки». 2011. № 6 (119). C. 7-15.
- Андреев И. М. Функции вакуоли в клетках высших растений//Физиология растений. 2001. Т. 48. С. 777-778.
- Андреева В. А. Фермент пероксидаза: участие в защитном механизме растений. М.: Наука, 1988. 129 с.
- Бухов Н.Г. Динамическая световая регуляция фотосинтеза//Физиология растений. 2004. Т. 51. С. 825-837.
- Гавриленко В. Ф., Жигалова Т. В. Большой практикум по фотосинтезу. М.: Издательский центр «Академия», 2003. 256 с.
- Газарян И. Г., Хушпульян Д. М., Тишков В. И. Особенности структуры и механизма действия пероксидазы растений//Успехи биологической химии. 2006. Т. 46. С. 303-322.
- Галибина Н. А., Красавина М. С., Новицкая Л. Л., Софронова И. Н. Ферменты метаболизации сахарозы при формировании аномалий карельской березы//Структурные и функциональные отклонения от нормального роста и развития растений под воздействием факторов среды: Материалы междунар. конф. Петрозаводск: Карельский научный центра РАН, 2011. С. 79-84.
- Галибина Н. А., Теребова Е. Н. Свойства клеточных оболочек тканей ствола Betula pendula Roth//Дендроэкология и лесоведение: Материалы всероссийской конф. Красноярск: Институт леса им. В. Н. Сукачева СО РАН, 2007. С. 32-35.
- Дымова О. В., Гриб И., Головко Т. К., Стржалка К. Состояние пигментного аппарата зимне-и летнезеленых листьев теневыносливого растения Ajuga reptans//Физиология растений. 2010. Т. 57. С. 809-818.
- Кретович В. Л. Биохимия растений. М.: Высш. шк., 1986. 503 с.
- Новицкая Ю. Е. Особенности физиолого-биохимических процессов в хвое и побегах ели в условиях Севера. Л.: Наука, 1985. 116 с.
- Полесская О. Г., Каширина Е. И., Алехина Н. Д. Изменение активности антиоксидантных ферментов в листьях и корнях пшеницы в зависимости от формы и дозы азота в среде//Физиология растений. 2004. Т. 51. С. 686-691.
- Попов В. К., Авраменко Р С., Филоненко Е. В. Способ диагностики узорчатой древесины карельской березы//Описание изобретения к патенту Российской Федерации. 1996. № 2063679.
- Рогожин В. В. Пероксидаза как компонент антиоксидантной системы живых организмов. СПб.: ГИОРД, 2004. 240 с.
- Черепанова Е. А. Хитин-специфичные пероксидазы растений: Дис.. канд. биол. наук. Уфа, 2005. 275 с.
- Шарова Е. И. Клеточная стенка растений. СПб.: Изд-во СПбГУ, 2004. 156 с.
- Borсhert R. Time course and spatial distribution of phenylalanine ammonia lyase and peroxidase activity in wounded potato tuber tissue//Plant Physiol. 1978. Vol. 62. P. 789-793.
- Brownleader M. D., Hopkins J., Mobasheri A. et al. Role of extension peroxidase in tomato (Lycopercicon esculentum Mill.) seedling growth//Planta. 2002. Vol. 210. P. 668-676.
- Dehon L., Macheix J. J., Durand M. Involvement of peroxidases in the formation of the brown coloration of heartwood in Juglans nigra//Journal of Experimental Botany. 2002. Vol. 53. P. 303-311.
- Donaldson L. A. Lignification and lignin topochemistry -an ultrastructural view//Phytochem. 2001. Vol. 57. P. 859-873.
- Fry S. C. Phenolic components of the primary cell wall and their possible role in the hormonal regulation of growth//Planta. 1979. Vol. 146. P. 343-351.
- Gove J. P., Hoyle M. C. The isozymic similarity of indoleacetic acid oxidase to peroxidase in bich and horseradish//Plant Physiol. 1975. Vol. 56. P. 684-687.
- Hawkins S., Boudet A. Defense lignin and hydroxycinnamyl alcohol dehydrogenase activities in wounded Eucalyptus gunnii//Forest Path. 2003. Vol. 33. P. 91-104.
- Jansen M. A. K., Van den Noort R. E., Tan M. Y. et al. Phenol-oxidizing peroxidases contribute to the protection of plants from ultraviolet radiation stress//Plant Physiol. 2001. Vol. 126. P. 1012-1023.
- Kawano T. Roles of the reactive oxygen species-generating peroxidase reactions in plant defense and growth induction//Plant Cell Rep. 2003. Vol. 21. P. 829-837.
- Kuzniak E. Transgenic plants: an insight into oxidative stress tolerance mechanisms//Acta physiol. Plant. 2002. Vol. 24. P. 97-113.
- Lichtenthaler H. K. Vegetation stress: an introduction to the stress concept in plants//J. Plant Physiol. 1996. Vol. 148. P. 4-14.
- McDougall G. J. Cell-wall proteins from Sitka spruce xylem are selectively insolubilised during formation of dehydrogenation polymers of coniferyl alcohol//Phytochem. 2001. Vol. 57. P. 157-163.
- Pucher G. W., Leavenworth C. S., Vickery H. B. Determination of starch in plant tissues//Analyt. Chem. 1948. Vol. 20. P. 850-853.
- Rizhsky L., Hallak-Herr E., Van Breusegem F. et al. Double antisence plants lacking ascorbate peroxidase and catalase are less sensitive to oxidative stress than single antisense plants lacking ascorbate peroxidase or catalase//Plant J. 2002. Vol. 32. P. 329-342.
- Wallace G., Fry S. C. Action of diverse peroxidases and laccases on six wall-related phenolic compounds//Phytochemistry. 1999. Vol. 52. P. 769-773.
- Zang J., Kirkham M. B. Drought-stress induced changes in activities of superoxide dismutase, catalase and peroxidase in wheat species//Plant cell physiol. 1994. Vol. 35. P. 785-791.
- Zhang J., Kirkham M. B. Enzymatic Responses of the Ascorbate-Glutathione Cycle to Drought in Sorghum and Sunflower Plants//Plant Sci. 1996. Vol. 113. P. 139-147.


