Активность системы липопероксидации на фоне применения комплекса реабилитации у спортсменов с патологией суставов нижних конечностей
Автор: Манаева Надежда Ивановна, Сумная Дина Борисовна, Кинзерский Антон Александрович, Садова Валентина Алексеевна, Титухов Ренат Юрьевич, Гурова Наталья Евгеньевна
Журнал: Человек. Спорт. Медицина @hsm-susu
Рубрика: Восстановительная и спортивная медицина
Статья в выпуске: 3 т.22, 2022 года.
Бесплатный доступ
Цель: изучить состояние процессов липидной пероксидации и определить клинико-биохимические маркеры патологии суставов нижних конечностей для составления программы и оценки эффективности реабилитации пациентов. Материалы и методы. На базе клиники профессора Кинзерского, ООО «CNS», ООО «СОНАР», кафедры спортивной медицины и физической реабилитации, кафедры биохимии и НИИ олимпийского спорта «УралГУФК» проходили курс реабилитации 74 спортсмена, из них 22 с острой стадией болезни Осгуда - Шлаттера (БОШ). У всех спортсменов исследовалось в сыворотке крови содержание витамина Д, АСТ, АЛТ, СРБ и ревматоидный фактор, содержание продуктов перекисного окисления липидов (ПОЛ) и Fe2+-аскорбат-индуцированное ПОЛ, всем назначался курс плазмотерапии по технологии PRP, кинезиотейпирование, инструментальная мобилизация мягких тканей, динамическая нейромышечная стабилизация. Результаты. Биохимические исследования показали наличие у спортсменов с БОШ дефицит витамина Д, меди, ионизированного кальция (при нормальных показателях общего кальция), фосфора, цинка, повышение уровня щелочной фосфатазы при нормальных показателях АсАТ и АлАТ, СРБ и ревматоидного фактора. До реабилитации было выявлено (p function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Патология суставов нижних конечностей у спортсменов, болезнь осгуда -шлаттера, хондропатия бугристости большеберцовой кости, реабилитация, липопероксидация
Короткий адрес: https://sciup.org/147239591
IDR: 147239591 | УДК: 616.72-007.248-577.125 | DOI: 10.14529/hsm220321
The lipid peroxidation system during rehabilitation in athletes with lower joint pathology
Aim. The paper aims to identify the status of lipid peroxidation processes and the clinical, biological and chemical markers of lower joint pathology to develop rehabilitation interventions and their assessment procedures. Materials and methods. Our rehabilitation course involved 74 athletes, including 22 athletes with acute Osgood-Schlatter disease (OSD). Rehabilitation services were provided at Professor Kinzerskiy Clinic, CNS, SONAR, the Department of Sports Medicine and Physical Rehabilitation, the Department of Biochemistry, and the Scientific and Research Institute of Olympic Sports (Ural State University of Physical Education). Blood samples were analyzed for vitamin D, AST, ALT, CRP, rheumatoid factor, lipid peroxidation products (LPP), Fe2+/ascorbate induced peroxidation products. The rehabilitation program consisted of PRP plasma therapy, kinesio taping, instrument-assisted soft tissue mobilization, and dynamic neuromuscular stabilization. Results. Blood biochemistry showed that athletes with OSD had decreased levels of vitamin D, copper, ionized calcium (against normal levels of total calcium), phosphorus, and zinc; increased levels of AP; normal levels of AST, ALT, CRP and rheumatoid factor. Before rehabilitation, increased levels of primary and secondary LPP were found with spectrophotometry compared to the control group (1.22 ± 0.061 and 1.15 ± 0.058 respectively, p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Активность системы липопероксидации на фоне применения комплекса реабилитации у спортсменов с патологией суставов нижних конечностей
N.I. Manaeva, ,
D.B. Sumnaya, ,
A.A. Kinzersky, ,
V.A. Sadova, ,
R.Yu. Titukhov, ,
N.E. Gurova, ,
Введение. Болезнь Осгуда – Шлаттера встречается у 12,9 % подростков, активно занимающихся спортом [5, 6]. В 2019 году Guld-hammer S. et al., опубликовали результаты наблюдения за пациентами, которые 4 года назад имели в анамнезе картину БОШ. Участники сообщили о продолжительности симптома OSD в течение 90 месяцев, причем 42,9 % сообщили о ежедневной боли в колене [3]. Несвоевременная диагностика БОШ и отсутст- 174
вие адекватного лечения помимо образования несросшихся костных фрагментов деформаций бугристости большеберцовой кости приводят к остеоартрозу коленного сустава у лиц молодого возраста [10]. При болезни Осгуда – Шлаттера (хондропатии бугристости большеберцовой кости) мы имеем дело с асептическим неспецифическим воспалением, где в первую очередь происходят изменения на клеточном уровне гомеостаза [4, 7]. Так, пер- вой реагирует система перекисного окисления липидов [2]. Клиницисты используют ультразвуковые данные для отслеживания течения данной патологии [14, 17]. Среди них могут быть тендопатия собственной связки наколенника, ее утолщение, утолщение сухожилий четырехглавой мышцы бедра, реактивный бурсит, отек хряща и неоваскуляризация в области бугристости [8, 16]. Все эти изменения появляются в моменте, когда уже идет активный воспалительный процесс [19]. На рентгенограмме коленного сустава может быть костная неровность с фрагментацией на большеберцовом бугорке, кортизированный костный фрагмент, превосходящий бугристость большеберцовой кости. В месте введения сухожилия надколенника также может наблюдаться умеренный отек мягких тканей, но выпота из сустава нет [1, 15]. МРТ в сагиттальной плоскости у пациентов с БОШ может выявить увеличение дистальных аспектов сухожилия надколенника, очаги гетеротопического окостенения с низкой интенсивностью сигнала и неравномерность или увеличение бугристости большеберцовой кости [2, 9]. Изменения на рентгенограммах и МРТ обнаруживаются также на поздних стадиях, когда уже происходят необратимые изменения в тканях [12, 18]. Отсутствие единой точки зрения на этиологию и патогенез этой болезни обуславливает применение подчас нерациональных методов лечения, нередко с невысокой эффективностью, что требует совершенствования методов реабилитации [18]. БОШ – это преимущественно самоограничивающийся апофизит большеберцового бугорка и прилежащего сухожилия надколенника у молодых активных пациентов с открытыми зонами роста. Профилактические стратегии включают растяжение четырехглавой мышцы и подколенного сухожилия и поэтому должны быть реализованы в повседневной практике для детей, которые регулярно занимаются спортом. В лечении и реабилитации широко используются различные медикаменты (противовоспалительная терапия), массаж, ЛФК и кинезиотейпирование [11]. Также описано применение инъекций аутоплазмы, обогащенной тромбоцитарной массой (АПОТМ) в область поражения [13]. Для спортсменов вопрос о необходимости сокращения сроков лечения и возвращения к тренировкам наиболее актуален, что заставляет клинициста по- стоянно искать новые, более эффективные методики реабилитации [12].
Материалы и методы исследования. На базе учебного центра Клиники профессора Кинзерского и ООО «Центр нейромышечной стабилизации», кафедры спортивной медицины и физической реабилитации, кафедры биохимии и НИИ олимпийского спорта ФГБОУ ВО «Уральский государственный университет физической культуры» проходили курс обследования и реабилитации 74 спортсмена, из них 22 с острой стадией болезни Осгуда – Шлаттера (БОШ). Исследование проводилось до и на 3-й неделе от начала реабилитации.
Критерии включения в исследование:
-
1) возраст спортсменов 11–19 лет;
-
2) отсутствие клинико-лабораторных маркеров острого инфекционного процесса, аутовоспалительного состояния и обострения хронических заболеваний;
-
3) подтвержденный диагноз хондропатии бугристости большеберцовой кости;
-
4) добровольное согласие пациента (его представителей);
-
5) отсутствие противопоказаний для применения различных методов реабилитации.
Критерии исключения:
-
1) спортсмены с установленным диагнозом «остеоартроз коленных суставов»;
-
2) неактивная стадия бош по клиникоинструментальным данным;
-
3) низкая комплаентность участника.
Всем спортсменам данной группы (n = 22) назначался курс плазмотерапии по технологии PRP Cortexil, классическое кинезиотейпи-рование комбинированным способом, ИММТ обеих нижних конечностей, после купирования острого болевого синдрома проводилась динамическая нейромышечная стабилизация (DNS). Кроме того, спортсменам назначался комплекс препаратов магния, витамина Д3, омеги-3, который составлялся индивидуально в зависимости от показателей, полученных в результате биохимического исследования.
Группа контроля (здоровые спортсмены) – 18 человек идентичного возраста.
Методы исследования. Спортсмены были осмотрены ревматологом и ортопедом, проведена дифференциальная диагностика (клиническая, лабораторная, инструментальная) хондропатии с другими аутоимунными, аутовоспалительными и инфекционными заболеваниями опорно-двигательного аппарата.
Пациентам проводились:
-
1) УЗИ коленных суставов с эластомет-рией на аппарате экспертного уровня Samsung Xario 2000. Рентгенография коленных суставов, МРТ;
-
2) лабораторное исследование осуществлялось в сети клиник ИНВИТРО, клинике Южно-Уральского государственного медицинского университета: общеклиническое исследование крови, СОЭ, СРБ, ревматидный фактор, АЦЦП, АМЦВ, креатинин, мочевина, АсАт, АлАт, общий и ионизированный кальций, фосфор, электролиты, билирубин и его фракции, общий белок и его фракции, коагулограмма, витамины группы В, витамин Д, магний. В сыворотке крови исследовалось содержание первичных, вторичных и конечных продуктов липопероксидации и Fe2+-аскорбат-индуцированное ПОЛ спектрофотометрическим методом;
-
3) гониометрия, тестирование по шкале оценки качества жизни SF 36, визуальная оценка боли по шкале ВАШ.
После суммации всех данных составлялся план реабилитации конкретного спортсмена: медикаментозное лечение (противовоспалительная терапия), кинезиотейпирование, фасциальные манипуляции, проведение инъекции обогащенной аутоплазмы в область поражения под ультразвуковым контролем, лечебная физкультура. Введение обогащенной тромбоцитами аутоплазмы по технологии Cortexil проводилось периартикулярно, курс из 3 инъекций 1 раз в 7 дней. Над областью поражения накладывались кинезиотейпы лимфодре- нажной и поддерживающей техникой для улучшения микроциркуляции и лимфотока. Совмещение этих двух техник позволило отменить применение НПВП для купирования болевого синдрома в связи с его отсутствием на фоне выраженного лимфодренажного и обезболивающего эффекта кинезиотейпирования.
Результаты исследований и их обсуждение. До начала реабилитации показатель шкалы боли по ВАШ был в среднем 7 ± 1,25, что соответствовало выраженной боли. Спортсмены клинически отмечали достоверное уменьшение болевого синдрома в среднем на 3 ± 0,5 сут (p < 0,05) от начала реабилитации. Через неделю от первого реабилитационного комплекса уровень ВАШ достоверно снизился и был 2 ± 0,25 (p < 0,05). При оценке данного показателя через месяц от первого посещения достоверно купирован болевой синдром (p < 0,05) в области коленного сустава (ВАШ = 0). При проведении гониометрии у пациентов с БОШ было выявлено, что среднее значение угла сгибания в коленных суставах составляло 90 ± 5,25°. Угол сгибания в коленных суставах достоверно увеличился в динамике через 4 недели от первичного осмотра в среднем на 10 ± 2,5° и составил 105 ± 4,5° (p < 0,05), против 110° группы контроля.
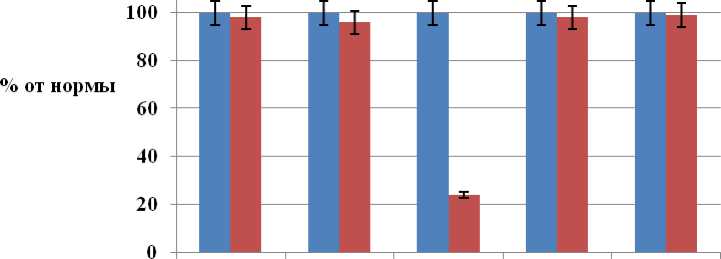
Биохимические исследования показали (рис. 1) наличие у спортсменов с БОШ дефицит витамина Д, меди, магния, ионизированного кальция (при нормальных показателях общего кальция), фосфора, цинка, повышение уровня щелочной фосфатазы при нормальных показателях АсАТ и АлАТ. Дефицит витами-
ACT А.ТГ Витамин Д РФ СРВ
Рис. 1. Наиболее значимые биохимические показатели в сыворотке крови в норме и у исследуемых пациентов с БОШ
Fig. 1. The most important serum biochemical parameters in healthy subjects and in patients with OSD
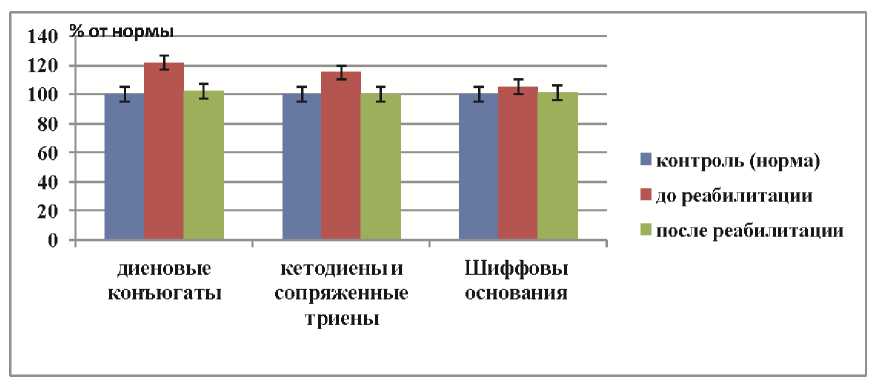
Рис. 2. Содержание в сыворотке крови первичных, вторичных и конечных продуктов перекисного окисления липидов до и после реабилитации
Fig. 2. Serum levels of primary, secondary and final products of lipid peroxidation before and after rehabilitation
■ контроль
■ группа с БОШ
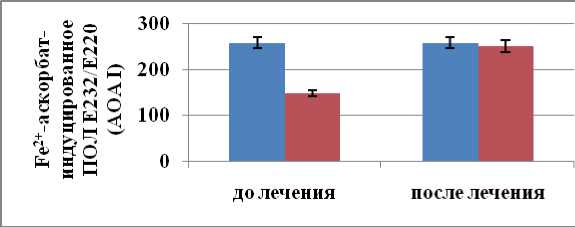
Рис. 3. Антиоксидантная активность сыворотки (АОАI) у спортсменов с БОШ на фоне реабилитации
Fig. 3. Serum antioxidant activity in athletes with OSD during rehabilitation на Д3 и магния был выявлен у всех обследованных спортсменов (74 человека).
Также произведена оценка содержания в сыворотке крови продуктов перекисного окисления липидов до и после восстановительного курса.
До реабилитации было выявлено (p < 0,05) спектрофотометрическим методом повышение содержания первичных и вторичных продуктов ПОЛ соответственно в 1,22 ± 0,061 и 1,15 ± 0,058 раза по сравнению с группой контроля. Эти изменения коррелировали (r = = –0,765–0,801) с ультразвуковыми и клиническими данными (выявлялась обратная зависимость: чем выше содержание продуктов ПОЛ в сыворотке крови, тем выраженнее болевой синдром, ограничение движений и вы-раженней отек и явления асептического воспаления по данным УЗИ в зоне пораженного сустава. После проведенной реабилитации через 3 недели от ее начала у пациентов с БОШ выявлялось значительное достоверное
(p < 0,05) снижение концентрации первичных, вторичных, конечных продуктов перекисного окисления липидов до показателей группы контроля (рис. 2). Данные изменения процессов липопероксидации происходили на фоне улучшения клинической картины в виде купирования болевого синдрома, увеличения объема движений и двигательной активности в целом.
Антиоксидантная активность сыворотки (рис. 3) у спортсменов с БОШ достоверно ниже нормы в 1,81 ± 0,091 раза (p < 0,05). После проведенной реабилитации антиоксидантная активность сыворотки возрастает в 1,7 ± 0,085 раза достоверно не отличается от группы контроля (p < 0,05). По данным сонографии, у спортсменов данной группы с БОШ уменьшались проявления заболевания в среднем на 5 ± 0,5 сут от первой инъекции аутоплазмы и полное купирование БОШ – к 4-й неделе от начала реабилитации. Причем использование кинезиотейпирования комбини- рованным методом отменяло применение НПВП в связи с отсутствием болевого синдрома. Все спортсмены данной группы вернулись к прежнему режиму тренировок в среднем через 18 ± 2,75 дня. Назначение спортсменам комплекса препаратов магния, витамина Д3, омеги-3, который составлялся индивидуально в зависимости от показателей, полученных в результате биохимического исследования, позволило восстановить дефицит данных веществ, что также важно для нормального функционирования опорно-двигательного аппарата.
Заключение. У спортсменов с БОШ наблюдается повышение активности системы перекисного окисления липидов. Данные изменения обнаруживаются на самой ранней стадии БОШ, что может применяться в качестве скрининга хондропатии у спортсменов, когда показатели активности воспалительного процесса (СОЭ, СРБ, ревматоидный фактор) еще не отличаются от нормы. В этот период уже имеются четкие признаки активности процесса на УЗИ, но они могут еще отсутствовать на рентгенографии.
Измерение содержания продуктов перекисного окисления липидов в сыворотке крови может быть использовано для оценки эффективности реабилитации при болезни Осгуда – Шлаттера. Эти изменения коррелируют с ультразвуковыми и клиническими данными. Во время интенсивного тренировочного процесса необходимо контролировать у спортсменов содержание витамина Д3 и магния, и своевременно проводить коррекцию дефицита. Дефицит витамина Д3 и магния был выявлен у всех обследованных спортсменов (74 человека).
Список литературы Активность системы липопероксидации на фоне применения комплекса реабилитации у спортсменов с патологией суставов нижних конечностей
- Бегун, П.И. Биомеханика опорно-двигательного аппарата человека: моногр. / П.И. Бегун, A.B. Самсонова. - СПб.: Кинетика, 2020. - 179 с. - (Биомеханика).
- Васильев, О.С. Методические рекомендации по практическому применению комплекса методик ранней диагностики, реабилитации, медико-биологическому сопровождению и профилактике состояний, связанных с «болезнями роста» у юных спортсменов: метод. рек. / под ред. проф. В.В. Уйба / О.С. Васильев. - М. : ФМБА России, 2019. - 78 с.
- Горбатенко, А.И. Использование обогащенной тромбоцитами аутоплазмы в консервативном лечении болезни Осгуда - Шлаттера у детей / А.И. Горбатенко // Вопросы практической педиатрии. - 2017. - Т. 12, № 3. - С. 66-71. - DOI: 10.20953/1817-7646-2017-3-66-71
- Горбатенко, А.И. Остеохондропатии у детей - поиск эффективных методов лечения / А.И. Горбатенко//Науч. мед. журнал «Морфология». - 2018. - № 3, Т. 153. - С. 78.
- Ермекова, М.А. Болезнь Осгуд - Шлаттера: возможности визуальной диагностики / М.А. Ермекова, М.Т. Алиякпаров, Т.И. Ромащенко // Караганд. гос. мед. университет. журн. «Медицинские новости». - 2017. - № 2. - С. 55-58.
- Кинзерский, А.Ю. Ультразвуковое исследование при травмах и заболеваниях коленного сустава: практ. рук. /А.Ю. Кинзерский. - Челябинск: Челяб. гос. мед. акад., 2010. - С. 26-29.
- Кумачный, А.Л. Способы и методы лечения болезни Осгуда - Шляттера с помощью оздоровительной физкультуры /А.Л. Кумачный, М.С. Москаленко, Ю.И. Шульгов // Символ науки. -2017. - № 6. - С. 113-116.
- Манаева, Н.И. Преимущества ультразвуковой диагностики для определения признаков хондропатии бугристости большеберцовой кости у детей на ранней стадии / Н.И. Манаева, Д.Б. Сумная, Р.Ю. Титухов //International Science Project. - 2020. - No. 35, Part 1. - P. 11.
- Сравнительная эффективность применения аутоплазмы и гиалуронатов у молодых пациентов при остеоартрите коленных суставов на фоне перенесенной хондропатии бугристости большеберцовой кости / Н.И. Манаева, Д.Б. Сумная, Е.В. Быков, Н.Е. Гурова // DIZZW 2020 (Germany). - 2021. - Vol. 1, no. 9. - Р. 26-30.
- Clinics in diagnostic imaging / F. Marino et al. // Radiol Med. - 2021. - Vol. 126 (8). -Р. 1085-1094.
- Gaschler, M.M. Lipid peroxidation in cell death / M.M. Gaschler, B.R. Stockwell // Biochem Biophys Res Commun. - 2017, Jan 15. - Vol. 482 (3). - P. 419-425.
- https://www.invitro.ru/analizes/for-doctors/2569/.
- Ladenhauf, H.N. Osgood-Schlatter disease: a 2020 update of a common knee condition in children / H.N. Ladenhauf, G. Seitlinger, D.W. Green // Singapore Med J. - 2019. - Vol. 60 (12). -P. 610-615. '
- Long-term Prognosis and Impact of Osgood-Schlatter Disease 4 Years After Diagnosis: A Retrospective Study / Clara Guldhammer, Michael Skovdal Rathleff, Hans Peter Jensen, Sinead Holden // Orthop J Sports Med. - 2019. - Vol. 7. - P. 12.
- Midtiby, S.L. Effectiveness of interventions ^ for treating apophysitis in children and adolescents: protocol for a systematic review and network meta-analysis / S.L. Midtiby, N. Wedderkopp, R.T. Larsen // Chiropr Man Therap. - 2018. - P. 26-41.
- Rathleff, M.S. Knee pain in children and adolescents /M.S. Rathleff, C.L. Straszek, L. Blond // Ugeskr Laeger. - 2019. - Vol. 25. - P. 181. ''
- Siddiq, M.A.B. Osgood-Schlatter Disease Unveiled Under High-frequency Ultrasonogram / M.A.B. Siddiq // Orthop J Sports Med. - 2018. - Oct 04. - P. 10.
- T2-mapping MRI evaluation of patellofemoral cartilage in patients submitted to intra-articular platelet-rich plasma (PRP) injections / F. Cobianchi Bellisari, L. De Marino, F. Arrigoni et al. // Radiol Med. - 2021. - Vol. 126 (8). - P. 1085-1094.
- Ultrasonography of the Osgood-Schlatter disease / K. Mahlfeld, R. Kayser, J. Franke, H. Merk // Ultraschall. Med. - 2001. - No. 22. - P. 182-185.


