Активность сукцинат- и лактатдегидрогеназы лимфоцитов, индуцированные АФК нейтрофилов и повреждение ДНК лейкоцитов в крови облучённых ионами углерода мышей
Автор: Хундерякова Н.В., Заичкина С.И., Дюкина А.Р., Митрошина И.Ю., Медведева В.П., Королева М.А., Кузнецова Е.А.
Рубрика: Научные статьи
Статья в выпуске: 4 т.32, 2023 года.
Бесплатный доступ
В настоящее время большое практическое значение представляют исследования, проводимые в целях совершенствования радиотерапии опухолей с применением ускоренных тяжёлых ионов, поскольку основную энергию они отдают в конце пробега в пике Брэгга, что увеличивает тяжесть радиационного поражения опухоли и позволяет минимизировать повреждение окружающих здоровых тканей. В данной работе определяли уровни активности лактатдегидрогеназы (ЛДГ) и сукцинатдегидрогеназы (СДГ) лимфоцитов, соотношение ЛДГ/СДГ, индуцированных активных форм кислорода (АФК) нейтрофилов и повреждений ДНК (%TDNA) лейкоцитов в крови через 1 сут после облучения мышей ускоренными ионами углерода с энергией 450 МэВ/нуклон в дозах 0,2-2 Гр в пике Брэгга. Обнаружили: активность СДГ увеличивалась при дозах 0,2-1 Гр и резко снижалась при дозе 1,5 Гр у всех мышей. При понижении активности СДГ у животных компенсаторно увеличивался гликолиз (активность ЛДГ), что, по-видимому, связано с развивающейся митохондриальной дисфункцией иммунных клеток. %TDNA лейкоцитов увеличивался в зависимости от дозы и сопровождался снижением функциональной активности нейтрофилов - уменьшалась зимозан-индуцированная продукция АФК. Таким образом, на фоне повышенного %TDNA и понижения активности СДГ большое значение приобретает гликолиз. Применённые методы являются высокочувствительными и могут быть использованы для выявления индивидуальных различий у животных, являющихся биологическими моделями в доклинических исследованиях.
Ускоренные ионы углерода, сукцинатдегидрогеназа, лактатдегидрогеназа, активные формы кислорода, повреждения днк
Короткий адрес: https://sciup.org/170201861
IDR: 170201861 | УДК: 591.111.1:577.346:599.323.4 | DOI: 10.21870/0131-3878-2023-32-4-123-133
Lymphocyte succinate and lactate dehydrogenase activity, induced ROS of neutrophils, and leukocyte DNA damage in the blood of mice irradiated with carbon ions
At the present time, the studies carried out to improve the radiotherapy of tumors using accelerated heavy ions are of great interest, since they give off the main energy at the end of the run at the Bragg peak, which increases the severity of radiation damage to the tumor and minimizes damage to surrounding healthy tissues. In this work, the levels of lymphocyte lactate dehydrogenase (LDH) and succinate dehydrogenase (SDH) activity, the ratio of LDH/SDH, induced reactive oxygen species (ROS) of neutrophils, and leukocytes DNA damage (%TDNA) in blood 1 day after accelerated carbon ions irradiation of mice with an energy of 450 MeV/nucleon in doses of 0.2-2 Gy in the Bragg peak were determined. Found: SDH activity increased at doses of 0.2-1 Gy and sharply decreased at a dose of 1.5 Gy in all mice. With a decrease in SDH activity, glycolysis (LDH activity) increased compensatory, which, apparently, is associated with the developing mitochondrial dysfunction of immune cells. The %TDNA of leukocytes increased depending on the dose and was accompanied by a decrease in the functional activity of neutrophils - the zymosan-induced ROS production decreased. Thus, against the background of an increased %TDNA and a decrease in SDH activity, glycolysis becomes of great importance. The applied methods are highly sensitive and can be used to detect individual differences in animals that are biological models in preclinical studies.
Текст научной статьи Активность сукцинат- и лактатдегидрогеназы лимфоцитов, индуцированные АФК нейтрофилов и повреждение ДНК лейкоцитов в крови облучённых ионами углерода мышей
В настоящее время большой интерес вызывает использование ускоренных тяжёлых ионов в радиотерапии опухолей. Клинические данные, полученные в специализированных центрах Японии и Германии при облучении онкологических пациентов ионами углерода, позволяют рассматривать этот вид излучения как перспективный, с благоприятными исходами и приемлемой токсичностью [1]. Изучение последствий воздействия ускоренных тяжёлых ионов на живые организмы актуально и в связи с планируемыми длительными космическими полётами. Космическое излучение может вызывать повреждения как прямым воздействием на молекулы ДНК, так и косвенно – через свободные радикалы. Известно, что в результате облучения тяжёлыми частицами в клетках увеличивается выход как свободных радикалов (например, активных форм кислорода и азота), так и генотоксичных молекулярных продуктов, таких как, например, H 2 O 2 [2-4]. Воздействие активных форм кислорода/азота (АФК/А) может приводить к различным повреждениям ДНК: разрывам цепей, повреждениям оснований и нуклеотидов [1, 4]. Известно также, что при облучении ускоренными ионами образуются сложные кластерные повреждения ДНК, которые трудно поддаются репарации или вовсе не репарируются. Кроме того, в результате воздействия
Хундерякова Н.В.* – ст. науч. сотр., к.б.н.; Заичкина С.И. – вед. науч. сотр., к.б.н.; Дюкина А.Р. – ст. науч. сотр., к.б.н.; Митрошина И.Ю. – науч. сотр., к.б.н.; Медведева В.П. – ст. лаборант; Королева М.А. – ст. лаборант; Кузнецова Е.А. – зав. лаб., к.б.н. ИТЭБ РАН.
ионизирующей радиации развивается дисфункция митохондрий и антиоксидантной системы клетки. Окислительные изменения могут продолжаться в течение нескольких дней и месяцев после первоначального воздействия, предположительно из-за непрерывного образования АФК/А [4]. Нами обнаружено длительное сохранение высокого уровня повреждений ДНК лейкоцитов к 75-м суткам после 12С-облучения мышей в пике Брэгга (6 Гр), что указывало на значительное повреждение клеток из разных клеточных пулов системы крови [5].
Повреждения ДНК являются биологическим индикатором таких процессов, как окислительный стресс, репарация ДНК и клеточная гибель. Уровни повреждений ДНК в лейкоцитах крови облучённых мышей в данной работе оценивали методом ДНК-комет. Щелочная версия этого метода позволяет выявить суммарный уровень повреждений ДНК: одно-, двунитевые разрывы и щелочелабильные (апуриновые/апиримидиновые) сайты [6]. Сохранение целостности ДНК в облучённой клетке часто ассоциировано с генерацией АФК. Несмотря на то, что мощным источником АФК в клетке являются митохондрии, их эффективное функционирование необходимо для обеспечения энергией репарационных процессов [4]. Исходя из этого, в представленной работе была проведена оценка активности ключевых ферментов дыхания митохондрий – сукцинатдегидрогеназы (СДГ) и гликолиза в цитозоле – лактатдегидрогеназы (ЛДГ), которые являются биомаркерами аэробного и анаэробного метаболизма в лимфоцитах крови [7, 8]. Поскольку сохранение нарушений окислительного метаболизма в пострадиационный период связано с хроническими воспалительными реакциями [4], то определяли также и уровень люминол-зависимой, зимозан-индуцированной продукции АФК в нейтрофилах. Используя животных в качестве биологических моделей, мы старались учитывать динамику индивидуальных изменений изучаемых показателей. В связи с этим, целью работы явилась оценка функционального состояния лейкоцитов крови по критериям: активности СДГ (митохондриального дыхания) и активности ЛДГ (гликолиза), соотношения ЛДГ/СДГ, индукции АФК в нейтрофилах и повреждений ДНК в лейкоцитах крови у индивидуальных мышей через 1 сут после их облучения (0,2-2 Гр) ускоренными ионами углерода с энергией 450 МэВ/нуклон в пике Брэгга.
Материалы и методы
Животные. Использовали белых беспородных мышей-самцов линии SHK в возрасте 8-9 недель, массой 30 ± 4 г. Животные содержались в стандартных условиях вивария Института теоретической и экспериментальной биофизики, Пущино (ИТЭБ РАН). Мышей содержали на 12-часовом свето-темновом режиме со свободным доступом к пище и воде. Мышей выводили из эксперимента декапитацией.
Облучение животных. В исследование было включено 29 мышей, разделённых на шесть групп в зависимости от дозы облучения (одна группа не облучена – контрольная). Мышей облучали ионами углерода в модифицированном (расширенном) пике Брэгга в дозах 0,2; 0,5; 1,0; 1,5 и 2,0 Гр (4-6 мышей в группе) на ускорительном комплексе У-70 (ИФВЭ НИЦ «Курчатовский институт», Протвино) в соответствии с [5]. Все биологические показатели лейкоцитов крови регистрировались через 1 сут после облучения всего тела животных.
Измерение активности СДГ и ЛДГ в лимфоцитах. Измерение активности дегидрогеназ по восстановлению нитросинего тетразолия (НСТ) проводили в свежеприготовленных мазках крови. Через 1-1,5 ч после забора крови мазки крови фиксировали 60% ацетоном, забуференным 10 мМ HEPES, в течение 30 с при комнатной температуре (рН 5,2-5,5), промывали и сушили. Эта мягкая фиксация ацетоном модулирует проницаемость мембраны иммобилизованных клеток для субстратов и никотинамидадениндинуклеотида (НАД). Фиксированный мазок инкубировали в течение 1 ч при 37 °С на водяной бане в среде, содержащей (в мМ/л) 125 KCl, 10 HEPES и 1,22 НСТ (рН 7,2±0,05). Во всех процедурах использовалась бидистиллированная вода. Добавление 5 мМ янтарной кислоты является основным тестом, характеризующим активность СДГ. Образец для оценки активности ЛДГ содержал 5 мМ молочной кислоты, 5 мМ малоновой кислоты и 0,5 мМ НАД. В цитобиохимических исследованиях восстановление НСТ на эндогенных субстратах снижается после добавления селективного ингибитора СДГ (малоновой кислоты); поэтому к образцу для измерения активности ЛДГ добавляли 5 мМ малоновой кислоты, чтобы исключить окисление микромолярных концентраций эндогенной янтарной кислоты. После инкубации мазки окрашивали 0,5% нейтральным красным в течение 8 мин. После окрашивания мазки исследовали под световым микроскопом (Leica DM2000 с цветной камерой Leica DFC425) при увеличении х1000 в условиях масляной иммерсии. Из каждого мазка отбирали по 50 лимфоцитов. Для поиска и захвата клеток использовалось программное обеспечение Bloodrunner. Для количественного морфологического анализа цветных изображений была разработана специальная программа Cell Composer, рассчитывали концентрацию продукта восстановления НСТ диформазана (в мкм2) в каждой клетке. Из-за большого размера выборки средние значения для каждого животного были статистически значимыми (p<0,001) во всех случаях. Результаты представлены отдельно для каждого животного в виде среднего значения в каждой пробе. Стандартное отклонение (SD) и ошибку среднего (M) рассчитывали на основании всей совокупности оценок количества диформазана.
Определение уровня зимозан-индуцированных АФК. Уровень продукции АФК в цельной крови измеряли методом люминол-зависимой зимозан-индуцированной хемилюминесценции (ХЛ) на 12-канальном приборе CHEMILUM-12 (Россия) по ранее описанной методике [9]. Измеряли уровень спонтанной ХЛ цельной крови, характеризующий базальный уровень активации нейтрофилов, а для определения резервных возможностей активации нейтрофилов проводили стимуляцию кислородного обмена с использованием опсонизированного зимозана. В качестве усилителя ХЛ использовали люминол. Опсонизированный зимозан использовали для индукции респираторного взрыва. Усиление ХЛ, индуцированное опсонизированным зимозаном, оценивали по отношению индуцированной ХЛ к спонтанной (Sind/spont), обозначаемому как индекс активации. Величины светлой площади под кривой определяли для спонтанной и индуцированной ХЛ (Sspont, Sind), а также индекс активации (AI) как отношение Sind/Sspont, характеризующий усиление ХЛ.
Метод ДНК-комет. Уровень повреждения ДНК в лейкоцитах мышей определяли щелочным вариантом метода в соответствии с [5]. Использовали стандартный фосфатно-солевой буфер (PBS), рН=7,2, содержащий 0,001 моль/л ЭДТА (PBS-EDTA). Вкратце, цельную кровь мышей разводили 1:5 PBS-EDTA и смешивали с равным объёмом 1% лекгоплавкой агарозы при 37 oC. Смесь наносили на стёкла, на которые был предварительно нанесён и высушен слой нормальной агарозы. После охлаждения и затвердевания слоя агарозы с клетками на его поверхность наносился новый слой 0,5% легкоплавкой агарозы. Стёкла помещали в лизирующий раствор (2,5 моль/л NaCl, 0,1 моль/л ЭДТА, 0,01 моль/л Трис-HCl, pH=10, 1% Triton X-100) при 4 oC на 20-24 ч. Затем стёкла переносили в щелочной раствор А (0,3 моль/л NaCl, 0,001 моль/л ЭДТА, pH>13) и инкубировали в течение 20 мин. Затем их помещали в электрофоретическую камеру и подвергали электрофорезу в течение 20 мин при 4 oC (напряжённость электрического поля 2 В/см). После электрофореза стёкла промывали дистиллированной водой и окрашивали в течение 1 ч PBS, содержащим 2,0 мкг/мл бромистого этидия. Препараты анализировали под флуоресцентным микроскопом ЛЮМАМ И-3 (ЛОМО, Санкт-Петербург). Уровень повреждений ДНК выражали в процентах ДНК в хвосте кометы (%TDNA) [6]. Базальный (контрольный) уровень повреждения ДНК в лейкоцитах крови определяли у необлучённых мышей. Для каждой экспериментальной единицы анализировали по три стекла.
Статистический анализ. Статистическую обработку данных проводили с помощью лицензионного программного обеспечения Microsoft Office Exсel 2007 и Statistica 10.0. Различие с использованием t-критерия Стьюдента (двупарный с неравным отклонением) считали статистически достоверным при значении р<0,05.
Результаты
Через 1 сут после облучения мышей в дозах 0,2-2 Гр изучали изменение активностей СДГ и ЛДГ в лимфоцитах, уровни АФК в нейтрофилах, а уровни повреждений ДНК – в лейкоцитах периферической крови одних и тех же животных. Для оценки энергетического состояния лимфоцитов были определены активности ключевого фермента митохондрий – СДГ и цитозольного фермента гликолиза – ЛДГ, а также соотношение ЛДГ/СДГ (рис. 1). Видно, что среднее значение активности СДГ увеличивалось в 3-5 раз в зависимости от дозы (0,2-1 Гр), в то же время внутри каждой группы животных при одной и той же дозе облучения активности СДГ и ЛДГ не были одинаковы (рис. 1а). Различия между мышами 1 и 3, 1 и 4, 5 и 9, 10 и 12, 10 и13, 10 и 14, 10 и 15, 16 и 17 статистически достоверны (p ≤ 0,05). При увеличении дозы до 1,5 Гр наблюдалось ингибирование активности СДГ во всей группе. При 2 Гр у одного животного (мышь № 22) активность СДГ увеличилась примерно в 5 раз по сравнению с контролем, а у трёх животных была снижена примерно до такого же уровня, как в группе при 1,5 Гр. На рис. 1б представлены дозовые зависимости отношения ЛДГ/СДГ у этих же мышей.
Соотношение ЛДГ/СДГ рассматривали в качестве показателя преобладания гликолиза над митохондриальным дыханием. Из рис. 1 видно, что у мышей, облучённых в дозе 1,5 Гр, резкое падение активности СДГ приводило к существенному увеличению значения ЛДГ/СДГ. Несмотря на то, что наблюдалось большое разнообразие ЛДГ/СДГ у индивидуумов при одной и той же дозе, у всех животных при уменьшении активности СДГ регистрировалось увеличение ЛДГ/СДГ.
На рис. 2 показан уровень продукции АФК в цельной крови животных при дозах 0,2-2 Гр. Видно, что индекс активации зимозан-индуцированной ХЛ нейтрофилов у всех животных снижался в зависимости от дозы.
На рис. 3 представлены %TDNA лейкоцитов у индивидуальных животных, облучённых в дозах 0,2-2 Гр.
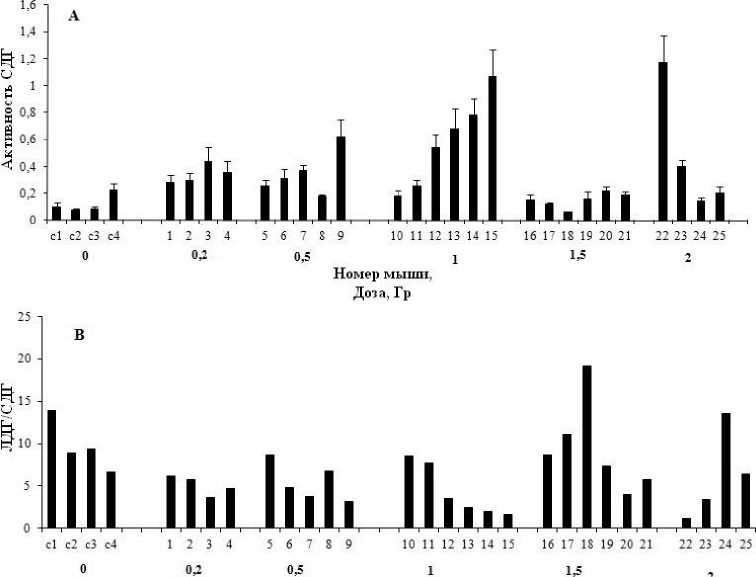
Номер мыши. Доза, Гр
Рис. 1. Зависимость активности СДГ (а) и отношения активностей ЛДГ/СДГ (б) в лимфоцитах крови мышей от дозы облучения ионами углерода в пике Брэгга.
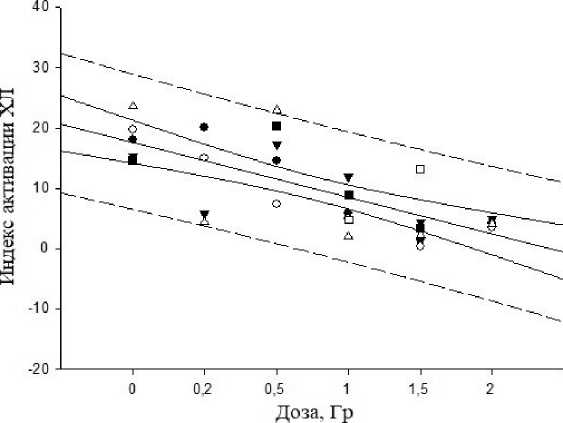
Рис. 2. Зависимость величины индекса активации хемилюминесценции в цельной крови индивидуальных животных от дозы облучения ионами углерода в пике Брэгга. Пунктирные линии – предсказательный интервал, чёрные линии – доверительный интервал (confidence intervals). Данные расположились линейно y=b 1 x+b 0 (коэффициент детерминации r=0,5) с коэффициентом угла наклона 3,05.
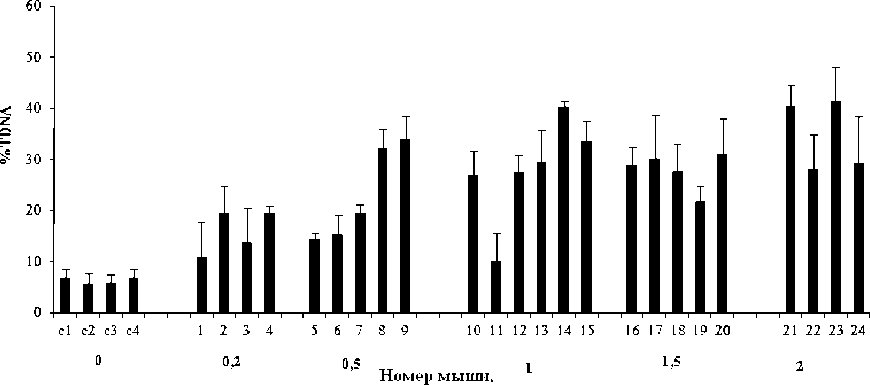
Доза. Гр
Рис. 3. Зависимость уровней повреждений ДНК (%TDNA) лейкоцитов крови у индивидуальных животных от дозы облучения ионами углерода в пике Брэгга (M ± SD).
Видно, что %TDNA увеличивался с ростом дозы, но у разных животных по-разному. Так, при дозе 0,5 Гр %TDNA у мышей № 8 и 9 (среднее значение %TDNA=32,9 ± 1,2%) достоверно отличался (p=0,01) от такового у мышей № 5, 6 и 7 (среднее значение %TDNA=16,4 ± 2,7%). При дозе 1 Гр у мышей № 10, 12-14 %TDNA достоверно отличался от такового у мыши № 11 (р<0,05). При дозах 1,5 и 2 Гр %TDNA оставался высоким. Достоверных отличий между индивидуумами при 1,5 Гр не наблюдалось, также их не было и при 2 Гр.
Обсуждение
Энергетическое обеспечение репарационных процессов в облучённых клетках осуществляется как за счёт работы митохондрий, так и гликолиза. Активность СДГ через 1 сут после облучения у индивидуумов увеличивалась в зависимости от дозы до 1 Гр и сопровождалась увеличением повреждений ДНК, что, по-видимому, свидетельствует об активной работе митохондрий и возросших потребностях клеток в энергозатратах при дозах 0,2-1 Гр. В этот срок, как было показано ранее, в клетках костного мозга 12С-облучённых мышей наблюдался высокий уровень экспрессии генов, вовлечённых в апоптоз и контроль клеточного цикла (BBC3, CDKN1A); при этом снижалось количество лейкоцитов в крови [5]. При увеличении дозы до 1,5 Гр наблюдался резкий спад активности СДГ у всех мышей в группе (рис. 1) при одновременном увеличении уровня гликолиза (ЛДГ/СДГ), что свидетельствует о существенных переменах в клеточном метаболизме при этой дозе. Очевидно, что при большей дозе облучения (1,5 Гр) через 1 сут более активно развивается митохондриальная дисфункция, чем при дозах 0,2-1 Гр, что приводит в этот срок к апоптозу и уменьшению количества лейкоцитов в кровяном русле. При снижении работы митохондрий замещающую функцию берёт на себя гликолиз. Сравнивая изменения активности СДГ с соответствующими величинами ЛДГ/СДГ у индивидуумов, видно, что у животных с высокой активностью СДГ регистрировалось уменьшение соотношения ЛДГ/СДГ при всех дозах. И, наоборот, при уменьшении активности СДГ регистрировалось увеличение ЛДГ/СДГ у этих же мышей.
Очевидно, что разнонаправленные изменения уровней повреждений ДНК у индивидуумов и активностей СДГ и ЛДГ связаны с различными потребностями клеток при регуляции обеспечения энергией, необходимой для восстановительных процессов и, возможно, со случайным распределением очагов поражений в клетках при прохождении пучка ускоренных ионов. Наблюдаемые эффекты через 1 сут после облучения опосредуются и клеточным обменом. Считают, что радиационно-индуцированный окислительный стресс может распространяться от клеток-мишеней к нецелевым клеткам-свидетелям через механизмы межклеточной коммуникации. Потомство этих клеток-свидетелей также испытывает нарушения окислительного метаболизма [4]. Поскольку при 2 Гр наблюдается разный ответ СДГ и ЛДГ/СДГ у разных животных, то очевидно, что доза 1,5 Гр существенна для выявления изучаемых показателей. Интересно отметить, что в лейкоцитах гамма-облучённой крови человека (0,1-1 Гр) через 5 ч после облучения увеличивались уровни экспрессии ряда генов, ответственных за контроль клеточного цикла и репарацию ДНК (CDKN1A, GADD45A, P53), а при 2 Гр наблюдалось их уменьшение; авторы этот факт никак не объясняют [10]. Очевидно, что выявленные зависимые от дозы в интервале 0,2-2 Гр изменения СДГ и ЛДГ обусловлены дисфункцией митохондрий. Разный уровень радиационного ответа по критериям активностей СДГ, ЛДГ и %TDNA у индивидуумов, облучённых в одной и той же дозе (рис. 1, 3), по-видимому, ассоциирован как с их генетическими и эпигенетическими особенностями, так и с составом субпопуляций лейкоцитов, основное количество которых у мышей представлено лимфоцитами. Несмотря на то, что лимфоциты считаются наиболее радиочувствительными среди лейкоцитов, всё же у мышей (как и у человека) после облучения (изучалось воздействие фотонов) выявляются субпопуляции лимфоцитов с разной радиочувствительностью [11]. Кроме того, Вилкинсом с соавт. удалось выявить при Х-облучении (1 Гр) разных субпопуляций лейкоцитов крови человека различные уровни апоптотических клеток у гранулоцитов, мононукле-аров, В-лимфоцитов, натуральных киллеров, CD4+ и CD8+ Т-лимфоцитов через 30 ч после облучения. Причём, эти различия были как в группе, так у индивидуальных животных [12]. Можно полагать, что у 12С-облучённых мышей индивидуальные различия %TDNA и активностей СДГ и ЛДГ так же зависят от соотношения разных субпопуляций лейкоцитов у индивидуумов.
Обнаруженное увеличение %TDNA лейкоцитов крови сопровождалось уменьшением зимозан-индуцированной способности нейтрофилов продуцировать АФК в зависимости от дозы (рис. 2), что указывает на снижение их резервных возможностей. По-видимому, это уменьшение продукции АФК может быть также обусловлено снижением количества нейтрофилов в пострадиационном периоде. Так, было показано, что через 1 сут после воздействия на мышей гамма-лучей или протонов в дозе 2 Гр снижалось количество циркулирующих в крови нейтрофилов [13, 14]. Дозозависимое уменьшение уровня продукции внутриклеточных АФК наблюдали и другие исследователи через 1 сут после гамма-облучения фибробластоподобных клеток человека. Однако, уровни митохондриальных АФК начинали увеличиваться лишь к началу вторых суток. При этом увеличивалась фрагментация митохондрий, что свидетельствовало о развитии митоходриальной дисфункции через 1 сут после облучения [15].
Таким образом, нами обнаружены существенные индивидуальные различия у 12С-облучён-ных животных по уровням повреждений ДНК, зимозан-индуцированных АФК, митохондриального дыхания и гликолиза в клетках крови. Исходя из представленных данных видно, что в пострадиационном периоде на фоне повышенного уровня повреждений ДНК и нарушения деятельности митохондрий (определённой по критерию активности СДГ) большое значение приобретает гликолиз. Можно полагать, что гликолиз служит не только в качестве дополнительного энергетического источника; возможно, что некоторые гликолитические ферменты могут быть ассоциированы с повреждениями и репарацией ДНК. Например, у известной как фермент гликолиза глице-ральдегид-3-фосфатдегидрогеназы выявлено много клеточных функций, не связанных с гликолизом, но связанных с её участием в ДНК-зависимых процессах [16].
Работа выполнена в рамках Государственного задания ИТЭБ РАН № 075-0102523-01.
Список литературы Активность сукцинат- и лактатдегидрогеназы лимфоцитов, индуцированные АФК нейтрофилов и повреждение ДНК лейкоцитов в крови облучённых ионами углерода мышей
- Mohamad O., Sishc B.J., Saha J., Pompos A., Rahimi A., Story M.D., Davis A.J., Kim D.W.N. Carbon ion radiotherapy: a review of clinical experiences and preclinical research, with an emphasis on DNA damage repair //Cancers (Basel). 2017. V. 9, N 6. P. 66. DOI: 10.3390/cancers9060066.
- Moreno-Villanueva M., Wong M., Lu T., Zhang Y., Wu H. Interplay of space radiation and microgravity in DNA damage and DNA damage response //NPJ Microgravity. 2017. V. 3. P. 14. DOI: 10.1038/s41526-017-0019-7.
- Vavitsas I., Kalachani K. Cosmic radiation and its effects on technology and health //10th Jubilee International Conference of the Balkan Physical Union, AIP Conf. Proc. 2019. V. 2075, N 1. P. 200018. DOI: 10.1063/1.5099028.
- Azzam E.I., Jay-Gerin J.P., Pain D. Ionizing radiation-induced metabolic oxidative stress and prolonged cell injury //Cancer Lett. 2012. V. 327, N 1-2. P. 48-60.
- Kuznetsova E.A., Sirota N.P., Mitroshina I.Y., Pikalov A.B., Smirnova E.N., Rozanova O.M. DNA damage in blood leukocytes from mice irradiated with accelerated carbon ions with an energy of 450 MeV/nucleon //Int. J. Radiat. Biol. 2020. V. 96, N 10. P. 1245-1253.
- Collins A.R., Oscoz A.A., Brunborg G., Gaivão I., Giovannelli L., Kruszewski M., Smith C.C., Stetina R. The comet assay: topical issues //Mutagenesis. 2008. V. 23, N 3. P. 143-151.
- Kondrashova M., Zakharchenko M., Khunderyakova N. Preservation of the in vivo state of mitochondrial network for ex vivo physiological study of mitochondria //Int. J. Biochem. Cell Biol. 2009. V. 41, N 10. P. 2036-2050.
- Хундерякова Н.В., Захарова Н.М. Оценка активности сукцинатдегидрогеназы и лактатдегидрогеназы в лимфоцитах крови у якутских сусликов Spermophilus undulatus при гибернации и в активном состоянии //Бюллетень экспериментальной биологии и медицины. 2020. Т. 169, № 4. С. 426-430.
- Заичкина С.И., Дюкина А.Р., Розанова О.М., Романченко С.П., Сирота Н.П., Кузнецова Е.А., Симонова Н.Б., Сорокина С.С., Закржевская Д.Т., Юсупов В.И., Багратишвили В.Н. Сочетанное воздействие низкоинтенсивного гелий-неонового лазера и рентгеновского излучения на in vivo клеточный ответ цельной крови и лимфоидных органов у мышей //Бюллетень экспериментальной биологии и медицины. 2016. Т. 161, № 5. С. 621-624.
- Saini D., Shelke S., Mani Vannan A., Toprani S., Jain V., Das B., Seshadri M. Transcription profile of DNA damage response genes at G₀ lymphocytes exposed to gamma radiation //Mol. Cell Biochem. 2012. V. 364, N 1-2. P. 271-281.
- Суворова Л.А., Нугис В.Ю. Динамика лейкоцитов и лейкограммы после однократного облучения человека в дозах менее 1 Гр //Медицинская радиология и радиационная безопасность. 2012. Т. 57, № 1. С. 30-38.
- Wilkins R.G., Wilkinson D., Maharaj H.P., Cybulski M.B, McLeanet J.R. Differential apoptotic response to ionizing radiation in subpopulations of human white blood cells //Mutat. Res. 2002. V. 513, N 1-2. P. 27-36.
- Romero-Weaver A.L., Wan X.S., Kennedy A.R. Kinetics of neutrophils in mice exposed to radiation and/or granulocyte colony-stimulating factor treatment //Radiat. Res. 2013. V. 180, N 2. P. 177-188.
- Sanzari J.K., Wan X.S., Krigsfeld G.S., Wroe A.J., Gridley D.S., Kennedy A.R. The effects of gamma and proton radiation exposure on hematopoietic cell counts in the ferret model //Gravit. Space Res. 2013. V. 1, N 1. P. 79-94.
- Kobashigawa S., Suzuki K., Yamashita S. Ionizing radiation accelerates Drp1-dependent mitochondrial fission, which involves delayed mitochondrial reactive oxygen species production in normal human fibroblast-like cells //Biochem. Biophys. Res. Commun. 2011. V. 414, N 4. P. 795-800.
- Косова А.А., Ходырева С.Н., Лаврик О.И. Роль глицеральдегид-3-фосфатдегидрогеназы в репарации ДНК //Биохимия. 2017. Т. 82, № 6. С. 859-872.


