Актуальные аспекты создания импортозамещающих лекарственных растительных препаратов
Автор: Куркин Владимир Александрович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Коррекция экологического неблагополучия
Статья в выпуске: 5-3 т.14, 2012 года.
Бесплатный доступ
Теоретически и экспериментально обоснованы методические и методологические подходы к созданию импортозамещающих лекарственных растительных препаратов адаптогенного, нейротропного, иммуномодулирующего, гепатопротекторного, антиоксидантного действия. Перспективным источником лекарственных препаратов вышеперечисленного спектра фармакологической активности являются родиола розовая ( Rhodiola rosea L.), сирень обыкновенная ( Syringa vulgaris L.), элеутерококк колючий [ Eleutherococcus senticosus (Rupr. et Maxim.) Maxim.], лимонник китайский ( Schizandra chinensis Baill.), мелисса лекарственная ( Melissa officinalis L.), лаванда колосовая ( Lavandula spica L.), гинкго двулопастный ( Ginkgo biloba L.), зверобой продырявленный ( Hypericum perforatum L.), зверобой пятнистый ( Hypericum maculatum Grantz.), расторопша пятнистая [ Silybum marianum (L.) Gaertn.], эхинацея пурпурная [ Echinacea purpurea (L.) Moench.], черника обыкновенная ( Vaccinium myrtillus L.), содержащие фенилпропаноиды и (или) флавоноиды.
Лекарственные растения, сырье, лекарственные препараты, флавоноиды, фенилпропаноиды, стандартизация, иммуномодуляторы, антиоксиданты, гепатопротекторы, ноотропы, анксиолитики, антидепрессанты, адаптогены
Короткий адрес: https://sciup.org/148201590
IDR: 148201590 | УДК: 615.32:
Actual aspects of the creation the domestic medicinal plant preparations
Theoretical and experimental there were substantiated the methodic and methodological approaches to the creation of the domestic phytopharmaceuticals, which have the adaptogenic, neurotropic, immunomodulating, hepatoprotective, antioxidative activities. As the perspective sources of the preparations with the above mentioned pharmacological activities are Rhodiola rosea L., Syringa vulgaris L., Eleutherococcus senticosus (Rupr. et Maxim.) Maxim., Schizandra chinensis Baill., Melissa officinalis L., Lavandula spica L., Ginkgo biloba L., Hypericum perforatum L., Hypericum maculatum Grantz., Silybum marianum (L.) Gaertn., Echinacea purpurea (L.) Moench., Vaccinium myrtillus L., containing the phenylpropanoids and (or) flavonoids.
Текст научной статьи Актуальные аспекты создания импортозамещающих лекарственных растительных препаратов
интерес представляют лекарственные растения, содержащие фенилпропаноиды и флавоноиды [2-5, 7].
Цель исследований : научное обоснование целесообразности создания и внедрения импортозамещающих лекарственных средств на основе растительного сырья, содержащего фенил-пропаноиды и флавоноиды.
Материалы и методы. В качестве объектов использованы корневища и корни родиолы розовой ( Rhodiola rosea L.), кора сирени обыкновенной ( Syringa vulgaris L.), корневища и корни элеутерококка колючего [ Eleutherococcus senticosus (Rupr. et Maxim.) Maxim.], семена и плоды лимонника китайского ( Schizandra chinensis Baill.), трава мелиссы лекарственной ( Melissa officinalis L.), цветки лаванды колосовой ( Lavandula spica L.), листья гинкго двулопастного ( Ginkgo biloba L.), трава зверобоя продырявленного ( Hypericum perforatum L.) и зверобоя пятнистого ( Hypericum maculatum Grantz.), плоды расторопши пятнистой [ Silybum marianum (L.) Gaertn.], трава эхинацеи пурпурной [ Echinacea purpurea (L.) Moench.], а также фенилпропа-ноиды и флавоноиды, выделенные из исследуемого ЛРС. В работе использованы тонкослойная хроматография (ТСХ), высокоэффективная жидкостная хроматография (ВЭЖХ), спектрофото-мерия, 1Н-ЯМР-спектроскопия, масс-спектрометрия, различные химические превращения.
Антидепрессантную активность оценивали с использованием теста «Отчаяние», оценку ноотропной активности проводили с помощью теста «Т-образный лабиринт» и теста «Открытое поле», анксиолитическую активность определяли методом «Приподнятый крестообразный лабиринт» и в условиях методики «конфликтная ситуация», психостимулирующую активность препаратов выявляли с помощью теста на снотворную активность («Тиопеталовый сон»), гепато-протекторную и антиоксидантную активность на модели токсического гепатита [6].
Результаты и обсуждение. В результате проведенных исследований из ЛРС выделены и охарактеризованы с использованием УФ-, ЯМР-спектроскопии, масс-спектрометрии, ТСХ и ВЭЖХ, различных химических превращений фенилпропаноиды (1-8) и флавоноиды (9-12), представляющие интерес с точки зрения химической стандартизации сырья и препаратов соответствующих лекарственных растений, а также проявления биологической активности. При этом обоснована необходимость введения в фармакогнозию фенилпропаноидов как самостоятельного класса биологически активных соединений (БАС), что нашло отражение в учебнике «Фармакогнозия» [2]. К фенилпропаноидам отнесены такие лекарственные растения, как родиола розовая, эхинацея пурпурная, элеутерококк колючий, сирень обыкновенная, растороп-ша пятнистая, лимонник китайский, лопух большой ( Arctium lappa L.), омела белая ( Viscum album L.). Фенилпропаноиды являются биогенетическим предшественником флавоноидов - одного из самых бурно развивающихся классов БАС, обладающих широким спектром фармакологической активности. За последние 10-15 лет число фармакопейных растений, содержащих флавоноиды в качестве ведущей группы БАС, возросло с 11 до 30 видов, среди которых уникальными являются гинкго двулопастный, эрва шерстистая ( Aerva lanata Juss.) и др. Кроме того, в 25 лекарственных растениях флавоноиды выступают в роли 2-ой или 3-ей групп действующих веществ, причем в этом случае они не только обусловливают фармакологический эффект, но и часто являются критерием качества сырья или лекарственных субстанций [2].
В результате проведенных исследований предложены новые подходы к химической стандартизации сырья лекарственных растений с использованием стандартных образцов роза-вина (1), триандрина (2), сирингина (3), лаван-дозида (4), розмариновой кислоты (5), цико-риевой кислоты (6), гамма-схизандрина (7), силибина (8), гиперозида (9), гинкгетина (9),
3,811-биас-пигенина (11), никотифлорина (12). Изучены зависимости спектральных и фармакологических свойств ряда фенилпропаноидов и флавоноидов от их химической структуры. На основе изучения физико-химических, химических, спектральных и фармакологических свойств фенилпропаноидов и флавоноидов обоснована целесообразность применения целого ряда импортозамещающих лекарственных средств. На основе сырья эхинацеи пурпурной разработаны иммуномодуляторы, превосходящие по фармакоэкономическим характеристикам зарубежные аналоги. В качестве перспективного гепатопротектора рассматривается пролонгированная лекарственная форма, получаемая из субстанции плодов расторопши пятнистой. Выраженная антиоксидантная активность выявлена для рутина, кверцетина, дигидрокверцетина, силибина, розавина, сухого экстракта родиолы розовой. Из цветков лаванды колосовой выделено новое природное соединение - лаван-дозид, обладающий седативной активностью. Установлено, что перспективным источником анксиолитиков является трава мелиссы лекарственной. Показано, что наиболее перспективными в плане создания тонизирующих и адаптогенных средств являются растения, содержащие производные коричных спиртов (родиола розовая, сирень обыкновенная, элеутерококк колючий и др.). Антидепрессантный эффект отмечен для экстракта элеутерококка жидкого и настойки зверобоя. Определено, что антидепрессантный эффект настойки зверобоя пятнистого более выражен по сравнению с таковым соответствующего препарата зверобоя продырявленного.
Из выделенных веществ наибольшую ан-тидепрессантную эффективность проявили си-рингин, розавин, триандрин и гиперозид. Выраженная ноотропная активность обнаружена для препаратов, разработанных на основе корневищ родиолы розовой и листьев гинкго двулопастного. С точки зрения влияния на ноотропную активность заслуживает внимания один из доминирующих флавоноидов листьев гинкго - гинк-гетин (9), а также доминирующий фенилпропа-ноид родиолы розовой - розавин (1).
Выводы: лекарственные растения, содержащие фенилпропаноиды и флавоноиды, являются перспективным источником гепатопротек-торных, антиоксидантных, иммуномодулирующих, адаптогенных, антидепрессантных, анксиолитических и ноотропных лекарственных средств.
Работа выполнена при поддержке проекта 02.740.11.0650 ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009-2013 годы.
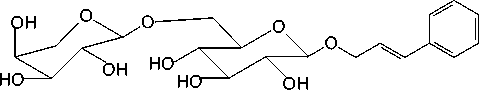
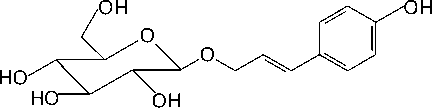
Розавин ( 1 ): родиола розовая
Триандрин ( 2 ): родиола розовая (биомасса)
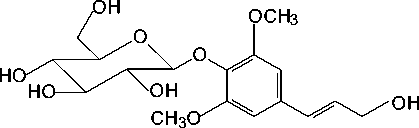
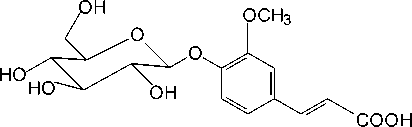
Сирингин , или элеутерозид В ( 3 ): элеутерококк колючий, сирень обыкновенная
Лавандозид ( 4 ): лаванда колосовая
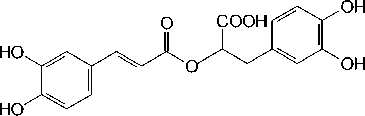
Розмариновая кислота ( 5 ): мелисса лекарственная
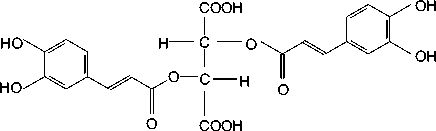
Цикориевая кислота ( 6 ):
эхинацея пурпурная
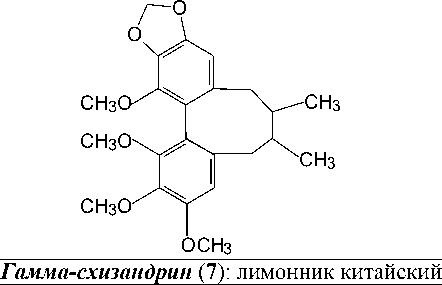
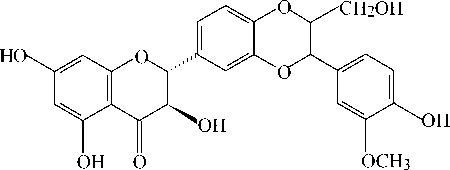
Силибин ( 8 ): расторопша пятнистая
Рис. 1 . Важнейшие фенилпропаноиды лекарственных растений
|
OCH 3 CH 3 O O HO O OH Oh O |
OH HO O OH O OH HO O OH O |
|
Гинкгетин ( 9 ): гинкго двулопастный |
З^-Бисапигенин ( 10 ): зверобой продырявленный |
|
HO O OH O - Gal OH о |
HO O O - Glc -O-Rha Oh O |
|
Гиперозид ( 11 ): зверобой продырявленный, зверобой пятнистый, береза бородавчатая |
Никотифлорин ( 12 ): гинкго двулопастный |
Рис. 2 . Флавоноиды исследуемых лекарственных растений
Список литературы Актуальные аспекты создания импортозамещающих лекарственных растительных препаратов
- Государственный реестр лекарственных средств. Т. 1. Официальное издание. -М.: ООО «Информационно-издательское агентство «Ремедиум», 2008. 1398 с.
- Куркин, В.А. Фармакогнозия: Учебник для студентов фармацевтических вузов. 2-е изд., перераб. и доп. -Самара: ООО «Офорт», ГОУ ВПО «СамГМУ», 2007. 1239 с.
- Куркин, В.А. Основы фитотерапии: Учебное пособие для студентов фармацевтических вузов. -Самара: ООО «Офорт», ГОУ ВПО «СамГМУ Росздрава», 2009. 963 с.
- Куркин, В.А. Фенилпропаноиды -перспективные природные биологически активные соединения. -Самара: СамГМУ, 1996. 80 с.
- Тюкавкина, Н.А. Биофлавоноиды. Химия, пища, лекарства, здоровье: Актовая речь. -М., 2002. 56 с.
- Хабриев, Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. -М.: Медицина, 2007. 832 с.
- Kurkin, V.A. Phenуlpropanoids from Medicinal Plants: Distribution, Classification, Structural Analysis, and Biological Activity//Chemistry of Natural Compounds. 2003. Vol. 39. No. 2. P. 123-153.
- Wagner, H. Pharmazeutische Biologie. Drogen und ihre Inhaltsstoffe. Stuttgart-New York: Gustav Fischer Verlag, 1993. 522 s.


