Альгинаты с различными молекулярными массами как сорбенты ионов кадмия и свинца
Автор: Макарова Ксения Евгеньевна, Хожаенко Елена Владимировна, Ковалев Валерий Владимирович, Подкорытова Елена Алексеевна, Хотимченко Родион Юрьевич
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Статья в выпуске: 3-6 т.15, 2013 года.
Бесплатный доступ
С помощью модифицированного метода кислотного гидролиза из альгиновой кислоты были получены олигоурониды с разными значениями молекулярных масс. Для определения молекулярно-массовых характеристик использовали высокоэффективную эксклюзионную хроматографию (ВЭЖХ). Способность полученных альгинатов связывать ионы кадмия и свинца была изучена in vitro. Для описания изотерм сорбции и оценки сорбционных показателей применяли сорбционные модели Лэнгмюра, Фрейндлиха и Брюне-Еммет-Теллера (БЭТ). Установлено, что среднемолекулярный и низкомолекулярный альгинаты обладают большей сорбционной способностью в отношении кадмия и свинца, чем высокомолекулярный альгинат.
Альгинат, сорбция, тяжелые металлы, свинец, кадмий
Короткий адрес: https://sciup.org/148202111
IDR: 148202111 | УДК: 612.396.11:615.322
Alginates with the various molecular masses as sorbents of cadmium and lead ions
By means of the modified method of acid hydrolysis from alginic acid were received oligouronides with different values of molecular masses. For definition the molecular-mass characteristics it was used high effective exclusive chromatography. The ability of the received alginates to connect ions of cadmium and lead was studied in vitro. To the description of sorption isotherms and estimation the sorption indicators it was applied Lengmuir, Friendlich's and Bryune-Emmet-Teller (BET)sorption models. It is established that middle-molecular and low-molecular alginates possess bigger sorption ability concerning cadmium and lead, than high-molecular alginate.
Текст научной статьи Альгинаты с различными молекулярными массами как сорбенты ионов кадмия и свинца
Загрязнение окружающей среды ионами тяжелых металлов представляет большую опасность для биосферы. Помимо непосредственного токсического действия на живые организмы тяжелые металлы имеют тенденцию к накоплению в пищевых цепях, что усиливает их опасность для человека [2, 10]. При поступлении в организм в токсических дозах с пищей, водой и вдыхаемым воздухом эти химические элементы приводят к развитию патологических изменений, затрагивающих все органы и системы [1, 5, 11]. В повседневной жизни люди редко задумываются о пагубном влиянии на состояние здоровья неблагоприятной экологической обстановки. Это связано со схожестью симптомов хронического отравления тяжелыми металлами и общего недомогания, вызванного стрессом и переутомлением. Поскольку выявить истинную причину недомогания бывает достаточно трудно, то, следовательно, профилактика подобных состояний представляется актуальной задачей.
В качестве перспективных соединений для профилактики отравлений тяжелыми металлами рассматриваются вещества природного происхождения (пектины, альгинаты, каррагинаны, фукоиданы) из группы пищевых волокон, необходимые организму для нормального функционирования пищеварительной системы и не обладающие побочными эффектами. В ряде научных работ была
Хотимченко Родион Юрьевич, аспирант доказана эффективность некрахмальных полисахаридов, как средств, способных связывать и выводить токсичные металлы из организма, такие как свинец, кадмий, ртуть [3, 6, 9, 12]. В этих работах применяли полисахариды с молекулярной массой более 40-50 кДа.
Цель работы: разработка методики получения низкомолекулярных альгинатов и проведение сравнительной оценки их связывающей активности в отношении ионов кадмия и свинца.
Материалы и методы. В качестве исходного сырья для получения альгинатов кальция различной молекулярной массы использовали коммерческий альгинат натрия («Aldrich»), содержание уроновых кислот в котором определяли спектрофотометрически с m-гидроксиди-фенилом [8]. Перед проведением гидролиза альгинат натрия переводили в кислотную форму путем реакции ионного обмена с 1 М раствором соляной кислоты. Полученную альгиновую кислоту суспендировали в 10-кратном избытке 0,5 М раствора соляной кислоты и проводили последующий гидролиз при температуре 90±0,5°С при интенсивном перемешивании в течение 2 часов для удаления гетерогенных (нерегулярных) участков молекул. По окончании гидролиза смесь охлаждали и отделяли жидкую фазу от нерастворимого осадка альгиновой кислоты центрифугированием при 2000g в течение 30 мин. Полученный осадок очищали от низкомолекулярных продуктов гидролиза путем суспендирования в 5-кратном объеме 0,5 М раствора соляной кислоты и последующего центрифугирования. Для получения среднемолекулярного альгината кальция, осадок альгиновой кислоты подвергали повторному 2-часовому гидролизу по вышеописанной методике. Жидкую фазу отделяли центрифугированием и в дальнейшем использовали для получения низкомолекулярного альгината. Полученный осадок переводили в раствор путем нейтрализации 1 М раствором гидроксида аммония до рН 4,0-5,0. Затем пробу разводили до конечной концентрации олигоуронидов 1-2 мг/мл, добавляли натриевую соль этилендиаминтетрауксусной кислоты (ЭДТА) до конечной концентрации 0,005 М и пропускали через ультрафильтрационную мембрану Milli-pore из регенерированной целлюлозы с пределом пропускания 30 кДа при стабилизированном давлении 0,3 МПа. Объем раствора в ячейке доводили до первоначальной величины добавлением 0,005 М раствора ЭДТА (рН 4,0-5,0) и процесс фильтрации повторяли. Данную процедуру проводили трижды. Полученный фильтрат аналогичным образом очищали от низкомолекулярных фракций на ультрафильтрационной мембране с пределом пропускания 10 кДа.
Низкомолекулярный альгинат кальция получали из жидкой фазы гидролизата, оставшегося после отделения осадка. Жидкую фазу нейтрализовали раствором 1 М гидроксида аммония до рН 4,0-5,0 и подвергали последовательному фракционированию на ультрафильтрационных мембранах с пределами пропускания 10 кДа и 3 кДа, как описано выше. Для получения низкомолекулярного альгината использовали фракцию олигоуронида, прошедшую через мембрану 10 кДа и задержавшуюся на мембране 3 кДа. Из полученных фракций олигоурониды осаждали в виде кальциевых солей добавлением 1 М раствора хлорида кальция, высушивали при 80ºС и стандартизовали по молекулярной массе.
Для определения молекулярной массы низкомолекулярных и среднемолекулярных альгинатов использовали высокоэффективную эксклюзионную хроматографию. В работе использовали хроматографическую систему Shimadzu LC-20 AD с рефрактометрическим детектором RID-10A и светорассеивающим лазерным детектором ELSD-LTII. Разделение проводили в колонках с гидрофильным полимерным сорбентом Shodex Asahipak GS-320 7E. В качестве элюента использовали 50 мМ ацетатно-аммиачный буфер, скорость элюирования 0,7 мл/мин. Молекулярную массу высокомолекулярного альгината кальция определяли вискозиметрическим методом [4]. Для оценки сорбционных характеристик экспериментальных образцов изучали их металлсвязывающую активность в отношении катионов свинца и кадмия по следующей методике. В емкость, снабженную магнитной мешалкой, вносили рассчитанный объем 0,1 М раствора нитрата свинца или кадмия, соответствующий его концентрации в растворе от 50 до 1200 мг/л, 1 мл 0,1 М ацетатного буфера со значением рН 6,0 и 10 мл 0,25% суспензии исследуемого образца. По показаниям рН-метра корректировали значение рН среды добавлением 0,1 М растворов гидроксида натрия или азотной кислоты. Объем реакционной смеси доводили до 20 мл дистиллированной водой и инкубировали при постоянном перемешивании в течение 60 мин при температуре 22-24°С. Раствор, содержавший несвя-завшиеся ионы кадмия или свинца, отделяли фильтрованием через гидрофильный фильтр Omnipore с размером пор 5,0 мкм. Определение остаточного содержания металла в жидкой фазе проводили комплексонометрическим методом. Количество связавшегося металла вычисляли по формуле:
Q=V(Ci-Ce)/M, где Q – количество связавшегося с сорбентом металла, мг/г; V – объем раствора в инкубационной емкости, л; Ci – начальная концентрация металла в суспензии, мг/л; Ce – равновесная концентрация металла в суспензии, мг/л; М – масса экспериментального образца, г [7].
Изучение количественных параметров сорбции осуществляли с использованием математических моделей Лэнгмюра, Фрейндлиха и Брюне-Еммет-Теллера (БЭТ). По результатам пяти экспериментов рассчитывали константы Лэнгмюра (максимальная сорбционная емкость [q max ] и коэффициент аффинитета [b]), Фрейндлиха (коэффициент связывающей емкости [K F ] и коэффициент интенсивности сорбции [n]) и БЭТ (коэффициент максимальной сорбционной емкости [Q]). Для оценки релевантности (достоверности) использования моделей рассчитывали коэффициент аппроксимации (R2).
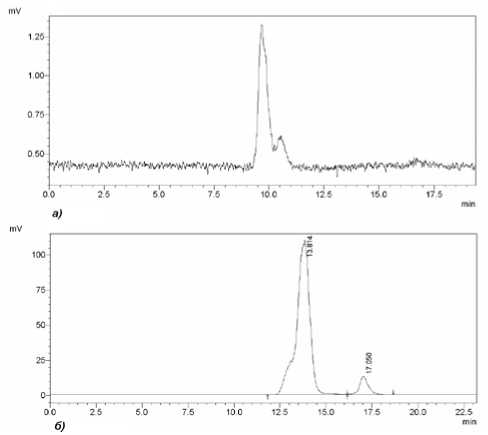
Рис. 1. Хроматограммы: а) альгинат кальция с молекулярно-массовым распределением 11,021,0 кДа; б) альгинат кальция с молекулярномассовым распределением 4,0-9,8 кДа
Результаты и обсуждение. Методом кислотного гидролиза получены экспериментальные образцы альгината кальция и стандартизованы по молекулярной массе с помощью ВЭЖХ. Молекулярно-массовое распределение низкомолекулярного альгината составило 4,0-9,8 кДа, среднемолекулярного – 11,0-21,0 кДа. Для высокомолекулярного альгината молекулярная масса определена виско-зиметрически и составила 403 кДа. Хроматограммы приведены на рис. 1. Также исходный высокомолекулярный альгинат был стандартизован по содержанию уроновых кислот – 77%. Сравнив коэффициенты аппроксимации математических моделей Лэнгмюра, Фрейндлиха и БЭТ, мы пришли к выводу, что более достоверной является модель
Лэнгмюра (R2>0,95). Модель Фрейндлиха позволяет вычислить сорбционные показатели с меньшей достоверностью (R2>0,90). Математическая модель БЭТ, описывающая многослойное связывание сорбатов однородными активными центрами сорбента, не применима для описания сорбции катионов кадмия и свинца альгинатами (R2<0,90).
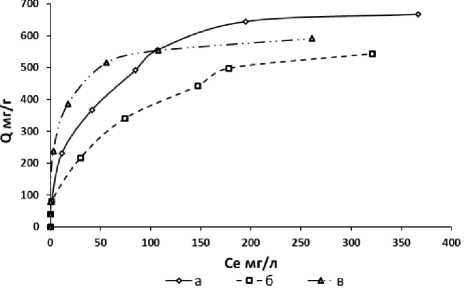
Рис. 3. Изотерма сорбции свинца при рН 6,0: а) низкомолекулярный альгинат, б) среднемолекулярный альгинат, в) высокомолекулярный альгинат
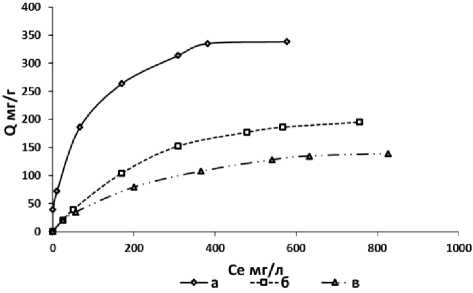
Рис. 2. Изотерма сорбции кадмия при рН 6,0: а) низкомолекулярный альгинат, б) среднемолекулярный альгинат, в) высокомолекулярный альгинат
Таблица 1. Экспериментальные константы Лэнгмюра и Фрейндлиха для связывания свинца образцами альгината кальция при рН 6,0
|
Образцы |
Модель Лэнгмюра |
Модель Фрейндлиха |
||||
|
q max , мг/г |
b, л/мг |
R2 |
K F , мг/г |
n |
R 2 |
|
|
высокомолекулярный альгинат Ca |
612,64±7,70 |
0,099±0,0081 |
0,999 |
213,81±63,37 |
5,21±1,70 |
0,909 |
|
среднемолекулярный альгинат Ca |
649,30±25,04 |
0,016±0,0031 |
0,995 |
53,39±12,59 |
2,39±0,28 |
0,962 |
|
низкомолекулярный альгинат Ca |
732,56±22,23 |
0,029±0,0051 |
0,990 |
105,33±47,80 |
3,00±0,85 |
0,904 |
Таблица 2. Экспериментальные константы Лэнгмюра и Фрейндлиха для связывания кадмия образцами альгината кальция при рН 6,0
|
Образцы |
Модель Лэнгмюра |
Модель Фрейндлиха |
||||
|
q max , мг/г |
b, л/мг |
R 2 |
K F , мг/г |
n |
R 2 |
|
|
высокомолекулярный альгинат Ca |
177,75±10,71 |
0,0046±0,00073 |
0,985 |
3,55±0,56 |
1,77±0,083 |
0,972 |
|
среднемолекулярный альгинат Ca |
279,98±18,11 |
0,0034±0,00050 |
0,979 |
2,69±0,43 |
1,48±0,059 |
0,960 |
|
низкомолекулярный альгинат Ca |
374,07±16,18 |
0,018±0,0038 |
0,991 |
32,52±9,19 |
2,56±0,34 |
0,945 |
По результатам экспериментов были построены изотермы Лэнгмюра (рис. 2-3) и определены сорбционные показатели (табл. 1-2). Из полученных данных следует, что максимальная сорбционная емкость низкомолекулекулярный и среднемолекулярных альгинатов превосходят таковую высокомолекулярного альгината в отношении свинца в среднем в 1,20 и 1,13 раза, а для кадмия в среднем в
2,10 и 1,37 раза, соответственно (табл. 1-2). Коэффициент аффинитета солей альгината кальция к катионам исследуемых металлов в большинстве случаев уменьшается при снижении молекулярной массы сорбентов. Данное наблюдение можно объяснить зависимостью прочности ионного комплекса сорбент-сорбат от размера участков молекулы полимера, вовлеченных в формирование комплекса.
Соответственно, для крупных молекул длина таких участков и прочность образованных ионных комплексов больше, чем у модифицированных молекул, полученных в ходе гидролиза.
Выводы: низкомолекуляный и среднемолекулярные альгинаты, полученные методом химического гидролиза, характеризуются способностью прочно и эффективно связывать ионы свинца и кадмия. Связывающая активность альгинатов зависит от молекулярной массы. Низкомолекулярный альгинат кальция обладает большей сорбционной емкостью, чем высокомолекулярный и среднемолекулярный образцы. Стандартизованные по молекулярной массе альгинаты могут быть рекомендованы в качестве основы для получения новых фармакологически активных веществ, предназначенных для профилактики и лечения интоксикации тяжелыми металлами.
Список литературы Альгинаты с различными молекулярными массами как сорбенты ионов кадмия и свинца
- Медик, В.А. Современные подходы к изучению заболеваемости населения//Проблемы социальной гигиены, здравоохранения и истории медицины. 2004. №1. С. 6-9.
- Ревич, Б.А. «Горячие точки» химического загрязнения окружающей среды и здоровье населения/под ред. В.М. Захарова. -М.: Акрополь, Общественная палата РФ, 2007. 192 с.
- Соболев, М.Б. Особенности лечения токсического действия тяжелых металлов у детей//Биомедицинский журнал. 2004. Т. 5. С. 191-198.
- Davidovich-Pinhas, M. A quantitative analysis of alginate swelling/M. Davidovich-Pinhas, H. Bianco-Peled//Carbohydrate polymers. 2010. Vol. 79. P. 1020-1027.
- Duruibe, J.O. Heavy metal pollution and human biotoxic effects/J.O. Duruibe, M.O.C. Ogwuegbu, J.N. Egwurugwu//International Journal of Physical Sciences. 2007. Vol. 2 (5). Р. 112-118.
- Eliaz, I. Integrative medicine and the role of modified citrus pectin/alginates in heavy metal chelation and detoxification-five case reports/I. Eliaz, E. Weil, B. Wilk//Forsch Komplementarmed. 2007. Vol.14 (6). Р. 358-364.
- Igwe, J.C. Adsorption isotherm studies of Cd (II), Pb (II) and Zn (II) ions bioremediation from aqueous solution using unmodified and EDTA-modified maize cob/J.C. Igwe, A.A. Abia//Ecletica Quimica. 2007. Vol. 32 (1). P. 33-42.
- Hung, C-C. Spectrophotometric determination of total uronic acids in seawater using cation-exchange separation and pre-concentration by lyophilization/C-C. Hung, P.H. Santschi//Analytica Chimica Acta. 2001. Vol. 427. P. 111-117.
- Khotimchenko, M. Comparative equilibrium studies of sorption of Pb (II) ions by sodium and calcium alginate/M. Khotimchenko, V. Kovalev, Y. Khotimchenko//Journal of Environmental Sciences. 2008. Vol. 20 (5). P. 827-831.
- Liao, G. Heavy metals contamination characteristics in soil of different mining activity zones/G. Liao, D. Liao, Q. Li//Transactions of Nonferrous Metals Society of China. 2008. Vol. 18 (1). P. 207-211.
- Martin, S. Human health effects of heavy metals/S. Martin, W. Griswold//Environmental Science and Technology Briefs for Citizens. 2009. Vol. 15. P.1-6.
- Matsunaga, T. Characterization of metal binding properties of rhamnogalacturonan II from plant cell walls by size-exclusion HPLC/ICP-MS/T. Matsunaga, T. Ishii//Analytical Sciences. 2004. Vol. 20 (10). P. 1389-1393.


