Алкалоиды бензилизохинолинового ряда
Автор: Хамидов И.И., Чалабаева З.М., Мамажонов Ж.Ш.
Журнал: Экономика и социум @ekonomika-socium
Рубрика: Основной раздел
Статья в выпуске: 10 (65), 2019 года.
Бесплатный доступ
Алкалоиды являются азотсодержащими соединениями основного характера, которые встречается в готовым виде в растениях. Алкалоиды классифицируется по строение гетероциклического основания. Имеются протобербериновые, хинолиновые, изохинолиновые и другие. В данной работе проанализировано некоторые виды физиологически активных веществ - алкалоидов бензилизохинолинового типа. А также, коротко обсуждены источники выделения, результаты взаимопревращения, реакционная способность бензилизохинолиновых алкалоидов типа макростомина и установления структуры некоторых алкалоидов с помощью физико-химических методов анализа.
Химия, соединения, алкалоиды, растения, физиологически активные, амины, первичные амины, вторичные амины, третичные амины, структура, органические соединение, бензилизохинолины, реакция, изменение, иасс-спектр, ямр-спектр
Короткий адрес: https://sciup.org/140245963
IDR: 140245963 | УДК: 547.94
Alkaloids of benzilizoxinolines
Alkaloids are azote containing compounds of the basic feature which occur naturally in plants. Alkaloids are classified according to the structure of heterocyclic basis. There are protoberberine, hinoline, izohinoline and other bases. In the given work there are analysed some types of physiologically active substances and so alkaloids of benzilizohinoline type. Moreover there are briefly discussed the sources of segregation, the results of inter trans formation, reactive ability of such benzilizohiniline alkaloid as macrostomine and setting the structure of some alkaloids by means of physical and chemical methods of analysis.
Текст научной статьи Алкалоиды бензилизохинолинового ряда
Бензилизохинолиновые алкалоиды по своей структуре делятся на 3 группы: 1-Бензилизохинолины (1-БИХ) (I) , 1-Бензилтетрагидроизохинолины (1-БТГИХ) (II) и N-Бензилтетрагидроизохинолины (NБТГИХ) (III) :
N
I
II
III
До настоящего времени в природе найдено более 30 алкалоида этой группы. Они довольно широко распространены в растительном мире и обнаружены в растениях семейств Berberidaceae, Papaveraceae, Ranunculaceae, Menispermaceae, Rhamnaceae, Monimiaceae, Leguminosae.
1-БЕНЗИЛИЗОХИНОЛИНЫ ТИПА МАКРОСТОМИНА
Представители этой подгруппы, первым из которых является макростомин (1), имеют в молекуле пирролидиновое кольцо в положении С-4 изохинолиновой части. В эту подгруппу входит 5 алкалоидов: макростомин (1), дегидронормакростомин (2), цис-N-окись макростомина
(3), транс-N-okucb макростомина (4) и аренин (5). Все они выделены из растений семейства Papaveraceae:
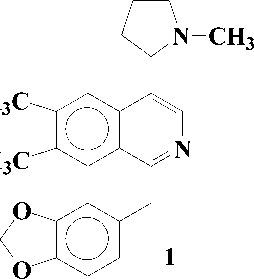
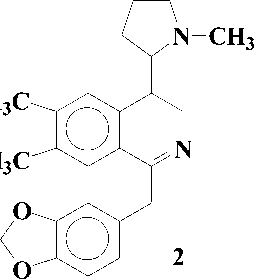
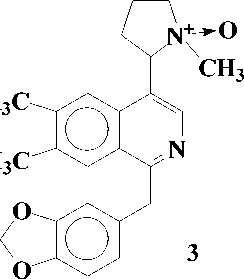
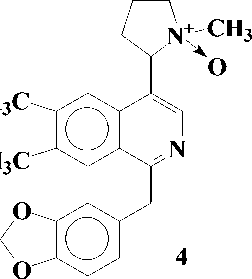
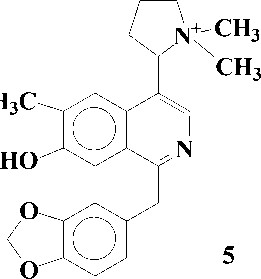
Присутствие пирролидинового кольца у макростомина (1), выделенного из P.macrostomine [1], установлено сравнением данных масс- и ПМР-спектров с таковыми никотина. Пик иона с m/z 84 (N-Me пирролидиний ион) в масс-спектре и два мультиплета при 1.5 - 2.2 м.д. (4Н) и при 3.0 - 3.6 м.д. (3Н) в ПМР-спектре характерны для пирролидинового кольца. При метилировании 1 метилируются оба атома азота и образуется 6, где протоны пирролидинового кольца и протон Н-3 в ПМР-спектре сдвигается в более слабое поле, чем у макростомина. Метилирование 6 CH3J приводит к раскрытию пирролидинового кольца (7):
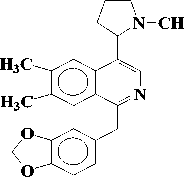
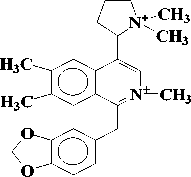
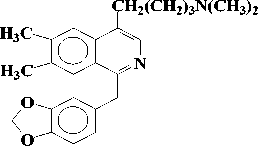
Описаны различные пути синтеза макростомина [2, 3].
Дегидронормакростомин (2) выделен из этого же растения [1].
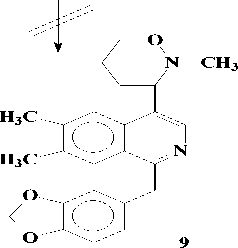
Позже авторами [4] из другого вида Papaver выделены две N-окиси макростомина - цис-(3) и транс-(4) изомеры, которые при восстановлении Zn в серной кислоте дают один продукт - макростомин (1). А последний при окислении с Н2О2 дает 3 и 4. В условиях пиролиза 3 и 4 в вакууме при 200о может произойти либо расширение пирролидинового кольца, либо перегруппировка по Коупу и могут образоваться два продукта ( 8 и 9), при восстановлении его Zn в H2SO4 получается продукт (10), который при ацетилировании дает О,N-диацетилпроизводное (11). Проявление метинового протона геминалного ацетоксильной группе при 6.27 м.д., свидетельствует о том, что при пиролизе происходит расширение пирролидинового кольца (по типу 8) [4]:
O
H 3 C
H 3 C
O
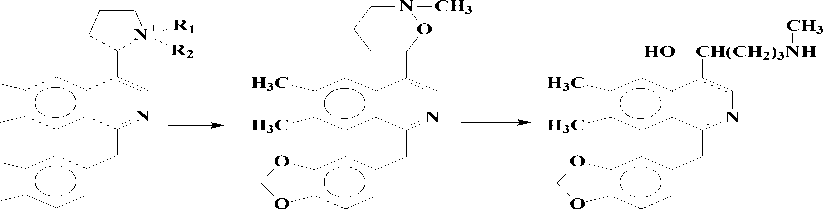
3. R 1 = O ; R 2 = CH 3
4. R 1 = CH 3 ; R 2 = O
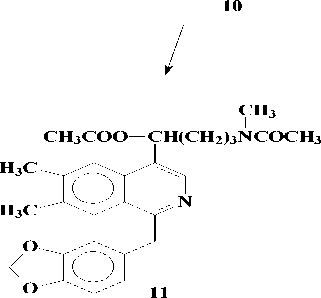
Деметилированным производным макростомина (1) [1] является аренин (5), выделенный из P.arenarium [5]. На этот факт указывают его спектрометрические данные. При метилировании 5 диазометаном образуется 1. Расположение ОН-группы в 5 установлено сравнением ПМР-спектров 5 и 1. В ПМР-спектре 5 сигнал протона С-8 смещен на 20 Гц в слабое поле по сравнению с таковым в спектре 1, а протоны кольца С и метиленовые протоны смещены примерно на 10 Гц в сильное поле. Эти смещения, по-видимому, связаны с изменением ориентации бензильной части молекулы 5 относительно макростомина (1) и объясняются заменой ОСН3-группы при С-7 в 1 гидроксильной группой в аренине (5).
Л И Т Е Р А Т У Р А
-
1. Isolation and Chemistry of the alkaloids from Papaver macrostomume Boiss et Huet / Mnatsakanyan V.A., Preininger V., Simanek V. et al. // Tetrahedron Lett. - 1974. - P. 851-854.
-
2. Wykypiel W., Seebach D. A nitrosamine route to macrostomine // Tetrahedron Lett. - 1980. - Vol. 21. - P. 1927-1929.
-
3. Bobbitt J.M., Sih J.C. Synthesis of isoquinolines. VII. 4-Hydroxy-1,2,3,4-tetrahydroisoguinolines // J. Org. Chem. - 1968. - Vol. 33. - P. 856859.
-
4. Алкалоиды Papaver arenarium / И.А.Исраилов, М.А.Манушакян, В.А.Мнацаканян, М.С.Юнусов // Химия природ. соедин. - 1984. - С. 76.
-
5. Строение аренина / Исраилов И.А., Манушакян М.А., Юнусов М.С. и др. // Химия природ. соедин. - 1978. - С. 417-418.
"Экономика и социум" №10(65) 2019
Список литературы Алкалоиды бензилизохинолинового ряда
- Isolation and Chemistry of the alkaloids from Papaver macrostomume Boiss et Huet / Mnatsakanyan V.A., Preininger V., Simanek V. et al. // Tetrahedron Lett. - 1974. - P. 851-854.
- Wykypiel W., Seebach D. A nitrosamine route to macrostomine // Tetrahedron Lett. - 1980. - Vol. 21. - P. 1927-1929.
- Bobbitt J.M., Sih J.C. Synthesis of isoquinolines. VII. 4-Hydroxy-1,2,3,4-tetrahydroisoguinolines // J. Org. Chem. - 1968. - Vol. 33. - P. 856-859.
- Алкалоиды Papaver arenarium / И.А.Исраилов, М.А.Манушакян, В.А.Мнацаканян, М.С.Юнусов // Химия природ. соедин. - 1984. - С. 76.
- Строение аренина / Исраилов И.А., Манушакян М.А., Юнусов М.С. и др. // Химия природ. соедин. - 1978. - С. 417-418.


