Алкилпирокатехины: подходы к синтезу и антирадикальные свойства
Автор: Ягунов Семен Евгеньевич, Хольшин Сергей Викторович, Кандалинцева Наталья Валерьевна
Журнал: Science for Education Today @sciforedu
Рубрика: Биологические, химические, медицинские науки
Статья в выпуске: 5 (15), 2013 года.
Бесплатный доступ
В настоящее время в литературе отсутствуют надежные данные о зависимости антиоксидантных свойств от строения в рядах многоатомных фенолов. В данной работе авторами c использованием различных подходов осуществлен синтез структурно-связанного ряда алкилированных производных пирокатехина. Проведена оценка антирадикальных свойств синтезированных 4-алкил- и 3,5-диалкилпирокатехинов в модельной реакции AIBN-инициированного окисления стирола при 50°С. Полученные данные с одной стороны имеют фундаментальное значение, а с другой, представляют интерес для разработки новых ингибиторов окисления.
Фенольные антиоксиданты, алкилпирокатехины, антиоксидантная активность
Короткий адрес: https://sciup.org/147137499
IDR: 147137499 | УДК: 547.56
Alkylpyrocatechols: synthesis and antiradical activity
Data on the dependence of the antioxidant properties of the structure in the ranks of polyhydric phenols are poorly understood. This article focuses on the synthesis of structurally related series of alkylated catechol with using different approaches. Antiradical properties of synthesized 4-alkyl-and 3,5-dialkylcatechols were studied in the model reaction of AIBN-initiated oxidation of styrene at 50 ° C. In this regard, the received data have fundamental importance, and also interest to the development of new inhibitors of oxidation.
Текст научной статьи Алкилпирокатехины: подходы к синтезу и антирадикальные свойства
Среди различных направлений исследований в области синтетических фенольных антиоксидантов наибольшее распространение получили работы, связанные с синтезом и изучением активности пространственно затрудненных одноатомных фенолов. В простых модельных системах противоокислительные свойства таких соединений различной структуры исследованы достаточно подробно, и многие исследователи полагают, что эффективность лучших из известных антиоксидантов данного класса близка к теоретическому пределу и продолжение поиска новых более эффективных ингибиторов в пределах данного класса соединений является малоперспективным.
* Статья подготовлена по результатам работы Международной научно-практической конференции «Свободные радикалы и антиоксиданты в химии, биологии и медицине» (1-4 октября 2013 г.) в рамках реализации Программы стратегического развития ФГБОУ ВПО «Новосибирский государственный педагогический университет» на 2012–2016 гг.

5(15) 2013
ISSN 2226-3365
В этой связи несомненный интерес представляют немногочисленные работы, посвященные производным других ароматических спиртов, в частности пирокатехина [1].
Наличие двух фенольных ОН-групп в соседних положениях в структуре пирокатехинового фрагмента приводит к образованию внутримолекулярной водородной связи, за счет которой происходит ослабление одной из связей О-Н, что приводит к резкому увеличению константы скорости взаимодействия с пероксидными радикалами в сравнении фенолом и другими двухатомными ароматическими спиртами. Было показано, что данное преимущество сохраняется для ди- трет -бутилзамещенных пирокатехинов: так, 3,5- и 3,6-ди- трет -бутилпирокатехины по константе скорости взаимодействия с пероксидными радикалами значительно превосходят ди- трет -бутилзамещенные фенолы и приближаются к токоферолам [2]. Пирокатехины также способны к образованию хелатных комплексов с катионами металлов переменной валентности. Другой особенностью пирокатехинов является низкая устойчивость орто -хиноны, образующиеся при их окислении, что обуславливает высокую активность последних в отношении алкильных радикалов, а также – дополнительную возможность регенерации активных фенольных ОН-групп по реакциям образования полиядерных полифенолов. Как следствие, пирокатехины обычно характеризуются более высокими коэффициентами ингибирования ( f = 3–4), нежели алкилзамещенные одноатомные фенолы ( f ≤ 2) [3].
Таким образом, алкилпирокатехины являются перспективным объектом для разработки на их основе новых антиоксидантных препаратов. Однако, данный класс соединений не являются доступным сырьем – особенности строения пирокатехина делают классические способы получения пространственно-затрудненных фенолов мало приемлемы для получения алкилпирокатехинов. В этой связи в настоящей работе реализованы различные подходы синтеза алкилпирокатехинов, с целью получения структурно-связанного ряда производных и изучения закономерностей изменения антиоксидантных свойств.
Алкилированием пирокатехина с высокими выходами удается получать лишь 3,5-ди- трет -бутил- и 3,5-диизопропилпи-рокатехины. В качестве алкилирующих агентов используются спирты в присутствии конц. H 2 SO 4 . С третичными спиртами реакция протекает при комнатной температуре, вторичные спирты реагируют в более жестких условиях [4].
OH
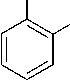
OH
OH
ROH
H 2 SO 4 rt or Δ
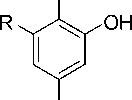
R
R= i-Pr, t-Bu
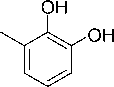
Использование данной стратегии для синтеза производных с меньшими алкильными заместителями или различными заместителями в положениях 3,5 не возможно. В этой связи для получения таких производных нами была реализована многостадийная схема синтеза предполагающая получение алкилпирокатехинов на основе соответствующим образом алкилированных фенолов введением дополнительной ОН-группы. Целевые соединения получали через промежуточный синтез 2-бром- и 2-этоксифенолов.
Все права защищены

5(15) 2013
ISSN 2226-3365
R 1
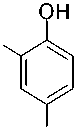
R 2
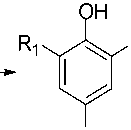
Br
R 2
1a-d
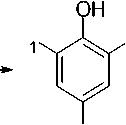
R 1
OEt
R 2
2a-d
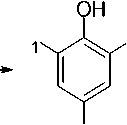
R 1
OH
R 2
3a,b,d
R 1
R 2
|
a |
b |
c |
d |
|
H |
Me |
t-Bu |
Me |
|
Me |
Me |
Me |
t-Bu |
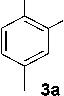
Бромфенолы 1a-d с высокими выходами получали взаимодействием соответствующих фенолов с бромом при комнатной температуре в среде CCl 4 . Взаимодействием бромфенолов 1a-d с этилатом натрия по Ульману с высокими выходами были получены соединения 3a-c. Данное превращение проводили в среде EtOH с добавками DMF и TMEDA для увеличения растворимости соединений CuI, что позвол-
В свою очередь изомерный этоксифенол
2d в аналогичных условиях не подвергался
де- трет -бутилированию и с высоким
выходом давал целевой 3-метил-5-трет-
бутилпирокатехин 3d .
2d
ило смягчить условия реакции и увеличить селективность ее протекания [5]. Производные 2a-d получены с выходами 93–99 %. Превращение 2-этоксифенолов в соответст-
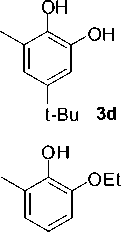

Таким образом нами был осуществлен
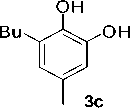
вующие пирокатехины осуществляли кипячением в конц. HBr. Стоит отметить, что этоксифенол 2с в используемых условиях наряду с О-дезалкилированием подвергался де-трет-бутилированию. Согласно данным ГЖХ скорости С- и О-дезалкилирования близки и промежуточные продукты
присутствуют в системе в сопоставимых
концентрациях, в системе накапливается продукт С- и О-дезалкилирования – пирокатехин 3а , таким образом данный путь
неприемлем для получения пирокатехина 3с .
2c

OEt
синтез структурно связанного ряда алкилпирокатехинов. Изучение антирадикальных свойств синтезированных соединений проводили в модельной реакции AIBN-инициированного окисления стирола при 50°C. В качестве реперного антиоксиданта был использован α-токоферол. Антирадикальную активность исследованных соединений характеризовали по величинам констант скоростей их взаимодействия с полипероксидными радикалами стирола (k).
. _. . • к •
ArOH + ROO ArO + ROOH
Начальные участки кинетических


OH
OH
кривых поглощения кислорода в условиях инициированного AIBN окисления стирола в
присутствии исследуемых веществ хорошо
спрямлялись в координатах уравнения
£[£2] [ДН]
-М1-Э
Все права защищены

5(15) 2013
ISSN 2226-3365
где Δ[O 2 ] – количество поглощенного кислорода, отнесенное к объему пробы; [RH] – концентрация окисляемого субстрата в пробе; k и k 1 – константы скорости реакции пероксидных радикалов с молекулами ингибитора и окисляемого субстрата соответственно; τ – период индукции; t – время.
По тангенсам углов наклона прямых в координатах Δ[O 2 ] / [RH] от –ln(1–t/τ) находили отношение k 1 /k . Абсолютные значения константы k вычисляли с использованием известного значения k 1 (107.7 л ∙ моль-1 ∙ с-1 [6]). Найденные нами значения констант k (с доверительным интервалом) приведены в таблице 1.
Таблица 1.
Значения констант скорости k взаимодействия ингибиторов с полипероксидными радикалами стирола при 50°C и число цепей обрываемых на одной молекуле ингибитора f.
|
Структура |
k ∙ 10-6 / л ∙ моль-1 ∙ с-1 |
f |
|
OH OH |
0.5±0.1 |
2.08 |
|
OH OH |
0.6±0.1 |
2.10 |
|
OH OH |
1.6±0.3 |
2.05 |
|
OH i-Pr OH i-Pr |
1.3±0.2 |
2.12 |
|
OH t-Bu OH t-Bu |
2.2±0.3 |
2.10 |
|
α-токоферол |
3.0±0.5 |
2.00 |
Установлено, что пирокатехины не имеющие алкильного заместителя в положении 3 в 2,5–3 раза уступают 3,5-диалкилпирокатехинам по величине константы k. Диметил- и диизопропилпирокатехины характеризовались близкими значениями константы k, в то время как для 3,5-ди-трет-бутилпирокатехина константа k принимала более высокие значения. Данная зависимость коренным образом отличается от закономерностей наблюдаемых для 2,6-
Все права защищены

5(15) 2013
ISSN 2226-3365
диалкилфенолов, где наибольшими значениями k характеризуются производные 2,6-диметилфенола. Так, для 2,4,6-триметилфенола величина k практически на порядок выше чем для ионола.
Таким образом, в рамках данной работы были предложены и успешно апробированы пути синтеза алкилированых производных пирокатехина на основе доступных алкилфенолов и пирокатехина. Определены кинетические параметры ингибирования AIBN-инициированного окисления стирола синтезированными соединениями. Выявлены предварительные данные о зависимости антирадикальной активности алкилпирокатехинов от структуры.
Экспериментальная часть
В работе были использованы коммерчески доступные реагенты и растворители (ABCR, Merck, Sigma-Aldrich, Reanal, Реахим). Растворители перед использованием очищали по стандартным методикам. 3,5-Ди- трет -бутилпирокатехин и 3,5-диизопропилпирокатехин получали по методикам описанным в работе [4].
Спектры ЯМР 1H записаны на приборе «Bruker AV-600», с рабочей частотой 600 МГц, растворитель CDCl 3 , стандарт CHCl 3 (δ 7.24 м.д.). ГХЖ анализ проводили на хроматографе Agilent 7820A, колонка – HP-5, 30 м х 0.32 мм, газ-носитель – азот. ВЭЖХ анализ проводили на приборе Agilent Infinity 1220, колонка – ZORBAX SB-C18, 5мкм, 4.6 мм х 150 мм. ТСХ осуществляли на пластинках Silufol (UV 254). Температуры плавления определяли в капилляре на приборе ПТП (ПО «Химлаборприбор», Россия).
В кинетических исследованиях использовали коммерческий α-токоферол («Acros Organics»). Величины k определяли в
Кинетику поглощения кислорода изучали с использованием высокочувствительного капиллярного волюмометра. Период индукции (τ) определяли как точку пересечения двух касательных проведенных к кинетической кривой, тангенсы углов наклона которых составляют 0.5 и 0.75 от тангенса угла наклона прямой неингибированной реакции.
Скорость инициирования ( W i ) определяли методом ингибиторов по времени окончания периода индукции окисления стирола в присутствии α-токоферола
Wi = 2[ArOH]о / τ где [ArOH]о – начальная концентрация ингибитора.
Эксперименты по окислению стирола проводили при W i = (1.9–2.1) ∙ 10-7 М∙с-1 и [ArOH] = (1.2-1.8) ∙ 10-4 М.
2-Бром-4-метилфенол (1a). К раствору пара -крезола (50 г, 462.36 ммоля) в 150 мл CCl 4 при перемешивании по каплям прибавляли раствор брома (77.59 г, 485.48 ммоля) в 100 мл CCl 4 (весь объем за 4 часа). Затем смесь выдержали при комнатной температуре 1 час, прибавили 100 мл 10%-ного водного раствора Na 2 SO 3 . Органический слой отделили, водную фазу обработали хлороформом (2х50 мл), органические фазы объединили, промыли водой, высушили над Na 2 SO 4 , растворитель отогнали, остаток 87.85 г (содержание основного вещества (СОВ) 86% по ГЖХ), перегнали в вакууме, получили 73.38 г (85%) продукта, т.кип. = 51-55°С (1 Торр). Найдено (%): C, 44.63; H, 3.89; C 7 H 7 BrO; Вычислено (%): C, 44.95; H, 3.77. Спектр ЯМР 1H (δ, м.д., J /Гц): 2.27 c (3 H, ArCH 3 ); 5.24 c (1 H, ArOH); 6.86 д (1 H, ArH,
Все права защищены

5(15) 2013
ISSN 2226-3365
J =7.8); 6.96 дд (1 H, ArH, J =8.4, J =1.8); 7.22 д (1 H, ArH).
Аналогично 1a получали соединения 1b-d .
2-Бром-4,6-диметилфенол (1b). Выход 93%, т.кип. = 60-65°С (1 Торр). Найдено (%): C, 47.51; H, 4.40; C 8 H 9 BrO; Вычислено (%):C, 47.79; H, 4.51. Спектр ЯМР 1H (δ, м.д., J /Гц): 2.30 c (3 H, ArCH 3 ); 2.60 c (3 H, ArCH 3 ); 5.40 c (1 H, ArOH); 6.86 д (1 H, ArH); 7.10 c (1 H, ArH).
2-Бром-4-метил-6- трет -бутилфенол (1c). Выход 92%, т.кип. = 80-83°С (1 Торр). Найдено (%): C, 54.20; H, 6.05; C 11 H 15 BrO; Вычислено (%): C, 54.34; H, 6.22. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.39 c (9 H, Ar- t -Bu); 2.27 с (3 Н, ArCH 3 ); 5.58 c (1 H, ArOH); 6.95 д (1 H, ArH); 7.11 д (1 H, ArH).
2-Бром-4- трет -бутил-6-метилфенол (1d). Выход 96%, т пл. = 45-47°С, т.кип. = 88-92°С (1 Торр). Найдено (%): C, 54.52; H, 6.03; C 11 H 15 BrO; Вычислено (%):C, 54.34; H, 6.22. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.28 c (9 H, Ar- t -Bu); 2.27 с (3 Н, ArCH 3 ); 5.29 c (1 H, ArOH); 7.00 д (1 H, ArH); 7.20 д (1H, ArH).
2-Этокси-4-метилфенол (2a). В 340 мл EtOH растворили Na (25.76 г, 1.12 моля), затем прибавили раствор 1a (52.37 г, 0.28 моля), CuI (11.20 г, 58.80 ммоля) и TMEDA (11.39 г, 98.00 ммоля) в 85 мл DMF. Смесь перемешивали 3.5 ч при 80 °С. Затем охладили, прибавили 1120 мл 2 М раствора NH 4 Cl, обработали толуолом (3х200 мл), органическую фазу промыли 2 М раствором NH 4 Cl, насыщенным раствором NaCl, высушили Na 2 SO 4 , растворитель отогнали. Остаток (41.95 г, СОВ 98% по ГЖХ) перегнали в вакууме, получили 36.36 г (85%) продукта в виде смолы, кристаллизующейся при охлаждении, т.пл. = 30-32°С, т.кип. = 72-80°С (1 Торр). Найдено (%): C, 71.28; H, 8.14; C 9 H 12 O 2 ; Вычислено (%): C, 71.03; H, 7.95.
Спектр ЯМР 1H (δ, м.д., J /Гц): 1.45 т (3 H, OCH 2 C H 3 , J =7.2); 2.26 c (3 H, ArCH 3 ); 4.07 к (2 H, OC H 2 CH 3 , J =6.6); 5.30 с (1 H, ArOH); 6.58 м (2 H, ArH); 6.72 д (1 H, ArH, J =7.8).
Аналогично 2a получали соединения 2b-d .
2-Этокси-4,6-диметилфенол (2b).
Выход 90%, т.пл. = 53-55°С, т.кип. = 67-75°С (1 Торр). Найдено (%): C, 71.29; H, 8.13; C 9 H 12 O 2 ; Вычислено (%): C, 71.03; H, 7.95. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.46 т (3 H, OCH 2 C H 3 , J =7.2); 2.19 c (3 H, ArCH 3 ); 2.23 c (3 H, ArCH 3 ); 4.06 к (2 H, OC H 2 CH 3 , J =6.6); 5.37 с (1 H, ArOH); 6.42 д (1 H, ArH, J =8.4); 6.46 д (1H, ArH).
2-Этокси-4-метил-6- трет -бутилфенол (2c). Выход 88%, т.пл. = 45-47°С. Найдено (%): C, 74.80; H, 9.75; C 13 H 20 O 2 ; Вычислено (%): C, 74.96; H, 9.68. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.37 с (9 H, Ar- t -Bu); 1.46 т (3 H, OCH 2 C H 3 , J =7.2); 2.24 c (3 H, ArCH 3 ); 4.07 к (2 H, OC H 2 CH 3 , J =7.2); 5.73 с (1 H, ArOH); 6.46 д (1 H, ArH); 6.57 д (1 H, ArH).
2-Этокси-4- трет -бутил-6-метилфенол (2d). Выход 96%, т.кип. = 85-95°С (1 Торр). Найдено (%): C, 75.10; H, 9.43; C 13 H 20 O 2 ; Вычислено (%): C, 74.96; H, 9.68. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.26 с (9 H, Ar- t -Bu); 1.45 т (3 H, OCH 2 C H 3 , J =7.2); 2.21 c (3 H, ArCH 3 ); 4.09 к (2 H, OC H 2 CH 3 , J =7.2); 5.38 с (1 H, ArOH); 6.63 м (2 H, ArH).
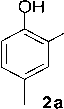
4-Метилпирокатехин (3a). 2a (3.04 г, 20.00 ммоль) кипятили с 12 мл 46 % раствора HBr (0.1 моля) 8 часов. Реакционную массу охладили, обработали толуолом (3х20 мл), органическую фазу промыли насыщенным раствором NaCl, высушили Na 2 SO 4 , растворитель отогнали, остаток перекристаллизовали из толуола, получили 1.79 г (72%) продукта с т.пл. = 67-69°С. Найдено (%): C, 67.45; H, 6.59, C 7 H 8 O 2 ; Вычислено (%): C, 67.73; H, 6.50. Спектр
Все права защищены

5(15) 2013
ISSN 2226-3365
ЯМР 1H (δ, м.д., J /Гц): 2.19 с (3 H, ArCH 3 ); 5.2 уш с (2 H, ArOH); 6.50 дд (1 H, ArH, J =7.2, J =1.8); 6.60 д (1 H, ArH, J =1.8); 6.66 д (1 H, ArH, J =7.2).
Аналогично 3a получали соединения 3b,d .
-
3,5- Диметилпирокатехин (3b). Выход 74%, т.пл. = 67.5-69°С (ср.лит. [7]: 69.5-71°С). Найдено (%): C, 69.36; H, 7.45, C 8 H 10 O 2 ; Вычислено (%): C, 69.54; H, 7.30. Спектр ЯМР 1H (δ, м.д., J /Гц): 2.19 с (6 H, ArCH 3 ); 5.09 уш с (2 H, ArOH); 6.43 д (2 H, ArH).
3-Метил-5- трет -бутилпирокатехин (3d). Выход 73%, т.пл. = 113-115°С. Найдено (%): C, 73.46; H, 8.80, C 11 H 16 O 2 ; Вычислено
(%): C, 73.30; H, 8.95. Спектр ЯМР 1H (δ, м.д., J /Гц): 1.24 с (9 H, Ar- t -Bu); 2.22 с (3 H, ArCH 3 ); 4.88 c (1 H, ArOH); 5.01 c (1 H, ArOH); 6.62 д (1 H, ArH); 6.64 д (1 H, ArH).
Взаимодействие 2-этокси-4-метил-6- трет -бутилфенола с HBr. Этоксифенол 2с (4.17 г, 20.00 ммоль) кипятили с 12 мл 46% раствора HBr (0.1 моля) 10 часов. Реакционную массу охладили, обработали серным эфиром (3х20 мл), органическую фазу промыли насыщенным раствором NaCl, высушили Na 2 SO 4 , растворитель отогнали, остаток перекристаллизовали из толуола, получили 1.16 г (70%) 3a .
Список литературы Алкилпирокатехины: подходы к синтезу и антирадикальные свойства
- Меньщикова Е. Б., Ланкин В. З., Кандалинцева Н. В. Фенольные антиоксиданты в биологии и медицине. -LAMBERT, 2012.
- Окисление, окислительный стресс, антиоксиданты: Всероссийская конференция молодых ученых и школа им. академика Н.М. Эммануэля. Доклады и тезисы. -М.: Изд-во РУДН, 2006. -С.146-147.
- Азатян Н. А., Карпухина Г. В., Белостоцкая И. С., Комиссарова Н. Л. Механизм ингибирования процессов окисления двухатомными фенолами//Нефтехимия. -1973. -№ 3. -С. 435-440.
- Масловская Л. А., Петрикевич Д. К., Тимощук В. А., Шадыро О. И. Синтез и антиокислительные свойства некоторых производных алкилированного пирокатехина//Журнал общей химии. -1996. -№ 11. -С. 1893-1898.
- Yagunov S. E., Kandalintseva N. V., Prosenko A. E. Copper-catalyzed coupling reaction in synthesis of new antioxidants/International Congress on Organic Chemistry. -Kazan, 2011. -September 18-23. -p 199.
- Поздеева Н. Н., Якущенко И. К., Александров А. Л., Денисов Е. Т. Механизм тормозящего действия гидрохинона, краун-гидрохинона и его комплексов с солями лития и магния при окислении стирола//Кинетика и катализ. -Новосибирск, 1991. -№ 6. -С. 1302-1309.
- Weller D. D., Stirchak E. P. Quassinoid Synthesis via o-Quinone Diels-Alder Reactions//J. Org. Chem. -1983. -Vol.48. -N. 25. -pp. 4873-4879.


