Амилоидогенез при нейродегенеративных заболеваниях: возрастная макулярная дегенерация и болезнь Альцгеймера
Автор: Ермилов В.В., Нестерова А.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Обзорные статьи
Статья в выпуске: 2 (62), 2019 года.
Бесплатный доступ
Геронтоофтальмологические заболевания (возрастная макулярная дегенерация, псевдоэксфолиативный синдром, псевдоэксфолиативная глаукома, старческая катаракта) представляют одну из важнейших проблем современной офтальмологии. Между тем лечение этих заболеваний продолжает строиться в основном на эмпирической основе из-за отсутствия не только достоверных данных об их этиологии, но даже единого мнения о патогенезе. В данном обзоре представлены современные взгляды на общность этиопатогенетических и морфологических проявлений болезни Альцгеймера и болезней глаза, связанных с возрастом, в аспекте амило-идогенеза. Подобный подход является перспективной попыткой уточнить механизмы возникновения и развития нейродегенеративных заболеваний, их маркеры, новые перспективы в лечении.
Амилоидогенез, болезнь альцгеймера, возрастная макулярная дегенерация, амилоидоз глаза
Короткий адрес: https://sciup.org/142224323
IDR: 142224323 | УДК: 617.735
Amyloidogenesis in the neurodegenerative diseases: age-related macular degeneration and Alzheimer's disease
Geronto-ophthalmological diseases (age-related macular degeneration, pseudo-exfoliative syndrome, pseudo-exfoliative glaucoma, senile cataract) are one of the most important problems of modern ophthalmology. However the treatments are remaining mainly in empirical approach, due to the lack of not only etiological evidences, but also a well-accepted theory of their pathogenesis. In this review, a new sight aiming on the etiopathogenetic commonness and morphological manifestations of the Alzheimer's disease (AD) and age-related macular degeneration (AMD) based with the aspect of amyloidogenesis is established. This review demonstrates the key note of AMD and AD pathogenesis is beta-amyloidopathy(Ap), which leading to cytotoxcity, neurodegeneration and the development of pathological apoptosis activated by the formation of intracellular Ap. This approach is a perspective attempt to predetermine new stratagies for the creation of ophthalmogeriatric and neuroprotective drugs affecting the pathogenesis and including all stages of Ap formation and pathological aggregation.
Текст научной статьи Амилоидогенез при нейродегенеративных заболеваниях: возрастная макулярная дегенерация и болезнь Альцгеймера
Демографические изменения, которые произошли в последние десятилетия, заставили все экономически развитые страны обратить более пристальное внимание на проблемы геронтологии и гериатрии. Согласно последним расчетам экспертов ООН, к настоящему времени доля людей старше 60 лет в экономически развитых странах составляет более 20 % [1]. Поэтому решение вопросов, связанных с возможностью продления периода трудоспособного возраста и поддержания качества жизни, занимает ведущее место в среде профессионалов различных медицинских специальностей. С этой точки зрения, невозможно переоценить значение функциональной состоятельности зрительного анализатора, особенно в старшей возрастной группе.
Причины возникновения слабовидения у пожилых лиц разнообразны, но одно из первых мест занимают дистрофические поражения сетчатой оболочки глаза, а именно возрастная макулярная дегенерация.
Возрастная макулярная дегенерация (ВМД) является ведущей причиной необратимого снижения центрального зрения, приводящей к слепоте, занимая третье место в структуре заболеваемости у пожилых больных после глаукомы и диабетической ретинопатии [2]. ВМД представляет собой дистрофический процесс в собственной сосудистой оболочке глаза – хориоидее, базальном комплексе или мембране Бруха (МБ) и в структурных элементах сетчатки с вовлечением фоторецепторов [3]. Одной из ведущих причин снижения центрального зрения при ВМД является накопление патологического белкового материала в МБ и субретинальном пространстве, что приводит к формированию друз [3, 6]. Результаты многочисленных гистохимических и иммуногистохимических исследований продемонстрировали присутствие патологического белка β-амилоида (Аβ) в друзах – морфологических спутниках ВМД [3, 8, 10]. Анализ современной отечественной и зарубежной литературы свидетельствует о нарастающем интересе к изучению локального старческого амилоидоза глаза и его связи с нейродегенеративными заболеваниями (НДЗ), в частности болезнью Альцгеймера (БА).
БА – нейродегенеративное заболевание, признанное сегодня одной из самых распространенных причин старческого слабоумия. От него страдает в среднем в мире 5 % пожилых людей в возрасте 65–80 лет и около 25 % в возрасте после 80 лет [10]. С увеличением продолжительности жизни количество больных БА в общей структуре возраст-ассоциированных заболеваний постоянно растет. Морфологическим субстратом БА является гибель нейронов. Как отмечают авторы многочисленных исследований, в основе гибели нейронов при болезни Альцгеймера лежат процессы образования сенильных бляшек, центральное место в которых занимают депозиты патологического белка Аβ, и образование внутриклеточных нейрофибрилляр-ных сплетений в результате гиперфосфорилирования тау-белка [4, 10].
Результаты большого количества молекулярно-биологических исследований последних десятилетий показали ведущую роль белков-предшественников амилоида в патогенезе возрастных заболеваний [4]. Формы НДЗ, в основе патогенеза которых лежат изменения структуры и/или нарушение метаболизма специфических белков, приводящие к их агрегации или формированию агрегатов патогенных пептидов с последующим образованием характерных белковых или пептидных отложений, в настоящее время предлагается классифицировать как про-теинопатии. В последнее время широкое распространение получила гипотеза, подтверждаемая результатами целого ряда исследований, согласно которой первичными цитотоксическими агентами при развитии прoтеинопатий являются нерастворимые олигомеры склонных к агрегации белков, одним из которых является Аβ [4].
ВМД и БА относятся к полиэтиологическим заболеваниям, которые связаны взаимодействием ряда факторов, включающих каскад реакций, в том числе и амилоидный, характеризующийся сложными нарушениями метаболизма в тканях головного мозга и сетчатки. Привлечение новейших методов исследования позволило выявить молекулярные механизмы, лежащие в основе патогенеза ВМД и БА. Авторами показано, что под влиянием окислительного стресса, химических модификаций, генетических мутаций и других факторов происходит переход нормального, но потенциально амилоидогенного белка из растворимой формы в патогенную, склонную к агрегации форму, которая образует олигомеры и протофибриллы [4, 8]. Из них на заключительном этапе образуются зрелые фибриллы, формирующие белковые отложения как внутри клеток, так и за их пределами с формированием бета-амилоидных бляшек в структурах головного мозга при БА и друз в межклеточном пространстве в структурах гематорети-нального барьера при ВМД [4, 8].
В работах последних лет, посвященных изучению БА, высказано предположение, что сетчатка, имея много общего с мозгом (эмбриональное происхождение, анатомические особенности, физиологические характеристики), может служить легко доступным и неинвазивным методом изучения патологии, имеющей место в головном мозге [3, 10]. К настоящему времени увеличилось количество данных, свидетельствующих о том, что морфологические признаки БА обнаруживаются как в головном мозге больных БА, так и в сетчатке больных БА и животных трансгенных моделей БА [10]. В связи с этим особый интерес представляет изучение сочетания церебрального амилоидоза при БА и старческого локального амилоидоза глаза при ВМД.
С помощью селективных методов выявления амилоида и его типов нами было исследовано 336 глаз и головной мозг, взятый у 171 трупа. В работе использован количественный метод оценки свечения амилоид-положительных структур глаза и головного мозга, для чего применяли фотометрическую насадку ФМЭЛ-1А. Оценку свечения окрашенных тиофлавином-Т препаратов проводили в условных единицах по методу Г. Г. Автандилова. Сочетанная локальная форма амилоидоза глаза встретилась в 60,5 % наблюдений. При сочетании ВМД и БА у женщин амилоид обнаружился в возрасте на 10 лет раньше и в 2 раза чаще, чем у мужчин. Анализ полученных данных показал, что по мере старения возрастает частота сочетанного старческого амилоидоза глаза и головного мозга. Результаты проведенного нами исследования позволили сделать вывод, что сочетание локальных форм амилоидоза характеризуется содружественным отложением Аβ в сосудах и веществе головного мозга, а также в сосудах хориоидеи и структурных элементах заднего отдела глаза с типичными для локальных форм старческого амилоидоза иммуногистохимическими характеристиками. При этом интенсивность свечения амилоидных отложений в сосудах головного мозга была более выражена, чем в сосудах хориоидеи. Необходимо подчеркнуть, что отложения Аβ локализовались в сосудах всех слоев хориоидеи, однако в сосудах хориока-пиллярной пластинки встречались чаще и были более интенсивными. Обнаружено, что процент больных со старческим локальным амилоидозом глаза наиболее высок у пациентов с БА. Результаты проведенного исследования продемонстрировали несомненную, на наш взгляд, общность этиопатогенетических и морфологических проявлений БA и ВМД.
Учитывая общность метаболизма АРР при ВМД и БА, который может протекать по амилоидогенному и неамилоидогенному пути, мы в своем исследовании сочли возможным предположить следующий механизм развития β-амилоидопатии и нейродегенерации при ВМД (см. рис.).
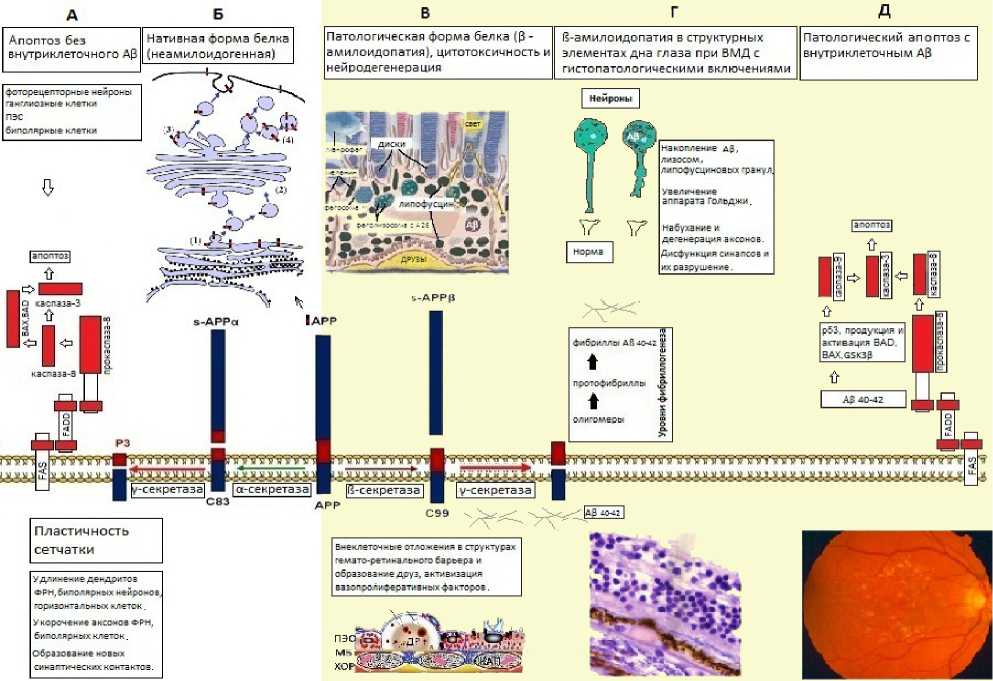
Рис. Развитие β-амилоидопатии при возрастной макулярной дегенерации:
А, Б – неамилоидогенный метаболизм АРР. FAS (first apoptotic signal) – трансмембранный белок, взаимодействующий с FAS-лигандом; FADD (Fas-associated death domain) – белок-адаптер, вызывающий активацию прокаспазы-8; BAD (Bcl-2-associated death promoter), BAX (Bcl-2-associated X protein) – белки митохондриального сигнального пути апоптоза; ФРН – фоторецепторные нейроны; 1 – ЭПС (эндоплазматическая сеть), 2 – аппарат Гольджи, 3 – лизосомы. 4 – эндосомы; sAPPα, P3, C83 – продукты неамилоидогенного расщепления АРР. В, Г, Д – амилоидогенный метаболизм АРР с патологическим апоптозом. МБ – мембрана Бруха, ХОР – хориоидея, ДР – друза, КАП – капилляры хориоидеи; sAPPβ, С99, Аβ40-42 – продукты амилоидогенного расщепления АРР; GSK3β (glucogen synthase kinase-3) – регуляторный белок, участвующий в активации р53; р53 – транскрипционный фактор, регулирующий активацию генов-активаторов апоптоза
В нормально стареющей и обладающей высокой степенью пластичности сетчатке [12] рецептор-опосредованному апоптозу подвергаются фоторецепторные нейроны, ганглиозные клетки и клетки ПЭС (см. рис. А). В результате взаимодействия Fas-лиганда и Fas-рецептора сигнал, идущий от мембраны, вызывает превращение неактивной прокаспазы-8 в её активную форму, которая, в свою очередь, активирует каспазу-3, а также инициирует митохондриальный сигнальный путь апоптоза.
Трансмембранный белок APP в норме присутствует во многих клетках, включая ПЭС, нейроны сетчатки и головного мозга (см. рис. Б).
Внутриклеточно АРР локализуется в аппарате Гольджи, эндоплазматической сети, лизосомах, эндосомах, ядерной оболочке, а также в клеточной мембране. Неамилоидогенный метаболический путь включает последовательное воздействие α- и γ-секретаз на АРР с образованием s-APPα, P3 и AICD (APP intracellular domain), участвующих в адекватном клеточном обмене.
В стареющем организме под влиянием факторов риска (см. рис. В) в клетках ПЭС и нейронах сетчатки снижается активность про-теосомно-лизосомальной системы, увеличивается количество фаголизосом, эндосом, гранул липофусцина. С возрастом в клетках ПЭС уменьшается количество меланиновых гранул и накапливаются фаголизосомы с высокотоксичными А2Е (бис-ретинилиден-этаноламин), изо А2Е и их окисленными эпоксиформами. Указанные внутриклеточные изменения вызывают развитие окислительного стресса и цитотоксичности.
В таких условиях метаболизм АРР протекает с участием β- и γ-секретаз, которые отделяют от APP склонные к β-кросстрансформации и фибриллогенезу полипептиды Аβ40 и Аβ42.
Этот процесс приводит к образованию олигомерных, префибриллярных и в конечном счете нерастворимых фибриллярных форм Аβ, откладывающихся в виде гистопатологических включений как внутриклеточно, так и внекле-точно (см. рис. Г). Амилоидогенный процессинг АРР заканчивается отложением Аβ в сетчатке, в материале друз, в структурах гематорети-нального барьера: мембране Бруха, сосудах хориоидеи (амилоидная ангиопатия). Внутриклеточный Аβ стимулирует аутофагию и способствует увеличению структурных компонентов аппарата Гольджи, количества лизосом и эндосом. Отложения внутриклеточного Аβ вызывают набухание и дегенерацию аксонов, дисфункцию синапсов и их разрушение.
Цитотоксический эффект внутриклеточного Аβ связан с его способностью активировать основной белок-«диспетчер» апоптоза – р53 (см. рис. Д), который, в свою очередь, напрямую инициирует каспазный каскад, а также ре-цептор-зависимый и митохондриальный сигнальные пути апоптотической гибели клеток.
Подобный механизм развития β-амилоидо-патии при ВМД, на наш взгляд, является вполне оправданным и учитывает современные представления о внутриклеточной патологии белков и механизмах клеточной гибели, основанные на достижениях молекулярной биологии [4–7, 9, 11, 13]. Таким образом, анализ новых обобщенных данных, полученных за последние годы в области изучения механизмов развития БА и ВМД, а также результаты наших собственных исследований позволяют выделить общее звено патогенеза в развитии этих заболеваний. Обнаружение сходных молекулярных механизмов патогенеза ВМД и БА, а также других НДЗ, включающих процессы патологической агрегации белков, формирования нерастворимых фибриллярных структур и депонирования их в виде гистопатологических включений в тканях мозга и заднего отдела глаза диктует целесообразность выделения группы заболеваний, характеризующихся наличием белковой патологии – протеинопатии. И при ВМД, и при БА лейтмотивом является агрегация нерастворимого протеина – Аβ, что позволяет, на наш взгляд, тракто- вать ВМД как протеинопатию, хотя работ, освещающих данное геронтоофтальмологическое заболевание в подобном контексте практически нет. Очевидно, что такой взгляд на проблему создает предпосылки для новых стратегий по созданию нейропротекторных и офтальмогериат-рических препаратов нового поколения.
Список литературы Амилоидогенез при нейродегенеративных заболеваниях: возрастная макулярная дегенерация и болезнь Альцгеймера
- Анисимов, В. Н. Эволюция концепций в геронтологии / В. Н. Анисимов, М. В. Соловьев. - СПб: Эскулап, 1999. - 130 с.
- Егоров, Е. А. Современные аспекты патогенеза, диагностики клиники и лечения возрастной макулярной дегенерации / Е. А. Егоров, И. А. Романенко // Офтальмология. - 2009. - Т. 6, № 1. - С. 97-103.
- Болезнь Альцгеймера и геронтоофтальмологические заболевания в аспекте амилоидогенеза / В. В. Ермилов [и др.] // Архив патологии. - 2013 -№ 2 - С. 37-42.
- Протеинопатии - формы нейродегенеративных заболеваний, в основе которых лежит патологическая агрегация белков / Т. А. Шелковникова [и др.] // Молекулярная билогия. - 2012.- Т. 46, № 3. - С. 402 - 415.
- Association of AMD-like retinopathy development with an Alzheimer's disease metabolic pathway in OXYS rats / O. S. Kozhevnikova // Biogerontology. - 2013. - № 14 (6). - Р. 753-762.
- Beta-amyloid deposition and functional impairment in the retina of the APPswe/PS1DeltaE9 transgenic mouse model of Alzheimer's disease / S. E. Perez [et al.] // Investigative Ophthalmology & Visual Science. - 2009. - № 50 (2). - Р. 793-800.
- Drusen proteome analysis: an approach to the etiology of age-related macular degeneration / J. W. Crabb [et al.] // Proc Natl Acad Sci U S A. - 2002. -№ 99. - Р. 14682-14687.
- Ermilov, V. The role of retinal pigment epithelium cells in amyloidogenesis of senile local eye amyloidosis with age-related macular degeneration 23rd European Congress of Pathology. 27 August -1 September 2011. Helsinki / V. Ermilov, O. Makhonina // Virchow's Arch. - 2011, - № 459 (Suppl. 1). - S1-S329, P. 190.
- Kayed, R. Common structure of soluble amyloid oligomers implies common mechanism of pathogenesis / R. Kayed, E. Head, J. E. Thompson // Science. - 2003. - № 300 (5618). - Р. 486-489.
- Ocular manifestations of Alzheimer's disease in animal models / M. Parnell // Int. J. Alzheimers Dis. -2012. - Vol. 39. - P. 187 - 204.
- Ostrovskij M. A. Molecular mechanisms of the damaging effect of light on the structure of the eye and the system of protection against such damage / M. A. Ostrovskij // Success of biological chemistry. - 2005. - № 45. - Р. 173-204.
- Picken, M. M. Amyloid and Related Disorders / M. M. Picken, A. D. Guillermo, A. Herrera // Berlin: Springer Science+Business Media, LLC. - 2012. - 419 p.
- Zhang C. Ajzheimer's Disease-Related Amyloidopathy in Visual Impairment / C. Zhang // J. Addict Res Ther. - 2012. - S5.


