Анаэробная инфекция при минно-взрывной травме конечностей
Автор: Пильников С.А., Войновский А.Е.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3-2 т.15, 2020 года.
Бесплатный доступ
Рассмотрены результаты двух методов ампутации конечности при минно-взрывной травме (МВТ) у 199 раненых с 1995-2011 гг. Ампутации конечности с ушиванием культи и дренированием ран выполняли 98 раненым в 1995-2001 гг. С 2002 г. 101 раненым применили метод предварительной ампутации конечности с гистохимической идентификации степени ишемии мышечной ткани. Грамотно выполненная предварительная ампутация с морфологической оценкой жизнеспособности тканей культи конечности позволили сократить частоту анаэробной инфекции с 19,4% до 10,9%, сократить количество реампутаций и уменьшить летальность в два раза - с 15,3 до 6,9%. В результате проведенного анализа лечения раненых с МВТ конечностей сделаны выводы о том, что основополагающим принципом при экстренных ампутациях конечности следует считать выполнение предварительной ампутации конечности c использованием диагностических разрезов с гистохимической идентификации ишемии тканей для оценки жизнеспособности тканей конечности и бипсии мышечной ткани для проведения экспресс гистологического исследования у раненых, что способствуют объективизации выбора уровня и техники ампутации и, таким образом, снижению частоты ранних послеоперационных осложнений. Анаэробная инфекция при МВТ конечностей с отсутствием яркой манифестированной клинической картины встречается у 15,1% раненых, что является причиной позднего хирургического лечения.
Конечность, культя, минно-взрывная травма, ампутация, реампутация, биопсия, анаэробная инфекция
Короткий адрес: https://sciup.org/140257760
IDR: 140257760 | DOI: 10.25881/BPNMSC.2020.31.31.013
Anaerobic infection in mine-explosive injury of the extremities
The results of two methods of limb amputation for mine-explosive trauma in 199 wounded from 1995-2011 are considered. Limb amputations with stump suturing and wound drainage were performed in 98 patients in 1995-2001. Since 2002, 101 patients have used the method of preliminary limb amputation with histochemical identification of the degree of muscle tissue ischemia. Correctly performed pre-amputation with morphological assessment of the viability of the limb stump tissues allowed reducing the frequency of anaerobic infection from 19.4% to 10.9%, reducing the number of reamputations and reducing the mortality rate by half-from 15.3 to 6.9%. In the result of the analysis of the treatment of the wounded with mine-explosive trauma limbs it is concluded that the fundamental principle in emergency amputation of a limb should be considered a preliminary amputation of the limb using the diagnostic sections with histochemical identification of tissue ischemia to evaluate the viability of the limb tissue and bepcii muscle tissue for a rapid histological studies in wounded that contribute to the objectivization of the choice of technique and level of amputation and, thus, to reduce the frequency of early postoperative complications. Anaerobic infection in limb mine-explosive trauma with the absence of a clear manifested clinical picture occurs in 15.1% of wounded patients, which is the reason for late surgical treatment.
Текст научной статьи Анаэробная инфекция при минно-взрывной травме конечностей
Выделение анаэробных форм инфекции при МВТ сохраняет актуальность, поскольку в патоморфологическом и клиническом плане имеются существенные отличия, которые необходимо учитывать в лечебно-диагностическом процессе [2].
Частота выделения неспорообразующих анаэробов при гнойных процессах в мягких тканях конечностей достаточно вариабельна и колеблется от 48,3% до 90% [3; 7], при этом монокультура анаэробов высевается только в 1,3–14,6%.
Летальность от этой инфекции в период Великой Отечественной войны (1941–1945 гг.) достигала 50%. До настоящего времени данное осложнение ранений отличается высокой летальностью от 18 до 26% [1]. Наши исследования показывают, что раненые с раневой анаэробной инфекцией поступают в хирургические стационары поздно, в разгар болезни. Недостаточная осведомленность, забывчивость, а то и незнание этого рода раневого осложнения приводят к грубейшим, роковым ошибкам — запоздалой диагностике, а, следовательно, к несвоевременному комплексному лечению, главным компонентом которого является хирургическое вмешательство.
Основными причинами развития хирургической инфекции являются травматичность оперативного вмешательства, неадекватное дренирование культи, нарушение техники ампутации, наличие госпитальной инфекции, нарушенный лимфатический дренаж культи, гипоксия тканей культи, исходная анемия и гипопротеинемия больного, наличие тяжелой эндогенной интоксикации, сниженный иммунный статус, антибиотикоустойчивость.
От правильной оценки границ жизнеспособной ткани зависит выбор оптимального уровня и объёма оперативного вмешательства. Данные литературы свидетельствуют о том, что большинство хирургов не применяют никаких диагностических тестов для определения уровня ампутации. Чаще всего они ориентируются только на клинические данные о состоянии конечности и ее макроскопическую визуальную оценку [5]. Использование традиционных методов оценки жизнеспособности мышечной ткани (ориентировка на цвет, сократимость, консистенцию и кровоточивость) не позволяет правильно установить границы зоны необратимых изменений [4; 6].
Несмотря на казалось бы разработанную тактику лечения анаэробной инфекции, результаты часто остаются

неудовлетворительными из-за малоизученного сложного патогенетического механизма развития инфекции и течения раневого процесса.
До сих пор отсутствуют дооперационная диагностика анаэробной инфекции, объективные критерии ее проведения и основное диагностическое значение имеет клиническая картина заболевания. В значительной мере субъективен объем некрэктомии, эмпирический характер носит проводимая антибиотикотерапия. Это связано с тем, что применяемые методы микробиологической диагностики по срокам не сопоставимы с темпами распространения анаэробной инфекции и развития осложнений.
Интраоперационно жизнеспособность тканей на уровне ампутации традиционно определяют, оценивая выраженность отека, равномерность кровенаполнения мышечной ткани, ее кровоточивость, сокращение мышечных волокон при механичесом раздражении и электрокоагуляции. Однако ни один из предложенных методов не позволяет достоверно судить о жизнеспособности тканей и прогнозировать заживление операционной раны на выбранном уровне [7].
Цель исследования : выявление частоты встречаемости, повышение эффективности диагностики и лечения раненых с анаэробной инфекцией конечностей при МВТ, являющейся одной из главных причин летальных исходов.
Материал и методы
Анализированы результаты лечения 199 раненых с МВТ в период с 1995 по 2011 гг. С 1995 по 2001 гг. пролечено 98 раненых (I группа), которым после ампутации конечностей накладывались первичные швы на культю. С 2002 по 2011 гг. у 101 раненого усовершенствована и применена хирургическая тактика предварительных ампутаций конечностей при МВТ на этапах медицинской эвакуации с наложением диагностических разрезов и гистохимической идентификации ишемии тканей с целью оценки жизнеспособности тканей конечности и операционной биопсии мышечной ткани для проведения экспресс гистологического исследования у раненых на этапе специализированной медицинской помощи (II группа исследования).
Группы пострадавших были сопоставимы по возрастному составу, этиологии, сопутствующим заболеваниям, а различались хирургической тактикой. Средний возраст раненых I группы составил 22,7±0,3, II группы — 27,6±0,4 лет.
Время выведения из шока и ампутации конечностей в сроки до 3 часов с момента ранения наблюдалось у 20,4% раненых I группы и у 77% — II группы.
У раненных I группы отмечалось наибольшее число — 43 (43,9%) пострадавших с минно-взрывным повреждениями (МВП). Помимо разрушений и отрыва конечностей у этих раненых отмечались переломы костей на других уровнях (76,8%). МВП, нанесенные кумулятивными гранатами внутри бронированной техники, обусловливали отрывы и разрушения конечностей у 42 чел (42,9%), ожоги — у 48 (48,9%), а также массивную кровопотерю и шок — у 89 чел (90,8%).
Разработанное комплексное лечение пациентов включало в себя: предварительную ампутацию конечности на этапах квалифицированной медицинской помощи, что предопределяло в дальнейшем реконструкцию культи, в том числе, реампутацию на этапе специализированной медицинской помощи, профилактику нагноения и ранние реконструктивно-восстановительные операции на культях.
Технически предварительная ампутация заключалась в иссечении только явно нежизнеспособных тканей, транспериостальном опиле кости по краю сократившихся мышц и усечении нервных стволов; швы на рану культи не накладывались. Такой вид операции позволял сохранить максимальную длину культи, что особенно важно при локализации повреждения вблизи крупных суставов.
Объектом исследования послужили 199 раненых, перенесших ампутацию конечностей по поводу МВТ, в том числе у 15 пострадавших была выполнена ампутация обеих нижних конечностей и у 3 — двух нижних и одной верхней конечностей. Поскольку целью работы являлось изучение раннего послеоперационного раневого осложнения — анаэробной инфекции, за единицу исследования была принята ампутация конечности, а число наблюдений составило 220.
На первом этапе для оценки частоты и характера анаэробной инфекции был проведен сквозной ретроспективный анализ результатов ампутаций нижних конечностей, выполненных по поводу МВТ у раненых I группы исследования.
Вторая часть исследования заключалась в наложении диагностических разрезов в проксимальных отделах поврежденного сегмента конечности и интраоперационной биопсии мышечной ткани для определения ее жизнеспособности 48 раненым, а также применения интраоперационного гистохимического экспресс-метода оценки активности лактатдегидрогеназы (ЛДГ) или сукцинатдегидрогеназы мышечной ткани на уровне ампутации (поскольку раннее ишемическое повреждение тканей сопровождается снижением активности дегидрогеназ) 12 пострадавшим II группы исследования и в проспективной оценке связи результатов данного исследования и ранних послеоперационных осложнений ампутации.
Способ основан на превращении водорастворимых тетразолиевых соединений при акцептировании ионов водорода в нерастворимые в воде темные пигменты — формазаны. Реакцию с нитросиним тетразолием (НСТ), предложенную Sandritter и Jetstadt в 1958 г., пата-логоанатомы использовали для выявления ранних стадий инфаркта миокарда.
ЛДГ (НАД+ оксидоредуктаза) — фермент класса оксидоредуктаз, катализирующий на последней стадии гликолиза обратимую реакцию окисления L-молочной кислоты до пировиноградной. L-лактат + НАД+ ↔ пируват + НАДН + H+ , где НАД+ — никотинамид аденин

динуклеотид; НАДН — никотинамид аденин динуклеотид, восстановленная форма.
При снижении активности ЛДГ, возникающем в условиях ишемического некроза мышц, равновесие реакции сдвинуто в сторону образования L-лактата. В то же время, ишемия тканей способствует высвобождению НАДН и H+ из клетки миоцита на его оболочку. Содержащиеся внеклеточно свободные ионы H+ и НАДН, дают первичную реакцию окрашивания с НСТ. Реакции с использованием НСТ протекают быстро и дают яркое и четкое контрастирование зон потери или отсутствия активности фермента, в связи с этим очень удобны для проведения макропробы.
В условиях операционной, после обработки операционного поля, скальпелем делали диагностические разрезы в проксимальных отделах поврежденного сегмента конечности и проводили интраоперационную биопсию мышечной ткани для определения ее жизнеспособности на предполагаемом уровне ампутации, толщина срезов около 3–5 мм. После изготовления подходящего биоптата с поперечным срезом мышечных волокон, его инкубировали в смеси растворов 0,02% НСТ и 1М раствора лактата при температуре 37–40 °С. Необходимую для проведения реакции кислотность (рН = 7,2–7,4) достигали использованием фосфатного буфера.
Определение степени ишемии проводилось визуально с фиксацией времени и степени окрашивания мышечной ткани. Для облегчения распознавания нами было выделено 2 стадии реакции: первая степень — окрашивание отдельных волокон, и вторая степень — тотальное окрашивание фрагмента мышцы. Соответственно учитывалось время, за которое проявлялась первая, и вторая стадии реакции. T1 соответствовало времени появления первой степени, Т2 — время наступления второй стадии реакции.
К гистологическим признакам ишемии относились расстройства кровообращения на уровне микроциркуля-торного русла, что проявлялось в первую очередь неравномерным кровенаполнением капилляров, нечеткостью границ ядер, набуханием и глыбчатостью цитоплазмы.
Результаты лечения
Из осложнений послеоперационного периода наиболее серьезным являлась анаэробная инфекция, которая была отмечена у 19 (19,4%) пострадавших 1-ой группы и 11 (10,9%) раненых — 2-ой группы.
Возбудителями анаэробной инфекции чаще являлись Clostridium bifermentas (31%), С. Perfringens (22%), С. Spo-rogenes (15%) и др. В 25% случаев установлено заражение только одним видом клостридии, в остальных случаях в ране имелась смешанная анаэробно-аэробная флора.
Быстрое омертвление и некроз мышечных волокон возникали под действием альфа-токсина, фосфолипазы и протеазы; альфа-токсин исключительно кардиотоксичен, митотоксин вместе с гиалуронидазой способствует стремительному распространению процесса по ходу сосудов и мышечных волокон. Ее развитию способствовали: на-
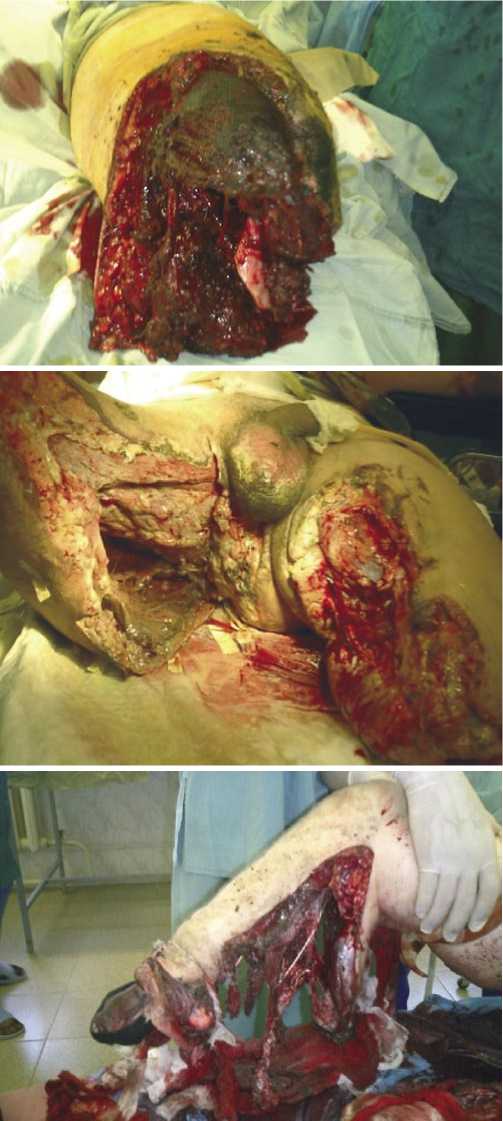
Рис. 1. Засорение раны культи бедра землей при отрыве нижней конечности.
личие в ране размозженных тканей, девитализированных мышц и других мягких тканей — 15%; длительное (более 2 ч) нарушение кровотока в ране вследствие наложенного жгута, шоковой гипотензии, переохлаждения — 6%; засорение раны землей и др. — 47% (Рис. 1); отсутствие аэрации раны вследствие залипания краев ран, плотной и тугой повязки — 12%; неправильно проведенная хирургическая обработка или поздно проведенная ампутация

(Рис. 2), когда клостридии уже начали распространяться по сосудам и мышцам — 20%.
Инкубационный период составлял от 3 час. (молниеносная форма) до 1–3 сут.
Газовая гангрена чаще была представлена двумя формами: клостридиальным целлюлитом (58%) и клостридиальным мионекрозом (42%). Важно максимально рано заподозрить анаэробную инфекцию, поскольку процесс развивается очень быстро и в запущенных случаях пострадавший делается инкурабельным.
Ее диагностика при изолированных ампутациях проводится по клиническим симптомам, однако в случаях политравмы она затруднена и при недостаточной настороженности может оказаться находкой на секционном столе, особенно у тяжелых пострадавших с черепномозговой травмой, изначально поступивших в коме и с нарушениями гемодинамики.
Первым делом у такого раненого нужно сделать перевязку и осмотреть рану культи конечности. Появление бледного отека с пятнами бронзового цвета, крепитация и тимпанит, скудное серозно-геморрагическое отделяемое, иногда с пузырьками газа из раны (Рис. 3) должны сразу насторожить врача.
Швы должны быть немедленно распущены, рана рыхло тампонирована тампонами с 3% раствором перекиси водорода. Наличие на рентгенограмме пузырьков газа, распространяющегося по ходу магистральных сосудов, клостридий, обнаруженных при срочной бактериоскопии, подтверждают подозрения. Однако у пациентов, получающих массивную антибактериальную терапию, развитие анаэробной инфекции может проходить атипично и более медленно.
Чем раньше начато лечение анаэробной инфекции, тем больше надежды на спасение жизни пострадавшего (Рис. 4).
Фундаментальным приоритетом в успехе терапии анаэробной инфекции и снижения летальности от нее является ранняя диагностика, своевременное хирургическое вмешательство в сочетании с дополнительным комплексным лечением гипербарической оксигенациией, мощной антибиотикотерапией, массивной инфузионной терапией.
УЗИ пораженных сегментов конечности, позволяет подтвердить диагноз анаэробной инфекции на основании обнаружения отечных, лишенных кровотока, некротизированных мышц, а КТ и МРТ в ряде случаев — заподозрить деструкцию мягкотканных структур и так же, как рентгенологическое исследование, обнаружить газ в жировой клетчатке или мышцах.
Пункционная биопсия мышц для гистологического исследования, микроскопия в поляризованном свете и электронная микроскопия позволяют констатировать развитие некробиотических процессов в поврежденной ткани только в определенный промежуток времени. Эти методы могут служить лишь подтверждением данных других методов диагностики. К сожаления на достовер-
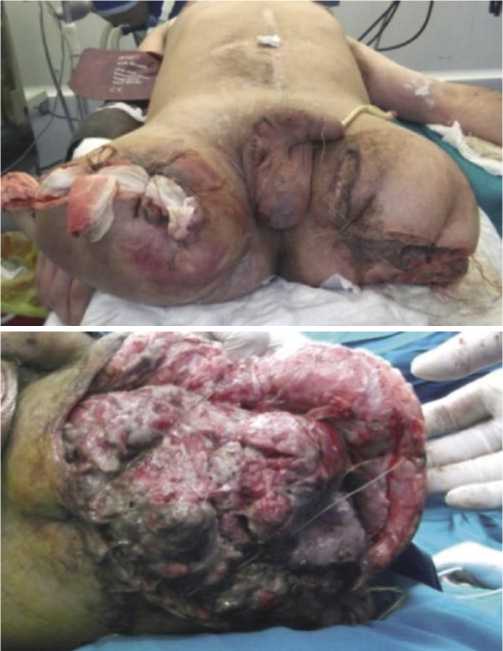
Рис. 2. Неполноценно проведенная ампутация обеих бедер при МВТ, с исходом в анаэробный целлюлит и миозит.
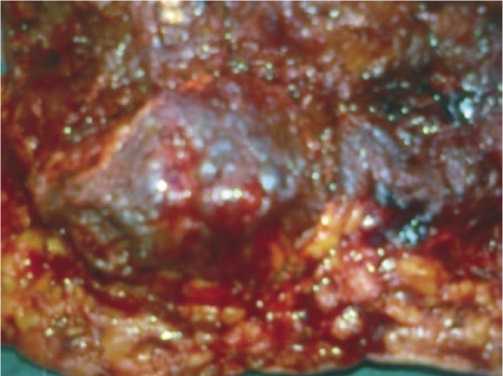
Рис. 3. Вид раны культи голени с участками мышечного некроза, серозногеморрагическим отделяемым и пузырьками газа.
ность при исследовании образцов биопсии также влияют ошибки, связанные с выполнением диагностического разреза в стороне от нежизнеспособных тканей.
Современные принципы лечения базируются на хирургическом методе, введении антибиотиков направленного действия и проведении гипербарической терапии. Эти принципы воплощают в жизнь на фоне современной
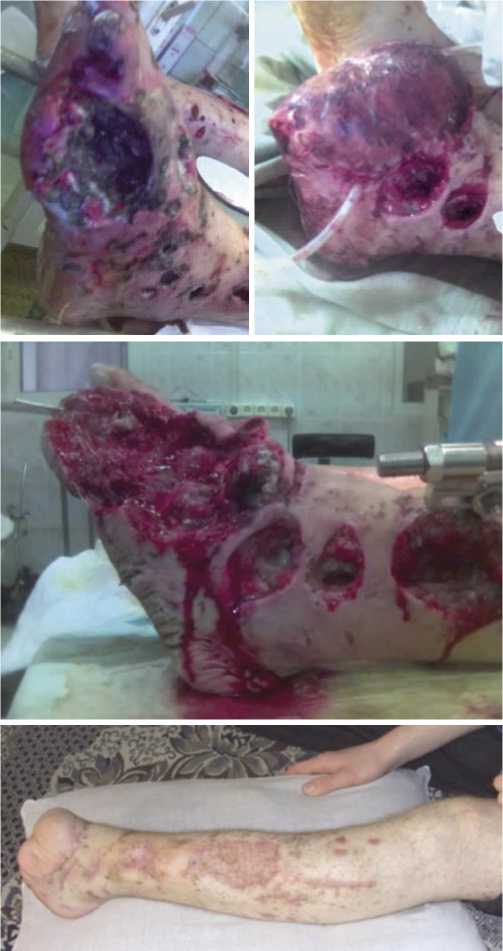
Рис. 4. Удачный исход клостридиального мионекроза левой стопы при МВТ.
интенсивной терапии. Как только заподозрена анаэробная инфекция культи, пострадавшего направляли в отдельную изолированную операционную и производили ревизию раны культи. При клостридиальном мионекрозе поражались все ткани культи. Подкожная клетчатка резко отечна, мышцы бледно-красные, сухие, из раны вытекала отечная жидкость серозно-геморрагического характера с неопределенным запахом, в умеренном количестве. Делали повторно мазки из отделяемой жидкости, подкожной клетчатки и разлагающихся мышц. После этого решали вопрос о дальнейшей тактике. Рассечение фасции культи и вскрытие межмышечных пространств при газовой инфекции, как это делают при банальной флегмоне, не дают эффекта, так как мышцы буквально пронизаны клостридиями, которые продолжают бурно распространяться.
Особенности ампутации при анаэробной инфекции: – при нежизнеспособной конечности уровень ампутации определяется уровнем погибших мышц, операция производится с элементами хирургической обработки с целью сохранения жизнеспособных тканей, необходимых для последующего закрытия раны;
– обязательно выполняется широкое раскрытие всех фасциальных футляров пораженных групп мышц на культе;
– целесообразно предварительно перевязывать магистральные сосуды на уровне, сохраняющем кровообращение культи, а жгут по возможности не применять;
– операция проводятся только под общим обезболиванием;
– независимо от типа операции недопустимо наложение швов на рану;
– необходимы повторные плановые ежедневные оперативные ревизии (под наркозом) раны с некрэктомией вплоть до полного очищения раны.
Только реампутация, а при необходимости и экзар-тикуляция конечности в пределах здоровых или слабо инфицированных тканей при наличии анаэробной инфекции дает шанс пострадавшему на выживание (Рис. 5).
Для решения вопроса об уровне реампутации (после смены перчаток), делали 2–3 диагностических разреза (инцизии) длиной до 5–7 см в проксимальной части пострадавшего сегмента конечности, с последующей ревизией жировой клетчатки, фасций и мышц, с биопсией пораженных тканей (Рис. 6).
Если мышечные ткани не изменены, обычного цвета, кровоточат, газ не выделяется, то раны тампонировали салфетками с 3% раствором перекиси водорода и делали разрез посредине расстояния между верхней третью сегмента конечности и уровнем ампутации. Если там мышцы не поражены, то это был примерный уровень ампутации. В пользу некротического целлюлита говорили очаги расплавления, характерный серый или грязно-серый цвет тканей и серозно-гнойное буроватого цвета отделяемое, часто с резким неприятным запахом. Резко отечные, цвета «вареного мяса», не кровоточащие и не сокращающиеся при раздражении мышцы указывали на клостридиальный мионекроз. После этого рану культи тампонировали салфетками с перекисью водорода, культю заворачивали в стерильную простыню. Грубейшими ошибками являются выполнение реампутации той же операционной бригадой без смены белья, инструментов и изоляции культи, а также определение уровня ампутации путем рассечения тканей культи проксимально до появления внешне здоровых мышц.
Вся бригада полностью меняла операционное белье, инструменты сбрасывала и полностью заменяла новыми. Обрабатывали и вновь перекрывали операционное поле. После этого производили реампутацию с предварительной перевязкой магистральных сосудов на уровне здоровых мышц. Накладывать жгут при газовой гангрене не-
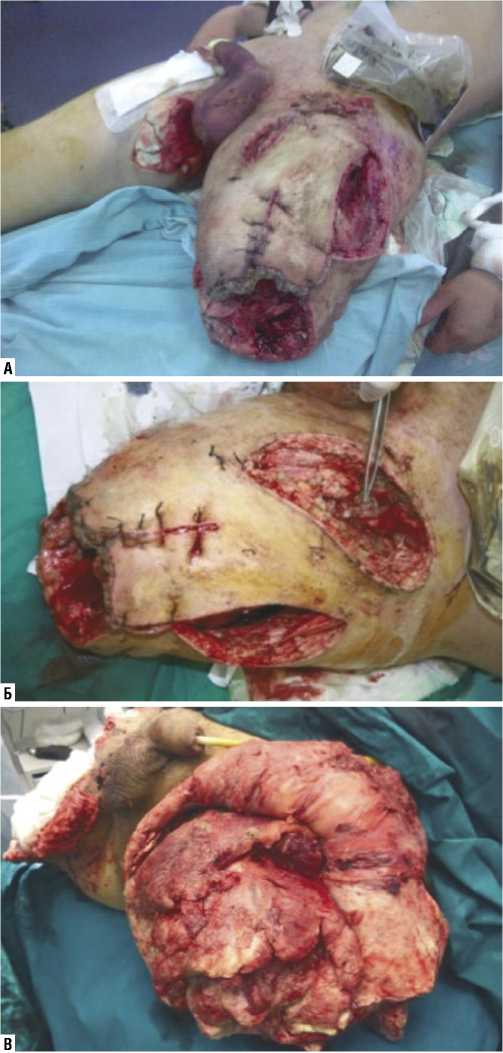
Рис. 5. А, Б — реампутация левого бедра с разрезами на проксимальных участках при МВТ, осложненной анаэробной инфекцией для определения правильности выбранного уровня; В — экзартикуляция.
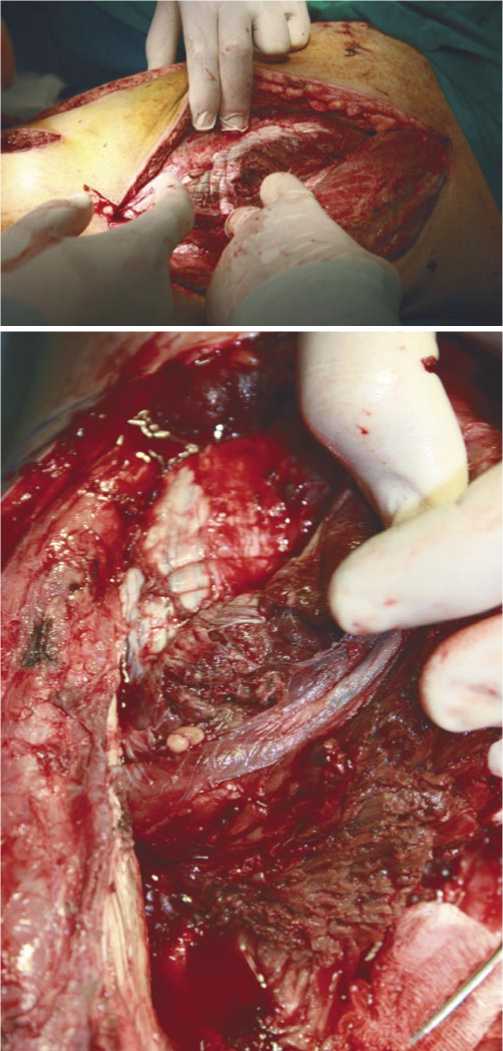
Рис. 6. Отрыв нижней конечности при МВТ на уровне нижней трети бедра. Выявление нежизнеспособных мышц при проведении диагностических разрезов проксимального участка сегмента конечности.
допустимо. При необходимости производили лампасные разрезы на проксимальном сегменте конечности, широко рассекая фасцию (Рис. 7) и после гемостаза рану рыхло тампонировали салфетками с перекисью водорода.
Результаты сопоставления скорости тотального окрашивания (T2) мышц передней (чаще m. vastus lateralis) и задней (чаще m. semimembranosus) групп конечности с частотой основных ранних послеоперационных осложнений показали, что чем быстрее происходило тотальное окрашивание участков мышц на уровне ампутации, тем выше была вероятность развития в раннем послеоперационном периоде осложнений, обусловленных некрозом мышц.
Как правило при сниженной активности фермента начальные изменения происходят на 1–2-й минуте в виде прокрашивания отдельных волокон. Затем на 4–10-й минуте в зависимости от степени ишемии появляются темно-синие участки. Нежизнеспособные мышцы сразу
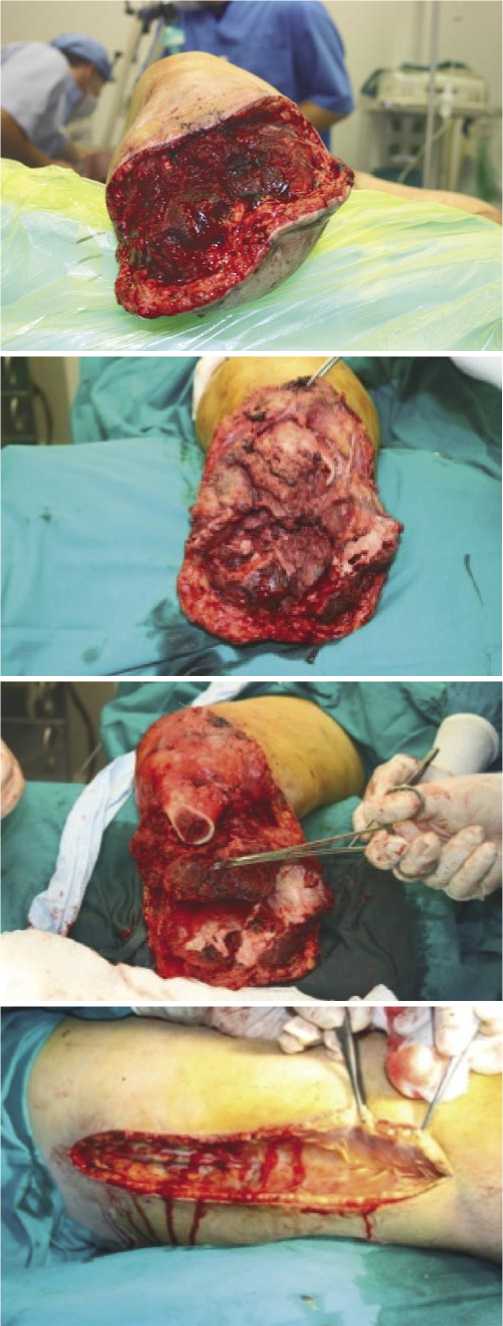
Рис. 7. Реампутация правой голени с лампасными разрезами на бедре при анаэробном целлюлите культи голени и бедра.
окрашиваются в темный, почти черный цвет, в то время как здоровые ткани не дают положительной реакции, сохраняя первоначальную окраску. Данный процесс наблюдается вплоть до 12–15-й минуты, после чего реакция окрашивания каскадным образом происходит во всех взятых на пробу участках мышц. Скорость реакции фиксировали по времени тотального окрашивания фрагмента мышечной ткани. Так, при скорости окрашивания мышечного биоптата 3–5 минут частота мионекроза составила 75%, 5–7 минут — 80%, в тех случаях, когда для образования формазана требовалось 10–14 минут, данное осложнение отмечалось лишь в 16,7% наблюдений.
Другими словами, частота возникновения ишемического некроза выше у пациентов с меньшим Т2 и наоборот, чем больше Т2, тем частота ишемического некроза ниже. Таким образом скорость тотального окрашивания фрагмента мышцы Т2, может считаться информативным показателем в прогнозировании ранних послеоперационных осложнений. Чем медленнее прокрашивается участок мышцы, тем ниже вероятность ее некроза. Параллельно с интраоперационным гистохимическим определением активности дегидрогеназ мышечной ткани нами было выполнено гистологическое исследование соответствующих участков мышц.
При гистологическом исследовании мышечной ткани на уровне ампутации нами были выявлены изменения, характерные для ишемии тканей различной степени. При скорости тотального окрашивания мышечной ткани более 10 минут, как правило, гистологические признаки ишемического некроза не определялись — отмечалось сохранение структуры миоцитов, в некоторых наблюдениях определялись явления интерстициального отека, микротромбы и признаки стаза в капиллярах. При тотальном окрашивании участка мышечной ткани в течение 6-10 минут определялись гистологические признаки ишемии различной степени в виде исчезновения поперечной исчерченности миоцитов, набухания и глыбчатости цитоплазмы, нечетких границ клеточных ядер. В артериях мелкого калибра и капиллярах выявлялись стазы крови, микротромбы и микрокровоизлияния с разрывом мелких сосудов. При этом на ранних сроках развития осложнения лейкоцитарная инфильтрация была выражена слабо. Для мышечной ткани, в которой образование формазанов происходило в течение 4–6 мин., более характерной была гистологическая картина выраженной ишемии, сопровождавшейся нарушением клеточной структуры мышечной ткани, кариолизисом, появлением участками некроза мышечной ткани, проявлявшимися в виде мио-маляции и фокусов полиморфноядерной лейкоцитарной инфильтрации.
Данные гистологического исследования биоптатов подтверждают надежность самой методики и выбранных нами критериев положительной реакции.
Как показали наши исследования, данные изменения коррелировали как со скоростью макроскопического гистохимического определения активности дегидрогеназ
мышечной ткани, так и с частотой ранних послеоперационных осложнений.
Полученные предварительные данные свидетельствуют об информативности макроскопического гистохимического экспресс-метода оценки активности лактатдегидрогеназы мышечной ткани для определения степени ишемии скелетной мышцы и для прогнозирования развития ишемического некроза, как раннего послеоперационного осложнения при ампутации нижних конечностей по поводу МВТ. Применение данного метода позволяет оценить степень ишемических изменений до появления «классических» признаков некробиоза в виде «мраморности» окраски, отека подкожной клетчатки, наличия тромбов в просветах артерий и вен, отсутствия кровоточивости, слабой реакции мышцы на раздражение электрокоагулятором. Полученные нами данные о соответствии результатов НСТ-теста и гистологической картины различных стадий ишемического некроза тканей конечности подтверждают значение предлагаемого экспресс-метода как объективного показателя жизнеспособности тканей.
Высокая скорость проведения реакции (максимальное время не превышало 15 минут) делает возможным использование метода в качестве интраоперационного критерия оценки жизнеспособности тканей и окончательного определения хирургической тактики. Так, с целью профилактики послеоперационных осложнений возможно во время ампутации иссечение отдельных мышц, когда наблюдается быстрое тотальное окрашивание биоптатов этих мышц, либо выполнение более проксимальной ампутации, при одинаково малом времени наступления тотального окрашивания во всех мышцах на выбранном уровне ампутации.
Таким образом, можно говорить о данном методе как об объективном инструменте, позволяющем количественно оценить степень жизнеспособности мышечной ткани до появления макроскопических изменений. Можно предположить, что после окончательной отработки методики, в том числе определения значений показателей положительной реакции гистохимической идентификации ишемии других мышц нижней конечности, предлагаемый метод займет место в широкой хирургической практике, что позволит улучшить результаты лечения данной тяжелой группы пострадавших.
При подтверждении диагноза анаэробной инфекции проводились необходимые санитарно-эпидемиологические мероприятия: перевязочный материал и операционное белье собирали в герметичные мешки, надежно упаковывали и выбрасывали или сжигали. Инструменты после мытья и двукратного замачивания в антисептиках автоклавировали, дважды производили генеральную уборку операционной. К работе в ней приступали после двукратных отрицательных бактериологических посевов.
До и после операции пострадавшего с анаэробной инфекцией изолировали в отдельном боксе с отдельным обслуживающим персоналом, бельем, перевязочным материалом и инструментом.
Антибиотики широкого спектра действия в той или иной степени обладают антиклостридиальным свойством, но их основная заслуга состоит в том, что они уничтожают другую патогенную флору, с которой часто состоят в ассоциации анаэробные бактерии. Банальная флора при размножении использует много кислорода, создавая условия для размножения клостридий. Для профилактики и лечения анаэробной инфекции необходимо применять те антибиотики, которые направленно действуют против анаэробов. К ним относятся препараты группы клиндамицина и ванкомицина. Они являются антибиотиками выбора для профилактики и лечения этой жизнеопасной инфекции.
Еще одно мощное средство борьбы с анаэробной инфекцией — гипербарическая оксигенация. Пассивная иммунизация антигангренозными сыворотками, которая ранее широко пропагандировалась, себя не оправдала и нами не проводилась.
Цель открытого ведения раны культи в течение 3-5-и суток — это профилактика хирургической инфекции культи, ликвидация условий для развития воспалительного процесса (повторные хирургические обработки, включающие в себя при необходимости проведение в ране некрэктомии, гемостаза, санации антисептиками).
По нашим данным, средний срок пребывания пациентов после МВТ, при данном виде осложнения в I группе составил 95,7±7,2 койко-дней, во II группе — 64,8±2,1 койко-дней, что на 30,9 суток больше, чем у раненых с неосложненным течением послеоперационного периода. Длительность стационарного лечения была высокой, в связи с: консолидацией переломов и множественными повреждениями сохранившейся конечности при МВТ, дополнительным временем для проведения курса восстановительного лечения, подготовкой пораженного сегмента к протезированию; проведением военно-врачебной комиссии и первичного протезирования. В дальнейшем эти военнослужащие, по их желанию продолжали военную службу на других должностях и им проводилось репротезирование конечностей за счет бюджета войск.
Летальность пострадавших с МВТ конечностей, осложненная анаэробной инфекцией составила 11,1%: в I группе исследования отмечена у 15 (15,3%) раненых, во II группе исследования — у 7 (6,9%). При одновременной ампутации двух конечностей двумя бригадами летальность отмечена в 50% случаев.
Выводы
-
1. Анаэробная инфекция при МВТ конечностей встречается у 15,1% раненых и вопреки общепринятому мнению, протекает при не ярко манифестированной клинической картине заболевания, что является причиной позднего хирургического лечения. Только динамика изменений местных проявлений и нарастание
-
2. Особенностью течения раневого процесса у пострадавших с анаэробной инфекцией конечностей при МВТ является пролонгированная до 14–15 суток I фаза раневого процесса, сопровождающейся высоким содержанием микробных и тканевых метаболитов.
-
3. Повторные плановые ежедневные хирургические ревизии раны культей конечности с некрэктомией вплоть до полного очищения раны являются важнейшим элементом профилактики развития анаэробной инфекции.
-
4. Разработанный интраоперационный экспресс-метод оценки активности лактатдегидрогеназы скелетных мышц, а также экспресс гистологическое исследование биоптатов мышц при проведении дополнительных инцизий в проксимальном отделе поврежденного сегмента конечности позволяют объективно оценить жизнеспособность тканей на уровне ампутации, а его применение будет способствовать объективизации выбора уровня и техники ампутации и, таким образом, снижению частоты ранних послеоперационных осложнений.
-
5. Применение предварительной ампутации конечности c использованием диагностических разрезов гистохимической идентификации ишемии тканей с целью оценки жизнеспособности тканей конечности и забора мышечной ткани для проведения экспресс гистологического исследования у раненых с МВТ позволило уменьшить число реампутаций, количество анаэробной инфекции с 19,4% до 10,9%, сроки лечения раненых и летальность в два раза, с 15,3 до 6,9%, привело к значительному росту количества органосохраняющих ампутаций на уровне голени с 53,6% до 62,2%.
-
6. Основной причиной летальности в первые двое суток при анаэробной инфекции является инфекционнотоксический шок (27%).
интоксикации позволяла заподозрить анаэробную инфекцию и решить вопрос в пользу экстренного хирургического вмешательства.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Анаэробная инфекция при минно-взрывной травме конечностей
- Горюнов С.В., Ромашов Д.В., Бутивщенко И.А., Ульянина А.А. Особенности клиники, диагностики и лечения больных с обширной анаэробной флегмоной мягких тканей. В кн.: Стандарты диагностики и лечения в гнойной хирургии. Тезисы докладов. - М., 2001. -С. 174-175.
- Goryunov SV, Romashov DV, Butivshchenko IA, Ul'yanina AA. Osobennosti kliniki, diagnostiki i lecheniya bol'nykh s obshirnoi anaerobnoi flegmonoi myagkikh tkanei. In: Standarty diagnostiki i lecheniya v gnoinoi khirurgii. Tezisy dokladov. Moscow, 2001. pp 174-175. (In Russ).
- Ерюхин И.А. Хирургические инфекции: новый уровень познания и новые проблемы // Инфекции в хирургии. - 2003. - Т. 1. - №1. - С. 2-7.
- Eryukhin IA. Khirurgicheskie infektsii: novyi uroven' poznaniya i novye problemy. Infektsii v khirurgii. 2003;1(1):2-7. (In Russ).
- Косачев И.Д., Ткаченко С.С., Дедушкин В.С. Взрывные повреждения // Воен.- мед. журн. - 1991. - №8. - С. 12-18.
- Kosachev ID, Tkachenko SS, Dedushkin VS. Vzryvnye povrezhdeniya. Voen.- med. zhurn. 1991;(8):12-18. (In Russ).
- Лежнев К.К. Сравнительная оценка методов определния жизнеспособности мягких тканей при огнестрельных повреждениях. Дис. … канд. мед. наук. - Л., 1990. - С. 19.
- Lezhnev KK. Sravnitel'naya otsenka metodov opredelniya zhiznesposobnosti myagkikh tkanei pri ognestrel'nykh povrezhdeniyakh. [dissertation] Leningrad; 1990. P. 19. (In Russ).
- Милюков В.Е., Полунин C.В. Современные методы определения жизнеспособности мышечной ткани при выборе объема операции // Хирургия. - 2011. - №4. - С. 73-77.
- Milyukov VE, Polunin CV. Sovremennye metody opredeleniya zhiznesposobnosti myshechnoi tkani pri vybore ob"ema operatsii. Khirurgiya. 2011;(4):73-77. (In Russ).
- Чехович Г.Г., Чаплинский В.В., Сюч М.И. Определение жизнеспособности механических повреждений мышечной ткани // Клин. Хир. - 1987. - №1. - С. 41-42.
- Chekhovich GG, Chaplinskii VV, Syuch MI. Opredelenie zhiznesposobnosti mekhanicheskikh povrezhdenii myshechnoi tkani. Klin. Khir. 1987;(1):41-42. (In Russ).
- Beazley RM, Polakavetz SM, Miller RM. Bacteroides infections a university surgical service. Surg., Gynec., Obstet. 1972;135(5):742-746.


