Анализ цитотоксичности гуминовых веществ пелоидов
Автор: Жернов Юрий Владимирович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Средства коррекции экологического неблагополучия
Статья в выпуске: 1-8 т.13, 2011 года.
Бесплатный доступ
В статье рассмотрены результаты анализа цитотоксичности всех фракций гуминовых веществ пелоидов с помощью методики МТТ-диагностики. МТТ-тест проводился на клетках Т-лимфомы линии KE37.1-IIIB. Была использована спектрофотометрическая регистрация при длине волны 570 нм прибором ИФА-ридером Tecan Infinite M200. На основании полученных экспериментальных данных определено, что гуминовые, гиматомелановые, фульвовые и гумусовые кислоты не обладают выраженной цитотоксичностью в интервале исследуемых концентраций.
Гуминовые вещества, пелоиды, цитотоксичность
Короткий адрес: https://sciup.org/148199951
IDR: 148199951 | УДК: 57.083.37
The analysis of peloids humic substances cytotoxicity
In article results of the analysis of cytotoxicity of all fractions of peloids humic substances by means of MTT-diagnostics DIAGNOSTICS technique are considered. The MTT-assay was spent on T-limfomy cells of line KE37.1-IIIB. It was used spectrophotometrical registration at wave length of 570 nanometers by the device IFA-reader Tecan Infinite M200. On the basis of the received experimental data it is defined that humic, hymatomelanic, fulvic acids and humic acids don't possess the expressed cytotoxicity in the range of investigated concentration.
Текст научной статьи Анализ цитотоксичности гуминовых веществ пелоидов
С момента открытия гуминовых веществ Францем Карлом Ахардом прошло 225 лет. За этот период был накоплен значительный материал по структуре и свойствам этих веществ, была определена их биологическая значимость для организма животных и человека. Уже в 1988 г. доктор медицины С.А. Виссер в своем выступлении на съезде Международного гуминового общества в Севилье (Испания) докладывал о возможности эффективного наружного и внутреннего применения гуминовых веществ при лечении ряда тяжелых заболеваний. На сегодняшний день доказаны многочисленные терапевтические эффекты гуминовых веществ: противовоспалительный, обезболивающий, противоотечный, гиперемический, антиревматический, антиоксидантный, антимикробный, противоопухолевый и другие. Но до сих пор в Российской Федерации не зарегистрировано в качестве лекарственного средства ни одного препарата, содержащего гуминовые вещества. В первую очередь это связано с их сложной нестехиометрической структурой. Данная проблема отягощается тем, что до сих пор не проведены исследования по оценки лекарственной цитотоксичности гуминовых веществ.
Цель исследования: оценка цитотоксичности природных высокомолекулярных органических соединений – гуминовых веществ пелоидов.
Объект исследования: фракции гуминовых веществ низкоминерализованных иловых сульфидных грязей (пелоидов): гуминовые (ГК), гиматомелановые (ГМК), фульвовые (ФК)
и гумусовые (ГсК) кислоты, которые различаются технологией извлечения из нативной грязи [1].
Гуминовые вещества относятся к поли-молекулярным полидисперсным соединениям нестехиометрического состава, имеющим стохастическое строение и включающим в свою структуру большинство известных функциональных групп органических соединений: карбонильные, спиртовые, карбоксильные, аминные и другие (рис. 1) [2].
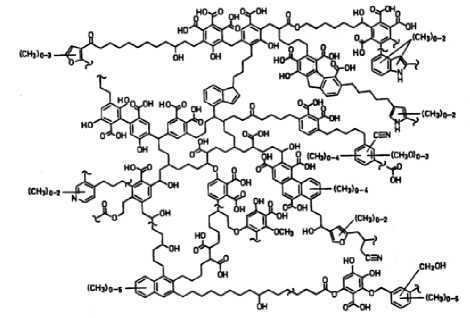
Рис. 1. Структурный фрагмент молекулы гуминовых кислот (по Schulten, 1994)
Для количественного описания структуры изучаемых в работе гуминовых веществ пелоидов можно использовать набор параметров, включающих в себя атомные отношения конституционных элементов и их распределение между основными структурными фрагментами (табл. 1).
Материалы и методы. В данной работе использовался МТТ-тест (MTT-assay), широко применяемый в клинико-лабораторных и экспериментальных исследованиях для оценки клеточной и лекарственной цитотоксичности. Данный тест основан на способности группы ферментов, катализирующих окислительновосстановительные реакции – митохондриальных и цитоплазматических дегидрогеназ живых метаболически активных клеток, конвертировать и восстанавливать производные тетразолия – бесцветный водорастворимый 3-(4,5- диметилтиазол-2-ил)-2,5-дифенил-2Н-тетразо-лиум бромид (синоним МТТ, желтый тетразол) в формазан (рис. 2) [3].
Таблица 1. Элементный состав, степень окисленности, бензоидности и коэффициенты экстинкции гуминовых веществ пелоидов
|
Определяемый показатель |
Фракции гуминовых веществ пелоидов |
|||||
|
ФК |
ГМК |
ГК |
ГсК |
|||
|
02 О К “ ч н О О ° О ° ’S Й а 5 5 о к ® Н н о Я 5 Й и m о |
углерод |
масс. |
28,58 ± 0,17 |
59,49 ± 0,19 |
55,18 ± 1,70 |
55,78 ± 0,01 |
|
мольн. |
19,01 ± 0,15 |
40,20 ± 0,17 |
42,89 ± 0,20 |
41,60 ± 0,74 |
||
|
водород |
масс. |
6,18 ± 0,19 |
5,22 ± 0,12 |
3,56 ± 0,36 |
4,01 ± 1,30 |
|
|
мольн. |
49,34 ± 1,60 |
42,33 ± 0,05 |
33,21 ± 0,24 |
35,88 ± 1,42 |
||
|
азот |
масс. |
2,10 ± 1,84 |
1,83 ± 1,69 |
5,16 ± 0,79 |
4,16 ± 0,91 |
|
|
мольн. |
1,20 ± 0,67 |
1,06 ± 0,54 |
3,44 ± 0,14 |
2,66 ± 0,58 |
||
|
кислород |
масс. |
58,90 ± 0,61 |
31,26 ± 0,14 |
34,10 ± 0,16 |
34,97 ± 0,14 |
|
|
мольн. |
29,36 ± 0,14 |
15,84 ± 0,05 |
19,88 ± 0,05 |
19,56 ± 0,07 |
||
|
сера |
масс. |
4,24 ± 1,47 |
2,2 ± 0,17 |
2,00 ± 0,01 |
1,08 ± 0,32 |
|
|
мольн. |
1,06 ± 0,16 |
0,56 ± 0,05 |
0,58 ± 0,25 |
0,30 ± 0,46 |
||
|
Н/С |
2,59 |
1,05 |
0,77 |
0,86 |
||
|
О/С |
1,55 |
0,39 |
0,46 |
0,47 |
||
|
степень окисленности |
+0,50 |
-0,26 |
+0,15 |
+0,08 |
||
|
степень бензоидности |
6,87 |
20,01 |
32,69 |
20,97 |
||
|
коэффициент экстинкции |
7,50 |
5,30 |
2,70 |
2,60 |
||
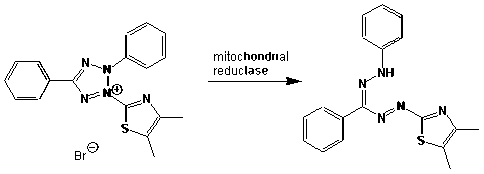
Рис. 2. Реакция перехода желтого тетразола (МТТ) в формазан, под действием митохондриальной редуктазы
Формазан кристаллизуется внутри клетки в виде фиолетово-голубых кристаллов. Перевод кристаллов формазана в раствор осуществляют с помощью подходящих органических растворителей, таких как, диметилсульфоксид (ДМСО), додецилсульфат натрия или изопропанол. Последующая спектрофотометрия этого раствора позволяет точно сопоставить изменение оптической плотности по отношению к контролю с изменением количества жизнеспособных клеток, а в цитотоксических исследованиях оценить специфическую гибель клеток, индуцированную тем или иным цитотоксическим агентом [4]. В качестве тест-культуры служили человеческие клетки Т-лимфомы линии KE37.1-IIIB. Клетки культивировали в модифицированной среде Dulbecco's Eagle's Medium (DME), содержащей 10% эмбриональной телячьей сыворотки, 4мМ L-глютамина, 1,5 г/л бикарбоната натрия, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина, при 37оС во влажной атмосфере с 5% СО2 [5]. Оценка гибели клеток линии KE37.1-IIIB, индуцированной гуминовыми веществами, проводилась с помощью ИФА-ридера Tecan Infinite M200. Для этого в лунки 96-луночной плоскодонной культуральной планшеты вносили по 100 мкл суспензии клеток (~105 кл/мл) и 100 мкл исследуемой концентрации (с учетом разбавления в лунке) препарата гуминовых веществ. Планшеты инкубировали в течение 24 часов. За 4 часа до окончания инкубационного периода вносили МТТ. МТТ-тест проводили по методике Niks M. и Otto M. [5]. В каждую лунку планшеты с клеточными суспензиями вносили 20 мкл раствора МТТ (5 г/л) и инкубировали на протяжении 4 ч при 37оС в темноте во влажной атмосфере c 5% СО2. По окончании инкубации супернатант осторожно удаляли с помощью планшетного насоса, а в каждую лунку добавляли по 200 мкл ДМСО. Осадок ресуспендировали и 10 мин инкубировали в темноте при комнатной температуре. Показания оптической плотности считывали на ИФА-ридере Tecan Infinite M200 при длине волны 570 нм. Гибель Т-лимфомных клеток рассчитывали путем сравнения оптической плотности контроля среды, принятой за 100%, с оптической плотностью в опытных пробах. Цитотоксичность исследуемое вещество проявляет, если его процентный показатель оптической плотности меньше 70%. Если показатель оптической плотности превышает 70%, то данное вещество не проявляет выраженной токсичности на культуру клеток.
Результаты. МТТ-тест показал, что все исследуемые фракции гуминовых веществ пе-лоидов в исследуемом интервале концентраций от 1% до 0,00125% не оказывают выраженную цитотоксичность к клеткам Т-лимфомы человека линии KE37.1-IIIB (рис. 3). Кроме этого, в ходе эксперимента было выявлено, что гуминовые вещества пелоидов усиливают протекторную функцию исследуемой тест-культуры, так как их показатели оптической плотности превышают показатели контроля. Наибольшим протекторным эффектом обладает фракция гиматомелановых кислот пелоидов.
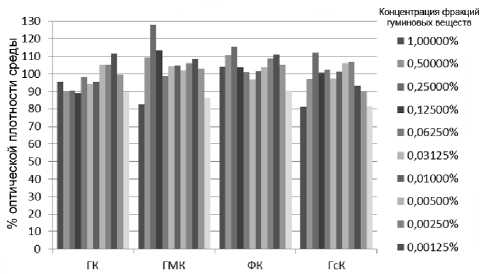
Рис. 3. Диаграмма показателей МТТ теста фракций гуминовых веществ пелоидов
Выводы: гуминовые, гиматомелановые, фульвовые и гумусовые кислоты пелоидов не обладают выраженной цитотоксичностью в интервале исследуемых концентраций, что дает возможность создания на их основе лекарственных фармако- и химиотерапевтических препаратов различного назначения. Отсутствие выраженной цитотоксичности гуминовых веществ пе-лоидов может быть обусловлена тем, что формирование живых систем организмов в процессе эволюции происходило именно в гуминовом фоне. Естественный гуминовый фон не оказывает неблагоприятного влияния на организм человека, а выполняет защитную функцию, выступая в качестве совокупности экзогенных антиоксидантных и протективных факторов.
Работа выполнена при поддержке гранта Международного гуминового общества (IHSS) на базе Институтов вирусологии и экологической химии (Institut für Ökologische Chemie (IOEC), Institut für Vi-rologie (VIRO)) Гельмгольц-Центра Мюнхен (Helmholtz Zentrum München) в 2011 г.
Список литературы Анализ цитотоксичности гуминовых веществ пелоидов
- Аввакумова, Н.П. Пелоидопрепараты как средство повышения эффективности пелоидотерапии. Сообщение 2. Способ получения пелоидопрепаратов гуминового ряда/Н.П. Аввакумова, Е.К. Баталова, А.И. Агапов//Вопросы курортологии, физиотерапии и лечебной физкультуры. 1999. № 2. С. 74-77.
- Чуков, С.Н. Структурно-функциональные параметры органического вещества почв в условиях антропогенного воздействия//СПб., Санкт-Петербургский государственный университет, 2007. С. 142.
- Mosmann, Tim. Rapid colorimetric assay for cellular growth and survival: application to proliferation and cytotoxicity assays//J. Immunol. Methods. 1983. Vol. 65 (1-2). Р. 55-63.
- Kremb, S. EASY-HIT: HIV Full-Replication Technology for Broad Discovery of Multiple Classes of HIV Inhibitors/S. Kremb, M. Helfer, W. Heller et al.//Antimicrobial Agents and Chemotherapy. December 2010. Vol. 54, No. 12. P. 5257-5268.
- Niks, M. Towards an optimized MTT assay/M. Niks, M. Otto//J. Immunol. Meth. 1990. Vol. 130, № 1. P. 149-151.


