Анализ данных оптической когерентной томографии у пациентов с различными вариантами глаукомного процесса
Автор: Калинин М.Е., Файзрахманов Р.Р., Павловский О.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.18, 2023 года.
Бесплатный доступ
Одним из важных аспектов в лечение глаукомы является, получение целевых показателей внутриглазного давления. Однако, необходимо учитывать состояния переднего отрезка глаза при проведении оперативного лечения пациентов с различными вариантами глаукомного процесса. Для повышения эффективности и безопасности дальнейшего хирургического лечения, стоит обратить внимание на данные оптической когерентной томографии переднего отдела глаза, на которой можно оценить состояние угла передней камеры, положение интраокулярной линзы. Был проведен анализ снимков оптической когерентной томографии 51 пациентов (51 глаз), были выявлены основные аспекты для дальнейшего использования при выборе тактики оперативного вмешательства.
Глаукома, вторичная глаукома, оптическая когерентная томография переднего отрезка глаза
Короткий адрес: https://sciup.org/140303514
IDR: 140303514 | DOI: 10.25881/20728255_2023_18_4_S1_90
Analysis of optical coherence tomography data in patients with various variants of the glaucoma process
One of the important aspects in the treatment of glaucoma is obtaining target values of intraocular pressure. However, it is necessary to take into account the conditions of the anterior segment of the eye when performing surgical treatment of patients with various types of glaucomatous process. With the development of technology at this stage, optical coherence tomography can help us in performing this task, which can assess the condition of the anterior chamber angle. Optical coherence tomography images of 51 patients (51 eyes) were analyzed in order to improve the efficiency and safety of further surgical treatment.
Текст научной статьи Анализ данных оптической когерентной томографии у пациентов с различными вариантами глаукомного процесса
Главными факторами развития диабетической ретинопатии (ДР) являются микрососудистые нарушения, которые в свою очередь влекут за собой грозные последствия в виде прогрессирующей потери зрения [1]. Витрэктомия через плоскую часть цилиарного тела широко используется, как методика выбора при лечении далекозашедшей пролиферативной диабетической ретинопатии, при разрастании фиброваскулярной ткани и тракционной отслойки сетчатки, а также при кровоизлияниях в стекловидное тело. В данный момент широко используются препараты ингибиторы сосудистого эндотелиального фактора роста (Vascular endothelial growth factor – VEGF), которые значительно повысили эффективность и безопасность витреоре-тинальной и антиглаукомной хирургии у пациентов с ДР [2; 3].
На данный момент в хирургическом лечении глаукомы появились методики, которые направлены на минимизацию травматизации конъюнктивы и склеры. Традиционные циклодеструктивные и фильтрационные методы лечения эффективны при лечении глаукомы, но имеют ряд послеоперационных осложнений [4]. Это связано с повреждениями тканей, окружающих цилиарное тело во время процедуры, а также при формировании доступа ab-anterior происходит воздействие на склеру и конъюнктиву, и возможна разгерметизация, а также в отдаленном послеоперационном периоде зарастание сформированного нового пути оттока [5; 6].
Цель
Изучить параметры переднего отрезка глаза у пациентов с НВГ после ВРХ для дальнейшей разработки метода хирургического лечения, восстанавливающего естественное состояние угла передней камеры.
Материалы и методы исследования
Проведен анализ снимков оптической когерентной томографии 51 пациентов (51 глаз), средний возраст пациентов составил 63,2±16,1 года. Все пациенты были разделены на три группы: 1-я группа (19 глаз): пациенты с НВГ и диабетическим макулярным отеком после витре-оретинальной хирургии; 2-я группа (17 глаз): пациенты с первичной открытоугольной глаукомой; 3-я группа (15 глаз): артифакичные пациенты, группа контроля. Пациенты с другими типами глаукомы, а также пациенты, ранее перенесшие лазерное и хирургическое лечение глаукомы, были исключены.

Результаты и обсуждение
Для детального исследования морфологических параметров переднего отдела глаза были определены показатели, характеризующие положение радужки, изменение угла передней камеры, расстояние от радужки до ИОЛ (Рис. 1). При анализе каждый показатель регистрировался в меридиане, который соответствует равномерному распределению относительно анатомической оси глаза от 1-го до 12-ти по типу распространения часов циферблата. Пристальное внимание было уделено секторам передней камеры, таким как верхний (superior –S), темпоральный (temporal – T), нижний (inferior – I) и назальный (nasalis – N), включающие S – 11, 12, 1 час, T – 2, 3, 4 часа, I – 5, 6, 7 часов, N – 8, 9, 10 часов.
Для определения тенденции угла передней камеры к сужению важным моментом является учет показателей, характеризующих положения радужки в нескольких осях. При изменении положения радужки относительно ИОЛ не исключено повышение ВГД. Вторым аспектом, характеризующим тенденции угла передней камеры к сужению, является показатель, определяющий степень открытости УПК в градусах. При изменении данных параметров может повышаться ВГД.
Для оценки состояния переднего отрезка у пациентов с неоваскулярной глаукомой с диабетическим макулярным отеком после витреоретинальной хирургии были
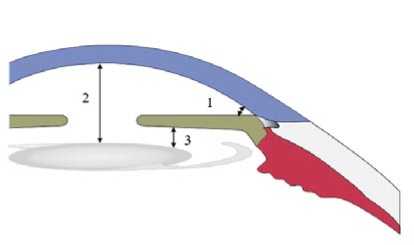
Рис. 1. Морфологические показатели переднего отрезка глазного яблока. Примечание: 1 – угол передней камеры глаза (УПК), 2 – глубина передней камеры от роговицы до края ИОЛ (ГПК), 3 – расстояние от радужки до ИОЛ в 2 мм от края оптической части ИОЛ (РИ).
проанализированы ранее указанные показатели УПК (табл. 1) и РИ (табл. 2). В качестве контроля были проанализированы идентичные показатели у пациентов с артифакией (группа контроля) и ПОУГ.
При обработке данных показатель УПК у пациентов группы 1 был достоверно ниже 23,79±10,22 градусов, чем у пациентов группы 2 который соответствовал 37,71±6,36 градусов и в группе 3 41,83±2,34 градусов (p = 0,027). Стоит отметить, что у пациентов группы 1 показатель УПК был меньше в 1,75 раза по сравнению с группой 2. Однако при анализе результатов в группе 2 с группой 3 по-
Табл. 1. Показатели угла передней камеры, градусы
|
S |
T |
I |
N |
|||||||||
|
УПК-11 |
УПК-12 |
УПК-1 |
УПК-2 |
УПК-3 |
УПК-4 |
УПК-5 |
УПК-6 |
УПК-7 |
УПК-8 |
УПК-9 |
УПК-10 |
|
|
23,79±10,22 |
24,41±11,94* |
21,91±10,58 |
22,22±9,85 |
23,30±10,04* |
23,87±8,99* |
24,65±9,96 |
21,21±11,23 |
24,98±10,23 |
23,56±8,87 |
24,21±9,68* |
21,84±8,74* |
|
|
til |
37,72±6,61 |
39,29±9,05 |
38,23±7,06 |
37,89±7,21 |
37,21±6,87 |
36,58±8,59 |
37,07±7,56 |
35,64±7,81 |
35,41±6,23 |
38,31±5,89 |
37,64±6,36 |
37,21±7,53 |
|
41,83±2,34 |
40,28±3,38 |
39,55±3,21 |
41,24±2,67 |
38,12±3,52 |
40,37±3,98 |
41,69±2,21 |
43,05±3,82 |
43,35±2,95 |
39,67±3,24 |
40,89±2,83 |
42,36±2,68 |
|
Примечание : УПК – угол передней камеры в градусах, УПК 1- УПК 12 – градация, соответствующая исследуемым меридианам, S – верхний сектор (superior), T – темпоральный сектор (temporalis), I – нижний сектор (inferior), N – назальный сектор (nasalis). * – p <0,05 в сравнении с данными пациентов группы B данные .оптической когерентной томографии.
Табл. 2. Расстояние от радужки до ИОЛ в 2 мм от края оптической части ИОЛ (РИ), в мкм
|
S |
T |
I |
N |
|||||||||
|
РИ-11 |
РИ-12 |
РИ-1 |
РИ-2 |
РИ-3 |
РИ-4 |
РИ-5 |
РИ-6 |
РИ-7 |
РИ-8 |
РИ-9 |
РИ-10 |
|
|
til |
986,8±126,78 |
1094,4±123,94* |
1121,3±115,81* |
928,1±121,67 |
1025,4±111,45* |
981,3±114,23* |
1085,9±128,11* |
988,4±131,29 |
976,5±124,74 |
1097,1±128,73* |
1004,9±116,65* |
943,4±126,99 |
|
706,98±73,78 |
625,9±52,05 |
683,5±64,24 |
701,8±81,25 |
585,1±68,36 |
633,5±58,47 |
651,3±64,21 |
728,6±58,35 |
658,4±61,37 |
598,8±69,74 |
625,4±52,48 |
711,8±61,58 |
|
|
716,78±62,96 |
654,28±73,31 |
597,1±68,36 |
627,6±57,58 |
687,5±58,47 |
586,4±72,21 |
626,7±61,56 |
638,28±65,76 |
724,28±68,11 |
618,28±75,33 |
701,28±63,79 |
655,28±69,48 |
|
Примечание : РИ – расстояние от радужки до ИОЛ в 2 мм от края оптической части ИОЛ, РИ 1- РИ 12 – градация, соответствующая исследуемым меридианам, S – верхний сектор (superior), T – темпоральный сектор (temporalis), I – нижний сектор (inferior), N – назальный сектор (nasalis).
* – p <0,05 в сравнении с данными пациентов группы B данные оптической когерентной томографии.
казатель УПК менее вариабельный в 1,1 раза. Данный аспект связан с тем, что в группе 1 появляется тенденция к сужению УПК за счет разрастания фиброваскулярной ткани.
При проведении секторальной оценки УПК выявлено достоверное отличие в меридианах 3, 4, 9, 10, 12. При сравнении секторального изменения показателей РИ и УПК определяется снижение вовлеченности в патологический процесс нижнего сектора, таким образом пролиферация УПК, характеризующаяся изменением положения радужки у пациентов группы 1, проходит неравномерно, данный аспект необходимо учитывать при проведения оперативного лечения пациентов этой категории. Тем не менее, несмотря на выявленную тенденцию, индивидуальный подход и диагностические мероприятия на дооперационном этапе являются обязательными.
При анализе указанных показателей у пациентов с НВГ с ДМО после ВРХ (группа 1) выявлено увеличение параметра РИ до 1086,8±116,78 мкм (p = 0,032) в сравнении с подобным показателем в группе 2, (p = 0,034) в сравнении с подобным показателем в группе 3, а у пациентов с ПОУГ (группа 2) до 663,51±58,91 мкм, в группе контроля до 656,78±62,96 мкм, показатели были сопоставимы.
При проведении секторального анализа показателя РИ достоверные изменения выявлены в следующих секторах 12, 1, 3–5, 8,9. При распределении данных меридиан на зону секторов определяется минимальная вовлеченность процесса сектора I, а также SI SN, учитывая, что ИОЛ имеет стабильное положение во всех случаях и во всех случаях не использовался альтернативный метод фиксации, подобная тенденция может быть основана на изменении гидродинамики и / или разной степени активности пролиферативного процесса. Для решения этой задачи основополагающим моментом является определение равномерности УПК при проведении ме-ридианальной и секторальной оценки.
ДР – наиболее частое микрососудистое осложнение сахарного диабета и в 4,8% всех случаев становится причиной слепоты [7–9]. При прогрессировании ДР происходит разрастание фиброваскулярной ткани и возникает риск развития тракционной отслойки сетчатки, в этом случае необходимо проведение витреоретинальных вмешательств, которые могут восстановить зрение и улучшить качество жизни пациента. Однако это может быть связано с множеством послеоперационных осложнений, одним из которых является развитие НВГ [10]. За последнее десятилетие быстрый прогресс в технологиях визуализации сетчатки и разработка новых методов лечения значительно улучшили результаты хирургического лечения пациентов с ДР [11–13].
Выводы
Таким образом, важно выделить основные значимые структурные различия между пациентами с разными вариантами глаукомного процесса.
Показатели РИ и УПК необходимо учитывать при проведения оперативного лечения пациентов и нужны методики хирургического лечения, которые учитывают эти факторы. Тем не менее, несмотря на выявленную тенденцию, индивидуальный подход и диагностические мероприятия на дооперационном этапе являются обязательными. Изменения показателей РИ и УПК у пациентов с НВГ связаны с разрастанием фиброзной и неоваскулярной мембраны, вследствие чего происходит ее подтягивание в сторону роговицы, эти параметры нужно использовать для определения тактики оперативного лечения, в результате чего будут устранены патофизиологические факторы возникновения и прогрессирования НВГ, снижение послеоперационных осложнений.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
doi: 10.1056/NEJMra1909637
Список литературы Анализ данных оптической когерентной томографии у пациентов с различными вариантами глаукомного процесса
- Tsiknakis N, Theodoropoulos D, Manikis G, et al. Deep learning for diabetic retinopathy detection and classification based on fundus images: a review. Comput Biol Med. 2021;135:104599. doi: 10.1016/j.compbiomed.2021. 104599
- Yokota R, Inoue M, Itoh Y, et al. Comparison of microincision vitrectomy and conventional 20-gauge vitrectomy for severe proliferative diabetic retinopathy. Jpn J Ophthalmol. 2015;59(5):288–294. doi: 10.1007/s10384-015-0396-y
- Smith JM, Steel DH. Anti-vascular endothelial growth factor for prevention of postoperative vitreous cavity haemorrhage after vitrectomy for proliferative diabetic retinopathy. Cochrane Database Syst Rev. 2015;2015(8):Cd008214. doi: 10.1002/14651858.CD008214.pub3
- Kaufman PL. Deconstructing aqueous humor outflow –The last 50 years. Exp Eye Res. 2020;197:108105.
- Ndulue JK, Rahmatnejad K, Sanvicente C, et al. Evolution of cyclophotocoagulation. J Ophthalmic Vis Res. 2018;13:55–61.
- Dave VP, Tyagi M, Narayanan R, et al. Intraocular endoscopy:A review. Indian J Ophthalmol. 2021;69:14–25.
- Resnikoff S, Pascolini D, Etya’ale D, et al. Global data on visual impairment in the year 2002. Bull World HealthOrgan.2004;82(11):844–51.
- Fong DS, Aiello LP, Ferris FR, et al. Diabetic retinopathy. Diabetes Care. 2004;27(10):2540–2553. doi: 10.2337/diacare.27.10.2540
- Yau GL, Silva PS, Arrigg PG, et al. Postoperative Complications of Pars Plana Vitrectomy for Diabetic Retinal Disease. Semin Ophthalmol. 2018; 33(1):126–133.doi:10.1080/08820538.2017.1353832
- Jampol LM, Glassman AR, Sun J. Evaluation and care of patients with diabetic retinopathy. N Engl J Med. 2020;382(17):1629–1637. doi: 10.1056/NEJMra1909637
- Файзрахманов Р.Р., Суханова А.В., Павловский О.А., Ларина Е.А. Роль ОКТ-ангиографии в исследовании ретинальной перфузии после эндовитреального вмешательства по поводу регматогенной отслойки сетчатки. Клиническая практика. 2020;11(3):61–67. [Fayzrakhmanov RR, Sukhanova AV, Pavlovsky OA, et al. The role of oct angiography in a study of retinal perfusion after endovitreal intervention due to rhegmatogenous retinal detachment. 2020;11(3):61–67. (In Russ).] doi:10.17816/clinpract33960
- Коновалова К.И., Шишкин М.М., Файзрахманов Р.Р. Эффективность многоэтапного хирургического лечения пролиферативной диабетической ретинопатии, осложненной начальной катарактой. Вестник офтальмологии. 2020;136(6):171–176. [Konovalova KI, Shishkin MM, Fayzrakhmanov RR. Effectiveness of multistage surgical treatment of advanced proliferative diabetic retinopathy complicated with primary cataract 2020;136(6):171–176. (In Russ).] doi:10.17116/oftalma2020136062171
- Современные аспекты терапии субмакулярных кровоизлияний на фоне макулярной дегенерации Файзрахманов Р.Р., Босов Э.Д., Шишкин М.М., Воропаев В.Ю., Суханова А.В., Чехонин Е.С., Миронов А.В.Вестник офтальмологии. 2022. Т. 138. № 2. С. 87-93. [Fayzrakhmanov RR, Bosov ED, Shishkin MM, et al. Modern aspects of the treatment of submacular hemorrhages secondary to macular degeneration. 2022;138 (2):87–93 (In Russ).] doi:10.17116/oftalma202213802187


