Анализ фазовых равновесий, реализующихся в системах Ni-Si-O и Ni-Si-С-О в условиях существования жидкого металла
Автор: Трофимов Евгений Алексеевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 15 (274), 2012 года.
Бесплатный доступ
Рассчитаны диаграмма состояния системы NiO-SiO 2 и поверхности растворимости компонентов в металле для систем Ni-Si-O и Ni-Si-C-O. Результаты работы могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, кремния и углерода в жидком никеле.
Диаграммы состояния, никелевый расплав, кремний, углерод, кислород, термодинамические расчёты
Короткий адрес: https://sciup.org/147156725
IDR: 147156725 | УДК: 669.24+541.123
Analysis of phase equilibria in the Ni-Si-O and Ni-Si-C-O systems under the condition of existence of nickel melt
Phase diagram of the NiO-SiO 2 system, as well as the surfaces of components’ solubility in metal melt for the Ni-Si-O and Ni-Si-C-O systems are calculated. Results can be used for analyzing technological processes related to interaction of oxygen, silicon and carbon in nickel melt.
Текст научной статьи Анализ фазовых равновесий, реализующихся в системах Ni-Si-O и Ni-Si-С-О в условиях существования жидкого металла
Системы Ni-Si-O и Ni-Si-C-O лежат в основе значительной части технологических процессов выплавки никеля и никелевых сплавов. Поэтому изучение взаимодействий, реализующихся в этих системах, и, в частности, термодинамических аспектов таких взаимодействий в металлическом расплаве, находящемся в равновесии с различными оксидными фазами, интересно как с практической, так и с теоретической точки зрения.
В настоящей работе поставлена задача проведения термодинамического анализа систем Ni-Si-O и Ni-Si-C-O в условиях существования металлического сплава на никелевой основе путём построения поверхностей растворимости компонентов в металле (ПРКМ) [1] для этих систем. Термодинамические параметры, использованные в ходе работы, сведены в табл. 1 и 2. Некоторая часть этих значений ранее была использована в работе [2], другие используются для такого расчёта впервые. Часть констант заимствована из работы [3], другая часть рассчитана с использованием данных, приводимых в этой же работе, а также работах [4, 5].
Таблица 1
Температурные зависимости констант равновесия реакций взаимодействия компонентов никелевого расплава
|
№ п/п |
Процесс |
Константа равновесия, K ; a - активность, мас. %; p - давление, атм |
Температурная зависимость 1g K |
|
1 |
(NiO) = [Ni] + [О] |
K = а [О] J a ( NiO ) |
-10 318 / T + 5,813 |
|
2 |
|NiO| = [Ni] + [O] |
K = a [0] |
-12 966 / T + 7,000 |
|
3 |
(SiO 2 ) = [Si] + 2[O] |
K = a ^] a [Si] [a ( SiO2 ) |
-33 467 / T + 12,338 |
|
4 |
|SiO 2 | = [Si] + 2[O] |
K = a iO] a [Si] |
-33 870 / T + 12,540 |
|
5 |
|Ni 2 SiO 4 |=2[Ni]+[Si]+4[O] |
K = a [0] a [Si] |
-60 610 / T + 26,984 |
|
6 |
{CO} = [C] + [O] |
K = a [O] a [C] / p CO |
-5093 / T - 1,878 |
|
7 |
(NiO) = [Ni] + [O] |
K = а [О] J a ( NiO ) |
-10 318 / T + 5,813 |
Температурные зависимости параметров взаимодействия в жидком никеле
Таблица 2
|
e i j |
Температурная зависимость |
e i j |
Температурная зависимость |
|
e SSii |
273,5 / Т |
e CC |
395 / T |
|
e O Si |
–73,1 / T |
e SOi |
–127,8 / Т |
|
e OC |
–160 / T |
e CO |
–120 / T |
|
e O O |
–41,7 / T |
Помимо прямого использования литературных значений, часть использованных в работе параметров (значение константы равновесия реакции образования Ni 2 SiO 4 , а также значения параметров взаимодействия первого порядка) были оптимизированы до достижения качественного непротиворечия результатов расчётов данным о картине фазовых равновесий в исследуемых системах.
Для расчёта активностей компонентов оксидного расплава в системе NiO–SiO 2 использовано приближение теории субрегулярных ионных расплавов [1]. Значения энергетических параметров теории, определённые по данным о диаграмме состояния этой системы, приведённым в справочнике [6]: Q 1112 = 29500 Дж/моль, Q 1122 = 20000 Дж/моль и Q 1222 = 72000 Дж/моль.
Результаты проведённого расчёта диаграммы состояния этой системы представлены на рис. 1.
На рис. 2 представлена рассчитанная ПРКМ системы Ni–Si–O, а также изотермы растворимости кислорода и кремния в жидком никеле. В области I определены составы металла, равновесного с оксидом никеля. В области II – составы металла, находящегося в равновесии с твёрдым силикатом никеля. Область III демонстрирует составы металла, равновесные с кремнезёмом (кристобалитом). Области IV и V демонстрируют составы металла, находящиеся в равновесии с оксидными расплавами: область IV – с расплавом, в составе которого значительное количество оксида никеля (область, соответствующая оксидному расплаву 1 слева от купола расслаивания на диаграмме состояния системы NiO–SiO 2 ), а область V – с расплавом, в котором преобладает оксид кремния (расплав 2 правее купола расслаивания на рис. 1).
На рис. 3 представлен увеличенный участок ПРКМ системы Ni–Si–O, на котором сосредоточе-
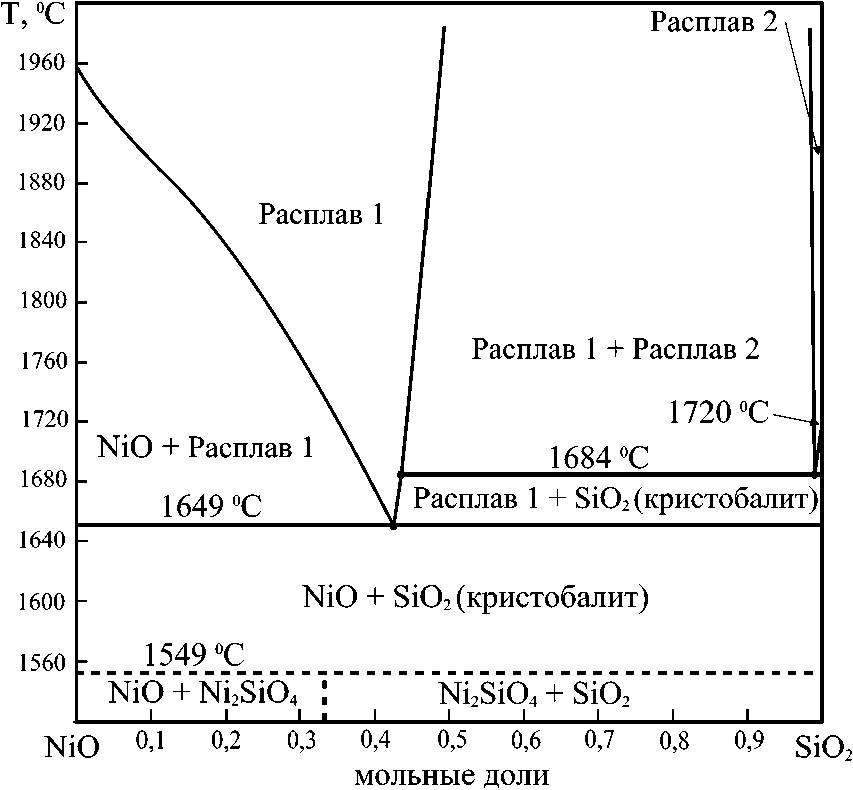
Рис. 1. Диаграмма состояния системы NiO–SiO 2
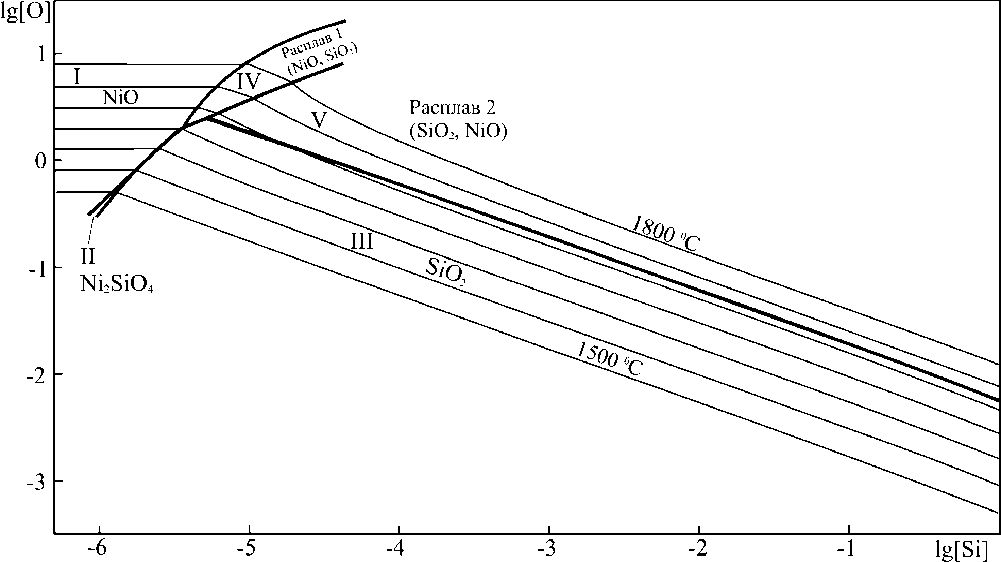
Рис. 2. ПРКМ системы Ni–Si–O
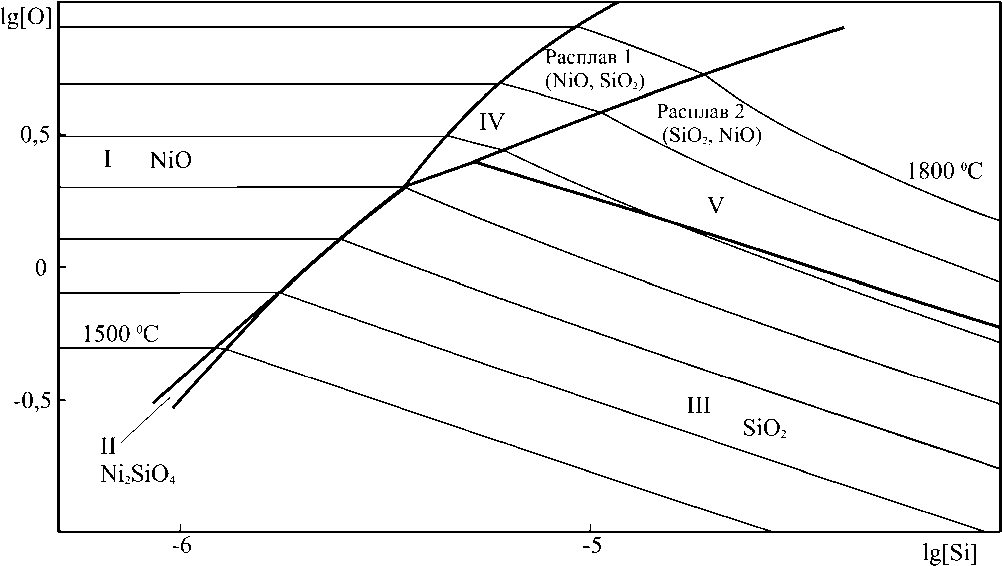
Рис. 3. Увеличенный фрагмент ПРКМ системы Ni–Si–O с границами фазовых равновесий
на основная часть границ областей фазовых равновесий в этой системе.
Последовательность окисления примесей, оптимальный температурный режим плавки, раскис-ленность расплава в реальных металлургических системах во многом определяются соотношением между содержащимися в жидком металле углеродом и кремнием. Информацию о фазовых равновесиях в системе Ni–Si–С–O позволяет получить ПРКМ этой системы.
В процессе расчёта координат ПРКМ были совместно проанализированы все возможные реакции между кислородом, никелем, кремнием и углеродом. На рис. 4 представлено изотермическое сечение ПРКМ при 1460 °С и суммарном давлении оксидов углерода 1 атм. В этих условиях система характеризуется наличием четырёх областей фазовых равновесий. В области I при малых концентрациях углерода и кремния соответствующие составы металла находятся в равновесии с твёрдым раствором NiO. При более высоком содержании кремния металл, соответствующий составам области II, находится в равновесии с твёрдым силикатом никеля. В ходе дальнейшего повышения концентрации кремния равновесной с металлом оксидной фазой становится кристобалит (область III).
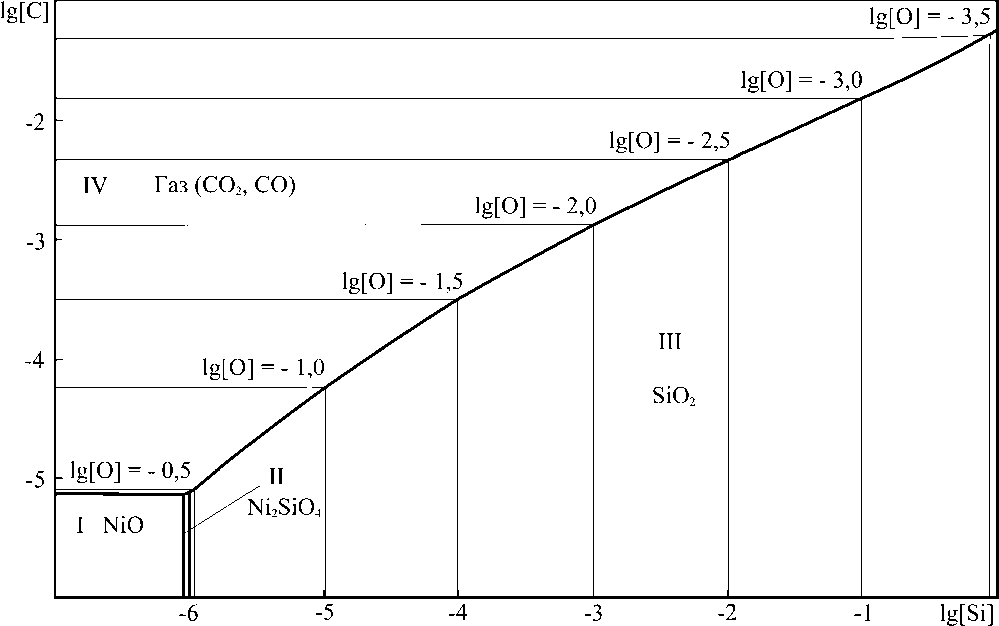
Рис. 4. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1460 °С
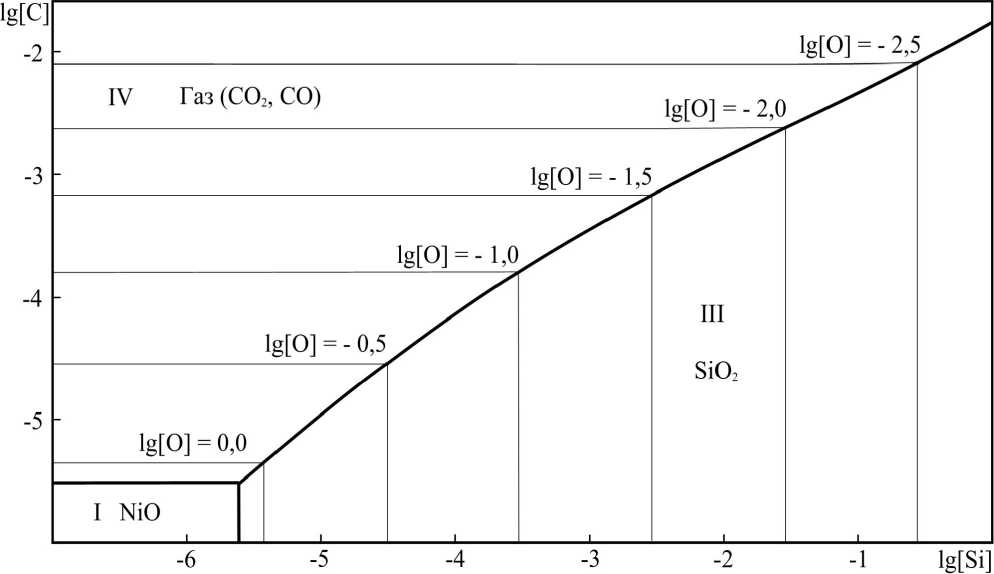
Рис. 5. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1600 °С
И наконец, при достаточном количестве углерода в составе металлического расплава (область IV) равновесной с металлом фазой является газовая смесь оксидов углерода.
С ростом температуры в картине реализующихся фазовых равновесий происходят изменения: область равновесия металла с силикатом никеля вырождается. Примером того, как выглядит изо- термический разрез диаграммы в этом случае, является представленный на рис. 5 разрез ПРКМ для температуры 1600 °С. Как меняются границы фазовых равновесий в исследуемой системе при изменении давления оксидов углерода, позволяет проследить сечение диаграммы, представленное на рис. 6. Сечение рассчитано исходя из суммарного давления оксидов углерода, равного 0,1 атм, и для температуры 1600 °С. Сопоставление диаграмм на рис. 5 и 6 позволяет сделать вывод, что понижение давления оксидов углерода смещает границы между металлом, равновесным с газом, и металлом, сопряжённым с конденсированными оксидными фазами, в сторону более низких концентраций углерода в жидком металле.
В ходе дальнейшего роста температуры в составе фаз, находящихся в равновесии с металлом, происходят изменения, соответствующие изменениям на диаграмме состояния оксидной системы NiO–SiO2.
При температуре 1649 °С появляется область равновесия металла с оксидным расплавом, в составе которого присутствует значительное количество оксида никеля (рис. 7), затем (при температуре 1684 °С) появляется область равновесия жидкого металла с оксидным расплавом справа от купола расслаивания на диаграмме состояния системы NiO–SiO 2 (рис. 8). И, наконец, при температуре 1720 °С исчезает область равновесия металла с твёрдым кремнезёмом (рис. 9).
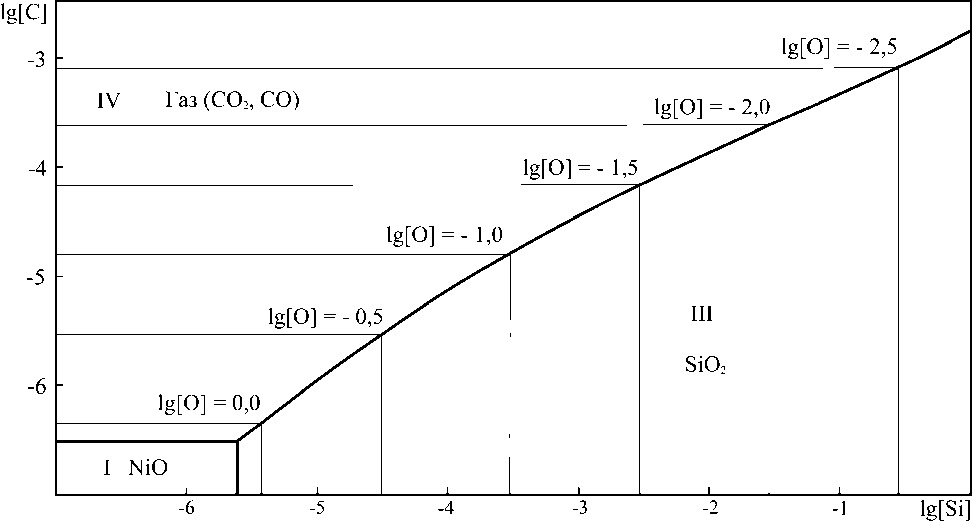
Рис. 6. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,01013 MПа и Т = 1600 °С
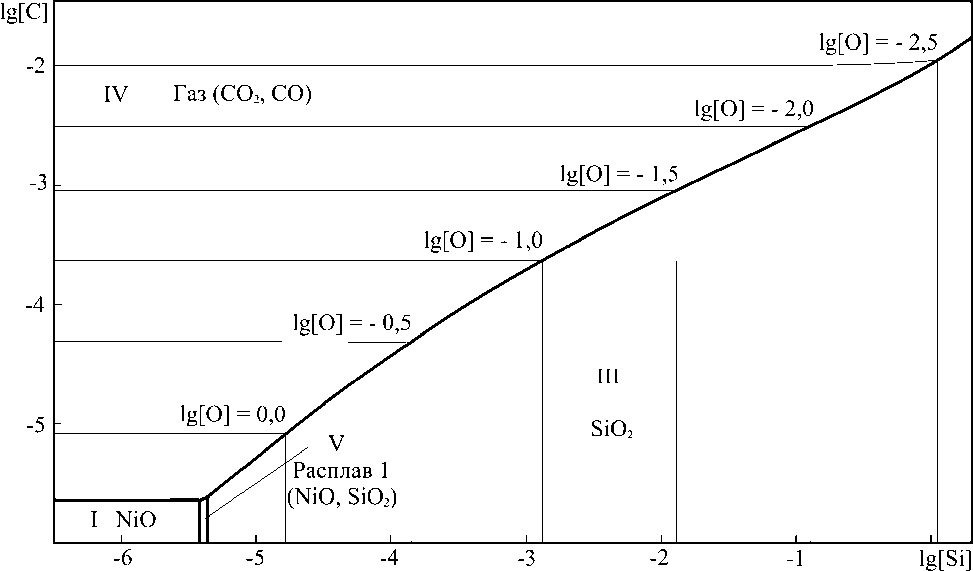
Рис. 7. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1670 °С
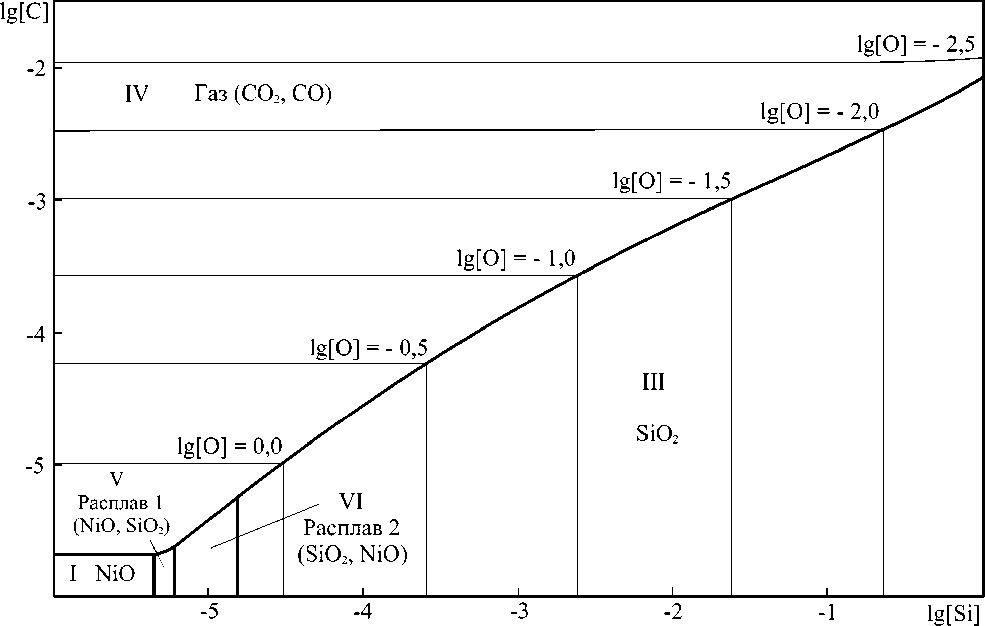
Рис. 8. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1700 °С
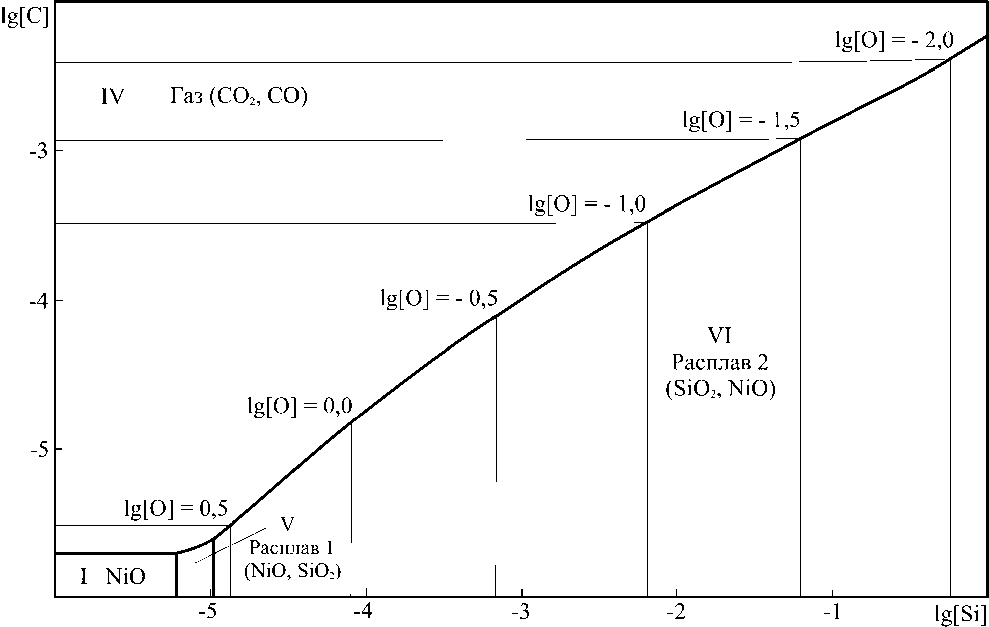
Рис. 9. Изотермический разрез ПРКМ системы Ni–Si–C–O при суммарном давлении оксидов углерода 0,1013 MПа и Т = 1750 °С
Представленные на приведённых выше рисунках диаграммы могут быть использованы в ходе разработки никелевых сплавов с повышенными уровнями полезных свойств, поскольку на механические характеристики никелевых сплавов неметаллические включения, образующиеся в процессе их выплавки, оказывают большое влияние. Построенные ПРКМ позволяют объяснять состав неметаллических включений в никеле и сплавах на его основе, а также позволяют определять то, как влияют на состав этих включений изменения различных технологических параметров.
Выводы
Посредством термодинамических расчётов построена диаграмма состояния системы NiO–SiO 2 , а также построены поверхности растворимости компонентов в металле (ПРКМ) для систем Ni–Si–O и Ni–Si–C–O. Разработанные диаграммы могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, углерода и кремния в жидком никеле.
Работа осуществлена при финансовой поддержке РФФИ, грант № 11-08-12046-офи-м-2011.
Список литературы Анализ фазовых равновесий, реализующихся в системах Ni-Si-O и Ni-Si-С-О в условиях существования жидкого металла
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Изд. Дом МИСиС. -2009. -520 c.
- Трофимов, Е.А. Анализ фазовых равновесий в системах Ni-С-О, Ni-Ca-O и Ni-Al-O в условиях существования жидкого металла/Е.А. Трофимов, Г.Г. Михайлов//Вестник ЮУрГУ. Серия «Металлургия». -2010. -Вып. 14. -№ 13 (189). -С. 4-7.
- Куликов, И.С. Раскисление металлов/И.С. Куликов -М.: Металлургия, 1975. -504 с.
- Физико-химические свойства окислов: справ./под ред. Г.В. Самсонова. -2-е изд., перераб. и доп. -М.: Металлургия, 1978. -472 с.
- Туркдоган, Е. Т. Физическая химия высокотемпературных процессов: пер. с англ./Е.Т. Туркдоган. -М.: Металлургия, 1985. -344 с.
- Диаграммы состояния силикатных систем: справ. Вып. 1: Двойные системы./Н.А. Торопов, В.П. Барзаковский, В.В. Лапин, Н.Н. Курцева. -Л.: Наука, Ленингр. отд., 1969. -822 с.


