Анализ фазовых равновесий в системах Ni-C-O, Ni-Ca-O и Ni-AI-0 в условиях существования жидкого металла
Автор: Трофимов Е.А., Михайлов Г.Г.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 13 (189), 2010 года.
Бесплатный доступ
Посредством термодинамических расчётов построены поверхности растворимости компонентов в металле (ПРКМ) для систем Ni-C-O, Ni-Ca-O и Ni-AI-O. Разработанные ПРКМ могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, углерода, кальция и алюминия в жидком никеле.
Никелевый расплав, углерод, кальций, алюминий, кислород, термодинамические расчёты
Короткий адрес: https://sciup.org/147156645
IDR: 147156645 | УДК: 669.24+541.123
Analysis of phase equilibria in the Ni-C-O, Ni-Ca-O and Ni-AI-0 systems in condition of existence of nickel melt
Using the thermodynamic calculations, the surfaces of components solubility in metal melt for the Ni-C-O, Ni-Ca-O and Ni-Al-O systems were plotted. The surfaces plotted can be used for analysis of technological processes related to interaction of oxygen, carbon, calcium and aluminium in nickel melt.
Текст научной статьи Анализ фазовых равновесий в системах Ni-C-O, Ni-Ca-O и Ni-AI-0 в условиях существования жидкого металла
Жидкий никель и его сплавы, выплавленные на воздухе, относятся к расплавам, для которых необходимо раскисление. В качестве реагентов для раскисления могут быть использованы элементы с большим сродством к кислороду, чем никель. К числу таких элементов относятся, в частности, углерод, кальций и алюминий [1,2].
Настоящая работа посвящена проведению термодинамического анализа систем Ni-C-O, Ni-Ca-O и Ni-Al-O в области температур 1500... 1800 °C при содержании никеля в системах более 90 % путём построения поверхностей растворимости компонентов в металле (ПРКМ) для этих систем.
Термодинамические константы, использованные в ходе работы, сведены в табл. 1 и 2. Большая часть этих значений заимствована из работ [1, 3], другие рассчитаны нами с использованием данных, приводимых в этих работах. Константы, характеризующие взаимодействие в системе Ni-O, получены в процессе обработки данных Neumann, Zhong и Chang о диаграмме состояния этой системы [4]. Зависимости для системы Ni-Ca-O получены с использованием результатов работы [5].
ПРКМ системы Ni-C-O рассчитана для двух вариантов состава газовой фазы. В первом случае суммарное парциальное давление углекислого и угарного газов было принято равным 1 атм. Во втором случае оно равняется 0,1 атм. Результаты рас чета представлены на рис. 1. В области I заданы составы металла, равновесного с твёрдым NiO, в области II - с газовой фазой (СО, СО2). На линии 1-2 определены составы металла, равновесного с жидкими оксидами и газовой фазой. Очевидно, что повышение давления оксидов углерода смещает межфазную границу 1-2 в сторону более высоких концентраций углерода в жидком металле.
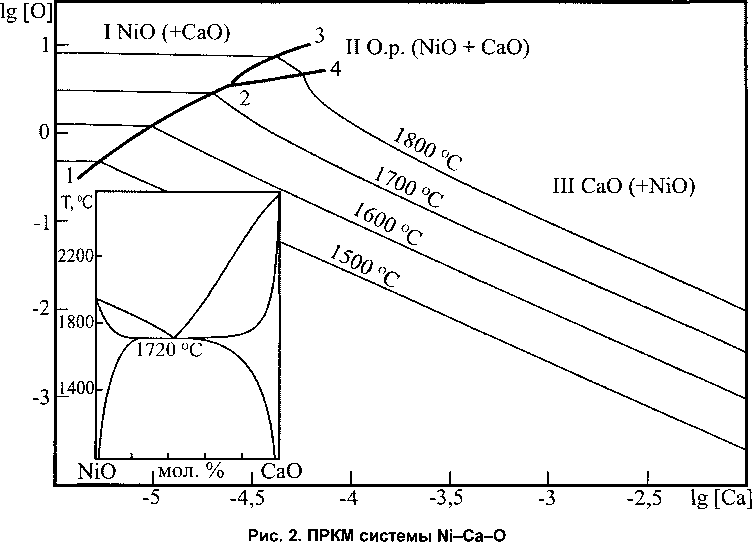
На рис. 2 представлена ПРКМ системы Ni-Ca-O, изотермы растворимости кислорода и кальция в жидком никеле.
Поскольку рассматриваемый интервал температур характеризуется наличием в системе оксидного расплава [б], для расчёта ПРКМ потребовалось рассчитать диаграмму состояния двойной оксидной системы NiO-CaO (вставка на рис. 2). В качестве исходных данных в ходе расчёта использованы данные М. Tikkanen, на которые ссылаются составители справочника [6]. Согласно представленным данным в этой системе существуют достаточно обширные области твёрдых растворов NiO в СаО и СаО в NiO. Это необходимо учитывать при расчёте. Для расчёта активностей компонентов твёрдых растворов и расплава в системе NiO-CaO использовалось приближение теории субрегулярных ионных растворов [7]. Определённые по экспериментальным данным значения энергетических параметров теории для оксидного
Таблица 1 Температурные зависимости констант равновесия реакций взаимодействия компонентов никелевого расплава
|
№ |
Процесс |
Константа равновесия К; а - активность, мае. %; р - давление, атм |
Температурная зависимость 1g К |
|
1 |
(NiO) = [Ni] + [О] |
К = «[О] /a(NiO) |
- 10318 /Т+ 5,813 |
|
2 |
|NiO = [Ni] + [О] |
X" = а^ / O|NiO| |
- 12966 /Т +7,000 |
|
3 |
{СО} = [С] + [О] |
К = «[о]а[С] / Рсо |
-5093 /Т- 1,878 |
|
4 |
{СО2} = [С] + 2[О] |
К = <7[0]<7[С] / Рсо2 |
- 15433 /7+2,852 |
|
5 |
(СаО) = [Са] + [О] |
К = а[О]Я[Са] /ti(CaO) |
- 15489/7+3,969 |
|
6 |
СаО = [Са] + [О] |
^^[OJ^Cal/^CaOl |
- 19430/7+5,350 |
|
7 |
|А12Оз| = 2[А1] +3[О] |
rz-__ 3 2 А - «[OJ^Al] |
-63924 / 7 + 21,027 |
|
8 |
NiAl2O4| = [Ni] + 2[А1] + 4[О] |
ь^ _ 4 2 А - ^[0]а[А1] |
-74480/7+25,805 |
Таблица 2
Температурные зависимости параметров взаимодействия в жидком никеле
|
Температурная зависимость |
e'j |
Температурная зависимость |
|
|
е°о |
-41,7/7 |
^Al |
337/7 |
|
е%а |
290/7 |
395 /7 |
|
|
А1 5 о |
- 82,6 / 7 |
£°А1 |
- 139,4 / 7 |
|
-69 /7 |
е°са |
-172/7 |
|
|
-160/7 |
е% |
-120/7 |
[О], мае %
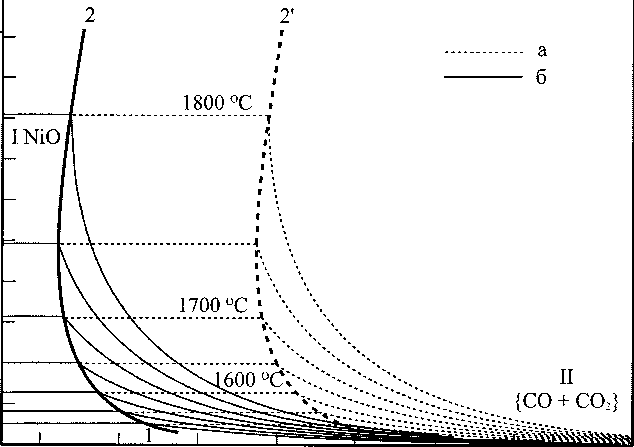
-6,8 -6,4 -6 -5,6 -5,2 -4,8 -4,4 -41g[C]
Рис. 1. ПРКМ системы Ni-C-O: а - суммарное давление оксидов углерода 0,1013 МПа; б - суммарное давление оксидов углерода 0,01013 МПа
расплава этой системы: 61112 = 3272 Дж/моль, 61122 = - 30 000 Дж/моль И 61222 = - 41 596 Дж/моль. Для твёрдых растворов аналогичные значения параметров: 61112 = 45 246 Дж/моль, 6н22=65 000 Дж/моль и 61222= 42 057 Дж/моль.
Линия 1-2 показывает составы металла, находящегося в равновесии с твёрдыми растворами NiO в СаО и СаО в NiO. Линия 2-3 демонстрирует составы металла, находящегося в равновесии с твёрдым раствором СаО в №0 и жидким расплавом оксидов никеля и кальция. Линия 2-4 показы вает составы металла, равновесного как с жидким шлаком, так и твёрдым раствором NiO в СаО. В области I определены составы металла, равновесного с твёрдым раствором на основе оксида никеля. В области II - составы металла, находящегося в равновесии с расплавом оксидов кальция и никеля. Область III демонстрирует составы металла, равновесные с твёрдым раствором на основе оксида кальция.
На рис. 3 представлены результаты расчёта ПРКМ системы Ni-Al-O.
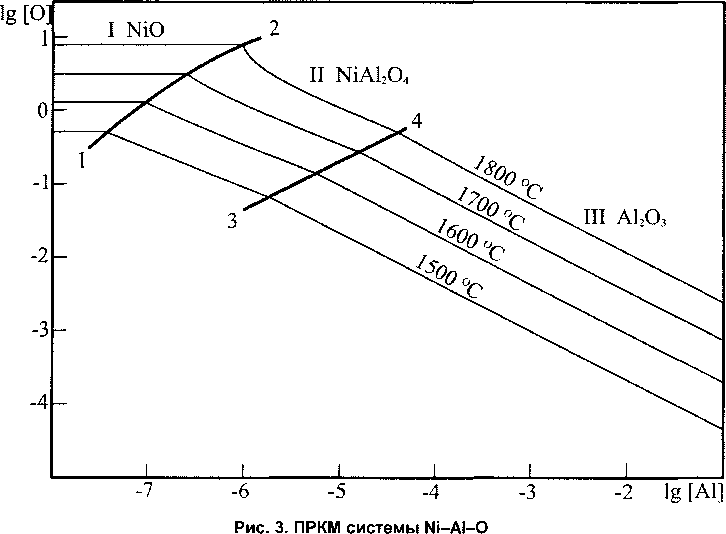
Линия 1-2 показывает составы жидкого металла, находящегося в равновесии с твёрдым №0 и твёрдой шпинелью (NiAl2O4). В области I определены составы металла, находящегося в равновесии с твердым оксидом никеля. В области II - составы металла, находящегося в равновесии со шпинелью NiAl2O4. Линия 3-4 показывает составы жидкого металла, находящегося в равновесии со шпинелью и твёрдым оксидом алюминия, а в области III определены составы жидкого металла, находящегося в равновесии с твёрдым А12О3.
Полученные диаграммы позволяют объяснить состав неметаллических включений в никеле, позволяют проектировать процессы рафинирования металлического расплава и моделировать технологически необходимые фазовые равновесия.
Выводы
Посредством термодинамических расчётов построены поверхности растворимости компонентов в металле (ПРКМ) для систем Ni-C-O, Ni-Ca-O и Ni-Al-O. Разработанные ПРКМ могут быть использованы для анализа технологических процессов, связанных с взаимодействием кислорода, углерода, кальция и алюминия в жидком никеле.
Список литературы Анализ фазовых равновесий в системах Ni-C-O, Ni-Ca-O и Ni-AI-0 в условиях существования жидкого металла
- Куликов, И.С. Раскисление металлов/КС. Куликов. -М.: Металлургия, 1975. -504 с.
- Производство отливок из сплавов цветных металлов/А.В. Курдюмов, М.В. Ликунов, В.М. Чурсин, Е.Л. Бибиков. -М.: Металлургия, 1986. -416 с.
- Расчёты металлургических процессов на ЭВМ/Д.И. Рыжонков, С.Н. Падерин, Г.В. Серов, Л.К. Жидкова. -М.: Металлургия, 1987.-231 с.
- Binary Alloy Phase Diagrams. Second Edition/Ed. T.B. Massalski -Ohio: ASM International, Materials Park, 1990. -Vol. 3. -P. 2831-2833.
- Fujio, I. Термодинамика расплавов Ni-Ca-O и Ni-Ta-Ca-O в равновесии с твердым СаО/I. Fujio, H. Mitsutaka, I. Hiroyasu//Tetsu to hagane = J. Iron and Steel Inst. Jap. -1996. -T. 82, № 6.-С. 465-470.
- Диаграммы состояния силикатных систем: справочник. Вып. 1: Двойные системы/Н.А. Торопов, В.П. Барзаковский, В.В. Лапин, Н.Н. Курцева. -Л.: Наука. Ленингр. отд., 1969. -822 с.
- Михайлов, Г.Г. Термодинамика раскисления стали/Г.Г. Михайлов, Д.Я. Поволоцкий. -М.: Металлургия, 1993. -144 с.


