Анализ иммуногистохимической экспрессии маркера апоптоза p-53 пахового лимфатического узла у крыс в посттравматическом периоде
Автор: Ланичева А.Х., Семченко В.В.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.34, 2026 года.
Бесплатный доступ
ВВЕДЕНИЕ. Изучение распределения p53-позитивных клеток в различных зонах лимфоузла необходимо для понимания системных последствий травмы и поиска потенциальных мишеней терапии. ЦЕЛЬ: оценить динамику численной плотности p53-позитивных лимфоцитов в различных структурно-функциональных зонах пахового лимфатического узла у крыс после механической травмы мягких тканей бедра. МАТЕРИАЛЫ И МЕТОДЫ. Эксперимент выполнен на 50 беспородных крысах (масса 180–200 г). Животные распределены на 5 групп: контроль (n=10) и 4 опытные (n=40) – сроки наблюдения 1, 3, 7 и 14 суток после травмы. Механическую травму бедра наносили с использованием специальной установки, моделирующей высокоэнергетическое повреждение. Иммуногистохимическое выявление p53 проводили на парафиновых срезах лимфоузлов с применением системы детекции UltraVision ONE. Статистический анализ проведен в среде R (версия 4.3.2) с использованием непараметрических методов: критерий Краскела-Уоллиса, критерий Манна–Уитни с поправкой Бонферрони, критерий Фридмана, тест Джонкхира–Терпстры и двухфакторный дисперсионный анализ на выровненных рангах (ART). РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ. Во всех зонах, за исключением первичных узелков и мозгового синуса, выявлено статистически значимое увеличение плотности p53-позитивных лимфоцитов в посттравматическом периоде (p<0,05; d Коэна -1,5). Наибольшие абсолютные значения зафиксированы в мозговых тяжах на всех сроках, минимальные – в синусной системе и первичных узелках. Критерий Фридмана подтвердил гетерогенность распределения p53 между зонами во все сроки. Тест Джонкхира–Терпстры выявил линейный положительный тренд в мозговых тяжах, вторичных узелках и субкапсулярном синусе, что указывает на прогрессирующее накопление p53⁺клеток. В корковом веществе и паракортикальной зоне наблюдался квадратичный тренд с пиком на 3–7 сутки. Установлено значимое взаимодействие факторов «время» и «зона», подтверждающее зональную специфичность реакции. Мощность исследования превысила 0,80 для большинства сравнений. ЗАКЛЮЧЕНИЕ. Механическая травма бедра у крыс индуцирует выраженную и зонально-специфичную динамику экспрессии p53 в паховом лимфоузле. Максимальная и прогрессирующая апоптотическая активность в мозговых тяжах, субкапсулярном синусе и вторичных узелках отражает ключевую роль этих зон в элиминации активированных лимфоцитов и завершении иммунного ответа. Полученные данные расширяют фундаментальные представления о реакции лимфоидной ткани на травму и могут служить основой для разработки методов коррекции посттравматических иммунных нарушений.
P53, апоптоз, лимфатический узел, травма, иммуногистохимия, крыса, морфометрия, статистический анализ
Короткий адрес: https://sciup.org/143185636
IDR: 143185636 | УДК: 616-001.1:616-097:616.428:57.086.6 | DOI: 10.20340/mv-mn.2026.34(1).1015
Analysis of immunohistochemical expression of the p-53 apoptosis marker in the inguinal lymph node of rats in the post-traumatic period
INTRODUCTION. Studying the distribution of p53-positive cells in various lymph node zones is essential for understanding the systemic consequences of trauma and identifying potential therapeutic targets. AIM: to evaluate the dynamics of p53-positive lymphocyte density in different zones of the rat inguinal lymph node after mechanical trauma to the thigh soft tissues. MATERIALS AND METHODS. The experiment was performed on 50 outbred rats (180–200 g), divided into 5 groups: control (n=10) and 4 experimental groups (n=40) at 1, 3, 7, and 14 days post-injury. Mechanical thigh trauma was induced using a specialized device simulating high-energy injury. Immunohistochemical detection of p53 was performed on paraffin sections using the UltraVision ONE system. Statistical analysis was performed in R (version 4.3.2) using non-parametric methods: Kruskal-Wallis test, Mann-Whitney test with Bonferroni correction, Friedman test, Jonckheere-Terpstra test, and two-way ANOVA on aligned ranks (ART). RESULTS AND DISCUSSION. In all zones except primary nodules and the medullary sinus, a significant increase in p53-positive lymphocyte density was observed post-trauma (p<0.05; Cohen's d-1.5). The highest values were recorded in the medullary cords at all time points, the lowest in the sinus system and primary nodules. The Friedman test confirmed heterogeneous p53 distribution between zones at all time points. The Jonckheere-Terpstra test revealed a positive linear trend in the medullary cords, secondary nodules, and subcapsular sinus, indicating progressive p53⁺ cell accumulation. A quadratic trend with a peak at days 3–7 was observed in the cortex and paracortical zone. A significant "time × zone" interaction confirmed the zonal specificity of the response. Study power exceeded 0.80 for most comparisons. CONCLUSION. Mechanical thigh trauma induces pronounced, zone-specific p53 expression dynamics in the inguinal lymph node. Maximal and progressive apoptotic activity in the medullary cords, subcapsular sinus, and secondary nodules reflects their key role in eliminating activated lymphocytes and resolving the immune response. These findings expand fundamental knowledge of lymphoid tissue reaction to trauma and may inform strategies for correcting post-traumatic immune disorders.
Текст научной статьи Анализ иммуногистохимической экспрессии маркера апоптоза p-53 пахового лимфатического узла у крыс в посттравматическом периоде
(1).1015
(1).1015
Lanicheva AKh, Semchenko VV. Analysis of immunohistochemical expression of the p-53 apoptosis marker in the inguinal lymph node of rats in the post-traumatic period. Morfologicheskie Vedomosti – Morphological newsletter. 2026;34(1):1015. (1).1015
На фоне механического воздействия на сегмент конечности в первую очередь возникает воспаление и выделение провоспалительных цитокинов (фактора некроза опухоли альфа, интерлейкинов) и выброс гормонов стресса (кортикостероиды, катехоламины) [1, 2]. Паховый лимфоузел – это первый региональный «фильтр» и «командный центр» для тканей травмированной конечности. Изучение апопто- за в лимфатическом узле позволяет оценить системные последствия после травмы, расшифровать механизмы, связывающие локальное повреждение с реакцией всего организма и найти мишени, направленные на предотвращение инфекционных осложнений и улучшения восстановления после серьезных травм [3, 4].
iASPP (Inhibitor of Apoptosis-Stimulating Protein of p53) – ключевой регулятор, который действует как специфический ингибитор опухоле- вого супрессора p53. Связываясь с p53, iASPP блокирует его способность индуцировать апоптоз (гибель клеток) и клеточный цикл, тем самым способствуя выживанию клеток, что часто используется раковыми клетками для защиты от апоптоза [5, 6].
Апоптоз считается жизненно важным компонентом различных процессов, направленным на поддержание гомеостаза в организме. Транзи-торная экспрессия p53 необходима для индукции стволовых клеток восстановления и контролируется отрицательной обратной связью, опосредованной Mdm2 [7, 8].
В общих чертах можно выделить внутренние и внешние пути активации апоптоза, а также взаимодействие между ними. Эти пути сходятся на системе протеаз, называемых «каспазами» (цистеинил-аспарагиновыми протеиназами), и существуют модуляторы, которые мультимери-зуют, активируют, усиливают или ингибируют каспазы [9, 10]. Активированные каспазы являются исполнителями программы апоптоза и выполняют эту функцию, расщепляя специфические клеточные субстраты. Белок p53 является ключевым регулятором клеточного цикла и апоптоза, играя центральную роль в поддержании геномной стабильности [11, 12]. Он функционирует как транскрипционный фактор, активируя экспрессию генов, ответственных за репарацию ДНК, остановку клеточного цикла или запуск апоптоза в случае значительных повреждений генома [13, 14].
При травмах нижних конечностей наибольший интерес представляет изучение паховых лимфатических узлов [15]. Однако, работ по детальному, сравнительному изучению различных зон паховых лимфатических узлов мало.
ЦЕЛЬ: оценить динамику численной плотности p53-позитивгых лимфоцитов в различных зонах лимфатического узла у крыс после механической травмы мягких тканей бедра.
МАТЕРИАЛЫ И МЕТОДЫ
Объектом исследования являлись белые беспородные крысы массой 180–200 г. Животных кон- трольной (n=10) и опытной групп (n=40) содержали в одинаковых условиях при свободном доступе к воде и пищи. С помощью специальной установки крысам наносили механическую травму бедра, моделирующую высококинетическое повреждение тканей [16]. Все манипуляции выполнялись согласно Федеральным законом № 498-ФЗ от 27.12.2018 г. «Об ответственном обращении с животными» и в соответствии с правилами Европейской конвенции по защите позвоночных животных (Страсбург, 1986). Исследование одобрено локальным этическим комитетом ФГБОУ ВО «Башкирский государственный медицинский университет» МЗ РФ (протокол № 3 от 18.03.2021). Группы формировались из общего потока травмированных животных путем рандомизации с помощью случайных чисел: группа I – контрольные животные (n=10); группа II – экспериментальные животные с механической травмой (n=40).
Забой производили под эфирным наркозом путем декапитации. Для иммуногистохимического исследования брали участок лимфатического узла размером 0,5×1,5 см через 1, 3, 7, 14 сут после нанесения травмы. Образцы фиксировали в 10% нейтральном растворе формалина на фосфатном буфере (ООО «Биовитрум», Россия), заливали в парафин и изготавливали делали серийные срезы толщиной 3–4 мкм, которые окрашивали гематоксилином и эозином (ООО «Медикс», Россия).
Для более детального изучения апоптотиче-ских реакций в клеточных структурах лимфатического узла использовали иммуногистохимический метод окрашивания. С помощью моноклональных антител выявляли апоптотический маркер p-53 (клон DO-7, каталожный номер М700101, разведение 1:50, Dako, Дания). Постановку иммуногистохимических реакций проводили согласно рекомендациям фирмы-производителя реагентов для иммуногистохимии (Dako, Дания). Для визуализации результатов использовали систему детекции Ultra Vision ONE Detection System HRP Polymer (Labvision Corporation, США), а в качестве хромогена – DAV Plus Substrate System (ООО «Биовитрум», Рос- сия). Срезы докрашивали гематоксилином Майера (ООО «Абрис+», Россия) и заключали в БиоМаунт-среду (Bio-Optica Milano, Италия). Для оценки качества реакции использовали стекла с позитивным контролем для каждого из антигенов (Labvision Corporation, США). Стеклопрепа-раты сканировали на цифровом сканере микроскопе Pannoramic 250 (3DHISTECH Ltd., Венгрия). Для оценки экспрессии p-53 определяли число иммунопозитивных клеток на площади среза равной 10 000 мкм2. Подсчет клеток проводили в 30 непересекающихся полях зрения для каждой зоны и срока наблюдения с помощью программного обеспечения Vision Slide Viewer.
Статистическую обработку данных проводили в среде R (версия 4.3.2, GNU General Public License, GPL) с использованием пакетов: dplyr, rstatix, PMCMRplus, ggplot2 и nparLD. Экспериментальный дизайн характеризовался вложенностью наблюдений: множественные поля зрения (до 30 на срок по каждой зоне) были получены от каждого животного (n=5). Для корректного анализа применяли двухэтапный подход. Для каждого животного рассчитывали медианное значение по всем полям зрения. Таким образом, единицей анализа выступало животное (n=10 на группу), что исключало псевдорепликацию и обеспечивало независимость наблюдений. Полученные агрегированные данные анализировали с использованием непараметрических методов, так как проверка нормальности распределения (критерий Шапиро-Уилкса) выявила отклонения от нормальности в части групп, а малый объем выборки (n=5) делал параметрические методы неоптимальными. Для оценки влияния фактора времени (контроль, 1, 3, 7, 14 сутки) на морфометрические показатели применяли критерий Краскела–Уоллиса (Kruskal–Wallis ANOVA) – для выявления общих различий между пятью независимыми временными группами. При обнаружении значимых различий (p<0,05) проводили пост-хок попарные сравнения с помощью критерия Манна–Уитни с поправкой Бонферрони. Сравнительный анализ численной плотности p53-позитивных лимфо- цитов между зонами лимфатических узлов проводили с помощью критерия Фридмана (Friedman ANOVA) с последующим пост-хок попарным сравнением между зонами (критерий Вил-коксона с поправкой Бонферрони).
Для оценки взаимодействия факторов «временная точка» и «анатомическая зона» использовали непараметрический двухфакторный дисперсионный анализ (Aligned Rank Transform, ART) с последующими пост-хок сравнениями. Данный метод позволил корректно анализировать взаимодействия без предположения о нормальности распределения. Направленные изменения во времени (наличие тренда) оценивали с помощью теста Джонкхира–Терпстры (Jonckheere–Terpstra test) для упорядоченных альтернатив.
На основе полученных данных рассчитана эмпирическая мощность исследования. Мощность составила >0,65 для различных зон, что подтвердило адекватность размера выборки (n=10 на группу) для выявления биологически значимых различий при α =0,05. Данные представлены в виде медианы, интерквартильного размаха (Me [Q1; Q3]) и Max-Min без экстремальных выбросов. Графическая визуализация выполнена с помощью ящиков с усами (boxplots).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На препаратах, окрашенных гематоксилином и эозином лимфатический узел представлен корковым и мозговым веществом, в корковом веществе различают первичные и вторичные лимфоидные узелки (рис. 1а). Во вторичных лимфоидных узелках различают герминативные центры, состоящие из малых лимфоцитов, принадлежащих к В-лимфоцитам (рис. 1b). Герминативный центр развивается только под влиянием антигенной стимуляции. Паракортикаль-ная зона располагается между корковым и мозговым веществом и представлена, в основном T-лимфоцитами (рис. 1c). Мозговое вещество представлено мозговыми тяжами, состоящими из ретикулярной ткани, в которых расположены преимущественно B-лимфоциты, макрофаги и плазматические клетки (рис. 1d).
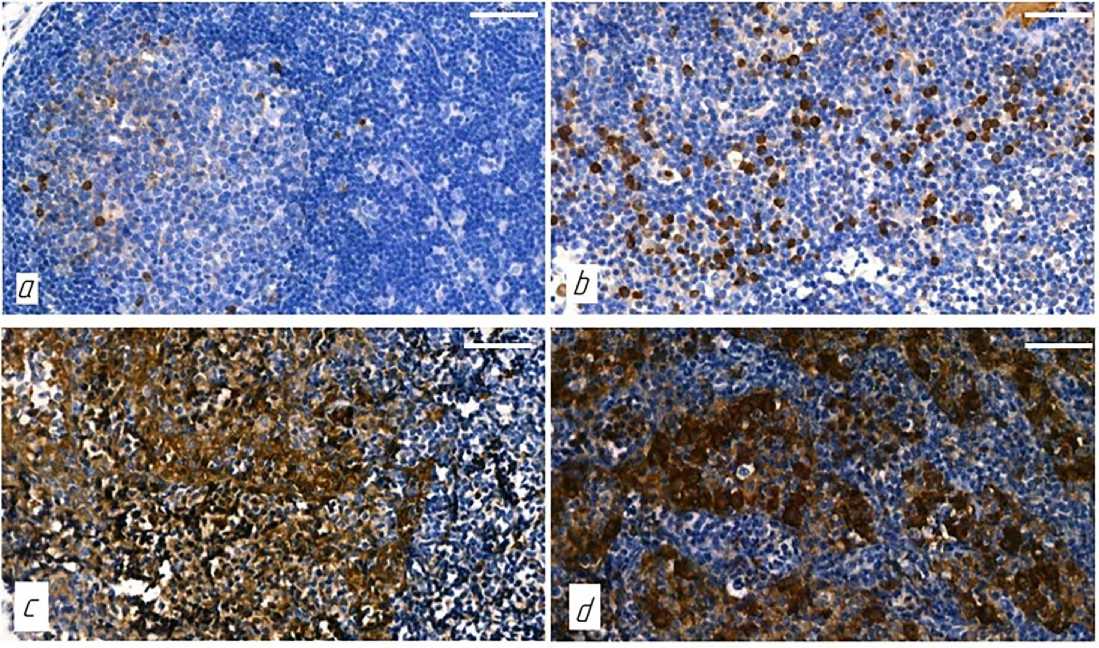
Рисунок 1. Паховый лимфатический узел интактных крыс: a – корковое вещество; b – вторичные лимфоидные узелки; c – паракортикальная зона; d – мозговое вещество. Окраска гематоксилином и эозином. Ув. 400, объектив 40, масштабный отрезок 30 мкм
Figure 1. Inguinal lymph node of intact rats: a – cortex; b – secondary lymphoid nodules; c – paracortical zone; d – medulla; hematoxylin and eosin staining. Mag. 400, objective 40, scale bar 30 µm
Морфометрический и статистический анализ р53-позитивных лимфоцитов (рис. 2) показали, что их численная плотность существенно различалась между зонами в контроле и после травмы (рис. 3; табл. 1, 2, 3 и 4).
В контрольной группе животных во вторичных лимфоидных узелках и в мозговых тяжах наблюдается незначительная экспрессия p-53 положительных лимфоцитов (рис. 2а, рис. 2b). В корковом веществе и мозговых тяжах лимфатических узлов происходят постоянные процессы созревания, активации и гибели клеток, которые контролируются регулятором апоптоза p53. Белок p-53 накапливается в фазе G1 клеточного цикла, готовя клетку к делению.
В первичных лимфоидных узелках пик экспрессии p-53 наблюдается через 1 сутки после травмы и остается выше контроля на всех сроках посттравматического периода. (рис. 2с, рис. 2d, рис. 3).
Повышение уровня p-53 необходимо для контроля пролиферации лимфоцитов, чтобы иммунный ответ на травму был адекватным, а не чрезмерным. Для этого он помогает запустить процесс репарации ДНК в делящихся клетках и, если повреждения клетки большие, то инициируют апоптоз для удаления потенциально опасных клеток [17, 18].
В паракортикальной зоне экспрессия p-53 через 1 сутки после травмы снижается, затем резко возрастает через 3 суток после травмы и через 7 и 14 суток продолжает оставаться выше контрольных значений (рис. 3).
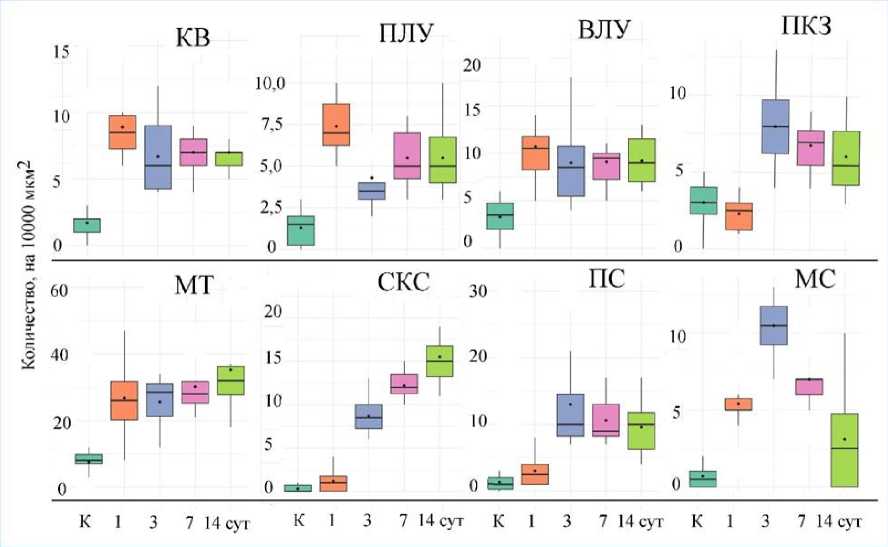
Рисунок 2. Иммуногистохимическая реакция p-53 в паховом лимфатическом узле у крыс контрольной группы и после механической травмы бедра: a – вторичные лимфоидные узелки контрольной группы; b – мозговые тяжи контрольной группы; с – мозговые тяжи через 7 суток после механической травмы; d – мозговые тяжи через 14 суток после механической травмы. Ув. 400, объектив 40, масштабный отрезок 30 мкм
Figure 2. Immunohistochemical reaction of p-53 in the inguinal lymph node of rats of the control group and after mechanical injury of the thigh: a – secondary lymphoid nodules of the control group; b – medullary cords of the control group; c – medullary cords 7 days after mechanical injury; d – medullary cords 14 days after mechanical injury. Mag. 400, objective 40, scale bar 30 µm4
Таблица 1. Результаты однофакторного анализа для сравнения временных групп по каждой зоне
Table 1. Results of one-way analysis for comparison of time groups for each zone
|
Зона |
Тест |
Статистика |
p-уровень |
Эффект ( η ²/H') |
|
КВ |
Крускал–Уоллис |
H=27,8 |
0,001 |
0,58 |
|
ПЛУ |
Крускал–Уоллис |
H=19,9 |
0,001 |
0,45 |
|
ВЛУ |
Крускал–Уоллис |
H=17,5 |
0,002 |
0,39 |
|
ПКЗ |
ANOVA Уэлча |
F=15,9 |
0,001 |
0,46 |
|
МТ |
Крускал–Уоллис |
H=22,0 |
0,001 |
0,49 |
|
СКС |
Крускал–Уоллис |
H=42,3 |
0,001 |
0,94 |
|
ПС |
Крускал–Уоллис |
H=31,8 |
0,001 |
0,71 |
|
МС |
Крускал–Уоллис |
H=29,1 |
0,001 |
0,65 |
Примечание: η ² (эта-квадрат) – доля дисперсии зависимой переменной, которая объясняется независимой переменной (фактором «Время») для каждой зоны. Фактор времени объясняет >39% всех различий. Практически вся вариабельность данных связана с травмой, а не с индивидуальными различиями крыс.
Паракортикальная зона – это зона T-лимфоцитов, а для иммунного ответа клетки в острую фазу иммунного ответа (1–3 сутки после травмы) должны пролиферировать. Так как после травмы конечности возникает временная гипоксия, в условиях которой стабилизируется фактор HIF-1α (Hypoxia Inducible Factor), активация которого приводит к деградации p-53 или подавлению его транкскрипционной активности, чтобы предотвратить избыточную гибель клеток в условиях стресса [19, 20].
В мозговых тяжах наблюдается максимально высокая плотность лимфоцитов, в сравнении с другими зонами лимфатического узла. Через 1,
3, 7 и 14 суток после травмы выраженная экспрессия, которая сохраняется на всех сроках (рис. 2c, рис. 2d, рис. 3; табл. 2).
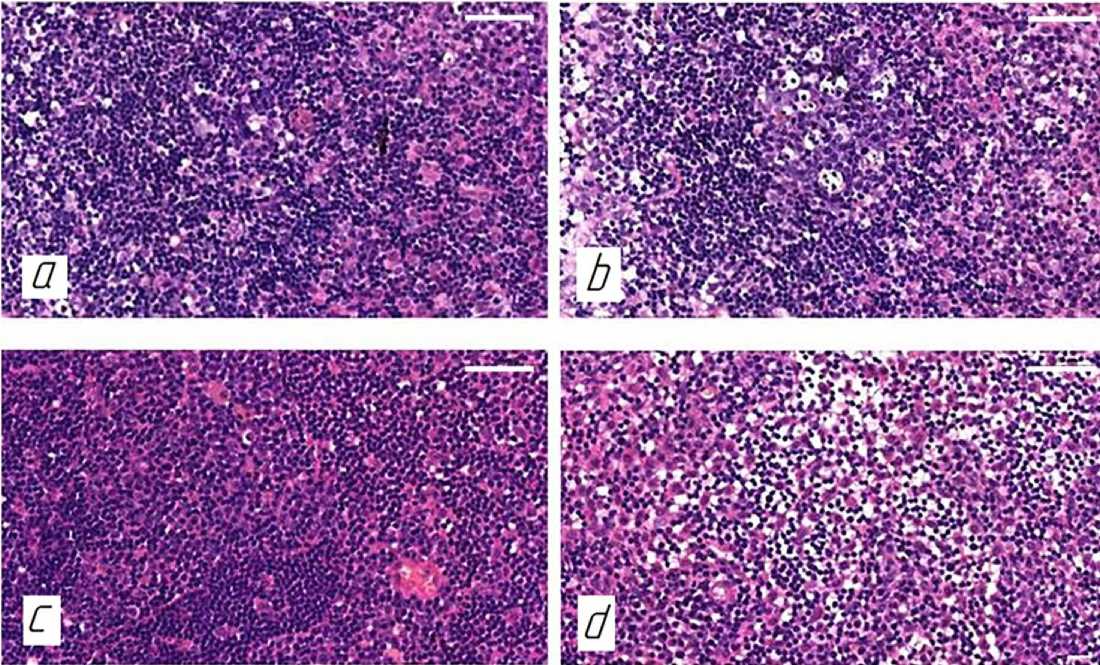
Рисунок 3. Количество р-53-позитивных лимфоцитов на 10000 мкм2 среза лимфоузла в контроле и после механической травмы бедра. Материал представлен как Me (Q2 – горизонтальная линия), интерквартильного размаха (Q1–Q3 – бокс), Max–Min (вертикальная линия). Ромб в боксе – среднее значение переменной для данного срока. Примечание . КВ – корковое вещество, ПЛУ – первичные лимфоидные узелки, ВЛУ – вторичные лимфоидные узелки, ПКЗ – паракортикальная зона, МТ – мозговые тяжи, СКС – субкапсулярный краевой синус, ПС – периузелковый синус, МС – мозговой синус
Figure 3. The number of p-53-positive lymphocytes per 10,000 µm2 of lymph node section in the control and after mechanical trauma to the thigh. The data are presented as Mean (Q2 – horizontal line), interquartile range (Q1–Q3 – box), and Max-Min (vertical line). The diamond in the box represents the mean value of the variable for a given period. Note: КВ – cortex, ПЛУ – primary lymphoid nodules, ВЛУ – secondary lymphoid nodules, ПКЗ – paracortical zone, MТ – medullary cords, СКС – subcapsular marginal sinus, ПС – perinodular sinus, MС – medullary sinus
Во всех временных точках критерий Фридмана показал высоко значимые различия между зонами (табл. 3), что подтверждает гетерогенность распределения p53⁺ лимфоцитов в лимфатическом узле. Мозговые тяжи последовательно занимают первое место по содержанию p53⁺ лимфоцитов на всех сроках (табл. 3 и 4). В кон- троле наибольшая разница между мозговыми тяжами и субкапсулярным синусом. Через 3 суток – между мозговыми тяжами и первичными узелками. Через 14 суток разница достигает максимума. Мозговой синус демонстрирует бимодальную вариабельность (высокая в контроле и на 14 сутки).
Таблица 2. Значимые пост-хок попарные сравнения между временными точками с поправкой Бонферрони (критерий Манна–Уитни)
Table 2. Significant post-hoc pairwise comparisons between time points with Bonferroni correction (Mann-Whitney test)
|
Зона |
Сравнение |
p–уровень |
Разность медиан |
d Коэна |
|
КВ |
К–1 |
0,001 |
–6,5 |
3,64 |
|
К–3 |
0,004 |
–4,0 |
1,78 |
|
|
К–7 |
0,001 |
–5,0 |
2,72 |
|
|
К–14 |
0,001 |
–4,5 |
2,48 |
|
|
ПЛУ |
К–1 |
0,001 |
–5,0 |
3,66 |
|
К–3 |
0,041 |
–1,5 |
1,01 |
|
|
К–7 |
0,003 |
–3,0 |
2,18 |
|
|
ВЛУ |
К–1 |
0,002 |
–6,5 |
1,84 |
|
К–3 |
0,013 |
–5,0 |
1,31 |
|
|
К–7 |
0,008 |
–6,0 |
1,66 |
|
|
К–14 |
0,004 |
–5,0 |
1,78 |
|
|
ПКЗ |
К–3 |
0,001 |
–5,0 |
2,19 |
|
1–3 |
0,001 |
–5,5 |
2,46 |
|
|
3–14 |
0,048 |
3,0 |
0,87 |
|
|
МТ |
К–1 |
0,001 |
–17,5 |
2,09 |
|
К–3 |
0,001 |
–18,5 |
2,42 |
|
|
К–7 |
0,001 |
–19,5 |
2,84 |
|
|
К–14 |
0,001 |
–23,0 |
2,61 |
|
|
СКС |
К–3 |
0,001 |
–8,5 |
4,80 |
|
К–7 |
0,001 |
–12,0 |
6,94 |
|
|
К–14 |
0,001 |
–15,5 |
5,89 |
|
|
1–3 |
0,001 |
–7,5 |
3,72 |
|
|
1–7 |
0,001 |
–11,0 |
5,56 |
|
|
1–14 |
0,001 |
–14,5 |
4,79 |
|
|
ПС |
К–3 |
0,001 |
–9,5 |
2,04 |
|
К–7 |
0,001 |
–8,5 |
2,36 |
|
|
К–14 |
0,001 |
–8,0 |
1,70 |
|
|
1–3 |
0,001 |
–8,0 |
1,72 |
|
|
МС |
К–1 |
0,001 |
–4,5 |
2,56 |
|
К–3 |
0,001 |
–10,0 |
4,95 |
|
|
К–7 |
0,001 |
–6,5 |
3,02 |
|
|
1–3 |
0,001 |
–5,5 |
2,34 |
|
|
3–14 |
0,001 |
8,0 |
2,22 |
|
|
7–14 |
0,003 |
4,5 |
1,26 |
Примечание. D Коэна – показатель эффекта. Размер эффекта для большинства значимых сравнений превышал 1,5, что соответствует наличию биологического значения
Таблица 3. Результаты сравнительного анализа численной плотности p53-позитивных лимфоцитов между зонами лимфатических узлов (критерий Фридмана для сравнения зон по срокам)
Table 3. Results of comparative analysis of the numerical density of p53-positive lymphocytes between lymph node zones (Friedman criterion for comparing zones by time)
|
Группы |
χ ² |
p-уровень |
Наиболее богатая зона |
Наиболее бедная зона |
|
Контроль (0) |
24,8; df=7 |
0,001 |
Мозговые тяжи (Me = 8,5) |
Субкапсулярный синус (Me = 0,0) |
|
1 сут. |
32,9; df=7 |
0,0001 |
Мозговые тяжи (Me = 26,0) |
Субкапсулярный синус (Me = 1,0) |
|
3 сут. |
42,3; df=7 |
0,0001 |
Мозговые тяжи (Me = 27,0) |
Первичные узелки (Me = 3,5) |
|
7 сут. |
38,7; df=7 |
0,0001 |
Мозговые тяжи (Me = 28,0) |
Первичные узелки (Me = 5,0) |
|
14 сут. |
36,9; df=7 |
0,0001 |
Мозговые тяжи (Me = 31,5) |
Мозговой синус (Me = 2,5) |
Примечание. Me – медиана, df – степень свободы.
Таблица 4. Значимые пост-хок попарные сравнения между зонами (критерий Вилкоксона с поправкой Бонферрони) Table 4. Significant post hoc pairwise comparisons between zones (Wilcoxon test with Bonferroni correction)
|
Сутки |
Количество значимых пар |
Ключевые значимые различия (p<0,05) |
|
0 |
12 из 28 |
МТ>вседругиезоны (p<0,001) ВЛУ>СКС (p=0,002) ПКЗ>СКС (p=0,004) |
|
1 |
18 из 28 |
МТ>вседругиезоны (p<0,001) ВЛУ>ПКЗ (p=0,003) КВ>СКС (p=0,001) |
|
3 |
22 из 28 |
МТ>всезоны (p<0,001) СКС>ПЛУ (p<0,001) Мозг.синус>Корк.вещ. (p=0,008) |
|
7 |
20 из 28 |
МТ>всезоны (p<0,001) СКС>ПЛУ (p<0,001) ПС>КВ (p=0,012) |
|
14 |
19 из 28 |
МТ>всезоны (p<0,001) СКС>МС (p<0,001) ПС>ПКЗ (p=0,015) |
В ранний период (1 сутки) для мозговых тяжей характерна ранняя активация плазматических клеток; для лимфоидных узелков – начало пролиферативного ответа; для синусов – минимальная активность. В острую фазу (3 сутки) для всех синусов характерна резкая активация (дренажная функция), максимальная дифференциация между зонами и пик воспалительного ответа. В фазу разрешения (7–14 сутки) сохраняется доминирование мозговых тяжей, происходит стабилизация синусной системы, уменьшается активность лимфоидных узелков.
С помощью теста Джонкхира-Терпстры линейный положительный тренд выявлен во вторичных лимфоидных узелках, мозговых тяжах и субкапсулярном краевом синусе, что свидетельствует о прогрессирующем накоплении p53-позитивных лимфоцитов в этих зонах. Квадратичный тренд в корковом веществе, паракорти-кальной зоне и периузелковом синусе указывает на пиковое изменение с последующей стабилизацией или снижением (табл. 5).
Таблица 5. Результаты теста Джонкхира-Терпстры для анализа временного тренда
Table 5. Results of the Jonckheere-Terpstra test for time trend analysis
|
Зона |
Статистика JT |
p-уровень |
Тренд |
|
КВ |
442,0 |
0,003 |
Квадратичный |
|
ПЛУ |
380,0 |
0,142 |
Отсутствует |
|
ВЛУ |
414,0 |
0,021 |
Линейный |
|
ПКЗ |
557,5 |
<0,001 |
Квадратичный |
|
МТ |
496,0 |
<0,001 |
Линейный |
|
СКС |
635,0 |
<0,001 |
Линейный |
|
ПС |
545,0 |
<0,001 |
Квадратичный |
|
МС |
343,0 |
0,587 |
Отсутствует |
Двухфакторный дисперсионный анализ выявил статистически значимое взаимодействие факторов «временная точка» и «анатомическая зона» [(F(28, 360)=7,89, p<0,001, η ²=0,38)], что указывает на различный характер временной динамики p53-позитивных лимфоцитов в разных зонах лимфатического узла.
Мощность общего теста (критерий Крускала– Уоллиса) для выявления различий между вре- менными группами более 0,80 по всем зонам. Для парных сравнений наименьшая мощность наблюдалась при сравнении 3-х и 14-х суток в паракортикальной зоне (0,63), а во всех остальных парах более 0,80.
Основные результаты, полученные в настоящем исследовании, могут быть интерпретированы следующим образом. Выраженные изменения наблюдались в мозговых тяжах, где количество p53-позитивных лимфоцитов прогрессивно увеличивалось от контрольных значений к 14 суткам после травмы. Максимальные абсолютные значения p53-позитивных лимфоцитов зафиксированы в мозговых тяжах на всех временных точках, что свидетельствует об особой роли этой зоны в клеточном ответе на травму. Наименьшие значения отмечались в контрольной группе во всех зонах. Линейный положительный тренд выявлен в мозговых тяжах и субкапсулярном краевом синусе, что свидетельствует о прогрессирующем накоплении p53-позитивных лимфоцитов в этих зонах. Квадратичный тренд в корковом веществе и па-ракортикальной зоне указывает на пиковое изменение с последующей стабилизацией или снижением. Общая мощность анализа значительно превысила общепринятый порог в 0,80. Это свидетельствовало о достаточном объеме выборки для выявления существующих эффектов. Значимое взаимодействие между факторами «временная точка» и «анатомическая зона» подтверждает, что различные зоны лимфатического узла по-разному реагировала на травматическое воздействие во времени.
ЗАКЛЮЧЕНИЕ
Травматическое повреждение бедра вызывает значительное увеличение численной плотности p53-позитивных лимфоцитов в паховом лимфатическом узле. Во всех исследованных зонах, за исключением первичных лимфоидных узелков и мозгового синуса, зафиксированы статистически значимые различия между контрольной группой и группами посттравматического периода (критерий Манна–Уитни с по- правкой Бонферрони). Размер эффекта (d Коэна) для большинства значимых сравнений превышал 1,5, что соответствует очень большому биологическому значению.
Мозговые тяжи являются доминирующей зоной накопления p53-позитивных лимфоцитов на всех сроках наблюдения. Согласно результатам критерия Фридмана, во всех временных точках (контроль, 1, 3, 7, 14 сутки) мозговые тяжи демонстрировали максимальные медианные значения, что достоверно отличало их от всех остальных зон.
Характер временной динамики экспрессии p53 имеет зональную специфичность. Линейный положительный тренд выявлен во вторичных лимфоидных узелках (p=0,021), мозговых тяжах (p<0,001) и субкапсулярном краевом синусе (p<0,001), что свидетельствует о прогрессирующем нарастании числа p53-позитивных клеток к 14-м суткам посттравматического периода. Квадратичный тренд установлен в корковом веществе (p=0,003), паракортикальной зоне (p<0,001) и периузелковом синусе (p<0,001), что отражает пиковое увеличение показателя на 3–7 сутки с последующей стабилизацией или снижением.
Наиболее ранние и выраженные изменения происходят в синусной системе и Т-зависимых зонах. В субкапсулярном краевом синусе и пара-кортикальной зоне статистически значимое увеличение p53-позитивных клеток регистрируется уже на 3-и сутки (p<0,001) с сохранением высоких значений до 14-х суток, что указывает на активные процессы миграции и апоптотиче-ской элиминации лимфоцитов на ранних этапах посттравматического периода.
Установлено статистически значимое взаимодействие факторов «время» и «анатомическая зона» [F(28, 360)=7,89, p<0,001, η ²=0,38)], что подтверждает гипотезу о различной чувствительности структурно-функциональных ком-партментов лимфатического узла к травматическому воздействию и независимом характере их временной динамики.
Исследование обладает достаточной статистической мощностью. Общая мощность критерия Краскела-Уоллиса для всех зон и мощность парных сравнений составила превышала 0,80, за исключением сравнения 3-х и 14-х суток в пара-кортикальной зоне (мощность 0,63), что подтверждает надежность полученных выводов.
Травматическое повреждение тканей инициирует сложный комплекс реакций со стороны иммунной системы, в котором лимфатические узлы выполняют ключевую роль, являясь не только дренажной системой, но и основным местом взаимодействия антигенпрезентирующих клеток с лимфоцитами. Белок p53, известный как супрессор опухолевого роста, играет важную роль в регуляции апоптоза и клеточного цикла, а его экспрессия в лимфоидных органах может служить индикатором стресс-индуцированной гибели клеток в ответ на травму.
Проведенное исследование позволило впервые детально охарактеризовать зональное распределение p53-позитивных лимфоцитов в паховом лимфатическом узле крыс в норме и в динамике после механической травмы мягких тканей бедра, выявить зоны с максимальной апоптотической активностью и установить характер временных трендов.


