Анализ экспрессии GFAP в пирамидном слое гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
Автор: Медников Дмитрий Сергеевич, Смирнов Алексей Владимирович, Тюренков Иван Николаевич, Куркин Денис Владимирович, Волотова Елена Владимировна, Бакулин Дмитрий Александрович
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 (73), 2022 года.
Бесплатный доступ
Представлены результаты иммуногистохимического исследования пирамидного слоя гиппокампа крыс с моделируемым стенозом общих сонных артерий с применением антител против кислого глиального фибриллярного белка (GFAP). Наиболее значимое увеличение экспрессии GFAP обнаружено в СА3 пирамидного слоя гиппокампа, где относительная площадь иммунопозитивного материала достоверно увеличилась на 6,6 % (р
Гиппокамп, крыса, стеноз общих сонных артерий, gfap
Короткий адрес: https://sciup.org/142235236
IDR: 142235236 | УДК: 616-005.4:611.813.14:616-092.9
Analysis of GFAP expression in the pyramidal layer of the hippocampus of rats in the carotid arteries stenosis experimental modeling
The article demonstrates the result of an immunohistochemical study of the pyramidal layer of the hippocampus of rats with simulated stenosis of the common carotid arteries using antibodies against glial fibrillary acidic protein (GFAP). The most significant increase in GFAP expression was found in CA3 of the pyramidal layer of the hippocampus, where the relative area of the immunopositive material significantly increased by 6.6 % (p
Текст научной статьи Анализ экспрессии GFAP в пирамидном слое гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
Среди множества функций астроцитарной глии, возможно, первостепенное значение имеет нейропротективная. Так, известно о роли астроцитов в защите от эксайтотоксического эффекта за счет активного удаления внеклеточного глутамата из синаптической щели [1, 2]. Помимо этого, астроциты принимают участие в регулировании концентрации внеклеточных ионов калия, синтезе и метаболизме ряда нейротрофических факторов, а также ангиогенезе [1]. Нейропротективная способность астроцитов может иметь решающее значение для ограничения степени ишемического повреждения и стать важным шагом к сосредоточению внимания на этих клетках как многообещающей мишени для терапии [3, 4].
Активация астроцитарной глии описана при различных патологических процессах, в том числе при ишемии головного мозга. Под активированными астроцитами понимается изменение фенотипа с перестройкой, в том числе основных белков цитосклета [1, 5].
К одним из важнейших промежуточных филаментов относится глиальный фибриллярный кислый белок (glial fibrillary acidic protein, GFAP). Участие в репаративных процессах, предполагаемое влияние на нейрогенез, значимая роль в направленном росте астроцитарных отростков и построении синаптических контактов обуславливают актуальность всестороннего изучения GFAP при хронической ишемии головного мозга [3, 6].
Имеются сведения о сниженной способности нейронов к выживанию, большем объеме повреждения и нарушенной нейропластичности у мышей с нокаутом GFAP на модели временной окклюзии средней мозговой артерии [7]. На модели фокальной ишемии головного мозга продемонстрирована усиленная экспрессия GFAP в СА1 гиппокампа, при этом GFAP-имму-нопозитивные астроциты одновременно усиленно экспрессировали даблкортин; в других исследованиях при моделировании ишемии выявлено усиление экспрессии GFAP в астроцитарной глии стриатума и черной субстанции, также несущей на себе метки делящихся про-гениторных клеток [8, 9].
Имеющиеся в литературе данные о функциях и роли GFAP при хронической ишемии головного мозга немногочисленны и во многом противоречивы, что актуализирует дальнейшее изучение.
ЦЕЛЬ РАБОТЫ
Качественными и количественными методами описать особенности экспрессии GFAP в пирамидном слое гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий.
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследование выполнено на 25 белых крысах-самцах. Животные были разделены на две группы: 1-я – контрольные крысы (n = 10), 2-я – крысы с моделируемым нарушением кровообращения (n = 15). Стеноз общих сонных артерий моделировался путем частичного ограничения кровотока с помощью наложения лигатур. Наркотизированное животное фиксировали, область шеи выбривали, обрабатывали 0,05%-м раствором хлоргексидина биглюконата. После выделения сонной артерии под нее подводили три лигатуры, располагаемые на расстоянии 2–3 мм друг от друга. Параллельно артерии закрепляли иглу (29G 1/2) от шприца (SFM Hospital Products GmbH, Германия), к которой привязывалась сонная артерия и которая затем убиралась таким образом, чтобы лигатуры оставались на заданном расстоянии. Оценку уровня локального кровотока осуществляли до и после стенозирования сонной артерии в двух точках, в месте сразу после наложения лигатур и в проекции средней мозговой артерии. После операции рану послойно ушивали, обрабатывали 0,05%-м раствором хлоргексидина биглюконата и 5%-м раствором йода, животных переносили в домашние клетки.
Через 20 дней после операции оценивалось психоневрологическое состояние, сохранность рефлексов, поведение и двигательная активность [10]. На 22-е сутки животных выводили из эксперимента с применением в качестве наркоза хлоралгидрата (400 мг/кг, интраперитонеально), декапитировали гильотинным методом, получали образцы головного мозга. Образцы головного мозга животных фиксировали в 10%-м растворе формалина, приготовленном на 0,2 mМ фосфатном буфере с дальнейшей гистологической проводкой и изготовлением серийных парафиновых срезов толщиной 5 мкм, которые окрашивали по стандартным методикам гематоксилином и эозином, тионином по Нисслю. При морфометрическом исследовании подсчитывали показатель удельного количества нейронов с признаками повреждения.
К признакам повреждения относили ги-перхромию ядра и цитоплазмы, веретеновидное сморщивание перикариона нейрона, деформацию перикариона нейрона в сочетании с гиперхромией ядра и цитоплазмы, а также гипохромию клетки (клетки-тени).
Иммуногистохимическое исследование проводили непрямым пероксидазно-антиперок-сидазным методом с использованием антител к GFAP (ready to use) согласно протоколу производителя, с использованием полимерной системы (Thermo Scientific, Fremont, CA). В качестве хромогена использовали DAB (диаминобензидин). Оценку изменения уровня экспрессии определяли путём подсчёта относительной площади (ОП) иммунопозитивного материала (ИМ) во всех зонах гиппокампа с использованием модуля Image Analysis программы ZEN 1.1.2.0 (Carl Zeiss Microscopy GmbH, Germany). Исследование микропрепаратов проводилось с помощью микроскопа «Axio Lab. A1» (Carl Zeiss Microscopy GmbH, Germany), фотодокументирование осуществляли камерой «AxioCam 105 color» (Carl Zeiss Microscopy GmbH, Germany).
Статистическую обработку данных проводили с использованием пакетов программ Statistica 6,0 (StatSoft, USA). Обобщенные данные представляли в виде медианы (Me) с указанием интерквартильного интервала [Q1;Q3]. Различия между группами оценивали по критерию Манна – Уитни (Mann – Whitney, U-test) и считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При гистологическом исследовании пирамидного слоя гиппокампа животных 2-й группы в СА1 было отмечено увеличение удельного количества нейронов с признаками повреждения, большинство среди которых составляли гиперхромные в сочетании с пикноморфной деформацией перикариона.
Удельное количество нейронов с признаками повреждения составило в этой зоне 31,2 [22,4; 41] %, что на 23 % больше по сравнению с группой 1 (см. табл.). Иммуногистохимическое исследование СА1 пирамидного слоя гиппокампа крыс с моделируемым стенозом сонных артерий с применением антител против GFAP не выявило достоверных отличий от контроля в относительной площади иммунопозитивного материала.
При гистологическом исследовании СА2 гиппокампа крыс 2-й группы достоверных отличий в удельном количестве поврежденных нейронов от контрольной группы не было выявлено. Наблюдались микроциркуляторные нарушения в виде умеренного перицеллюлярного и периваскулярного отека, единичных диапедез-ов эритроцитов и эритроцитарных стазов. При иммуногистохимическом исследовании СА2 пирамидного слоя гиппокампа крыс с моделируемым стенозом сонных артерий с применением антител против GFAP обнаружено увеличение экспрессии, увеличение ОП GFAP-позитивного материала составило здесь по сравнению с контролем 6,3 % (p < 0,01) и достигло 10,3 [7,8; 12,6] % (рис. 1). При гистологическом исследовании СА3 пирамидного слоя гиппокампа крыс 2-й группы обнаружено достоверное увеличение удельного количества поврежденных нейронов на 8,7 % по сравнению с контролем (p < 0,01) (см. табл.). Цитоархитектоника СА3 пирамидного слоя имела схожий характер с зонами СА1 и СА2, среди поврежденных пирамидных нейронов преобладали гиперхромные в сочетании с веретеновидно сморщенными перикарионами. При иммуногистохимическом исследовании СА3 пирамидного слоя гиппокампа крыс с моделируемым стенозом сонных артерий выявлено максимальное среди всех зон увеличение относительной площади GFAP-позитивного материала – на 6,6 % по сравнению с контролем (p < 0,001).
В СА3 сохранялась характерная для СА1 и СА2 картина расположения астроцитов – преимущественно за пределами пирамидного слоя, в пирамидном слое присутствуют активно ветвящиеся астроцитарные отростки (рис. 2). При гистологическом исследовании СА4 пирамидного слоя гиппокампа крыс 2-й группы достоверных отличий в удельном количестве поврежденных нейронов не выявлено, микроциркуляторные расстройства имели тот же характер, что и в остальных зонах: умеренный периваскулярный и перицеллюлярный отек, единичные эритроцитарные диапедезы. При иммуногистохимическом исследовании в пирамидном слое СА4 крыс 2-й группы также выявлено достоверное увеличение относительной площади GFAP-позитивного материала – на 3,3 % по сравнению с контролем (p < 0,001), таким образом, данный показатель составил 5,6 [5,1; 7] % (см. табл.). Как и в остальных зонах, в СА4 характер экспрессии был преимущественно выраженным.
Изменение удельного количества пирамидных нейронов с признаками повреждения и относительная площади GFAP-позитивного материала в пирамидном слое гиппокампа крыс с моделируемым стенозом общих сонных артерий
|
Параметр |
Контроль |
Моделируемый стеноз общих сонных артерий |
||||||
|
СА1 |
СА2 |
СА3 |
СА4 |
СА1 |
СА2 |
СА3 |
СА4 |
|
|
Удельное количество нейронов с признаками повреждения, % |
8,2 [6,8; 9,7] |
6,8 [4,5; 8,9] |
6,3 [4,6; 9] |
4,4 [2,9; 7,0] |
31,2 [22,4; 41]*** |
10,2 [7,1; 18] |
15 [8,2; 22,1]** |
7,7 [3; 10,2] |
|
Относительная пло щадь ИРМ, GFAP, % |
5,1 [4,2; 6,5] |
4,0 [2,2; 5,0] |
1,5 [1,0; 2,6] |
2,3 [1,8; 2,7] |
9,8 [6,1; 11,3] |
10,3 [7,8; 12,6] ** |
8,1 [5,3; 9,4] *** |
5,6 [5,1; 7] *** |
Примечание: *** p < 0,001 – различия достоверны по сравнению с контрольной группой, ** р < 0,01 – различия достоверны по сравнению с контрольной группой (использован критерий Манна – Уитни). Данные представлены в виде медианы с указанием интерквартильного размаха (Me [Q1; Q3]).
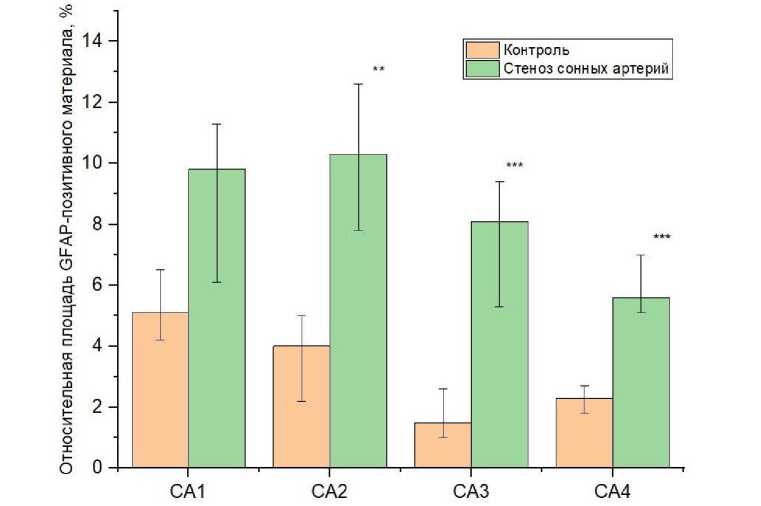
Рис. 1. Динамика изменения относительной площади GFAP-позитивного материала при моделировании стеноза общих сонных артерий:
*** – р < 0,001, ** – р < 0,01 – различия достоверны по сравнению с контрольной группой (использован критерий Манна – Уитни)
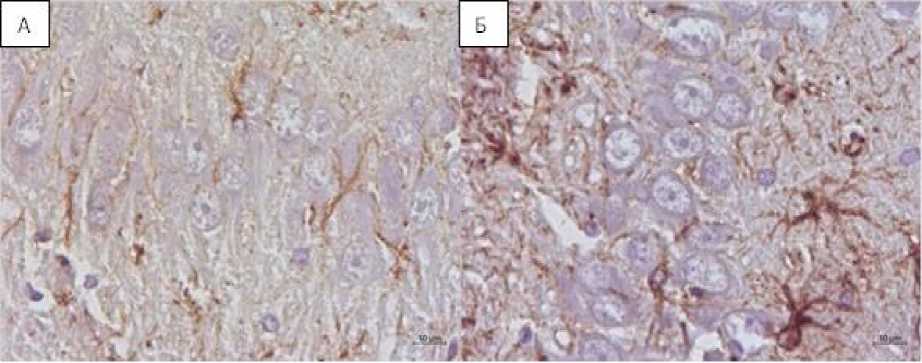
Рис. 2. Иммуногистохимическое исследование СА3 зоны гиппокампа крыс с применением антител против GFAP: А – контрольная группа; Б – группа крыс с моделируемым стенозом общих сонных артерий, увеличение площади и усиление интенсивности ИРМ. Ув. ×400, докраска гематоксилином
Выявленное нами достоверное увеличение относительной площади GFAP-позитивного материала в СА2, СА3 и СА4 пирамидного слоя гиппокампа крыс с моделируемым стенозом сонных артерий свидетельствует об активации астроцитарной глии, что согласуется с литературными данными, описывающими подобный астроглиальный ответ у крыс на различных моделях ишемии головного мозга [8, 9, 11]. Мы полагаем, что в гиппокампе крыс из обеих экспериментальных групп развивается реактивный астроглиоз, имеющий адаптивный характер и направленный на формирование глиального рубца с ограничением зоны поражения, а также и на трофическую поддержку нейронов в условиях ишемии. Выявленное достоверное увеличение удельного количества поврежденнных нейронов в зонах СА1 и СА3 пирамидного слоя гиппокампа крыс свидетельствует о большей чувствительности этих зон к хронической ишемии, вызванной стенозированием сонных артерий по сравнению с зонами СА2 и СА4 [12, 13].
ЗАКЛЮЧЕНИЕ
Таким образом, при экспериментальном моделировании стеноза сонных артерий в СА2, СА3 и СА4 пирамидного слоя гиппокампа крыс отмечается достоверное усиление экспрессии GFAP, при этом в СА3 увеличение относительной площади GFAP-позитивного материала сопровождается достоверным увеличением количества поврежденных нейронов, что свидетельствует о развитии адаптивных изменений, реактивной активации астроцитов и формировании глиального рубца.
Список литературы Анализ экспрессии GFAP в пирамидном слое гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
- Hol E. M., Pekny M. Glial fibrillary acidic protein (GFAP) and the astrocyte intermediate filament sys-tem in diseases of the central nervous system // Curr. Opin. Cell. Biol. 2015. Vol. 32. P. 121–130.
- Особенности структурных изменений пирамидного слоя гиппокампа крыс при гравитационном воз-действии в каудо-краниальном векторе с учетом экспрессии GFAP / А. В. Смирнов, М. В. Шмидт, Д. С. Медников [и др.] // Журнал анатомии и ги-стопатологии. 2017. Т. 6, № 2. С. 75–82.
- GFAP is necessary for the integrity of CNS white matter architecture and long-term maintenance of myelination / W. Liedtke, W. Edelmann [et al.] // Neuron. 1996. Vol. 17, № 4. P. 607–615.
- Tayebati S., Tomassoni K. D., Amenta F. Neuroin-flammatory markers in spontaneously hypertensive rat brain: an immunohistochemical study // CNS Neurol. Disord. Drug Targets. 2016. Vol. 15, No. 8. P. 995–1000.
- Особенности экспрессии HSP70, HSP90 и GFAP в гиппокампе крыс при моделировании гипертензивной энцефалопатии / А. В. Смирнов, Д. С. Медников, М. В. Шмидт [и др.] // Клиническая и экспе-риментальная морфология. 2017. Т. 22, № 2. С. 59–64.
- Sofroniew M. V., Vinters H. V. Astrocytes: biology and pathology / M. V. Sofroniew // Acta Neuropa-thology. 2010. Vol. 119. P. 7–35.
- High susceptibility to cerebral ischemia in GFAP-null mice / H. Nawashiro, M. Brenner, S. Fukui [et al.] // J. Cereb. Blood Flow Metab. 2000. Vol. 20, No. 7. P. 1040–1044.
- Neurogenesis in the striatum of the adult human brain / A. Ernst, K. Alkass, S. Bernard // Cell. 2014. Vol. 156. P. 1072–1083.
- Postinjury inhibition of miR-181a promotes restora-tion of hippocampal CA1 neurons after transient fore-brain ischemia in rats / B. B. Griffiths, Y. B. Ouyang, L. Xu [et al.] // eNeuro. 2019. Vol. 6, № 4.
- Функциональные и морфологические изменения в пирамидном слое гиппокампа крыс при энцефалопатии, вызванной длительными воздей-ствиями гравитационных перегрузок / И. Н. Тюренков, А. В. Смирнов, Д. С. Медников Д. С. [и др.] // Российский физиологический журнал им. И. М. Сеченова. 2019. Т. 105, № 3. С. 339–349.
- Release of glial fibrillary acidic protein is related to the neurovascular status in acute ischemic stroke / M. T. Wunderlich, M. Goertler // Eur. J. Neurol. 2006. Vol. 13, No. 10. P. 1118–1123.
- Экспрессия сериновой рацемазы в гиппокампе крыс при моделировании хронических нарушений мозгового кровообращения / А. В. Смирнов, Д. С. Медников, М. В. Шмидт [и др.] // Вестник волгоградского государственного медицинского университета. 2017. Т. 62, № 2. С. 47–51.
- Морфометрическое исследование пирамидного слоя гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий / Д. С. Медников, А. В. Смирнов, И. Н. Тюренков [и др.] // Волгоградский научно-медицинский журнал. 2021. № 2. С. 36–41.


