Анализ маркеров воспаления и маркеров апоптоза тромбоцитов при проведении антикоагулянтной терапии у пациентов с COVID-19
Автор: Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д., Поваров В.О., Никифоров А.А., Максаев Д.А., Чобанян А.А., Сучков И.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.18, 2023 года.
Бесплатный доступ
Цель исследования: провести анализ маркеров воспаления MCP1, IP 10 и маркеров апоптоза тромбоцитов фосфатидилсерина и кальретикулина при проведении антикоагулянтной терапии (АКТ) у пациентов с COVID-19. Материал и методы. В исследование включено 370 пациентов. Больные были разделены на 3 группы: 1 группа - 190 человек, которые получали низкомолекулярный гепарин (НМГ); 2 группа - 123 человека, принимавшие нефракционированный гепарин (НФГ); 3 группа - 57 человек, принимавших прямые оральные антикоагулянты (ПОАК) . Всем пациентам при поступлении и в конце стационарного лечения проводилась оценка общих лабораторных показателей, а также динамика специфических маркеров воспаления (IP-10 и MCP-1) и апоптоза тромбоцитов (фосфатидилсерин и кальретикулин) с июля 2021 по январь 2022 гг.
Венозные тромботические осложнения, антикоагулянтная терапия, коронавирусная инфекция, маркеры воспаления, апоптоз тромбоцитов
Короткий адрес: https://sciup.org/140303496
IDR: 140303496 | DOI: 10.25881/20728255_2023_18_4_45
Analysis of inflammatory markers and platelet apoptosis markers during anticoagulant therapy in patients with COVID-19
Purpose of the study: to analyze the inflammatory markers MCP1, IP 10 and platelet apoptosis markers phosphatidylserine and calreticulin during anticoagulant therapy (ACT) in patients with COVID-19. Material and methods. The study included 370 patients. The patients were divided into 3 groups: group 1 - 190 people who received low molecular weight heparin (LMWH); Group 2 - 123 people taking unfractionated heparin (UFH); Group 3 - 57 people taking direct oral anticoagulants (DOACs). All patients upon admission and at the end of hospital treatment were assessed for general laboratory parameters, as well as the dynamics of specific markers of inflammation (IP-10 and MCP-1) and platelet apoptosis (phosphatidylserine and calreticulin) from July 2021 to January 2022.
Текст научной статьи Анализ маркеров воспаления и маркеров апоптоза тромбоцитов при проведении антикоагулянтной терапии у пациентов с COVID-19
Антикоагулянтная терапия (АКТ) имеет широкий диапазон применения в клинической практике, который захватывает практически любой раздел медицины [1]. Кроме лечебной цели, она также выполняет задачу профилактики венозных тромботических осложнений
(ВТЭО) при различных факторах риска в травматологии и ортопедии, акушерстве и гинекологии и т.д. [2].
Но иногда в организме возникают совсем нестандартные явления, связанные с развитием тромбоза, которые могут быть вызваны выраженным воспалительным процессом [3]. Тогда механизм тромбообразования может

Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
быть заключен в единую систему гипервоспалительного ответа, который возник при атаке других видов живой природы на организм человека [4].
Пандемия COVID-19 преподнесла научному сообществу возможность изучения новых представлений о развитии тромбозов и эффективности применения известных вариантов АКТ у больных коронавирусной инфекцией [5]. Исследование COVID-19 ассоциированного тромбоза должно проводиться не только с помощью стандартных тестов коагуляции и воспаления, но также затрагивать патофизиологические механизмы данного заболевания [6].
Особый интерес среди лабораторных маркёров представляют показатели, которые встречаются одновременно при воспалении и гиперкоагуляции. К ним относятся белок-хемоаттрактант моноцитов-1 (MCP-1) и индуцируемый интерфероном гамма-белок-10 (IP-10), которые являются воспалительными цитокинами, связанные с тромбозом [7]. Высокий уровень цитокина MCP-1 был обнаружен в плазме крови пациентов с венозным тромбозом, а высокая концентрация IP-10 наблюдалась при эндотелиальной дисфункции, а это в свою очередь является предиктором тромбообразования [8]. Z. Varga и соавт. подтвердили в своём исследовании наличие прямой вирусной инвазии вируса SARS-CoV-2 в эндотелиальные клетки, что приводит к диффузному воспалению эндотелия и апоптозу клеток [9]. Данный механизм приводит к повреждению тромбогенной базальной мембраны, что обуславливает активацию тромбоцитов и факторов свертывания.
При апоптозе возрастает концентрация кальрети-кулина и фосфатидилсерина, которые связаны кальций зависимым образом [10]. Фосфатидилсерин представляет собой белок, который может экспонироваться на поверхности тромбоцитов и при их активации, происходит выработка тромбина, способствующего свертыванию [11]. Кальретикулин является кальций связывающий белком, функциями которого являются шаперонная функция и регуляция кальциевого гемостаза [12]. Кальретикулин способен связывать витамин К–зависимые факторы свертывания крови и ингибировать тромбоз, что было продемонстрировано в экспериментальной работе Kuwabara K. и соавторов на собачьей модели острой окклюзии коронарной артерии [13].
На основе способности IP-10, MCP-1, взаимодействовать как с тромботическим, так и с воспалительным каскадами, а также возможности фосфатидилсерина и кальретикулина принимать участие в апоптозе клеток крови и активации тромбоцитов, в нашем исследовании мы провели анализ данных показателей при использовании различных антикоагулянтных препаратов у пациентов с COVID-19.
Цель исследования : провести анализ маркеров воспаления MCP1, IP 10 и маркеров апоптоза тромбоцитов фосфатидилсерина и кальретикулина при проведении антикоагулянтной терапии у пациентов с COVID-19.
Материал и методы
Проведено проспективное наблюдательное клиническое исследование, включившее 370 пациентов, среди которых 235 женщин и 135 мужчин в возрасте от 54 до 71 года с подтвержденным COVID-19. Клиническая часть исследования выполнена на базе ковидных госпиталей ГБУ Рязанской области «Городская клиническая больница скорой медицинской помощи» и ГБУ Рязанской области «Областная клиническая больница».
Больные разделены на 3 группы в зависимости от назначенного антикоагулянта: 1 группа — назначен низкомолекулярный гепарин (НМГ) — 190 человек; 2 группа — назначен нефракционированный гепарин (НФГ) — 123 человека; 3 группа — пациенты, постоянно принимавшие прямые оральные антикоагулянты (ПОАК) амбулаторно по поводу сопутствующих заболеваний сердечно-сосудистой системы (фибрилляция предсердий) — 57 человек.
Критерии включения:
– пациенты старше 18 лет с подтвержденной коронавирусной инфекцией;
– письменное информированное согласие на участие в исследовании.
Критерии не включения в исследование:
-
– возраст менее 18 лет;
-
– беременные женщины;
-
– крайне тяжелые, агонирующие пациенты;
-
– невозможность назначения АКТ.
У всех больных оценивали клинико-анамнестические данные (пол, возраст, степень тяжести COVID 19), проводили ультразвуковое дуплексное сканирование (УЗДС) вен нижних конечностей и лабораторные показатели при поступлении и при выписке из стационара.
Среди общих лабораторных анализов оценивались С-реактивный белок (СРБ), ферритин и прокальцитонин (ПКТ), уровень активированного частичного тромбопластинового времени (АЧТВ), международного нормализованного отношения (МНО), протромбинового времени (ПВ), фибриногена и Д-димера. Лабораторные исследования специфических маркеров воспаления и апоптоза выполнялись в Центральной научно-исследовательской лаборатории ФГБОУ ВО «Рязанский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения РФ. Содержание MCP-1, IP-10, фосфатидилсерина и кальретикулина измеряли в сыворотке крови, которую получали центрифугированием 5 мл образца цельной крови и хранили при -80 °С до дальнейшего использования.
Статистическую обработку данных проводили с помощью программного обеспечения IBM SPSS Statistics 26. Для анализа качественных показателей применялись критерии Хи-квадрат Пирсона и Фишера. Оценка распределения количественных показателей проводилась с использованием критерия Колмогорова-Смирнова и Шапиро-Уилка (р>0,05).
Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
Проведение исследования одобрено решением локального этического комитета в ФГБОУ ВО «Рязанский государственный медицинский университет имени академика И.П. Павлова» Министерства здравоохранения РФ, протокол №3 от 11 октября 2021 г., и зарегистрировано на платформе ClinicalTrials.gov (идентификатор NCT05143567).
Результаты
Анализ возрастных категорий показал, что группы были сопоставимы по возрасту, объему вирусного поражения легких и степени тяжести COVID 19, но по гендерному признаку женщин было больше, чем мужчин (Табл. 1).
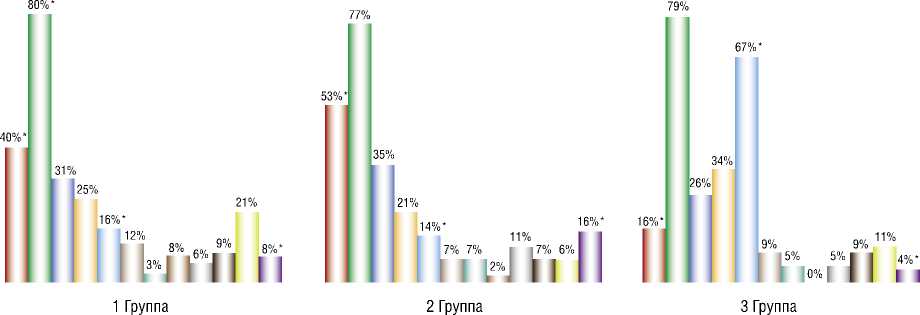
Сопутствующая патология в исследуемых группах представлена на рисунке 1, из которого следует что наибольшая частота заболеваний приходится на гипертоническую болезнь, ожирение и сахарный диабет.
Пациентов с ожирением, которые принимали ПОАК было мало (16% случаев), и в основном это были больные с ожирением 1 степени. В то же время при фибрилляции предсердий наблюдается обратная тенденция: данные пациенты (67% случаев) продолжали принимать ПОАК по поводу сопутствующей кардиологической патологии. Также обращает внимание, что у пациентов, получавших НМГ и НФГ (1 и 2 группы) были больные с ХЗВ (1 группа — 8,0% случаев, 2 группа — 16,0% случаев, р = 0,03), которые являются факторами риска ВТЭО.
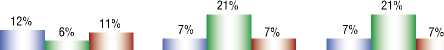
При проведении АКТ у особо тяжелых пациентов, на фоне коронавирусной инфекции, наблюдалось ухудше- ние состояния и данных больных переводили в отделение реанимации (Рис. 2). В реанимации пациентов переводили сначала на неинвазивную вентиляцию легких (НИВЛ), а при еще большем ухудшении состояния на ИВЛ. Перевод больного на ИВЛ сопровождался неблагоприятным прогнозом (100% летальность), и высокая частота смертности наблюдалась у пациентов получавших НФГ.
Табл. 1. Клинико-анамнестическая характеристика сравниваемых групп (Ме(Q1–Q3))
|
Показатель |
Группа НМГ (n = 190) |
Группа НФГ (n = 123) |
Группа ПОАК (n = 57) |
р |
|
Возраст |
63 (56-70) |
61 (50,5-68) |
63 (52,5-71) |
0,213 |
|
Пол n (%) - мужской |
85 (4,7) |
35 (28,2) |
15 (26,8) |
0,003 |
|
- женский |
105 (55,3) |
89 (71,8) |
41 (73,2) |
|
|
Компьютерная томография, n (%) - 0 |
11 (5,8) |
0 (0) |
2 (3,6) |
|
|
- 1 |
43 (22,6) |
23 (18,5) |
11 (19,6) |
0,025 |
|
- 2 |
81 (42,6) |
53 (42,7) |
17 (30,4) |
|
|
- 3 |
45 (23,7) |
37 (29,8) |
24 (42,9) |
|
|
- 4 |
10 (5,3) |
11 (8,9) |
2 (3,6) |
|
|
Степень тяжести COVID 19, n (%) - Легкая |
21 (11,1) |
6 (4,8) |
7 (12,5) |
0,021 |
|
- Средняя |
94 (49,5) |
50 (40,3) |
19 (33,9) |
|
|
- Тяжелая |
58 (30,5) |
48 (38,7) |
26 (46,4) |
|
|
- Крайне тяжелая |
17 (8,9) |
20 (16,1) |
4 (7,1) |
Примечание : НМГ — низкомолекулярный гепарин, НФГ — нефракцио-нированный гепарин, ПОАК — прямые оральные антикоагулянты.
I ■ Ожирение
I ■ Сахарный диабет
Фибрилляция предсердий Бронхиальная астма
-
■ Язвенная болезнь желудка Хроническая болезнь почек
I ■ Гипертоническая болезнь Ишемическая болезнь сердца Онкология
-
■ ■ Хроническая обструктивная болезнь легких
-
■ ■ Постинфарктный кардиосклеров
-
■ ■ Хронические заболевания вен
Рис. 1. Сопутствующая патология в исследуемых группах. Примечание: различия по ожирению: * — р<0.001, НМГ-НФГ р = 0.764, НМГ-ПОАК р = 0.024*, НФГ-ПОАК р<0.001. Различия по фибрилляции предсердий: * — р<0.001 НФГ-НМГ р = 0.924, НМГ-ПОАК р<0.013, НФГ-ПОАК р = 0.017. Различия по хроническим заболеваниям вен: * — р<0.001, НМГ-НФГ р = 0.671, НМГ-ПОАК р = 0.003, НФГ-ПОАК р = 0.002*.
Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
НИВЛ ИВЛ Летальность
I ■ нмг
I I НФГ II ПОАК
Рис. 2. Частота применение НИВЛ и ИВЛ в отделении реанимации и летальность в группах исследования. Примечание: НМГ — низкомолекулярный гепарин, НФГ — нефракционированный гепарин, ПОАК — прямые оральные антикоагулянты, НИВЛ — неинвазивная вентиляция легких, ИВЛ — инвазивная вентиляция легких.
Табл. 2. Динамика исследуемых показателей у пациентов группы НМГ
|
Показатель |
V0 (исх.) |
V1 |
p |
|
IP-10, пг/мл |
344.45 (163.17–648.23) |
36.07 (9.03–101.88) |
<0.001* |
|
МСР-1, пг/мл |
95.9 (65.75–144.8) |
61.3 (44.45–108.3) |
<0.001* |
|
Кальретикулин,пг/мл |
5.33 (2.7–12.6) |
5.26 (2.89–12.95) |
0.698 |
|
Фосфатидилсерин, пг/мл |
64.25 (44.63–86.5) |
76.15 (56.25–110.55) |
0.012* |
|
Эритроциты, х 1012/л |
4,77 (4,41–5,08) |
4.52 (4.1–4.93) |
0.065 |
|
Гемоглобин, г/л |
135 (122–145) |
127 (115–137) |
0.091 |
|
Лейкоциты, х 10 9 /л |
6,7 (4,7–9,2) |
5.18 (4.3–8.69) |
<0.001* |
|
Тромбоциты, х 10 9 /л |
189 (144–260) |
219 (176–302.5) |
0.009* |
|
СОЭ, мм/ч |
23 (11–33) |
14 (6–20) |
<0.001* |
|
Глюкоза, ммоль/л |
6.51 (5.7–7.96) |
5.07 (4.86–8.5) |
0.068 |
|
СРБ, мг/л |
57,8 (24–101,3) |
6.8 (1.7–15) |
<0.001* |
|
Ферритин, мкг/л |
738 (210–967) |
364 (324–497) |
<0.001 |
|
ПКТ, нг/мл |
0.357 (0.348–0.469) |
0.124 (0.054–0.364) |
0.014* |
|
АЧТВ, с |
34,25 (25,9–36,8) |
34.5 (26.3–36.95) |
0.954 |
|
ПВ, с |
13,2 (12,2–14,2) |
12 (11.05–12.95) |
0.076 |
|
Фибриноген, г/л |
6,2 (5,4–6,8) |
3.37 (2.8–4.92) |
<0.001* |
|
МНО |
1,11 (1,03–1,2) |
1.01 (0.95–1.09) |
0.079 |
|
D-димер, нг/мл |
0,68 (0,4–0,75) |
0.42 (0.36–0.465) |
0.016* |
Примечание : НМГ — низкомолекулярный гепарин; НФГ — нефракци-онированный гепарин; IP-10 — интерферон-гамма-индуцированный белок-10; МСР-1 — моноцитарный хемоаттрактантный белок-1;
СОЭ — скорость оседания эритроцитов; СРБ — С-реактивный белок; АЧТВ — активированное частичное тромбопластиновое время;
ПВ — протромбиновое время; МНО — международное нормализованное отношение; р — уровень значимости при сравнении средних значений исследуемых показателей в начале и конце терапии, полужирным шрифтом выделены значимые отличия.
Проведенный анализ динамики лабораторных показателей у пациентов, принимавших НМГ (1 группа), показал достоверное уменьшение концентрации общих и специфических провоспалительных маркеров: СРБ, ферритина, лейкоцитов, СОЭ, прокальцитонина, IP 10 и MCP1 (Табл. 2). Концентрация фосфатидилсерина увеличивается в конце АКТ, а уровень кальретикулина без достоверных отличий. В коагулограмме наблюдается снижение уровня фибриногена и Д-димера.
Пациенты принимавшие НФГ (2 группа) характеризуются тем, что среди общих лабораторных показателей снижается только уровень СРБ и СОЭ, но уровень фер-
Табл. 3. Динамика исследуемых показателей у пациентов группы НФГ
|
Показатель |
V0 (исх.) |
V1 |
p |
|
IP–10, пг/мл |
225.94 (86.93–490.45) |
50.2 (22.99–112.28) |
<0.001* |
|
МСР–1, пг/мл |
79.95 (50.7–125) |
71.45 (47.2–112.9) |
0.387 |
|
Кальретикулин,пг/мл |
2.92 (1.78–4.46) |
2.81 (1.01–4.51) |
0.102 |
|
Фосфатидилсерин, пг/мл |
66.7 (47.1–92.1) |
55.75 (43.2–91.6) |
0.346 |
|
Эритроциты, х 1012/л |
4,7 (4,3–5,03) |
4.5 (4.1–4.78) |
0.073 |
|
Гемоглобин, г/л |
138 (129–147) |
130 (120–142) |
0.127 |
|
Лейкоциты, х 10 9 /л |
6,8 (4,9–8,95) |
10.5 (8.1–13.55) |
<0.001* |
|
Тромбоциты, х 10 9 /л |
195 (166,5–256,5) |
258 (184–322.5) |
0.013* |
|
СОЭ, мм/ч |
19 (8–33,5) |
10 (2–22) |
0.003* |
|
Глюкоза, ммоль/л |
7.32 (6.1–9.5) |
9.3 (6.6–13.7) |
0.003* |
|
СРБ, мг/л |
66,3 (38–126,9) |
7.6 (4.05–13.35) |
<0.001* |
|
Ферритин, мкг/л |
848 (596–953) |
578.2 (367–986) |
0.233 |
|
ПКТ, нг/мл |
0.097 (0.07–0.173) |
0.066 (0.05–0.174) |
0.244 |
|
АЧТВ, с |
33,75 (27,8–40,5) |
29.6 (25.9–36.9) |
0.635 |
|
ПВ, с |
12,4 (11,2–13,4) |
11.6 (10.85–12.7) |
0.037* |
|
Фибриноген, г/л |
5,5 (3,28–5,55) |
2.43 (1.9–3.52) |
<0.001* |
|
МНО |
1,06 (0,98–1,14) |
1 (0.93–1.08) |
0.065 |
|
D–димер, нг/мл |
0,62 (0,37–1,01) |
0.48 (0.27–0.83) |
0.429 |
Примечание : НМГ — низкомолекулярный гепарин; НФГ — нефракци-онированный гепарин; IP–10 — интерферон–гамма–индуцированный белок–10; МСР–1 — моноцитарный хемоаттрактантный белок–1;
СОЭ — скорость оседания эритроцитов; СРБ — С–реактивный белок; АЧТВ — активированное частичное тромбопластиновое время;
ПВ — протромбиновое время; МНО — международное нормализованное отношение; р — уровень значимости при сравнении средних значений исследуемых показателей в начале и конце терапии, полужирным шрифтом выделены значимые отличия.
ритина и лейкоцитов без достоверных отличий (Табл. 3). Среди специфических маркеров снижается только IP 10, а МСР-1, фосфатидилсерин и кальретикулин без динамики. В коагулограмме наблюдается уменьшение протромбинового времени и фибриногена, но уровень Д-димера достоверно не снижается.
У больных, продолжавших получать ПОАК (3 группа), отмечено снижение концентрации IP 10, СОЭ, СРБ и нарастание концентрации ферритина, Д-димера (Табл. 4). Уровень МСР-1, фосфатидилсерина и кальретикулина у данных пациентов без достоверных отличий от начала АКТ. В коагулограмме наблюдается только нарастание концентрации Д-димера к концу стационарного лечения.
Также проведен статистический анализ специфических маркеров воспаления и апоптоза между группами в конце стационарного лечения. Отмечено, что концентрация IP-10 меньше у пациентов, принимавших НМГ. По уровню МСР-1 в конце проведения АКТ достоверных отличий не получено. Значения кальретикулина и фос-фатидилсерина высокие только у пациентов получавших НМГ.

Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
Табл. 4. Динамика исследуемых показателей у пациентов группы ПОАК
|
Показатель |
V0 (исх.) |
V1 |
p |
|
IP–10, пг/мл |
228.35 (80.8–534.16) |
39.24 (10.73–87.9) |
<0.001* |
|
МСР–1, пг/мл |
76.15 (41–112.1) |
58.25 (44.6–87.7) |
0.124 |
|
Кальретикулин,пг/мл |
3.61 (2.18–6.38) |
3.38 (1.79–6.78) |
0.783 |
|
Фосфатидилсерин, пг/мл |
57.7 (42.8–80.02) |
52.75 (42.6–86.4) |
0.805 |
|
Эритроциты, х 1012/л |
4,45 (4,2–4,83) |
4.25 (4–4.64) |
0.088 |
|
Гемоглобин, г/л |
132 (125–139,5) |
127 (120–135) |
0.132 |
|
Лейкоциты, х 10 9 /л |
7,6 (5,35–11,65) |
9.9 (7.59–11.8) |
0.072 |
|
Тромбоциты, х 10 9 /л |
235,5 (174–322) |
205 (177.5–307.5) |
0.727 |
|
СОЭ, мм/ч |
27 (15–43) |
12.5 (2.5–23.5) |
0.002* |
|
Глюкоза, ммоль/л |
7.55 (5.4–9.85) |
9.45 (6.65–13.25) |
0.036* |
|
СРБ, мг/л |
47,7 (17,2–104,4) |
9.1 (4.55–19.65) |
<0.001* |
|
Ферритин, мкг/л |
432,5 (278–884) |
579 (402–952) |
0.176 |
|
ПКТ, нг/мл |
0.055 (0.04–0.145) |
0.062 (0.045–0.085) |
0.877 |
|
АЧТВ, с |
30,9 (27,8–36,8) |
27.3 (24.8–32.8) |
0.104 |
|
ПВ, с |
11,85 (10,9–13) |
11.7 (10.9–12.6) |
0.153 |
|
Фибриноген, г/л |
4,4 (3–5,66) |
4.1 (2.8–5.25) |
0.075 |
|
МНО |
1,06 (0,98–1,14) |
1.05 (0.98–1.14) |
0.143 |
|
D–димер, нг/мл |
0,54 (0,39–0,84) |
0.7 (0.415–0.9) |
0.008* |
Примечание : НМГ — низкомолекулярный гепарин; НФГ — нефракци-онированный гепарин; IP–10 — интерферон–гамма–индуцированный белок–10; МСР–1 — моноцитарный хемоаттрактантный белок–1;
СОЭ — скорость оседания эритроцитов; СРБ — С–реактивный белок;
АЧТВ — активированное частичное тромбопластиновое время;
ПВ — протромбиновое время; МНО — международное нормализованное отношение; р — уровень значимости при сравнении средних значений исследуемых показателей в начале и конце терапии, полужирным шрифтом выделены значимые отличия.
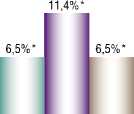
Анализ частоты развития ВТЭО показал, что во 2 группе имеет место высокая частота тромбоза легочных артерий de novo без источника в нижних конечностях — 11,40% случаев, которая была выявлена у умерших больных по данным аутопсии (Рис. 2). Также у пациентов, принимавших НФГ, имеет место высокая частота развития ТГВ и ТЭЛА с источником в нижних конечностях, по сравнению с пациентами, принимавших НМГ и ПОАК.
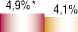
При анализе кровотечений наблюдается высокая частота возникновения фатальных больших кровотечений у пациентов, принимавших НФГ (2 группа) и представлены большими желудочно-кишечными, бронхиальными кровотечениями (Рис. 4).
Для оценки прогностической эффективности исследуемых параметров, мы связали полученные результаты тромботических осложнений, варианты АКТ, клиникоанамнестические данные и специфические маркеры. Методом логистической регрессии и ROC анализом установлено, что значение исходного уровня МСР-1 больше 90 пг/л повышает шансы развития ТЭЛА в 10,742 (1,135-101,647) раз (р = 0,038). Наличие ТГВ у пациента повышает шансы развития ТЭЛА в 15,757 (2,614-94,984)
Табл. 5. Межгрупповое сравнение лабораторных показателей в конце стационарного лечения (Ме(Q1–Q3))
|
Показатель |
Группа НМГ (n = 190) |
Группа НФГ (n = 123) |
Группа ПОАК (n = 56) |
p |
|
IP-10, пг/мл |
36.07 (9.03–101.88) |
50.2 (22.99–112.28) |
39.24 (10.73–87.9) |
р = 0.048* НМГ-НФГ р = 0.005* НМГ-ПОАК р = 0.176 НФГ-ПОАК р = 1 |
|
МСР-1, пг/мл |
61.3 (44.45–108.3) |
71.45 (47.2–112.9) |
58.25 (44.6–87.7) |
р = 0.348 |
|
Кальре-тикулин, пг/мл |
5.26 (2.89–12.95) |
2.81 (1.01–4.51) |
3.38 (1.79–6.78) |
р<0.001* НМГ-НФГ р<0.001* НМГ-ПОАК р = 0.024* НФГ-ПОАК р = 0.764 |
|
Фосфати-дилсерин, пг/мл |
76.15 (56.25–110.55) |
55.75 (43.2–91.6) |
52.75 (42.6–86.4) |
р = 0.001* НМГ–НФГ р = 0.021* НМГ–ПОАК р = 0.005 НФГ–ПОАК р = 0.913 |
Примечание : НМГ — низкомолекулярный гепарин, НФГ — нефракцио-нированный гепарин, ПОАК –прямые оральные антикоагулянты, IP–10 — интерферон–гамма–индуцированный белок–10;
МСР–1 — моноцитарный хемоаттрактантный белок–1.
1,6%
1,1%
■ I
0,5%
1 Группа 2 Группа 3 Группа
ТГВ ■ I ТЭЛА ■ ТЭЛА+ТГВ
Рис. 3. Частота ВТЭО в исследуемых группах (* — р < 0,05).
1 Группа 2 Группа 3 Группа
I I Большие Значимые Малые
Рис. 4. Частота различных вариантов кровотечений в исследуемых группах (* — р < 0,05).
раз (р = 0,003). Применение НФГ вместо НМГ или ПОАК повышает шансы развития ТЭЛА в 9,741 (1,088-87,213) раз (р = 0,042). Наличие ожирения повышает шансы развития ТЭЛА в 1,948 (1,001-3.791) раз (р = 0,0495). Площадь под ROC-кривой составила 0,895±0,06 с 95% ДИ: 0,777-1. При пороге классификации 0,07388 чувствительность 75%, специфичность — 95% (Рис. 5).
Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
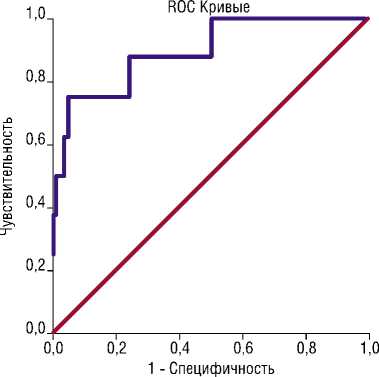
Рис. 5. Проверка прогностической модели прогнозирования ТЭЛА основанная на исходном уровне МСР1, наличии ТГВ, варианта антикоагулянтной терапии, наличия ожирения методом ROC-анализа.
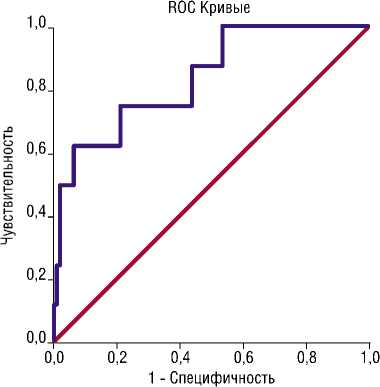
Рис. 6. Проверка прогностической модели прогнозирования ТЭЛА основанная на исходном уровне IP 10, наличии ТГВ, ожирения методом ROC-анализа.
Другая модель прогнозирования ТЭЛА основана на исходном уровне IP-10, наличии ТГВ у пациента, наличии ожирения у пациента с НКИ. Повышение исходного уровня интерферона на 700 пг/мл повышает шансы развития ТЭЛА в 7,936 (2,066-30,3) раз (р = 0,003). Наличие ТГВ у пациента повышает шансы развития ТЭЛА в 15,757 (2,614-94,984) раз (р = 0,003). Применение НФГ вместо НМГ или ПОАК повышает шансы развития ТЭЛА в 9,741 (1,088-87,213) раз (р = 0,042). Площадь под ROC-кривой составила 0,843±0,072 с 95% ДИ: 0,702-0,983. При пороге классификации 0,1142 чувствительность 62,5%, специфичность — 93,9% (Рис. 6).
Другая модель основана на маркере апоптоза тромбоцитов, наличию факторов риска ВТЭО и применение ИВЛ. Методом логистической регрессии и ROC анализом установлено, что повышение исходного уровня фосфатидилсерина выше 62,75 пг/мл снижает шансы развития ВТЭО в 1,033 (1,005-1,062) раз (р = 0,02). Наличие ХЗВ у пациента повышает шансы развития ВТЭО в 9.015 (2,784-29,191) раз (р<0,001). Применение ИВЛ у пациента повышает шансы развития ВТЭО в 7,925 (2,397-24,377) раз (р = 0,02). Площадь под ROC-кривой составила 0,858±0,056 с 95% ДИ: 0,748-0,968. Значимость модели — <0,001 (Рис. 7). При пороге классификации 0,072 чувствительность 75%, специфичность — 89,2%.
Обсуждение
Данные литературы указывают на высокую частоту развития ВТЭО при коронавирусной инфекции. Поэтому COVID-19-ассоциированный тромбоз можно назвать «сателлитом» инфекции SARS-CoV-2, который может сопровождать ее и после выписки из стационара. Причем особенностью данного инфекционного заболевания, является то, что ТЭЛА не всегда является осложнением ТГВ, а может встречаться первично в легочных артериях и быть тромбозом de novo [15]. По данным нашего ис-
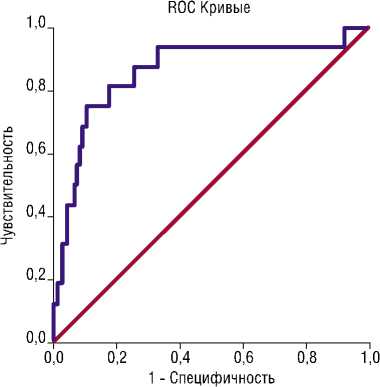
Рис. 7. Проверка прогностической модели прогнозирования ВТЭО основанная на исходном уровне фосфатидилсерина, наличии хронических заболеваний вен и применения искусственной вентиляции легких методом ROC-анализа.
следования, высокая частота ТЭЛА de novo отмечена у пациентов, получавших НФГ — 11,40% случаев, по сравнению с пациентами, принимавших НМГ — 1,1% и ПОАК — 0% (р<0,05).
Данные систематического обзора показывают, что частота развития ВТЭО больше в отделении реанимации, чем в стационаре. Так, например, в стационаре частота ТГВ составляет 20% случаев, ТЭЛА — 13% случаев, а в отделении реанимации частота данных осложнений растет до 28% случаев ТГВ и 19% случаев ТЭЛА [16]. По результатам нашего исследования перевод больного в реанимацию на ИВЛ из-за прогрессирования вирусного поражения легких, сопровождался 100% летальностью. Таким образом, тромботические события, возникающие при коронавирусной инфекции опосредованы COVID-
Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
19-ассоциированным гипервоспалительным синдромом, поэтому мы оценили взаимосвязь между воспалением и тромбозом, проанализировав динамику маркеров воспаления и апоптоза при использовании различных вариантов АКТ.
По данным нашего исследования в начале АКТ имеет место высокая концентрация провоспалительных показателей (СРБ, МСР-1, IP-10, ферритин, прокальцитонина, лейкоцитов) и коагуляционных маркеров (Д-димер, фибриноген). В конце АКТ наблюдается статистически достоверное увеличение концентрации фосфатидилсе-рина у пациентов, получавших НМГ, который является проапоптотическим белком, обладающим мощным прокоагулянтным потенциалом. Также следует отметить, что при высоких концентрациях данного показателя у пациентов получавших НМГ имеет место низкая частота ТГВ в сравнении с пациентами на НФГ (1,6% случаев против 6,5% случаев соответственно, р<0,05) и аналогично низкая частота ТЭЛА (1,1% случаев против 11,45% случаев соответственно, р<0,05). Также в конце АКТ у пациентов, получавших НМГ (1 группа) повышается концентрация кальретикулина, который является кальций-зависимым белком с антикоагулянтной активностью. Таким образом, у пациентов с низкой частотой ВТЭО (1 группа) имеет место увеличение концентрации как антиапоптотического белка, так и проапоптотического. Данный феномен можно объяснить тем, что наличие инициаторов апоптоза, необходимых для поддержания активности данного процесса, сопряжено с существованием факторов, препятствующие его развитию. К их числу от носится влияние антиапоп-тотических белков (Bcl-2) и кальретикулина.
Полученный результат вводит в диссонанс касаемо взаимосвязи апоптоза тромбоцитов и тромбоза, однако если рассмотреть лабораторные показатели в совокупности, которые отражают воспаление и коагуляцию, то становится очевидным, что при COVID-19 возникает целая серия взаимосвязанных процессов, которые могут повлиять на развитие ВТОЭ.
Динамика маркеров воспаления МСР-1 и IP-10 показывает то, что они снижаются совместно с общими показателями воспаления и коагуляции у пациентов, получавших терапию НМГ, эффективностью которой является низкая частота ВТЭО за весь период стационарного лечения. Диагностическая и прогностическая значимость данных маркеров отображена в литературных данных. MCP-1 экспрессируется макрофагами в ответ на действие широкого спектра цитокинов, но может также продуцироваться и фибробластами, эндотелиальными клетками [17]. IP-10 представляет собой белок, секретируемый моноцитами, эндотелиальными клетками, также в ответ на воспаление. IP-10 угнетает восстановление эндотелия при наличии любого воспалительного фактора, что объясняет распространенный эндотелиит, который наблюдается у пациентов с тяжелой и критической стадией COVID-19 [18]. По данным Yu Chen и соавторов уровень IP-10 и MCP-1 в сыворотке крови пациентов с крайне тяжелой степенью коронавирусной инфекции был выше, чем у пациентов с тяжелой степенью COVID-19, что доказывает, что IP-10 и MCP-1 являются биомаркерами, связанными с тяжестью заболевания. Кроме того, авторами установлено, что уровень IP-10 и MCP-1 был высоким у пациентов с повышенным уровнем Д-димера по сравнению с пациентами с низким уровнем Д-димера, следовательно, IP-10 и MCP-1 могут быть связаны с риском возникновения тромбоза у пациентов с COVID-19 [19].
Возвращаясь к АКТ следует отметить то, что НМГ имеют способность связываться с P- и L-селектином и различными цитокинами: интерлейкином 8 — IL-8, NAP-2, MIP-la, и в том числе MCP-1 [20–21]. Это подтверждено в нашем исследовании, когда у пациентов, принимавших НМГ, наблюдается статистически достоверное снижение концентрации MCP-1, а у пациентов принимавших НФГ и ПОАК уровень показателя был без тенденции к снижению. При этом данная динамика происходила при снижении уровня СРБ и ферритина у всех пациентов, но наиболее низкие концентрации общих воспалительных маркеров наблюдались у пациентов, получавших НМГ.
Таким образом, динамика специфических маркеров воспаления и апоптоза отражают сложный механизм нового патологического процесса — COVID-19-ассоции-рованного тромбоза и указывают на то, что этот процесс требует многостороннего подхода к пониманию возникновения тромботических осложнений. Однако, все эти сложные механизмы происходят с пациентами имеющие ранее известные факторы риска ВТЭО и сопутствующие заболевания, которые в совокупности с лабораторными показателями и вариантами АКТ нашли отражение в наших прогностических моделях возникновения ВТЭО. К таким факторам относятся ожирение, наличие ХЗВ, применение ИВЛ, которые в свое время также были выделены учеными как причина ВТЭО.
Заключение
Исходный уровень маркеров воспаления и апоптоза тромбоцитов у пациентов с COVID-19 имеет высокие значения, что обусловлено несколькими патофизиологическими процессами происходящими при гипервоспалительном ответе организма на вирус. Снижении уровня провоспалительных маркеров СРБ, ферритина, IP-10, МСР 1 и коагуляционных маркеров (Д-димера и фибриногена) наиболее выраженно у пациентов получавших НМГ. Повышение исходного уровня МСР-1 больше 90 пг/л повышает шансы развития ТЭЛА в 10,742 (1,135-101,647) раз (р = 0,038), а увеличение концентрации IP 10 на 700 пг/мл повышает шансы развития ТЭЛА в 7,936 (2,066-30,3) раз (р = 0,003). Статистически значимое повышение маркеров апоптоза (фосфатидилсерина и кальретикулина) отмечены у пациентов, получавших профилактику ВТЭО низкомолекулярным гепарином. Повышение исходного уровня фосфатидилсерина выше 62,75 пг/мл снижает шансы развития ВТЭО в 1,033 (1,005-1,062) раз (р = 0,02).

Агапов А.Б., Калинин Р.Е., Мжаванадзе Н.Д. и др.
АНАЛИЗ МАРКЕРОВ ВОСПАЛЕНИЯ И МАРКЕРОВ АПОПТОЗА ТРОМБОЦИТОВ ПРИ ПРОВЕДЕНИИ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ У ПАЦИЕНТОВ С COVID-19
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Анализ маркеров воспаления и маркеров апоптоза тромбоцитов при проведении антикоагулянтной терапии у пациентов с COVID-19
- Калинин Р.Е., Сучков И.А., Агапов А.Б. и др. Анализ факторов риска венозных тромбоэмболических осложнений и различных вариантов антикоагулянтной терапии у пациентов с новой коронавирусной инфекцией // Российский медико-биологический вестник имени академика И.П. Павлова. — 2023. — №31(2). — С.243-50. [Kalinin R.E., Suchkov I.A., Agapov A.B. et al. Analysis of risk factors for venous thromboembolic complications and different variants of anticoagulant therapy in patients with novel coronavirus infection. Rossijskij mediko-biologicheskij vestnik imeni akademika I.P. Pavlova. 2023; 31(2): 243-50. (In Russ.)] doi: 10.17816/PAVLOVJ110956.
- Селиверстов Е.И, Лобастов К.В., Илюхин Е.А. и др. Профилактика, диагностика и лечение тромбоза глубоких вен. Рекомендации российских экспертов // Флебология. — 2023. — №17(3). — С.152-296. [Seliverstov EI, Lobastov KV, Ilyukhin EA, et al. Prevention, Diagnostics and Treatment of Deep Vein Thrombosis. Russian Experts Consensus. Flebologiya. 2023; 17(3): 152-296. (In Russ.)] doi: 10.17116/flebo202317031152.
- Бородина И.А., Селезнева И.А., Борисова О.В. и др. Группы крови и секреторное состояние при COVID-19 // Наука молодых (Eruditio Juvenium). — 2021. — №9(4). — С.589-96. [Borodina IA, Selezneva IA, Borisova OV, et al. Blood groups and secretory state in COVID-19. Nauka molodyh (Eruditio Juvenium). 2021; 9(4): 589-596. (In Russ.)] doi: 10.23888/HMJ202194589-596.
- Xu Z, Shi L, Wang Y, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir Med. 2020; 8(4): 420-422. doi: 10.1016/S2213-2600(20)30076-X.
- Wang T, Chen R, Liu C, Liang W, Guan W, Tang R, et al. Attention should be paid to venous thromboembolism prophylaxis in the management of COVID19. Lancet Haematol. 2020; 7: e362-3. doi: 10.1016/S2352-3026 (20)30109-5.
- Carsana L, Sonzogni A, Nasr A, et al. Pulmonary post-mortem findings in a series of COVID-19 cases from northern Italy: a two-centre descriptive study, Lancet Infect, Dis, 2020; 20(10): 1135-1140. doi: 10.1016/S1473-3099 (20)30434-5.
- Mercier O, Arthur Ataam J, Langer NB, Dorfmuller P, Lamrani L, Lecerf F, et al. Abnormal pulmonary endothelial cells may underlie the enigmatic pathogenesis of chronic thromboembolic pulmonary hypertension. J Heart Lung Transplant. 2017; 36(3): 305-14.
- Lupieri A, Smirnova NF, Solinhac R, Malet N, Benamar M, Saoudi A, et al. Smooth muscle cells-derived CXCL10 prevents endothelial healing through PI3Kγ-dependent T cells response. Cardiovasc Res. 2020; 116: 438-49. doi: 10.1093/CVR/CVZ122.
- Varga Z, Flammer AJ, Steiger P, Haberecker M, Andermatt R, Zinkernagel AS, Mehra MR, Schuepbach RA, Ruschitzka F, Moch H. Endothelial cell infection and endotheliitis in COVID-19. Lancet. 2020; 395(10234): 1417-1418. doi: 10.1016/S0140-6736(20)30937-5.
- Dai E, Stewart M, Ritchie B, Mesaeli N, et al. Calreticulin, a potential vascular regulatory protein, reduces intimal hyperplasia after arterial injury. Arterioscler Thromb Vasc Biol. 1997; 17(11): 2359-68. doi: 10.1161/01.atv.17.11.2359.
- Rezende SM, Simmonds RE, Lane DA. Coagulation, inflammation, and apoptosis: different roles for protein S and the protein S-C4b binding protein complex. Blood. 2004; 103(4): 1192-201. doi: 10.1182/blood-2003-05-1551.
- Zimmerman KA, Xing D, Pallero MA, Lu A, et al. Calreticulin Regulates Neointima Formation and Collagen Deposition following Carotid Artery Ligation. J Vasc Res. 2015; 52(5): 306-20. doi: 10.1159/000443884.
- Kuwabara K, Pinsky DJ, Schmidt AM, et al. Calreticulin, an antithrombotic agent which binds to vitamin K-dependent coagulation factors, stimulates endothelial nitric oxide production, and limits thrombosis in canine coronary arteries. J Biol Chem. 1995; 270(14): 8179-87. doi: 10.1074/jbc. 270.14.8179.
- Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 14 (27.12.2021). М.: Министерство здравоохранения Российской Федерации, 2021. — 233с. Доступно по: https://static.minzdrav.gov.ru/system/attachments/attaches/000/059/041/original/ВМР_COVID-19_V14_27-12-2021.pdf. Ссылка действительна на 20.06.2023. [Interim guidelines. Prevention, diagnosis and treatment of novel coronavirus infection (COVID-19). Version 14 (27.12.2021). Moscow: Ministerstvo zdravoohraneniya Rossijskoj Federacii, 2021. 233 рp. Available at: https://static.minzdrav.gov.ru/system/attachments/attaches/000/059/041/original/ВМР_COVID-19_V14_27-12-2021.pdf. Accessed: 20.06.2023. (In Russ.)]
- Morici N, Podda G, Birocchi S, et al. Enoxaparin for thromboprophylaxis in hospitalized COVID-19 patients: The X– COVID-19 Randomized Trial. Eur J Clin Invest. 2022; 52(5): e13735. doi: 10.1111/eci.13735.
- Cui S, Chen S, Li X, et al. Prevalence of venous thromboembolism in patients with severe novel coronavirus pneumonia. J Thromb Haemost. 2020; 18(6): 1421-4. doi: 10.1111/jth.14830.
- Van Den Borne P, Quax PHA, Hoefer IE, Pasterkamp G. The multifaceted functions of CXCL10 in cardiovascular disease. BioMed Res Int. 2014: 893106. doi: 10.1155/2014/893106.
- Mir Seyed Nazari P, Marosi C, Moik F, et al. Low systemic levels of chemokine C-C motif ligand 3 (CCL3) are associated with a high risk of venous thromboembolism in patients with glioma. Cancers (Basel). 2019; 11(12): 2020. doi: 10.3390/cancers11122020.
- Chen Y, Wang J, Liu C, et al. IP-10 and MCP-1 as biomarkers associated with disease severity of COVID-19. Molecular Medicine. 2020; 26(1). doi: 10.1186/s10020-020-00230-x.
- Walenga JM, Jackson CM, Kessler CM. Low molecular weight heparins differ substantially: impact on developing biosimilar drugs. Semin Thromb Hemost. 2011; 37(3): 322-327. doi: 10.1055/s-0031-1274515.
- Калинин Р.Е., Сучков И.А., Агапов А.Б., Мжаванадзе Н.Д., Максаев Д.А., Чобанян А.А. Коагулопатия и факторы риска у пациентов с тяжёлой степенью COVID-19 // Тромбоз, гемостаз и реология. — 2022. — №4. — С.64-74. [Kalinin RE, Suchkov IA, Agapov AB, Mzhavanadze ND, Maksaev DA, Chobanyan AA. Coagulopathy and risk factors in patients with severe COVID-19. Thrombosis, hemostasis and rheology. 2022; 4: 64-74. (In Russ.)] doi: 10.25555/THR.2022.4.1042.


