Анализ нарушений связывания кортикостероидов с белками плазмы крови в патогенезе острой лучевой болезни
Бесплатный доступ
Анализ нарушений связывания кортикостероидов с белками плазмы крови при остром лучевом синдроме позволяет уточнить механизмы и закономерности патологических изменений гормонального уровня организма в патогенезе острой лучевой болезни. Актуальность исследования определяется наличием в настоящее время рисков возникновения новых техногенных катастроф и угрозы радиационной безопасности. Полученные результаты позволяют расширить ряд теоретических положений радиобиологии об основных закономерностях связывания кортикостероидов с белками плазмы крови с учётом её различных фракций, позволяющих определить роль свободных кортикоидов в гормональном эффекте при острой лучевой болезни. Целью настоящей работы является исследование основных закономерностей связывания кортикостероидов с белками плазмы крови в патогенезе острой лучевой болезни животных. Опыты проведены на 20 кроликах-самцах и 475 белых беспородных крысах. Предварительно экспериментальные животные были адаптированы к условиям эксперимента. Общее g-облучение животных проводили на электронном гамма-облучателе (ЭГО-2) при средней мощности дозы 5,75 Гр/мин. Кроликов облучали в дозе 8 Гр, крыс - в дозе 8,5 Гр. Общее содержание 11-оксикортикостероидов (11-ОКС), мкг%, определяли флюориметрическим методом в авторской модификации. Количество свободных кортикостероидов определялось по разнице содержания их в цельной плазме и в её белковой фракции после разделения на сефадексе G-25. Получены результаты, демонстрирующие изменения фракционного состава 11-ОКС в плазме крови в патогенезе острой лучевой болезни у животных с моно- и двухфазной кривой адренокортикальной реакции на облучение. Обнаружены нарушения связывания кортикостероидов с белками плазмы крови, следствием чего является увеличение свободных, биологически активных гормонов в разгаре лучевой болезни. Наличие в плазме крови не связанных с белками и более мобильных вследствие этого стероидов может вызвать гиперкортикоидное состояние при нормальном или даже сниженном уровне гормонов в крови. Длительное влияние «скрытого» гиперкортицизма, таким образом, может являться фактором, усугубляющим клиническое течение острой лучевой болезни.
Ионизирующее излучение, острая лучевая болезнь, кора надпочечников, адренокортикальная реакция, кортикостероиды, плазма крови, белково-стероидное взаимодействие, гиперкортицизм, связанные 11-окс, свободный гормон
Короткий адрес: https://sciup.org/170195742
IDR: 170195742 | УДК: 616-001.28-092+616.453 | DOI: 10.21870/0131-3878-2022-31-3-131-138
On the problem of impaired binding of corticosteroids to blood plasma proteins in the pathogenesis of acute radiation sickness
The study of violations of the binding of corticosteroids to blood plasma proteins in acute radiation syndrome allows us to clarify the mechanisms and patterns of pathological changes in the hormonal level of the body in the pathogenesis of acute radiation sickness. The relevance of the study is determined by the current risks of new man-made disasters and the threat to radiation safety. The results of the study make it possible to expand a number of theoretical positions of radiobiology on the main regularities of the binding of corticosteroids to blood plasma proteins, taking into account its various fractions, which make it possible to determine the role of free corticoids in the hormonal effect in acute radiation sickness. The purpose of this work is to study the main patterns of binding of corticosteroids to blood plasma proteins in the pathogenesis of acute radiation sickness in animals. The experiments were carried out on 20 male rabbits and 475 outbred rats. Previously experimental animals were adapted to the conditions of the experiment. The total g-irradiation of animals was carried out on the EGO-2 unit at an average dose rate of 575 R/min. Rabbits were irradiated at a dose of 8 Gy, rats at a dose of 8,5 Gy. The total content of 11-OCS was determined by the fluorimetric method in the author's modification. The amount of free corticosteroids was determined by the difference in their content in whole plasma and in its protein fraction after separation on Sephadex G-25. Results have been obtained demonstrating changes in the fractional composition of 11-OCS in blood plasma in the pathogenesis of acute radiation sickness in animals with mono- and biphasic curves of adrenocortical response to irradiation. Disturbances in the binding of corticosteroids to blood plasma proteins were found, resulting in an increase in free, biologically active hormones in the midst of radiation sickness. The presence in the blood plasma of non-protein-bound and therefore more mobile steroids can cause a hypercorticoid state with normal or even reduced levels of hormones in the blood. The long-term effect of "hidden" hypercortisolism, therefore, may be a factor that aggravates the clinical course of acute radiation sickness.
Текст научной статьи Анализ нарушений связывания кортикостероидов с белками плазмы крови в патогенезе острой лучевой болезни
Воздействие на организм ионизирующей радиации в дозах, вызывающих развитие острой лучевой болезни, неизменно сопровождается изменением гормонального уровня организма. Общие закономерности и механизмы воздействия ионизирующих излучений на реакцию гипофизарно-адренокортикальной системы, а также роль связывания кортикостероидов с белками плазмы крови при действии радиации раскрыты в ряде современных адаптационных теорий [1-7]. Проблеме белково-стероидного взаимодействия при различных патологических процессах, в том числе и при остром лучевом синдроме, в организме животных и человека, начиная с середины прошлого столетия, были посвящены многочисленные работы зарубежных и отечественных учёных. Однако в современных научных работах данная проблематика практически не освещается.
В современных зарубежных работах вопросы белково-стероидного взаимодействия раскрыты в ряде клинических исследований, посвящённых изучению вопросов связывания кортикостероидов с белками плазмы крови в гормональном взаимодействии гипоталамо-гипофизарно-
Омельчук Н.Н. - зав. кафедрой, д.б.н., проф. РУДН.
надпочечниковой системы при различных патологических состояниях организма человека [8-15]. В отечественной науке по проблеме белково-стероидного взаимодействия и специфике нарушений связывания кортикостероидов с белками плазмы крови при остром лучевом синдроме имеются лишь отдельные публикации, в том числе и автора настоящего исследования [16-19].
Таким образом, следует признать, что в настоящее время имеет место недостаточный научно-практический интерес к проблеме белково-стероидного взаимодействия в патогенезе острой лучевой болезни. Отметим теоретическую значимость данной проблемы, решение которой позволяет уточнить ряд положений радиобиологии об основных закономерностях связывания кортикостероидов с белками плазмы крови с учётом её различных фракций, что даёт возможность выявить роль свободных кортикоидов в гормональном эффекте при острой лучевой болезни. Возможность проведения более точного прогноза течения лучевой болезни, а также использования полученных результатов в лечебно-диагностической практике в отношении пациентов с лучевой болезнью и пациентов с нарушением эндокринного статуса отражает практическую значимость исследуемой проблемы.
Материалы и методы
Эксперименты были проведены на 20 кроликах-самцах породы шиншилла, весом 3,0-3,5 кг и на 475 белых крысах-самцах линии Wistar, весом 180-200 г. Для исключения неспецифических воздействий на посттрадиционную реакцию коры надпочечников всех животных предварительно в течение 10-15 дней адаптировали к условиям эксперимента, ежедневно проводя ряд процедур, необходимых для проведения данного опыта, во время которого животных помещали в аппарат, не включая его. Сроки, необходимые для адаптации, устанавливали экспериментально на основании оценки уровня кортикостероидов в крови животных: если в течение 3 ч после воздействия неспецифических факторов содержание кортикостероидов в крови находилось в пределах нормальных величин, животных считали адаптированными к условиям эксперимента.
Общее γ-облучение животных проводили на установке ЭГО-2 при средней мощности дозы 575 Р/мин. Животных облучали в дозе, вызывающей острую лучевую болезнь IV стадии: кроликов облучали в дозе 8 Гр, крыс – в дозе 8,5 Гр. Исследуемые показатели у облучённых животных определяли в динамике лучевой болезни. Сроки наблюдения после облучения в экспериментах на кроликах и крысах были различными. Внимание обращалось на характер изучаемых процессов сразу после облучения (через 1-3 ч) и в разгаре острой лучевой болезни (1-30 сут), поскольку, как известно, реакция коры надпочечников на ионизирующее излучение состоит из двух фаз: ранней (в первые часы после облучения) и поздней (через несколько дней после облучения).
Общее содержание 11-ОКС, мкг%, в плазме периферической крови определяли с помощью флюорометрического метода Guillemin et al. [20] в авторской модификации. Применяемый метод основан на способности 11-ОКС флюоресцировать в спирто-кислотном реагенте. Эта реакция кортикостероидов в этанолсернокислотном реагенте специфична для 11-ОКС. В указанных реагентах после протонизации ∆4- 3-кетогруппы в кислой среде происходит взаимодействие ∆4- 3-кетогруппы с II-гидроксильной группой других молекул кортикостероидов. В результате образуются устойчивые межмолекулярные комплексы, которые дают полосу поглощения с максимумом при 470 ммк и специфичную полосу флюоресценции при 525 ммк. Интенсивность флюоресценции измеряли на спектрофлюорометре ХИТАЧИ МР-2 при длине волны возбуждения 470 ммк, флюоресценции – 525 ммк. Интенсивность флюоресценции исследуемых субстратов в каждом опыте сравнивали с интенсивностью флюоресценции растворов соответствующих кортикостероидов различной концентрации.
Для определения свободной и связанной с белком фракций 11-ОКС использовали метод гельфильтрации De Moor et al. [21] в авторской модификации. Гель-фильтрация наименее трудоёмка, позволяет определить специфическое связывание 11-ОКС с кортикостероидсвязывающим глобулином (КСГ), причём в отличие от других методов, даёт возможность измерить абсолютную величину связывания. Количество свободных кортикостероидов определялось по разнице содержания их в цельной плазме и в её белковой фракции после разделения на сефадексе G-25.
Результаты и их обсуждение
Изменения фракционного состава 11-ОКС в плазме крови кроликов после облучения в дозе 8 Гр представлены на рис. 1.
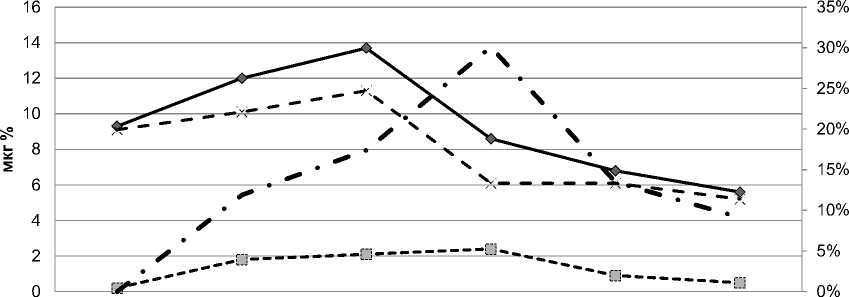
До облучения 30 мин. час после 1,5-2 часа после 4 сутки после 6 сутки после 8 сутки после облучения облучения облучения облучения облучения
—о— Общий уровень 11-ОКС Свободные 11-ОКС
— * —Связанные 11-ОКС Свободные 11-ОКС, %
Рис. 1. Изменение фракционного состава 11-ОКС в плазме крови кроликов после облучения в дозе 8 Гр.
При этом были обнаружены значительные изменения белково-стероидного комплекса. У здоровых кроликов все циркулирующие в крови кортикостероиды практически полностью связаны с белками плазмы крови. Через 30 мин и особенно через 1,5-2 ч после облучения свободные 11-ОКС обнаруживались у всех обследованных животных. Свободная фракция гормона на этот срок достигала в среднем 17,4% от общего количества кортикостероидов. Особенно заметное увеличение содержания свободного гормона в крови кроликов наблюдалось через 4 суток после облучения. Около 30,1% от общего количества гормонов находилось в свободном состоянии. Появление не связанной с белком фракции гормона наблюдалось на фоне нормального или даже сниженного общего уровня стероидов в крови, что, вероятно, может вызвать гиперкортикоидное состояние.
Получены результаты изменения общего содержания 11-ОКС в крови в динамике лучевой болезни у животных с двухфазной кривой. Содержание у крыс в крови 11-ОКС суммарно и по фракциям после облучения в дозе 8,5 Гр показано на рис. 2.
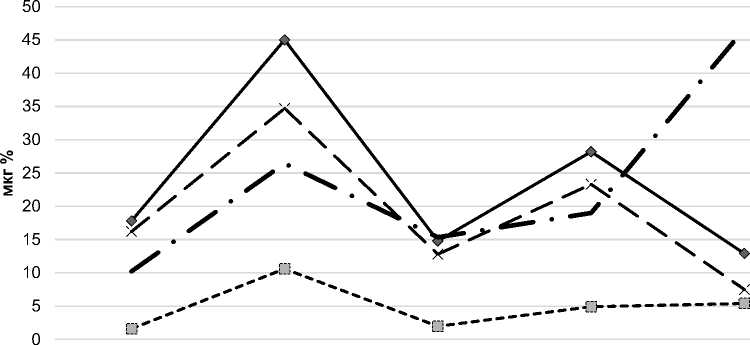
До облучения 1 час после 1 сутки после 3 сутки после 10 сутки после облучения облучения облучения облучения
• Общий уровень 11-ОКС
Свободные 11-ОКС
45%
40%
35%
30%
25%
20%
15%
10%
5%
0%
^■^■^ ^' Связанные 11-ОКС
^^^^™ • Свободные 11-ОКС, %
Рис. 2. Изменение фракционного состава 11-ОКС в плазме крови крыс после облучения в дозе 8,5 Гр.
У здоровых крыс около 9% кортикостероидов находилось в свободном состоянии. Через 1 ч после облучения общий уровень 11-ОКС в крови резко повышался, через сутки возвращался к норме, вновь поднимался на 3-и сутки лучевой болезни и падал на 10-е сутки ниже исходного.
Концентрация свободных 11-ОКС через 1 ч после облучения также повышалась, составляя 23,8% от общего уровня гормона, и нормализовалась через сутки. Затем она вновь увеличивалась, оставаясь повышенной на 3-и и 10-е сутки лучевой болезни. Заслуживает внимания, что у крыс на 3-и сутки лучевой болезни в период вторичной реакции, когда общий уровень 11-ОКС более, чем в 2 раза превышал этот показатель по сравнению с показателем на 10-е сутки, свободные кортикостероиды составляли 17,1% от общего уровня, а на 10-е сутки при общем уровне кортикостероидов даже ниже нормы около 42% кортикостероидов, содержащихся в крови, не были связаны с белками плазмы крови.
Таким образом, как у крыс, так и у кроликов, в динамике острой лучевой болезни наблюдается период скрытого гиперкортицизма, который характеризуется ростом концентрации свободного гормона на фоне даже сниженного общего уровня кортикостероидов в плазме крови. Содержание свободной фракции увеличивается в первые часы и в разгаре лучевой болезни, причём в первые часы это увеличение происходит на фоне повышенного общего содержания кортикостероидов, а в разгаре лучевой болезни на фоне как повышенного, так и сниженного общего уровня.
Заключение
Обобщение полученных результатов в экспериментах на двух видах животных, позволило вывести несколько закономерностей.
-
1. После действия ионизирующей радиации нарушается связывание кортикостероидов с белками плазмы крови, следствием чего является увеличение свободных, биологически активных гормонов в разгаре лучевой болезни.
-
2. Независимо от колебаний общего уровня кортикостероидов, содержание их свободной фракции на всём протяжении лучевой болезни было повышенным. Особенно отчётливо это повышение проявлялось в первые часы после облучения и в разгаре лучевой болезни.
-
3. У крыс адренокортикальная реакция на облучение носит характер двухфазной кривой. В отличие от крыс, у кроликов в пределах времени наблюдения после снижения общего уровня кортикостероидов в крови не отмечалось вторичного гиперкортицизма. Напротив, по мере развития лучевой болезни секреция адренокортикальных гормонов у этих животных продолжала снижаться.
-
4. Наличие в плазме не связанных с белками и более мобильных вследствие этого стероидов, может вызвать гиперкортикоидное состояние при нормальном или даже сниженном общем уровне гормонов в крови. Длительное влияние «скрытого» гиперкортицизма, таким образом, может явиться фактором, усугубляющим клиническое течение острой лучевой болезни.
Список литературы Анализ нарушений связывания кортикостероидов с белками плазмы крови в патогенезе острой лучевой болезни
- Анохин П.К. Очерки физиологии функциональных систем. М.: Книга по Требованию, 2021. 450 с.
- Кузин А.М. Структурно-метаболическая теория в радиобиологии. М.: Наука, 1986. 282 с.
- Кудрицкий Ю.К., Георгиевский А.Б. Адаптационная гипотеза биологической эффективности ионизирующего излучения //Атомная энергия. 1992. Т. 13, № 1. С. 27-32.
- Меерсон Ф.З. Физиология адаптационных процессов. М.: Наука, 1986. 638 с.
- Гребенюк А.Н., Стрелова О.Ю., Легеза В.И., Степанова Е.Н. Основы радиобиологии и радиационной медицины: Учебное пособие. СПб.: ООО Издательство ФОЛИАНТ, 2012. 232 с.
- Докшина Г.А. Эндокринные и метаболические аспекты лучевой болезни. Томск: Издательство Томского ун-та, 1984. 223 с.
- Мороз Б.Б., Кендыш И.Н. Радиобиологический эффект и эндокринные факторы. М.: Атомиздат, 1975. 228 с.
- Fernandez-Real J.M., Pugeat M., Grasa M., Broch M., Vendrell J., Brun J., Ricart W. Serum corticosteroid-binding globulin concentration and insulin resistance syndrome: a population study //J. Clin. Endocrinol. Metab. 2002. V. 87, N 10. P. 4686-4690.
- Gagliardi L., Ho J.T., Torpy D.J. Corticosteroid-binding globulin: the clinical significance of altered levels and heritable mutations //Mol. Cell Endocrinol. 2010. V. 316, N 1. P. 24-34.
- Klieber M.A., Underhill C., Hammond G.L., Muller Y.A. Corticosteroid-binding globulin, a structural basis for steroid transport and proteinase-triggered release //J. Biol. Chem. 2007. V. 282, N 40. P. 29594-29603.
- Lewis J.G., Borowski K.K., Shand B.I., George P.M., Scott R.S. Plasma sex hormone-binding globulin, corticosteroid-binding globulin, cortisol, and free cortisol levels in outpatients attending a lipid disorders clinic: a cross-sectional study of 1137 subjects //Horm. Metab. Res. 2010. V. 42, N 4. P. 274-279.
- Lewis J.G., Elder P.A. Corticosteroid-binding globulin reactive centre loop antibodies recognise only the intact natured protein: elastase cleaved and uncleaved CBG may coexist in circulation //J. Steroid. Biochem. Mol. Biol. 2011. V. 127, N 3-5. P. 289-294.
- Mihrshahi R., Lewis J.G., Ali S.O. Hormonal effects on the secretion and glycoform profile of corticosteroid-binding globulin //J. Steroid. Biochem. Mol. Biol. 2006. V. 101, N 4-5. P. 275-285.
- Sivukhina E.V., Jirikowski G.F., Bernstein H.G., Lewis J.G., Herbert Z. Expression of corticosteroid-bind-ing protein in the human hypothalamus, co-localization with oxytocin and vasopressin //Horm. Metab. Res. 2006. V. 38, N 4. P. 253-259.
- Zhou A., Wei Z., Stanley P.L., Read P.J., Stein P.E., Carrell R.W. The S-to-R transition of corticosteroid-binding globulin and the mechanism of hormone release //J. Mol. Biol. 2008. V. 380, N 1. P. 244-251.
- Омельчук Н.Н. Актуальные вопросы профилактики острой лучевой болезни //Национальное здоровье. 2018. № 1. С. 70-75.
- Омельчук Н.Н. Метод оценки функциональной активности коры надпочечников с учётом физиологической роли разных фракций кортикостероидов в крови у здоровых и облучённых животных //Национальное здоровье. 2018. № 1. С. 58-64.
- Омельчук Н.Н. Влияние тироксина на общий уровень кортикостероидов и связывающую способность кортикостероидсвязывающего глобулина в плазме крови после облучения //Национальное здоровье. 2018. № 1. С. 65-69.
- Поздеев А.В. Экспериментальное исследование содержания кортизола в крови при радиационном облучении //Вестник Курской государственной сельскохозяйственной академии. 2013. № 7. С. 53-54.
- Guillemin R., Clayton G.W., Lipscomb H.S., Smith J.D. Fluorometric of rat plasma and adrenal, corti-costerone concentration; a note on technical details //J. Lab. Clin. Med. 1959. V. 53, N 3. P. 830-832.
- De Moor P., Hoirwegh K., Heromans G., Declerck-Raskin M.M. Protein binding of corticosteroid studied by gel filtration //J. Clin. Invest. 1962. V. 41, N 4. P. 816-827.


