Анализ побочного сочетанного воздействия радиойодной и лучевой терапии у больных раком щитовидной железы
Автор: Хвостунов И.К., Крылов В.В., Родичев А.А., Шепель Н.Н., Коровчук О.Н., Кочетова Т.Ю., Хвостунова Т.И., Жиронкина А.С.
Рубрика: Научные статьи
Статья в выпуске: 4 т.30, 2021 года.
Бесплатный доступ
Радиойодтерапия (РЙТ), которая назначается после радикального хирургического лечения, является «золотым стандартом» в лечении больных дифференцированным раком щитовидной железы (ДРЩЖ). При наличии отдалённых метастазов РЙТ становится практически безальтернативным методом лечения. Вместе с тем, при её применении возможно побочное действие, связанное с облучением здоровых органов и тканей циркулирующим в кровяном русле радиоактивным йодом (131I). Для исследования радиационной безопасности использования РЙТ важна достоверная оценка побочного радиационного воздействия на соматические клетки пациента. Дополнительным негативным фактором, способным усилить побочное воздействие РЙТ, может быть облучение органов и тканей пациента в результате проведения дистанционной лучевой терапии (ДЛТ). Цитогенетическое обследование при помощи анализа хромосомных аберраций в лимфоцитах периферической крови способно решить задачу оценки суммарной лучевой нагрузки для каждого пациента. Такая возможность обусловлена тем, что опредёленные виды хромосомных аберраций являются специфическими радиационными маркерами, накопление которых однозначно свидетельствует о радиационном воздействии, а по частоте их встречаемости можно оценить величину поглощённой дозы. В данном случае лимфоциты крови служат моделью всех соматических клеток, включая клетки костного мозга. Предметом исследования в настоящей работе было изучение при помощи цитогенетического обследования дополнительного вклада ДЛТ, выполненной наряду с РЙТ, в общее побочное облучение организма пациентов. В работе был выполнен статистический анализ вклада ДЛТ в побочное радиационное воздействие. Анализ был проведён в общей группе из 43 пациентов, среди которых 5 человек получали ДЛТ дополнительно к РЙТ. Все пациенты получали РЙТ в отделении радионуклидной терапии МРНЦ им. А.Ф. Цыба (Обнинск). Цитогенетическое обследование пациентов было выполнено в лаборатории радиационной цитогенетики того же Центра. Результаты проведённого исследования доказывают, что при анализе закономерностей формирования побочного радиационного воздействия на тех пациентов, которые получили как РЙТ, так и ДЛТ, их следует выделять в отдельную группу. Наличие дополнительного облучения за счёт ДЛТ может приводить не только к существенному завышению, но и к ложноположительному занижению частоты радиационных маркеров вследствие угнетения лимфоцитов из-за высокой суммарной радиационной нагрузки. Такой эффект занижения можно ожидать при многократных курсах РЙТ с суммарной введённой активности 131I (Σact) более 1200 мКи. Абсолютная величина суммарной очаговой дозы при ДЛТ, вероятно, значимой роли не играет. В целом, категория пациентов, которым назначались как РЙТ, так и ДЛТ, требует особого персонализированного подхода.
Радиойодтерапия, дистанционная лучевая терапия, радиофармпрепарат, радиойод, побочная доза, хромосомные аберрации, лимфоциты крови
Короткий адрес: https://sciup.org/170191712
IDR: 170191712 | УДК: 616.441-006.6-085.849.1 | DOI: 10.21870/0131-3878-2021-30-4-40-51
Analysis of side effect in thyroid cancer patients received combined treatment with radioiodine and external beam radiotherapy
Radical surgery is the mainstay for differentiated thyroid cancer, radioiodine therapy followed by the surgery is the “gold standard” treatment modality indicated after the surgery. Radioiodine therapy becomes practically non-alternative treatment for patients with distant metastases. However, orally administered radioiodine may be also absorbed into the bloodstream and can damage surrounding normal organs and tissues and cause side effect. To test radioiodine therapy safety side effects of the radionuclide on somatic cells should be accurately assessed. In addition, external beam radiotherapy can also damage adjacent normal organs and tissues and thereby increases radioiodine therapy side effect. It is possible to evaluate patient-specific total radiation dose with the use of cytogenetic assay of chromosome aberrations level in peripheral blood lymphocytes because some types of chromosome aberrations are specific radiation markers clearly indicating that the cells have been exposed to radiation. Radiation absorbed dose can be estimated by the number of the aberrations occurrence frequency, and the value of side radiation dose greatly depends on a patient personality. In this case peripheral blood lymphocytes are thought of as a model of somatic and bone marrow cells. The paper present results of application of cytogenetic assay for estimating side effects caused by exposure of adjacent organs and tissues to external beam radiotherapy and surrounding somatic cells to radioiodine therapy. Results of statistical analysis of external beam radiotherapy related side effect contribution to the total side effect are present in the paper. The joint group of 43 patients was involved in the study, all patients received radioiodine therapy and 5 of them received also external beam radiotherapy in addition to radioiodine therapy. All patents received radioiodine therapy in the Radionuclide Therapy Department, A. Tsyb MRRC in Obninsk. Cytogenetic assay was carried out in the Radiation Cytogenetics Laboratory, A. Tsyb MRRC. Results of the study and examination of regularities of radioiodine therapy and external beam radiotherapy related side effects development make it evident that patients received combining radioiodine therapy and external beam radiotherapy should present special group with the treatment plan different from that for the radioiodine therapy exposed group. Exposure to external radiation may cause not only significant overestimation but also a false-positive underestimation of the number of radiation-specific markers because of lymphocytes inhibition following exposure to high total radiation dose. Inhibition effect may be a result of overestimating multiple radioiodine therapy administrations to achieve total 131I activity (Σact) exceeds 1200 mCi. The absolute value of the total focal radiotherapy dose is probably irrelevant. In general, patients assigned to both radioiodine therapy and external beam radiotherapy require personalized approach to treatment.
Текст научной статьи Анализ побочного сочетанного воздействия радиойодной и лучевой терапии у больных раком щитовидной железы
Тенденции развития современной медицины связаны с достижениями активно разрабатываемого направления 4П-медицины, построенной на принципах персонализированного подхода к здоровью человека и интегрирующей в себя понятия персонализации (индивидуальный подход к каждому пациенту), предикции (создание вероятностного прогноза здоровья), превентивности (предотвращение появления заболеваний) и партисипативности (мотивированное участие
Хвостунов И.К.* – зав. лаб., д.б.н.; Крылов В.В. – зав. отдел., д.м.н.; Родичев А.А. – врач-радиолог, к.м.н.; Шепель Н.Н. – ст. науч. сотр., к.б.н.; Коровчук О.Н. – науч. сотр.; Кочетова Т.Ю. – науч. сотр.; Хвостунова Т.И. – науч. сотр.; Жиронкина А.С. – науч. сотр. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
пациента) [1]. Персонализированный подход указан первым из 4-х «П». Его роль в онкологии в эпоху новых знаний о молекулярно-генетических механизмах, с появлением новых препаратов и методов, становится всё более значимой [2].
Результаты комплексных исследований радиационного воздействия на тканевом и клеточном уровнях являются основой для повышения эффективности существующих схем радионуклидной терапии (РНТ), включая разработку новых подходов и обоснование мер по ограничению нежелательных воздействий [3, 4]. Персонализированный подход при РНТ может быть реализован, в том числе, посредством учёта воздействия радиации на организм конкретного больного [5]. Это особенно важно в случаях, когда у пациента имеются отклонения от стандартных (для его заболевания) показателей, и когда применяются несколько методов, обладающих негативным побочным действием.
Совершенствование персонализированного подхода при назначении радиойодтерапии (РЙТ) для лечения дифференцированного рака щитовидной железы (ДРЩЖ) может позволить повысить эффективность и безопасность лечения, особенно в случаях применения многократных курсов с накоплением большой введённой активности 131I. Следует отметить, что персонализированный подход особенно актуален для больных ДРЩЖ, получающих многократные курсы РЙТ [5, 6], для детей и подростков, вынужденных получать РЙТ [7, 8], для пациентов с почечной недостаточностью [9], а также в случае комбинации с иными методами лечения, в частности, при назначении дистанционной лучевой терапии (ДЛТ). Как правило, необходимость проведения ДЛТ вызвана наличием определённых неблагоприятных обстоятельств, таких как: невозможность радикальной операции вследствие широкой инвазии опухоли, наличие крупных костных или иных метастазов, требующих дополнительного локального облучения и ряда других факторов. Таким образом, пациенты, получившие РЙТ в комбинации с ДЛТ, представляют собой особую группу, имеющую риски, связанные с дополнительным побочным радиационным воздействием.
РЙТ, выполняемая после хирургического лечения, является эффективным, безопасным, а при наличии отдалённых метастазов и безальтернативным методом, позволяющим успешно завершить лечение [10]. Вместе с тем, она обладает и побочным действием, обусловленным облучением здоровых органов и тканей циркулирующим в кровяном русле 131I после его перорального приёма [11, 12]. Для исследования радиационной безопасности применения РЙТ важна достоверная оценка побочного радиационного воздействия на здоровые соматические клетки пациента. При этом надёжная оценка побочного внутреннего облучения необходима с учётом индивидуальных особенностей пациентов, поскольку известно, что величина побочной дозы облучения значительно варьирует от пациента к пациенту [13]. По этой причине выявление значимости различных клинико-дозиметрических показателей пациентов в отношении общего побочного облучения является важной и актуальной задачей [14, 15]. Изучение роли дополнительной ДЛТ в сочетании с проведением РЙТ составило предмет исследования в настоящей работе.
Прямым экспериментальным методом оценки побочной дозы у больных ДРЩЖ в результате РЙТ является регулярная повторная радиометрия после приёма радиоактивного йода. Такой метод позволяет получить динамику активности радиоактивного йода в теле пациента и рассчитать поглощённую дозу. Ряд проведённых таким методом обследований пациентов при РЙТ позволил выявить общие закономерности накопления и выведения радиофармпрепарата (РФП), сформулировать терапевтические рекомендации и доказать безопасность РЙТ [11, 16, 17]. Вместе с тем, очевидно, что данный метод является трудоёмким, дорогостоящим и требует соблюдения особых мер радиационной безопасности в процессе выполнения измерений. Необходимо отметить, что радиометрия может показать процесс «накопления-выведения», но не может отразить особенности биологической реакции на облучение у конкретного пациента. Такие реакции могут существенно варьировать, поэтому требуется персонализированный подход при проведении РЙТ.
Цитогенетическая биологическая дозиметрия рекомендована МАГАТЭ в качестве стандартного метода для широкого использования [18]. Радиационно-индуцированные хромосомные аберрации в соматических клетках являются надёжными маркерами радиационного воздействия. Прирост аберраций хромосом в результате РЙТ позволяет оценить побочную дозу и охарактеризовать индивидуальную радиочувствительность пациента, поскольку при этом исследуется не только интенсивность радиационного воздействия, но и способность клеток восстанавливать повреждения ДНК. Таким образом, цитогенетическая биодозиметрия позволяет учесть индивидуальные особенности пациента при оценке последствий РЙТ. Повышенный уровень аберраций может указывать на риски развития нежелательных побочных явлений и требовать коррекции схемы лечения.
Цель настоящего исследования состояла в оценке побочных радиационных эффектов, проявляющихся при сочетании ДЛТ и РЙТ в сравнении с применением РЙТ без ДЛТ, путём анализа относительной значимости вклада дополнительной ДЛТ по результатам цитогенетического обследования.
Материалы и методы
Для решения поставленной задачи был выполнен сравнительный статистический анализ результатов цитогенетического обследования двух групп больных ДРЖЩ. Первая группа состояла из 38 пациентов, которые получали только РЙТ. Во второй группе было 5 пациентов, которые помимо РЙТ дополнительно получали ДЛТ с суммарной очаговой дозой (СОД) в диапазоне от 25 до 56 Гр (табл. 1). Схема цитогенетического обследования представляла собой сравнительный анализ двух образцов крови, взятых у пациента до начала однократного курса РЙТ и сразу после его выписки из специализированного стационара, когда уровень мощности дозы опускался ниже 20 мкЗв/ч на расстоянии 1 м от пациента. Для цитогенетического анализа использовали образцы крови, которые брались у всех обследованных лиц в соответствии с действующим законодательством РФ и нормами медицинской этики после получения информированного согласия. Аберрации изучались метафазным методом в клетках первого митоза стандартным методом и методом FISH (fluorescence in situ hybridization) в соответствии с рекомендациями МАГАТЭ [18]. При анализе детерминировали дицентрики (dic), центрические кольца (rc), полные транслокации (tc) и неполные транслокации (ti). Результаты анализа методом FISH были представлены в виде частоты транслокаций на число геном-эквивалентных (GE) метафаз [18]. Детали методики цитогенетического анализа были опубликованы ранее [3].
В первую группу вошли 7 мужчин и 31 женщина. Возраст варьировал в пределах 1,6-71,9 лет. Однократное введение радиоактивного йода получали 18 человек, два и более раз – 20 пациентов. Всего в группе было проведено 60 обследований стандартным и 23 обследования FISH-методом. Во вторую группу вошли: 1 мужчина и 4 женщины. Возраст пациентов варьировал от 31 до 58 лет. Всего в группе было проведено 8 обследований стандартным и 6 обследований FISH-методом. Число проанализированных метафаз на одного пациента в первой группе варьировало в пределах от 250 до 1186 при стандартном обследовании и в пределах от 312 до 1202 – при FISH-методе. Всего было проанализировано 63638 метафаз стандартным методом и
43703 – методом FISH. Во второй группе число метафаз на одного пациента варьировало в пределах от 250 до 949 при стандартном обследовании и в пределах от 1000 до 1200 метафаз – при FISH-методе. Всего в данной группе было проанализировано 8044 метафазы стандартным методом и 6200 – методом FISH.
Поскольку группы I и II существенно различались по статистической мощности, то в рамках поставленной задачи была возможность сопоставить лишь индивидуальные результаты обследования пациентов группы II со среднегрупповыми результатами проведённого ранее обследования пациентов группы I [19]. При проведённом сопоставлении учитывались стандартные ошибки средних значений частот детектированных аберраций. Статистическую обработку полученных результатов и регрессионный анализ осуществляли с помощью стандартных алгоритмов, представленных в приложениях Microsoft Excel и OriginLab-6.0. Для сопоставления результатов обследования пациентов группы I и группы II использовались оценки параметров регрессионной зависимости с учётом 95% доверительных и предсказательных интервалов.
Результаты и обсуждение
В табл. 1 представлены клинико-дозиметрические показатели пациентов из группы II. Все пациенты получали длительную РЙТ в пределах от 9 до 22 курсов. Дополнительная ДЛТ пациентам назначалась до начала РЙТ по ряду причин: патологический перелом бедренной кости (#20, #21), неполное удаление первичной опухоли на шее (#35, #49) и нерадикальная операция на регионарных метастазах (#39). За исключением случая с пациентом #35, проведение дополнительной ДЛТ происходило за несколько месяцев до начала длительного курса РЙТ.
Таблица 1
Клинико-дозиметрические показатели пациентов группы II c дополнительной ДЛТ
|
Код Пол / Число курсов Введённая Σact, пациента возраст, лет Диагноз РЙТ* мКи* , лет |
СОД при ДЛТ, Гр |
|
25 38 50 56 40 |
– число курсов РЙТ и суммарная активность на дату последнего обследования;
* – время между ДЛТ и первым курсом РЙТ.
В табл. 2 представлены результаты регрессионного анализа зависимости частоты радиационных маркеров от суммарной введённой активности 131I за все предшествующие курсы РЙТ для пациентов из группы I [19]. Для анализа была использована линейная зависимость со стандартной оценкой статистических показателей. При выполнении анализа учитывались статистические погрешности исходных данных с оценкой коэффициента корреляции (R), среднеквадратичной ошибки оценки (S D ), размером выборки (N) и уровнем значимости (p).
В табл. 3 представлены изменения частоты нестабильных и стабильных маркеров по результатам проведённого цитогенетического обследования пациентов из группы II, которое заключалось в выполнении анализа двух последовательных заборов крови: до и сразу после очередного курса РЙТ. Индивидуальные изменения данных показателей были сопоставлены со средними значениями, оценёнными ранее в группе I для пациентов без дополнительной ДЛТ.
В результате два значения из восьми для нестабильных аберраций (#20, #35) статистически значимо на уровне 95% отличались от средних значений в группе I. Результаты анализа изменения стабильных маркеров у пациентов из группы II не отличались от средних значений в группе I.
Таблица 2
Параметры регрессионной зависимости частоты аберраций хромосом
(Y, абер./100 клеток) от суммарной введённой активности 131I (Σact, мКи) за все предшествующие курсы РЙТ: Y=c+α Σact по результатам цитогенетического обследования пациентов группы I без ДЛТ
|
Категория анализа |
c±SE* |
α, мКи-1±SE* |
R |
Sd |
N |
p |
|
Дицентрики+центрические кольца |
||||||
|
до РЙТ |
0,319±0,061 |
(0,514±0,023) 10-2 |
0,818 |
2,06 |
60 |
<0,0001 |
|
после РЙТ |
1,88±0,12 |
(0,542±0,027) 10-2 |
0,726 |
2,46 |
60 |
<0,0001 |
|
Полные+неполные транслокации |
||||||
|
до РЙТ |
1,11±0,22 |
(0,978±0,062) 10-2 |
0,893 |
1,74 |
23 |
<0,0001 |
|
после РЙТ |
4,32±0,47 |
(0,896±0,084) 10-2 |
0,839 |
1,52 |
23 |
<0,0001 |
* SE – стандартная ошибка среднего.
Таблица 3
Прирост частоты радиационных маркеров вследствие РЙТ у пациентов из группы II по сравнению со средними величинами из группы I
|
Вид прироста маркеров |
Средний прирост в группе I M±SE |
Индивидуальный прирост частоты аберраций в группе II, ∆ i ±SE |
||||
|
#20 |
#21 |
#35 |
#39 |
#49 |
||
|
(dic+rc)/100 клеток |
2,62±0,25 |
-2,04±1,59* (N i =21) |
0,80±2,40 (N i =17) |
-1,80±2,54 (N i =7) 4,60±2,42 (N i =9) 6,37±1,88* (N i =9) 3,80±2,74 (N i =10) |
5,20±1,62 (N i =8) 0,80±2,15 (N i =9) |
|
|
(tc+ti)/ 100 GE-клеток |
3,48±0,52 |
1,92±4,52 (N i =7) |
2,45±4,22 (N i =22) |
|||
* – статистически значимое отличие от среднего по группе I на уровне 95%; N i – номер текущего курса РЙТ для пациента из группы II.
Следует отметить, что величины средних значений прироста частоты нестабильных аберраций варьируют в широком пределе от -2,04 до 6,37 аберраций/100 клеток [19]. Достоверное отличие индивидуальных показателей от среднего значения по группе I, которое составляет 2,62 аберраций/100 клеток, было обнаружено только для двух из восьми значений, что объясняется, в частности, высокими значениями стандартной ошибки среднего. Эти ошибки определяются суммой погрешностей контрольной и результирующей частоты маркеров.
В табл. 4 представлена частота нестабильных и стабильных радиационных маркеров у пациентов из группы II до и после однократного курса РЙТ в зависимости от накопленной к моменту обследования суммарной активности РФП (вторая колонка). Индивидуальные показатели приведены в сравнении со средними частотами для пациентов из группы I, которые рассчитывались по регрессионным соотношениям (табл. 2) для тех же суммарных активностей. Из числа величин нестабильных маркеров показатели 50% пациентов группы II (8 из 16) статистически значимо отличались от показателей пациентов группы I. Для стабильных маркеров такая доля составила 66,7% (4 из 6).
Таблица 4
Частота радиационных маркеров до и после РЙТ у пациентов из группы II по сравнению со средними величинами из группы I
|
Вид частоты |
Σact, |
Средняя частота аберраций в группе I при Σact |
Индивидуальная частота аберраций в группе II, M±SE |
||||
|
маркеров |
мКи |
#20 |
#21 |
#35 |
#39 |
#49 |
|
|
(dic+rc)/100 клеток до РЙТ |
1708 1435 621 864 864 972 515 650 |
9,10 7,69 3,51 4,76 4,76 5,32 2,97 3,66 |
4,40±0,94* |
3,20±1,13* |
9,00±1,34* 5,20±1,02 3,85±0,84 7,60±1,23 |
1,20±0,49* 5,40±1,04 |
|
|
(dic+rc)/100 клеток после РЙТ |
1789 1516 756 972 972 1080 650 785 |
11,58 10,10 5,98 7,15 7,15 7,73 5,40 6,14 |
2,36±0,66* |
4,00±1,26* |
7,20±1,20 9,80±1,40 10,22±1,04* 11,40±1,51* |
6,40±1,13 6,20±1,11 |
|
|
(tc+ti)/100 GE-клеток до РЙТ |
621 515 1708 1708 |
7,18 6,14 17,81 17,81 |
13,10±,05* |
15,02±2,19* |
11,82±1,94* |
14,06±2,12 |
|
|
(tc+ti)/100 GE-клеток после РЙТ |
756 1768 |
11,09 20,16 |
16,93±2,33* |
16,51±2,10 |
|||
– статистически значимое отличие от среднего по группе I на уровне 95%.
На рис. 1 показаны частоты стабильных (левая колонка) и нестабильных (правая колонка) радиационных маркеров в лимфоцитах крови обследованных пациентов до и после однократного курса РЙТ в зависимости от суммарной введённой активности 131I. Точками показаны индивидуальные результаты пациентов из группы II с дополнительной ДЛТ, а сплошными линиями – регрессионные зависимости для пациентов из группы I без ДЛТ (табл. 2). На всех панелях сплошная линия означает линейную регрессию, пунктирные линии – 95% доверительный интервал, точечные линии – интервал предсказания.
В настоящей работе было выполнено исследование влияния дополнительной ДЛТ на побочное радиационное воздействие на пациентов с диагнозом ДРЩЖ, проходящих РЙТ. Задача решалась путём сопоставления результатов цитогенетического обследования пациентов, получивших как РЙТ, так и ДЛТ, с результатами обследования пациентов, которым ДЛТ не назначалась. Для этого были использованы полученные ранее результаты обследования группы I без ДЛТ [19] с результатами настоящей работы по группе II с ДЛТ. Результаты группы I были представлены в форме среднегрупповых показателей (табл. 2) и оценённых регрессионных зависимостей (табл. 3) с учётом доверительных и предсказательных интервалов (рис. 1). Результаты группы II были представлены в форме индивидуальных показателей (табл. 3, 4).
Сопоставление результатов I и II групп показало, что прирост (изменение) частоты нестабильных радиационных маркеров вследствие однократного назначения РЙТ в группе II варьирует в широких пределах и в большинстве случаев отличается от средних показателей в группе I (табл. 4). Однако статистически значимое отличие средних величин выявлено только для 2 из 8 показателей. Причина заключается в большой статистической погрешности оценки среднего прироста маркеров в группе II. Причина такой погрешности заключается в том, что все пациенты получали повторные курсы РЙТ (от 7 до 21 раза), поэтому погрешность прироста складывается из погрешностей как до, так и после РЙТ (табл. 4). Аналогичный вывод следует из сопоставления прироста частот стабильных маркеров, хотя величина выборки для сравнения в данном случае слишком мала.
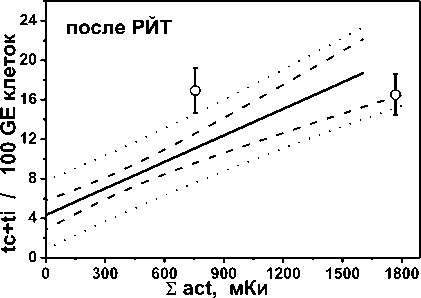
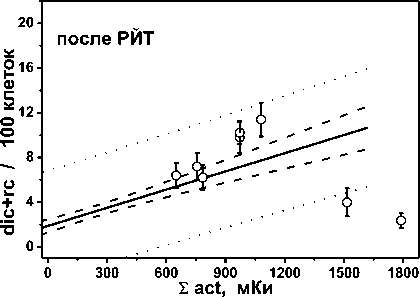
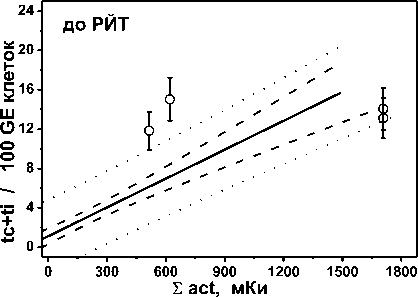
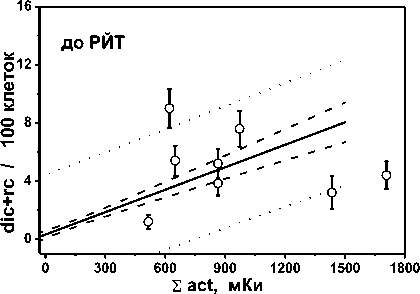
Рис. 1. Частота стабильных (левая колонка) и нестабильных (правая колонка) радиационных маркеров в лимфоцитах крови обследованных пациентов до и после однократного курса РЙТ в зависимости от суммарной введенной активности 131I. Точками показаны индивидуальные результаты пациентов из группы II с ДЛТ, линиями – регрессионные зависимости для пациентов из группы I без ДЛТ, табл.2. Сплошная линия – линейная регрессия, пунктир – 95% доверительный интервал, точечная линия – 95% интервал предсказания.
Проведённое ранее обследование пациентов группы I [19] показало, что в отличие от прироста частоты маркеров, абсолютные величины частот как до, так и после курса РЙТ статистически значимо коррелируют с суммарной величиной введённой активности 131I (табл. 3). Результаты по группе II были сопоставлены с выявленными закономерностями по группе I, что представлено в табл. 4 и на рис. 1. Значимые отличия средних частот были выявлены для 50% нестабильных маркеров и 66,7% – для стабильных, с учётом показателей как до, так и после РЙТ (табл. 4). Поскольку малый размер выборки результатов в группе II не позволяет выполнить оценку регрессионных соотношений, то индивидуальные показатели группы II были сопоставлены с регрессионными соотношениями группы I с учётом их доверительных и предсказательных интервалов (рис. 1).
Так, для нестабильных маркеров до РЙТ 25% (2 из 8) показателей попадают в доверительный интервал, 37,5% (3 из 8) попадает в интервал предсказания и 37,5% (3 из 8) не попадают даже в интервал предсказания. Последнее означает, что эти три показателя с вероятностью 95% не следуют выявленной зависимости в группе I. Соответственно, для нестабильных маркеров после РЙТ 12,5% (1 из 8) показателей попадают в доверительный интервал, 62,5% (5 из 8) – в интервал предсказания и 25% (2 из 8) не попадают в интервал предсказания. Для стабильных маркеров до РЙТ в доверительный интервал не попадает ни одна величина, 50% (2 из 4) попадает в интервал предсказания и 50% (2 из 4) не попадают даже в интервал предсказания. Соответственно, для стабильных маркеров после РЙТ 50% (1 из 2) показателей попадают в доверительный интервал и 50% (1 из 2) не попадают в интервал предсказания.
Заключение и выводы
Несмотря на низкую статистическую мощность группы II, проведённое исследование приводит к следующим предварительным выводам.
Оценки побочного радиационного воздействия в двух группах различаются, поэтому при цитогенетическом обследовании пациентов с дополнительной ДЛТ следует выделять в отдельную группу. Дополнительное облучение при ДЛТ ожидаемо должно приводить к более высокому уровню радиационных маркеров. Однако, как показало проведённое исследование, дополнительная ДЛТ может приводить как к существенному превышению, так и к ложноположительному занижению частоты радиационных маркеров. Вероятной причиной низкой частоты маркеров при очень высоких величинах суммарной введённой пациенту активности 131I может быть подавление способности лимфоцитов крови к стимулированному делению, что необходимо для цитогенетического анализа. Такой эффект занижения можно ожидать при суммарной введённой активности 131I более 1200 мКи. Абсолютная величина СОД при этом, вероятно, роли не играет.
Таким образом, категория пациентов с дополнительной ДЛТ требует особо тщательного персонализированного подхода. Необходимость дополнительной ДЛТ обусловлена большей распространённостью опухолевого процесса и худшим общим прогнозом. Кроме того, тем больным, которым необходима ДЛТ, может потребоваться намного больше курсов РЙТ, чем тем, кому она не была показана.
Список литературы Анализ побочного сочетанного воздействия радиойодной и лучевой терапии у больных раком щитовидной железы
- Пальцев М.А., Белушкина Н.Н., Чабан Е.А. 4П-медицина как новая модель здравоохранения //Журнал ОРГЗДРАВ: новости, мнения, обучение. 2015. Т. 2, № 2. С. 48-55.
- Михель И.В. Философские очерки о 4-П медицине, биоэтике и будущем человека. Саратов: Сарат. гос. техн. университет, 2016. 208 с.
- Khvostunov I.K., Saenko V.A., Krylov V.V., Rodichev A.A., Yamashita S. Cytogenetic biodosimetry and dose-rate effect after radioiodine therapy for thyroid cancer //Radiat. Environ. Biophys. 2017. V. 56, N 3. P. 213-226.
- Столбовой А.В., Залялов И.Ф. Радиобиологические модели и клиническая радиационная онкология //Онкология. Журнал им. П.А. Герцена. 2016. Т. 6. С. 88-96.
- Robbins R.J., Schlumberger M.J. The evolving role of 131I for the treatment of differentiated thyroid carcinoma //J. Nucl. Med. 2005. V. 46, N 1 Suppl. P. 28S-37S.
- Dorn R., Kopp J., Vogt H., Heidenreich P., Carroll R.G., Gulec S.A. Dosimetry-guided radioactive iodine treatment in patients with metastatic differentiated thyroid cancer: largest safe dose using a risk-adapted approach //J. Nucl. Med. 2003. V. 44, N 3. P. 451-456.
- Родичев А.А., Гарбузов П.И., Дроздовский Б.Я., Крылов В.В., Гусева Т.Н., Давыдов Г.А., Паршин В.С., Ильин А.А., Чеботарева И.В. Двадцатилетний опыт радиойодтерапии отдалённых метастазов дифференцированного рака щитовидной железы у детей и подростков //Вестник РОНЦ им. Н.Н. Блохина РАМН. 2009. Т. 20, № S2. С. 19-20.
- Хвостунов И.К., Крылов В.В., Родичев А.А., Шепель Н.Н., Коровчук О.Н., Кочетова Т.Ю., Пятенко В.С., Хвостунова Т.И. Оценка побочного радиационного эффекта радиойодтерапии для детей и подростков на основе цитогенетического обследования. Достижения и перспективы детской онкологии: тезисы VII съезда детских онкологов России с международным участием, Москва, 25-26 октября 2018 г. //Приложение к журналу Онкопедиатрия. 2018. Т. 5, № 3. С. 15.
- Holst J.P., Burman K.D., Atkins F., Umans J.G., Jonklaas J. Radioiodine therapy for thyroid cancer and hyperthyroidism in patients with end-stage renal disease on hemodialysis //Thyroid. 2005. V. 15, N 12. P. 1321-1331.
- Крылов В.В., Гарбузов П.И., Кочетова Т.Ю., Шуринов А.Ю., Бородавина Е.В. Терапевтическая радиология. Национальное руководство. Глава 34. Радионуклидная терапия /под ред. А.Д. Каприна и Ю.С. Мардынского. М.: ГЭОТАР-Медиа, 2018. С. 637-665.
- Brill A.B., Stabin M., Bouville A., Ron E. Normal organ radiation dosimetry and associated uncertainties in nuclear medicine, with emphasis on iodine-131 //Radiat. Res. 2006. V. 166, N 1. P. 128-140.
- Van Nostrand D. The benefits and risks of I-131 therapy in patients with well-differentiated thyroid cancer //Thyroid. 2009. V. 19, N 12. P. 1381-1391.
- Haenscheid H., Lassmann M., Luster M., Thomas S.R., Pacini F., Ceccarelli C., Ladenson P.W., Wahl R.L., Schlumberger M., Ricard M., Driedger A., Kloos R.T., Sherman S.I., Haugen B.R., Carriere V., Corone C., Reiners C. Iodine biokinetics and dosimetry in radioiodine therapy of thyroid cancer: procedures and results of a prospective international controlled study of ablation after rhTSH or hormone withdrawal //J. Nucl. Med. 2006. V. 47, N 4. P. 648-654.
- Kulkarni K., Van Nostrand D., Atkins F.B., Aiken M., Burman K., Wartofsky L. The frequency with which empiric amounts of radioiodine "over-" or "under-" treat patients with metastatic well-differentiated thyroid cancer //Thyroid. 2006. V. 16, N 1. P. 1-5.
- Stabin M.G., Sharkey R.M., Siegel J.A. RADAR commentary: Evolution and current status of dosimetry in nuclear medicine //J. Nucl. Med. 2011. V. 52, N 7. P. 1156-1161.
- Luster M., Clarke S.E, Dietlein M., Lassmann M., Lind P., Oyen W.J.G., Tennvall J., Bombardieri E. Guidelines for radioiodine therapy of differentiated thyroid cancer //Eur. J. Nucl. Med. Mol. Imaging. 2008. V. 35, N 10. P. 1941-1959.
- Verbürg F.A., Lassmann M., Mäder U., Luster M., Reiners C., Hänscheid H. The absorbed dose to the blood is a better predictor of ablation success than the administered 131-I activity in thyroid cancer patients //Eur. J. Nucl. Med. Mol. Imaging. 2011. V. 38, N 4. P. 673-680.
- Cytogenetic analysis for radiation dose assessment: a manual. Technical Reports Series No. 405. Vienna: IAEA, 2001. 127 p.
- Хвостунов И.К., Крылов В.В., Родичев А.А., Шепель Н.Н., Коровчук О.Н., Кочетова Т.Ю., Пятенко В.С., Хвостунова Т.И., Жиронкина А.С. Значимость персональных клинико-диагностических показателей при оценке побочного радиационного воздействия у больных раком щитовидной железы, получающих радиойодтерапию //Радиация и риск. 2021. Т. 30, № 2. С. 101-112.


