Анализ состава микробиоты при пародонтите тяжелой степени
Автор: Маркелова Е.В., Цуканова И.В., Первов Р.Ю.
Журнал: Международный журнал гуманитарных и естественных наук @intjournal
Рубрика: Медицинские науки
Статья в выпуске: 6-2 (81), 2023 года.
Бесплатный доступ
Целью выполненного исследования являлся анализ степени зависимости клинических проявлений генерализованного пародонтита тяжелой степени в полости рта от состава микробиоты пародонтального кармана и оценка роли мукозального иммунитета. Проведено обследование 12 пациентов в возрасте 37,3± 6,3 лет с диагнозом хронический генерализованный пародонтит (ХГП) тяжелой степени (9 женщин и 3 мужчины) проживающих на территории Приморского края. Анализ результатов исследования позволил установить, что в группе наблюдения в 100% случаях были выявлены Porphyromonas endodontalis, Tannerella forsythia, Fusobacterium nucleatum. В 91,6% - Porphyromonas gingivalis, 75% - Treponema denticola, 66,6% - Prevotella intermedia, 16% - Aggregatibacter actinomycetemcomitans. После проведенного лечения в 16% случаев было выявлено отсутствие Treponema denticola, однако в 8,3% случаев, напротив, отмечалось появление Treponema denticola. Установлено, что при воспалительных заболеваниях пародонта наибольшее значение имеет состояние мукозального иммунитета. Вероятно, может быть значимым количественная оценка методом Дентоскрин. Для более значительного изменения качественного состава содержимого пародонтального кармана (ПК) необходим более длительный период, а также применение антисептической и антибактериальной терапии.
Мукозальный иммунитет, пародонтит, микрофлора, микробиота, полость рта, пародонтальный карман
Короткий адрес: https://sciup.org/170199827
IDR: 170199827 | DOI: 10.24412/2500-1000-2023-6-2-69-73
Analysis of microbiota composition in severe periodontitis
The aim of the study was to analyze the degree of dependence of clinical manifestations of severe generalized periodontitis in the oral cavity on the periodontal pocket microbiota composition and to evaluate the role of mucosal immunity. 12 patients (9 females and 3 males) aged 37.3±6.3 years diagnosed with severe chronic generalized periodontitis (CGP) and residing in the Primorsky region were examined. The analysis of the research results showed that in the observation group, Porphyromonas endodontalis, Tannerella forsythia, Fusobacterium nucleatum were detected in 100% of cases; in 91.6% of cases - Porphyromonas gingivalis, 75% - Treponema denticola, 66.6% - Prevotella intermedia, 16% - Agregatibacter actinomycetemcomitans. After treatment, the absence of Treponema denticola was detected in 16% of cases, but in contrast, the appearance of Treponema denticola was observed in 8.3% of cases. The state of mucosal immunity was found to be the most important in inflammatory periodontal diseases. Probably, quantitative assessment by the Dentoscreen method can be significant. For a more significant change in the qualitative composition of the periodontal pocket (PC) content, a longer period of time is required, as well as the use of antiseptic and antibacterial therapy.
Текст научной статьи Анализ состава микробиоты при пародонтите тяжелой степени
По данным И.Г. Синевой и соавт. (2021), Ш.Ш. Шадиевой и соавт. (2021), распространенность воспалительных заболеваний пародонта варьируется от 90%до 98% [1, 2]. Пародонтитом тяжелой степени страдают 11% взрослого населения [3]. Воспалительные заболевания пародонта занимают второе место по частоте встречаемости стоматологических заболеваний и представляет серьезную медикосоциальную проблему [4]. Болезни пародонта, наряду с кариесом зубов и его осложнениями, являются самыми распространенными стоматологическими заболеваниями в мире, которые ведут к множеству осложнений и в конечном итоге к вторичной адентии [5].
Пародонтологическое лечение является основой, которая будет влиять на тактику лечение и план ведения пациента. Распространенность заболеваний пародонта оста- ется на достаточно высоком уровне и не имеет тенденции к снижению и характеризуется неуклонным ростом и широкой распространенностью у лиц не только пожилого возраста, но и представителей молодого возраста [6]. Кроме того, состояние пародонта взаимосвязано с общим состояние организма и оказывает при наличии воспалительных реакций негативное влияние на системы организма человека [7].
Заболевания пародонта склонны к персистирующему течению, хронизации и прогрессированию, которое сопровождается разрушением не только связачного аппарата зуба, но и потерей костной ткани и как следствие последующей утратой зуба [8]. В связи с этим необходимо рассматривать этиологию возникновения, а также возможность предупредить прогрессирование заболеваний пародонта.
Высокая распространенность воспалительных заболеваний пародонта определяет необходимость углубления и конкретизации представлений об этиологии и патогенезе этого заболевания [7].
В вопросе об этиологии заболеваний пародонта выделяют четыре основных фактора:
-
1) Наличие биопленки и продуктов жизнедеятельности микроорганизмов в этих образованиях;
-
2) Факторы полости рта (мукозальный иммунитет), способные усиливать или ослаблять пародонтопатогенный потенциал микроорганизмов и продуктов их обмена;
-
3) Воздействие стоматологических ортопедических конструкций;
-
4) Общие системные факторы, регулирующие метаболизм полости рта [9-12].
Многочисленные исследования показывают, что лишь немногие из более чем 700 микроорганизмов, присутствующих в ротовой полости, имеют высокий патогенный потенциал и могут стать причиной развития заболеваний пародонта. Заболевания пародонта чаще имеют полимик-робный характер [13].
Основное патогенное действие данных микроорганизмов заключается в способности продуцировать различные метаболиты, которые вместе с факторами вирулентности приводят либо к прямому разрушению окружающих тканей пародонта, либо к инактивации иммунного ответа организма. Наличие в десневой борозде высокопатогенных видов как Aggregatibacter actino-mycetemcomitans, Porphyromonas gingivalis, Tannerella forsythensis, Treponema denticola [11-15].
Цель исследования: исследовать спектр микробной флоры пародонтального кармана с помощью качественной ПЦР тест-системы «Дентоскрин» при пародонтите тяжелой степени до и после лечения через 7 дней.
Материалы и методы исследования
Проведено обследование 12 пациентов в возрасте от 37,3±6,3 лет с диагнозом хронический пародонтит тяжелой степени тяжести (3 мужчины и 9 женщин), проживающих на территории Приморского края.
У всех пациентов группы наблюдения проводили определения следующих клинических показателей: глубины пародон-тальных карманов, индекс гигиены, индекс кровоточивости, подвижность зубов до и через 7 дней после удаления множественных твердых поддесневых и наддесневых отложений. В день санации пародонта и через 7 дней после был проведен забор содержимого пародонтального кармана для оценки его состава в тест-системе «Ден-тоскрин».
У всех пациентов, включенных в исследование, клинические и рентгенологические данные соответствовали тяжелой степени пародонтита в хронической форме.
Было проведено лечение, которое включало удаление над- и поддесневых отложений на всю глубину зондирования под местной анестезией.
Статистическая обработка результатов исследования проводилась при помощи электронных таблиц Microsoft Exeel и включала расчет «пошкаловых» показателей (средняя величина М с учетом ошибки отклонения m) и их суммирование с расчетом интегрального индекса гигиены (M+_m). Сравнение двух групп оценивали с помощью критерия Стьюдента. Различия считали достоверными, при p <0,05.
Для изучения механизмов взаимосвязи параметров применялся корреляционный анализ. При оценке величины и направленности корреляционной зависимости применяли коэффициент корреляции Пирсона.
Результаты исследования и их обсуждение.
Анализ результатов исследования позволил установить, что в группе наблюдения в 100% случаях были выявлены Porphyromonas endodontalis, Tannerella forsythia, Fusobacterium nucleatum. В 91,6% – Porphyromonas gingivalis, 75% – Treponema denticola, 66,6% – Prevotella intermedia,16% – Aggregatibacter actinomycetemcomitans. После проведенного лечения в 16% случаев было выявлено отсутствие Treponema denticola, однако в 8,3% случаев, напротив, отмечалось появление Treponema denticola.
После проведенного удаления биопленки и твердых зубных отложений на всю глубину пародонтального кармана спустя 7 дней всеми пациентами отмечалось отсутствие неприятного запаха и значительное снижение кровоточивости или полное отсутствие при чистке зубов.
Клиническое обследования выявило, что индекс гигиены до лечения в среднем составил 3,46 ±0,021 после лечения 1,31± 0,02 (p<0,001). Индекс кровоточивости у всех пациентов был достаточно высоким и колебался в среднем 2,7± 0,21, а после проведенного лечения 0,18±0,21 (p<0,01).
При анализе результатов до и после терапии по данным лабораторного исследования «Дентоскрин» существенных различий в составе микрофлоры не выявлено.
Индекс гигиены и индекс кровоточивости до и через 7 дней после лечения
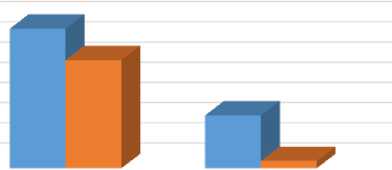
1 2
-
■ Ряд1 ■ Ряд2
Рис. 1. Индекс гигиены (синий цвет) и индекс кровоточивости (оранжевый цвет) до и через 7 дней после лечения
Клинический случай №6.
Жалобы: Кровоточивость при чистке зубов, неприятный запах изо рта, боль, возникающая при пережевывании пищи.
Внутриротовой осмотр: ИГ 4,3. ИК 3,0. Десна кровоточит при зондировании, ПК до 9-10 мм, гнойное отделяемое.
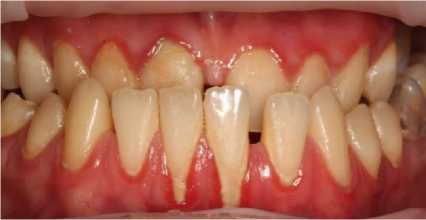
Рис. 2.Состояние мягких тканей пациента М. до лечения
Лечение: Под инфильтрационной анестезией Скандонест проведено удаление над- и поддесневых отложений (RSD) при помощи ультразвукового аппарата Prophylaxis Master. Обработка воздушно- порошковой смесью эритритола (EMS).
Наложения повязок ХД.
Даны рекомендации: Тщательное соблюдения домашней гигиены полости рта.
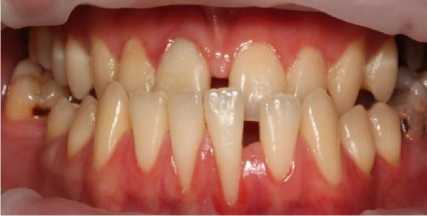
Рис. 3. Состояние мягких тканей Пациента М. на 7 сутки после проведенного лечения
Выводы
Резюмируя вышеизложенное, можно сделать вывод, что при воспалительных заболеваниях пародонта наибольшее значение имеет состояние мукозального им-
Для более значительного изменения качественного состава содержимого паро-донтального кармана (ПК) необходим более длительный период, а также применение антисептической и антибактериальной мунитета. терапии.
Вероятно, может быть значимым коли чественная оценка методом Дентоскрин.
Список литературы Анализ состава микробиоты при пародонтите тяжелой степени
- Синев И.И. Усовершенствование ортопедического метода в комплексном лечении пациентов с локализованным пародонтитом средней степени тяжести: дис. ... канд. мед. наук: 14.01.14. - Самара, 2021. - 146 с.
- Шадиева Ш., Гиязова М. Сочетанная патология: заболевания пародонта и гастродуо-денальной зоны // Stomatologiya. - 2021. - №2 (83). - С. 80-83.
- Ризаев Э.А., Агабабян И.Р., Арзикулова М.Ш.К. Аутоиммунное воспаление как причинно-следственная связь пародонтита и атеросклероза // Вопросы науки и образования. -2022. - № 6 (162).
- Прокопенко М.В. Применение фитопрепаратов в лечении легкой формы хронического генерализованного пародонтита: дис. ... канд. мед. наук: 14.01.14. - Воронеж, 2021. -151 с.
- Aral K., Milward M.R., Kapila Y., Berdeli A., Cooper P.R. Inflammasomes and their regulation in periodontal disease: a review // Periodontal Research. - 2020. - Vol. 55, № 4. - P. 473487. DOI: 10.1111/jre.12733.
- Саулин М.П. Патофизиологические механизмы регуляции заболеваний тканей пародонта и методы их коррекции: дис. ... канд. мед. наук: 14.03.03. - Москва, 2019. - 133 с.
- Беспалова А.Ю., Утробина И.И., Мокашева Е.Н., Мокашева Е.Н. Взаимосвязь этио-патогенеза заболеваний сердечно-сосудистой системы и ротовой полости // European J. Natural History. - 2022. - № 2. - С. 44-49.
- Терапевтическая стоматология: учебник в 3-х ч. Ч. 2. Болезни пародонта / Г.М. Барер, Б.Ю. Суражев, Т.И. Лемецкая // под ред. Г.М. Барер. - Москва: ГЭОТАР-Медиа, 2021. - 224 с.
- Цепов Л.М., Николаев А.И., Голева Н.А. Факторы, определяющие сопративляемость пародонта патогенным воздействиям // Пародонтология. - 2008. - № 2. - С. 3-9
- Керимханов К.А., Иорданишвили А.К. Протетический пародонтит: возможность профилактики // Пародонтология. - 2023. - Т. 28, № 1. - С. 83-88.
- Ушницкий И.Д., Иванова А.А., Пинелис И.С., Юркевич А.В., Михальченко Д.В. Современные этиологические и патогенетические аспекты воспалительнодеструктивных процессов тканей пародонта // Эндодонтия Today. - 2019. - № 17 (4). - С. 46-49. - [Электронный ресурс]. - Режим доступа: https://doi.org/10.36377/1683-2981-2019-17-4-46-49 (дата обращения: 24.05.2023).
- Хабилов, Н. Л., Ирсалиева Ф.Х. Состояние микроциркуляции в тканях пародонта при протезировании искусственными коронками из разных конструкционных материалов // Врач-аспирант. - 2010. - Т. 39, № 2.2. - С. 268-274.
- Тобоев Г.В., Епхиев А.А., Калинина Е.А. Перспективная оценка эффективности направленной костной регенерации при лечении тяжелой формы хронического пародонтита // Современные проблемы науки и образования. - 2018. - № 4. - С. 180.
- Романова Р.О., Кашлевская М.Е., Зябликов М.Ю. Пародонтопатогенные бактерии -Основной фактор возникновения и развития пародонтита // Гуманитарные. естественнонаучные и технические аспекты современности: материалы XXXIII Всероссийской научно-практической конференции (г. Ростов-на-Дону, 30 июня 2021 г.): в 2-х частях. Часть 1. - Ростов-на-Дону: издательство ВВМ, 2021. - С. 129-133.
- Джавадова Л.М. Современные представления об этиологии и патогенезе воспалительных заболеваний пародонта (обзор литературы) // Достижения науки и образования. -2022. - №4 (84).


