Анализ уровня лабораторного маркера ишемии головного мозга с оценкой нейрокогнитивного статуса при оперативном лечении патологических извитостей ВСА
Автор: Батрашов В.А., Борщев Г.Г., Юдаев С.С., Землянов А.В., Марынич А.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.17, 2022 года.
Бесплатный доступ
В данной статье проведен анализ лабораторного маркера ишемии головного мозга на различных этапах лечения с оценкой нейро-когнитивного статуса пациентов специализированным опросником на до- и послеоперационных этапах в зависимости от степени сосудисто-мозговой недостаточности. В результате выявлено, что уровень маркера NSE статистически значимо ниже при использовании временного шунта (17,5±3,4 мкг/л), чем при операциях без шунта (20,1±2,7 мкг/л) (p
Нейронспецифическая енолаза, нейрокогнитивный статус, патологическая извитость, ишемия головного мозга
Короткий адрес: https://sciup.org/140296409
IDR: 140296409 | DOI: 10.25881/20728255_2022_17_3_28
Analysis of the level of a laboratory marker of cerebral ischemia with an assessment of neurocognitive status in the surgical treatment of pathological tortuosity of the ICA
This article analyzes the laboratory marker of cerebral ischemia at various stages of treatment with the assessment of the neurocognitive status of patients by a specialized questionnaire at the pre- and postoperative stages, depending on the degree of cerebrovascular insufficiency. As a result, it was revealed that the level of the NSE marker is statistically significantly lower with the use of a temporary shunt (17.5±3.4 mcg/l) than with operations without a shunt (20.1 ±2.7 mcg/l) (p
Текст научной статьи Анализ уровня лабораторного маркера ишемии головного мозга с оценкой нейрокогнитивного статуса при оперативном лечении патологических извитостей ВСА
Одним из современных методов диагностики ишемии головного мозга (ГМ) представляется обнаружение на интраоперационном этапе ишемии на уровне нейронов ГМ. Согласно современным исследованиям в качестве маркеров тканевого повреждения мозга в последние годы предлагается использовать ряд нейроспецифических белков, входящих в состав нервной и глиальной ткани и появляющихся в крови в повышенных концентрациях при различных повреждениях мозга, такими белками являются: протеин-S100 и нейронспецифическая енолаза (NSE) [1]. Основным маркером повреждения нервной ткани является NSE, который является внутриклеточным ферментом нейронов ГМ и периферической нервной ткани. NSE является общим нейронспецифическим маркером всех дифференцированных нейронов [2]. Качественные и количественные определения этого белка в спинномозговой жидкости или сыворотке крови дают ценную информацию о степени выраженности повреждений нейронов и нарушениях общей целостности гематоэнцефалического барьера. Была выявлена взаимосвязь показателей NSE с прогнозированием течения и последствия перенесенного инсульта в отдаленном периоде [3]. Существует небольшое количество исследований, при которых уровень данного протеина изучался при операциях каротидной эндартерэктомии (КЭ). Исследований уровня

Батрашов В.А., Борщев Г.Г., Юдаев С.С. и др.
АНАЛИЗ УРОВНЯ ЛАБОРАТОРНОГО МАРКЕРА ИШЕМИИ ГОЛОВНОГО МОЗГА С ОЦЕНКОЙ НЕЙРОКОГНИТИВНОГО СТАТУСА ПРИ ОПЕРАТИВНОМ ЛЕЧЕНИИ ПАТОЛОГИЧЕСКИХ ИЗВИТОСТЕЙ ВСА данного фермента при операциях по поводу патологических извитостей внутренних сонных артерий (ПИ ВСА) в отечественной и зарубежной литературе нет.
В настоящее время остается неоднозначной оценка клинической симптоматики у пациентов с ПИ ВСА, в особенности у больных, не переносивших инсульт и тран-зиторную ишемическую атаку (ТИА) (так называемые, асимптомные пациенты). Отмечено, что у этих пациентов гемодинамически значимая извитость ВСА и ее коррекция могут приводить к изменению симптоматики, выражающейся в динамике нейрокогнитивного статуса.
Тем не менее, эффект резекции патологической извитости на когнитивные функции остается противоречивым. Это обусловлено неоднозначностью определения когнитивного статуса, методов, типов проводимых тестов, а также времени оценки когнитивных функций. Наиболее часто термин «когнитивные функции» подразумевает такие высшие мозговые функции как зрительно — пространственное восприятие, исполнительные функции, внимание, концентрацию и оперативную память, речь. В своем исследовании мы придерживались именно этого определения понятия.
Характеристика больных и методов исследования
В исследование включено 40 пациентов с гемодинамически значимой ПИ ВСА, которым была показана хирургическая коррекция извитости. Среди всех исследуемых пациентов в 25 (62,5%) случаях ПИ протекала «бессимптомно», 3 (7,5%) больных ранее переносили ТИА, в 6 (15%) наблюдениях в анамнезе отмечались признаки дисциркуляторной энцефалопатии (ДЭ) и у 6 (15%) ишемический инсульт. Все пациенты были с I–IV степенями сосудисто-мозговой недостаточности (СМН). Среди обследованных больных 16 (40%) человек имели высшее образование, 24 (60%) — среднее специальное.
Для определения динамики маркера ишемии головного мозга при резекции извитости ВСА была проведена оценка NSE на 3-х этапах исследования путем забора венозной крови 40 пациентам. Первый этап — в предоперационном периоде (за 1 сутки до операции), второй этап — в интраоперационном периоде (в конце пережатия ВСА) и третий этап — в раннем послеоперационном периоде (на 3 сутки после операции). Референтные значения нейронального повреждения ГМ данного маркера расценивали согласно инструкциям производителей NSE <13 мкг/л, при превышении этого маркера в сыворотке крови принято считать имеющее повреждение нейронов ГМ.
Оценка когнитивного статуса представляла собой оценку клинической симптоматики пациентов перед оперативным вмешательством, а также тестирование пациентов специализированным опросником — Монреальской шкалой когнитивной оценки (МоСА- тестом). Всем 40 пациентам проведен скрининг когнитивных нарушений с помощью MoСA теста, оценивающего различные когнитивные функции: зрительно — про- странственное восприятие (тест рисования часов и куба), исполнительные функции (задание по созданию альтернирующего пути и проверки способности к абстрактному мышлению), внимание, концентрацию и оперативную память (серийное вычитание по 7 и воспроизведение цифрового ряда в прямом и обратном порядках), речь (называние животных, повторение двух синтаксически сложных предложений и тест на лексическую беглость речи), ориентировку. Специфичность метода составляет около 90 %. Монреальская когнитивная шкала пригодна для выявления не только выраженных, но и умеренных когнитивных нарушений, что характерно для молодых пациентов с патологическими извитостями ВСА.
С целью оценки когнитивного статуса пациентов проводилось тестирование согласно Монреальской шкале оценки когнитивных функций на двух этапах — до оперативного вмешательства (в день госпитализации пациента) и в отдаленном послеоперационном периоде (через 6 месяцев после операции).
Результаты
На первом этапе исследования (перед операцией) было обнаружено повышение изучаемого показателя (среднее значение составило 16,35 мкг/л). Это обусловлено хронической ишемией головного мозга вследствие гемодинамически значимой извитости ВСА (нередко двусторонней).
На втором этапе исследования определялась тенденция к увеличению содержания анализируемого параметра (среднее значение 20,04±2,84 мкг/л) в результате усугубления ишемии ГМ в процессе оперативного лечения. Основными причинами подобных изменений могут служить церебральная гипоперфузия и интраоперационная гипоксия ГМ.
На последнем этапе исследования зарегистрирована тенденция к снижению NSE (среднее значение 12,40 мкг/л) в сравнении с предоперационным, что связано со снижением ишемии головного мозга в связи с улучшением кровотока по сонной артерии после оперативного вмешательства.
Анализ уровня нейронспецифической енолазы (NSE)в зависимости от типа извитости
Нами была произведена сравнительная характеристика маркера ишемии ГМ (NSE) у пациентов с разными типами извитости ВСА на всех трех этапах исследования. Данную оценку проводили с целью определения наиболее гемодинамически значимого типа извитости, вызывающего ишемию ГМ.
Распределение по типам извитости ВСА среди 40 пациентов: кинкинг n = 11, коулинг n = 8, S-образный тип n = 12, С-образный тип n = 9 (Рис. 1).
На первом этапе исследования среди всех типов извитости наибольшее значение NSE выявлено у пациентов с кинкингом (среднее значение 19,6 мкг/л), что имеет статистически значимые отличия (Рис. 2)

^™ Кинкинг (27,5%)
^" Койлинг (20%)
S-образный тип (30%)
^" С-образный тип (22,5%)
22,50
20,00.
17,50.
15,00.
12,50.
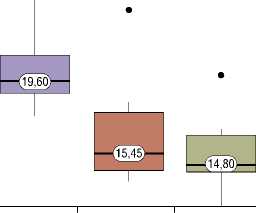
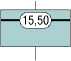
Рис. 1. Распределение по типам извитостей.
Тип извитости
^" Кинкинг ^" С-образная ^™ Койлинг ^" S-образная
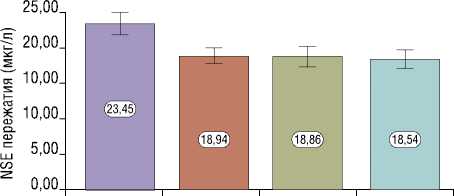
На втором этапе исследования NSE также была выше у пациентов с кинкингом (23,45±2,33 мкг/л) (Рис. 3), что характеризует этот тип извитости как наиболее гемодинамически значимый и на этапе пережатия ВСА.
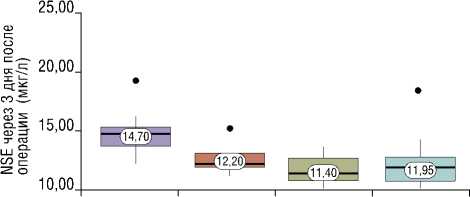
На третьем этапе наименьшие значения NSE были отмечены у пациентов с С-образным типом (Ме = 11,40 мкг/л). Так как данный тип извитости имеет более плавный характер извитого участка, а после оперативного лечения артерия имеет практически прямой ход, что характеризует меньшую ишемию головного мозга. Наибольшее значение NSE отмечалось у пациентов с кинкингом (Ме = 14,70 мкг/л), как более тяжелого типа извитости, однако после оперативного лечения значения NSE у пациентов с кинкингом снижались, что характеризует эффективность операции у пациентов с этим типом извитости (Рис. 4).
Оценка NSE в зависимости от использования временного шунта
Следующим этапом исследования маркера ишемии стало определение его уровня на интраоперационном этапе в зависимости от использования временного внутрипросветного шунта (ВВШ). Нами был выполнен статистический анализ данных (Таблица 1).
Согласно полученным результатам мы видим, что уровень маркера NSE статистически значимо ниже при использовании ВВШ, чем при операциях без шунта. Временное выключение кровотока по сонным артериям во время операции резекции извитости ВСА сопровождается обязательным достоверным повышением концентрации маркера повреждения ГМ (p<0,05) с последующим восстановлением маркеров на 3-е сутки после операции.
Табл. 1. Анализ NSE на этапе пережатия сонных артерий в зависимости от использования ВВШ
|
Показатель |
Категории |
NSE после пережатия (мкг/л) |
p |
||
|
M±SD |
95% ДИ |
n |
|||
|
Интраоперационная защита |
Без шунта |
20,1±2,7 |
19,1–21,1 |
32 |
<0,05 |
|
На шунте |
17,5±3,4 |
14,6–20,4 |
8 |
||
Примечание : * — различия показателей статистически значимы (p<0,05). Исходя из полученных данных при сравнении уровня NSE на этапе пережатия сонных артерий в зависимости от использования ВВШ, нами были установлены статистически значимые различия (p<0,05) (используемый метод: t–критерий Стьюдента).
Рис. 2. Анализ уровня NSE с разными типами извитости на дооперационном этапе (При сравнении уровня NSE с разными типами извитости на дооперационном этапе, были установлены статистически значимые различия (p<0,05) (используемый метод: Критерий Краске-ла–Уоллиса).
Тип извитости
^™ Кинкинг ^" С-образная ^" Койлинг ^" S-образная
Рис. 3. Анализ уровня NSE с разными типами извитости на этапе пережатия сонных артерий (При сравнении уровня NSE с разными типами извитости на этапе пережатия сонных артерий, нами были выявлены статистически значимые различия (p<0,05) (используемый метод: F–критерий Фишера).
Тип извитости
^™ Кинкинг ^" С-образная
^« Койлинг ^« S-образная
Рис. 4. Анализ уровня NSE с разными типами извитости через 3 дня после операции (При сравнении уровня NSE через 3 дня после операции в зависимости от типа извитости, были установлены статистические различия (p<0,05) (используемый метод: Критерий Краскела–Уоллиса).
Батрашов В.А., Борщев Г.Г., Юдаев С.С. и др.
АНАЛИЗ УРОВНЯ ЛАБОРАТОРНОГО МАРКЕРА ИШЕМИИ ГОЛОВНОГО МОЗГА С ОЦЕНКОЙ НЕЙРОКОГНИТИВНОГО СТАТУСА ПРИ ОПЕРАТИВНОМ ЛЕЧЕНИИ ПАТОЛОГИЧЕСКИХ ИЗВИТОСТЕЙ ВСА
Из полученных данных по изучению уровня маркера ишемии мы можем сделать вывод, что, несмотря на использование интраоперационных методов оценки ишемии ГМ (определение ретроградного давления (РД) во ВСА и оценки линейной скорости кровотока (ЛСК) при транскраниальной допплерографии (ТКДГ)), которые позволяют определить показания к использованию ВВШ, уровень ишемии нейронов ГМ остается высоким при операциях без использования ВВШ. Также зачастую не удается провести оценку ЛСК при ТКДГ ввиду отсутствия акустического окна, в связи с этим оценка ишемии ГМ лишь методом оценки РД из ВСА остается неэффективным методом, приводящим к развитию ишемических осложнений. Таким образом, комплексная оценка ишемии ГМ на интраоперационном этапе может проводиться с использованием лабораторного маркера ишемии в рутинной практике с целью достоверной оценки ишемии на уровне нейронов ГМ, в частности к данному методу можно прибегать при невозможности оценки ЛСК при ТКДГ.
Динамика нейрокогнитивного статуса в зависимости от степени СМН до- и после резекции ПИ ВСА
Нами был проведен анализ данных анкетирования до оперативного вмешательства в зависимости от степени СМН, с целью определения наиболее тяжелой степени СМН, отображающей когнитивные нарушения (таблица 2).
Согласно представленным данным мы видим, что наиболее значимые когнитивные нарушения на доопе-рационном этапе отмечены у пациентов с IV степенью СМН (пациенты, перенесшие в анамнезе ишемический инсульт), наименьшие у пациентов с I степенью СМН (асимптомных).
Ишемический инсульт, при котором происходит необратимое повреждение нейронов ГМ, вызывает стойкие неврологические расстройства и нередко когнитивно-мнестические, вызывая в отдаленном периоде нарушения зрительно — пространственного восприятия, исполнительных функций, внимания, концентрации и оперативной памяти, в ближайшем постинсультном периоде нарушения речи, ориентировку. В связи с этим согласно опроснику у пациентов с IV степенью СМН когнитивные нарушения более значимые (Me = 23 балла). Пациенты с III и II степенью СМН (ДЭ и ТИА. Ме =25 баллов) также имеют когнитивные нарушения, но менее выраженные, чем у пациентов с IVстепенью СМН. Касаемо пациентов с дисциркуляторной энцефалопатией, это связано с развитием хронической недостаточности мозгового кровообращения, которая в свою очередь вызывает хроническую ишемию нейронов ГМ, что связано с развитием у таких пациентов когнитивных расстройств.
У пациентов с ТИА не возникает стойких неврологических нарушений, т.к. данное состояние является тран-зиторным, ишемия разрешается в ближайшие 24 часа, соответственно выраженных когнитивных нарушений у таких пациентов не отмечается.
Табл. 2. Анализ данных анкетирования до оперативного вмешательства в зависимости от степени СМН
|
Показатель |
Категории |
Анкета до операции (баллы) |
p |
||
|
Me |
Q 1 –Q 3 |
n |
|||
|
СМН |
Асимптомные |
26 |
25–27 |
25 |
0,042* |
|
ТИА |
25 |
25–26 |
3 |
||
|
ДЭП |
25 |
24–25 |
6 |
||
|
Ишемический инсульт |
23 |
22–24 |
6 |
||
Примечание : * — различия показателей статистически значимы (p<0,05). В результате анализа данных анкетирования до оперативного вмешательства в зависимости от степени СМН, нами были выявлены статистически значимые различия (p = 0,042) (используемый метод: Критерий Краскела–Уоллиса).
Табл. 3. Анализ данных анкетирования после операции в зависимости от степени СМН
|
Показатель |
Категории |
Анкета после операции (баллы) |
p |
||
|
Me |
Q 1 –Q 3 |
n |
|||
|
СМН |
Асимптомные |
28 |
27–28 |
25 |
0,026* |
|
ТИА |
27 |
26–27 |
3 |
||
|
ДЭП |
26 |
26–27 |
6 |
||
|
Ишемический инсульт |
25 |
24–26 |
6 |
||
Примечание : * — различия показателей статистически значимы (p<0,05). Согласно полученным данным при сравнении данных анкетирования после операции в зависимости от степени СМН, были установлены существенные различия (p = 0,026) (используемый метод: Критерий Краскела–Уоллиса).
У пациентов с I степенью СМН (асимптомных) в среднем не отмечается нарушений когнитивного статуса согласно данным опросника. Однако, в виду наличия у таких пациентов гемодинамически значимой извитости ВСА, уровень когнитивных нарушений остается на нижней границы нормы (Ме = 26 баллов).
Далее мы провели анализ данных анкетирования после оперативного вмешательства в зависимости от степени СМН, с целью определения динамики когнитивных нарушений после оперативного вмешательства (таблица 3).
Исходя из полученных данных, мы можем отметить, что у пациентов после оперативного вмешательства (через 6 месяцев) в среднем повышается количество баллов, полученных в ходе анкетирования по всем степеням СМН. Однако, пациенты имеющие IV степень СМН через 6 месяцев после проведенного оперативного лечения имеют признаки когнитивных нарушений (Ме = 25 баллов). Эти данные демонстрируют нам, что проведенная операция по поводу ПИ ВСА у таких пациентов снижает общие когнитивные нарушения, но перенесенный ишемический инсульт в анамнезе влечет за собой долгое восстановление когнитивных функций.
Хорошее восстановление когнитивных функций отмечено у пациентов с ТИА (Ме = 25 баллов до операции, Ме = 27 баллов после операции) и ДЭ (Ме = 25 баллов до операции, Ме = 26 баллов после операции). Вероятно, это
связано с меньшими когнитивными расстройствами до оперативного вмешательства, а также обратимый характер ишемии у пациентов с ТИА.
Заключение
Таким образом, изучение динамики маркеров повреждения головного мозга при выполнении операций на сонных артериях при патологических извитостях открывает дополнительные возможности для исследования гипоксических процессов в ткани головного мозга как в интраоперационном, так и в раннем послеоперационном периодах. Комплексная оценка ишемии ГМ на интраоперационном этапе может проводиться с использованием лабораторного маркера ишемии в рутинной практике с целью достоверной оценки ишемии на уровне нейронов ГМ, в частности к данному методу можно прибегать при невозможности оценки ЛСК при ТКДГ.
При проведении анкетирования специализированным опросником в отдаленном послеоперационном периоде после резекции ПИ ВСА отмечается улучшение когнитивных функций в сроки до 6 месяцев после проведенной операции. При этом у пациентов с IV степенью СМН также отмечаются признаки нарушения когнитивных функций. Пациенты с I, II, III степенью CМН демонстрируют лучшие показатели когнитивного статуса, в сравнении с IV ст. СМН.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Анализ уровня лабораторного маркера ишемии головного мозга с оценкой нейрокогнитивного статуса при оперативном лечении патологических извитостей ВСА
- Dalman JE, Beenakkers IC, Moll FL, Leusink JA. Transcranial Doppler monitoring during carotid endarterectomy helps to identify patients at risk of postoperative hyperperfusion. J. Vasc Endovasc Surg. 1999; 18: 222-227.
- Молочный В.П., Макарова Т.Е., Головкова Н.Ф., Обухова Г.Г. Нейро-специфическая енолаза и глиофибрилярный кислый протеин крови и цереброспинальной жидкости как маркер повреждения ткани мозга при бактериальных гнойных менингитах у детей // Дальневосточный медицинский журнал. - 2012. - №2. - С. 48-51.
- Rigamonti A., Scandroglio M., Minicucci F., Magrin S., et al. A clinical evaluation of near-infrared cerebral oximetry in the awake patient to monitor cerebral perfusion during carotid endarterectomy. J. Clin Anesth. 2005; 17(6): 426-430.


