Анестезиологическое обеспечение тотального эндопротезирования крупных суставов
Автор: Пригородов М.В., Поминова И.В., Носкова И.Л., Ташкаев И.В., Вирста A.M.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Анестезиология и реаниматология
Статья в выпуске: 2 т.9, 2013 года.
Бесплатный доступ
Цель: повысить качество анестезиологической защиты при протезировании крупных суставов на основе стабильного состояния энергетического обмена. Материал и методы. Выполнили проспективное, рандомизированное исследование на основе проведения управляемой гемодилюции с двойным маскированием. В первой группе пациентов (32, из них 19 женщин) управляемую гемодилюцию (УГ) не проводили. Вторую группу больных (31-17) составили пациенты сУГ. Выбрали три этапа обследования: до операции, травматичный этап операции, после операции. Анализировали параметры центральной гемодинамики (СИ (л/мин/м2) и ОПСС (дин*сек"1*см"5), газообмена (D02 (мл/мин) и V02 (мл/мин), энергетического обмена (ккал/мин; ккал/сут). Использовали пакет статистических программ Statistics 6,0 для непраметрической обработки полученных данных. Результаты. Параметры центральной гемодинамики в обеих группах больных изменялись не существенно и не различались между группами. В обеих группах больных отмечено существенное снижение Д02. Различий D02 между группами на всех этапах исследования не выявили. Потребление кислорода в первой группе существенно снизилось к травматичному этапу операции, а к следующему этапу поднялось до исходного уровня. Потребление кислорода в группе с УГ выросло к травматичному этапу операции, но затем возвратилось к исходному уровню. В группе больных с УГ потребление кислорода было существенно выше, чем у пациентов без УГ, на всех этапах исследования. Нашли существенное падение энергетического обмена в первой группе больных на травматичном этапе операции, с последующим восстановлением энергетического потенциала. Отмечен несущественный рост энергообмена на травматичном этапе операции во второй группе, с последующим снижением до исходного уровня. Энергообмен на всех этапах исследования был существенно выше во второй группе. Логистический регрессионный анализ установил, что управляемая гемодилюция связана с ростом энергетического обмена на этапе до операции, на травматичном этапе вмешательства и после него. Заключение. Установили связь роста энергообмена с УГ при радикальном вмешательстве на тазобедренном суставе. Существенный энергетический дефицит у пациентов без УГ на травматичном этапе операции позволяет констатировать высокую вероятность возникновения сердечно-сосудистых осложнений.
Анестезиологическое обеспечение, тотальное эндопротезирование тазобедренного сустава., энергетический обмен
Короткий адрес: https://sciup.org/14917714
IDR: 14917714
Текст научной статьи Анестезиологическое обеспечение тотального эндопротезирования крупных суставов
1 Введение . Ежегодно в мире за год производится от 500 тыс. до 1,5 млн тотальных замещений тазобедренного сустава [1–3]. В США и Германии их выполняется более 150 тыс. [4]. По данным Н. В. Корнилова [5] в России при общей годовой потребности взрослого населения в 296 тыс. эндопротезов ТБС, этот показатель составляет всего лишь 20–30 тыс. штук.
При эндопротезировании крупных суставов нижних конечностей в настоящее время применяются различные виды анестезиологического пособия [6]. Традиционная общая анестезия не обеспечивает адекватной защиты структур центральной нервной системы от интраоперационной боли и сама по себе приводит к изменениям гомеостаза, являясь компонентом операционного дистресса [7], особенно у лиц пожилого и старческого возраста.
С. Ю. Бастрикин, А. М. Овечкин и Н. М. Федоровский [8] считают спинально-эпидуральную анестезию (СЭА) методом выбора анестезии при ТЭП крупных суставов:
-
а) спинальный компонент анестезии обеспечивает не только анестезию во время операции и хорошую релаксацию мышц, необходимую для ортопедических манипуляций на конечности;
-
б) комбинация спинальной (СА) и эпидуральной анестезии (ЭА) делает возможным использовать для субарахноидального введения минимальные дозы 0,5% спинального бупивакаина (10-12,5 мг), что сводит до минимума вероятность развития клинически значимой артериальной гипотонии;
-
в) эпидуральный компонент позволяет расширить границы сенсорного блока во время операции, а также обеспечить адекватное послеоперационное обезболивание;
-
г) СЭА — метод выбора анестезии при операциях в тех случаях, когда отсутствуют противопоказания (табл. 1).
Сведений о применении при эндопротезировании крупных суставов нижних конечностей комбинированных методов анестезии, а также данных об их влиянии на гемодинамику и тем более на энергетический обмен у больных с сердечно-сосудистой патологией немного, и они носят противоречивый характер [9, 10].
Следовательно, существует известный диссонанс между необходимостью наращивания объемов эндопротезирования крупных составов и отсутствием оптимальной защиты при проведении данной операции. Это несоответствие определило цель нашего исследования.
Цель : повысить качество анестезиологической защиты при протезировании крупных суставов на основе стабильного состояния энергетического обмена.
В связи с целью исследования были поставлены следующие задачи:
Адрес: 410012, г. Саратов, ул. Б. Казачья, 112
Тел.: +79170274052
-
ис следовать энергетический обмен у больных, подвергшихся ТЭП ТБС без управляемой гемодилюции;
-
из учить энергетический обмен у больных, подвергшихся ТЭП ТБС с управляемой гемодилюцией;
разработать оптимальное анестезиологическое обеспечение у больных с ТЭП ТБС на основе энергетического обмена.
Материал и методы . В ОАР № 1 Клинической больницы им. С. Р. Миротворцева Саратовского государственного медицинского университета разработана оригинальная методика анестезиологического обеспечения тотального эндопротезирования тазобедренных суставов (ТЭП ТБС). Этический комитет одобрил протокол исследования.
Проведено проспективное, рандомизированное, слепое исследование. Всех пациентов, подвергшихся ТЭП ТБС, разделили на две группы. Рандомизация методом конвертов — проведение управлямой гемодилюции. Выделили три этапа: до операции, травматичный этап операции, после операции. В первой группе пациентов (32 больных — 19 женщин) управляемую гемодилюцию (УГ) не проводили. Вторую группу (31 больной — 17 женщин) составили пациенты с УГ.
Методика анестезиологического обеспечения. В табл. 1 представлены противопоказания к проведению СЭА при операциях ТЭП КС. Анестезиологическая защита при операциях тотального эндопротезирования крупных суставов нижней конечности построена на основе методики, предложенной С. Ю. Бастрикиным, А. М. Овечкиным, Н. М. Федоровским [8], в виде спинально-эпидуральной анестезии и послеоперационной эпидуральной анальгезии. Разработана оригинальная методика анестезиологического обеспечения тотального эндопротезирования тазобедренных суставов (ТЭП ТБС), которая в отличие от оригинала предусматривает проведение управляемой гемодилюции из расчета 15 мл/кг на фоне развития регионарной анестезии. Перед началом операции объем введенных кристаллоидов и коллоидов достигает 30 мл/кг. Качественный состав инфузионной терапии создавали на основе данных КОД и осмолярности плазмы, количественный состав определяли на основе клинических данных: состояния кожи и подкожно-жировой клетчатки, гематокрита, ЦВД [11, 12].
Интраоперационный мониторинг. Включал в себя гарвардский стандарт, анализ параметров центральной гемодинамики (СИ (л/мин/м2) и ОПСС (дин*сек-1*см-5) с помощью аппарата Vivid E, «General Electric Co Medical Systems», США. Газообмен (DO2 (мл/мин) и VO2 (мл/мин) исследовали на основании данных газоанализатора КОС и газов крови Rapid lab» 348», Германия. С помощью оригинального устройства изучали энергетический обмен (ккал/мин и ккал/сут) [13].
Статистическая обработка полученных результатов. В среде Exell создали электронную базу данных. Использовали пакет статистических програм Statistica 6,0. Критический уровень значимости
Противопоказания к проведению СЭА при операциях ТЭП КС
Абсолютные противопоказания
Относительные противопоказания
|
Отказ пациента |
Тромбоцитопения < 100000 |
|
Выраженная гипокоагуляция, тромбоцитопения <50000 |
Сопутствующие неврологические заболевания с прогрессирующим неврологическим дефицитом |
|
Доза гепарина, полученная пациентом < чем за 1,5 ч, или доза низкомолекулярного гепарина, полученная пациентом < чем за 12 ч до пункции эпидурального пространства (ЭП). Прием пациентом тиклопидина < чем за 14 дней до пункции ЭП, клопидогреля < 7 дней до пункции ЭП, варфарина < 5 дней до пункции ЭП |
Неспособность идентифицировать эпидуральное или субарахноидальное пространство после 4–5 попыток |
Таблица 2
Антропометрические показатели, параметры гемодинамики и газообмена в общей группе до операции
Результаты. В общей группе получили следующие данные описательной статистики, представленные в табл. 2.
Все обследованные больные были старшего возраста, имели средний рост и избыток массы тела. Исследованные показатели гемодинамики больных находились в пределах возрастной нормы. У всех больных отмечена анемия легкой степени тяжести, сниженное содержание кислорода в артериальной и венозной крови. Энергопотребность всех больных находилась на физиологическом уровне (табл. 3).
Различий между группами пациентов по антропометрическим данным (рост, масса тела, пол), ASA, травматичности вмешательства не нашли. В табл. 4 представлены параметры центральной гемодинамики в первой и второй группах больных. В группе больных без УГ СИ вырос к травматичному этапу операции, на следующем этапе снизился (p<0,82). СИ в группе больных УГ, в отличие от пациентов первой группы, снизился к травматичному этапу операции, а затем вырос после ее окончания (p<0,50). ОПСС в первой группе больных незначительно снизил-
Показатели газообмена в общей группе до операции
|
Параметры |
Median |
25,000th |
75,000th |
|
VО2 кос и газы крови |
133,395 |
61,221 |
319,009 |
|
МОД (л/мин) |
4,800 |
3,800 |
5,300 |
|
VО2 дых газы |
282,500 |
252,500 |
332,000 |
|
Элиминация СО2 |
338,665 |
305,654 |
405,349 |
|
Энергопотребность, ккал/мин |
1,373 |
1,227 |
1,614 |
|
Энергопотребность, ккал/сут |
1977,048 |
1767,096 |
2323,469 |
Таблица 4
Периоперационные показатели СИ/ОПСС, DO2/VO2, ккал/мин и ккал/сут (Mean end Std. Dev.) в группах
|
Показатели |
Группы |
До операции |
Травматичный этап |
После операции |
|
СИ/ОПСС |
1-я группа 2-я группа |
3,78±0,67/1551±235 4,19±0,44/1521±239 |
3,81±0,45/1335±108 3,93±0,39/1392±131 |
3,76±0,49/1353±104 4,10±0,56/1291±130 |
|
DO 2 /VO 2,,, |
1-я группа 2-я группа |
903±230/265±21 979±146/335±51ХХХ |
692±135/184±28 668±106/375±116ХХХ |
473±93***/264±22*** 506±130***/334±52ХХХ |
|
ккал/мин и ккал/сут |
1-я группа 2-я группа |
1,29±0,10/1852±152 1,63±0,25/2343±358 |
0,90±0,14/1289±198 1,82±0,56/2622±810 |
1,37±0,12/1874±146 1,65±0,28/2358±341 |
П р и м еч а н и е : Сдвиги показателя в группе: *** — p<0,01; различия показателя между группами — ХХХ — p<0,01.
ся к травматичному этапу операции, а затем вырос (p<0,17). ОПСС во второй группе больных прогрессивно снизился (p<0,08). Параметры центральной гемодинамики на всех этапах исследования не различались между группами больных (p=0,36; p=0,72; p=0,58 и p=0,85; p=0,46; p=0,40).
В группе больных без УГ отмечено неуклонное и существенное снижение ДО2 (p<0,01). Потребление кислорода в этой же группе больных существенно снизилось к травматичному этапу операции, а затем поднялось до исходного уровня (p<0,01). В группе больных УГ доставка кислорода существенно снижалась (p<0,01), тогда как потребление кислорода выросло к травматичному этапу операции, но после операции возвратилось к исходному уровню (p<0,81). Различий DO2 между группами больных на всех этапах исследования не выявили (p=0,73; p=0,87; p=0,86). У больных с УГ потребление кислорода было существенно выше, чем у пациентов без ее применения, на всех этапах исследования (p=0,02; p=0,01; p=0,03) (табл. 4).
В табл. 4 отмечено изменение энергетического обмена у больных с проводимой гемодилюцией и без неё. Отмечено существенное падение энергетического обмена (ккал/мин) в группе больных без УГ на травматичном этапе операции, с последующим восстановлением энергетического потенциала (p<0,01). Отмечен несущественный рост энергообмена (ккал/ мин) на травматичном этапе операции во второй группе больных, с последующим снижением до исходного уровня (p<0,84). Энергообмен на всех этапах исследования был существенно выше в группе больных с УГ (p=0,03; p=0,01; p=0,03).
На рис. 1–3 представлена связь роста энергетического обмена на всех этапах исследования с проводимой управляемой гемодилюцией. Развитие управлямой гемодилюции сопровождается ростом энергообмена (p=0,01), продолжающимся на травматичном этапе операции (p=0,01) и после ее окончания (p=0,01).
Обсуждение. Центральная гемодинамика на протяжении всего периода наблюдения в обеих группах существенно не изменялась и не различалась между группами обследованных больных. Следовательно, управляемая гемодилюция не оказала существенного влияния на основные параметры центральной гемодинамики.
Если DO2 в обеих группах больных снижалась за счет интраоперационной кровопотери и уменьшения сатурации в ответ на спинально-эпидуральную блокаду, то VO2 выросло к травматичному этапу операции только у больных с УГ, вернувшись затем к исходному уровню. На всех этапах исследования этот показатель был выше у больных с УГ. Следовательно, управляемая гемодилюция вызывает активацию метаболизма.
Отмечены разнонаправленные сдвиги у обследованных больных: под влиянием УГ энергетический обмен изменялся в группе оперированных больных в разных направлениях: к травматичному этапу операции у больных с УГ он вырос, а у больных без УГ снизился. В последующем у больных в обеих группах энергообмен вернулся к дооперационному уровню. Следовательно, УГ вызывает повышение энергетического обмена.
Установленная при помощи логистического регрессионного анализа связь УГ с ростом энергообмена свидетельствует об активации последнего под влиянием УГ.
Заключение. Проведенное исследование основных параметров центральной гемодинамики, газообмена и энергетического обмена позволило установить связь роста энергообмена с управляемой гемодилюцией. Выявленное на травматичном этапе операции снижение метаболизма при недостаточной доставке кислорода за счет относительно низкого объема циркулирующей крови у больных без управляемой гемодилюции на фоне падения энергетического обмена может служить пусковым механизмом
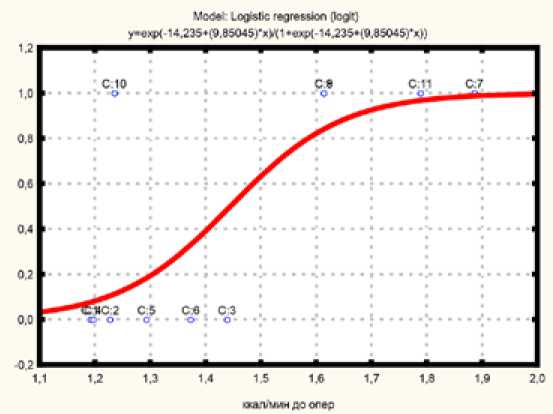
Рис. 1. Связь энергетического обмена с началом управляемой гемодилюции
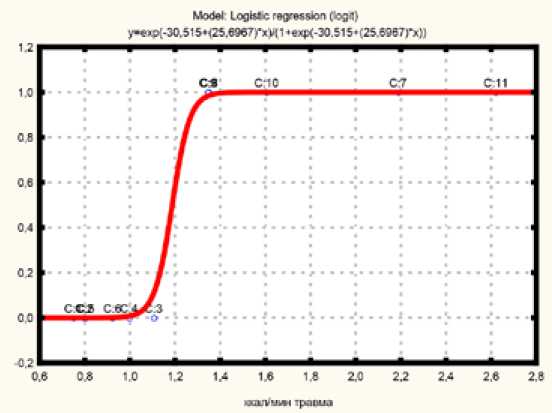
Рис. 2. Связь энергетического обмена с продолжающейся управляемой гемодилюцией
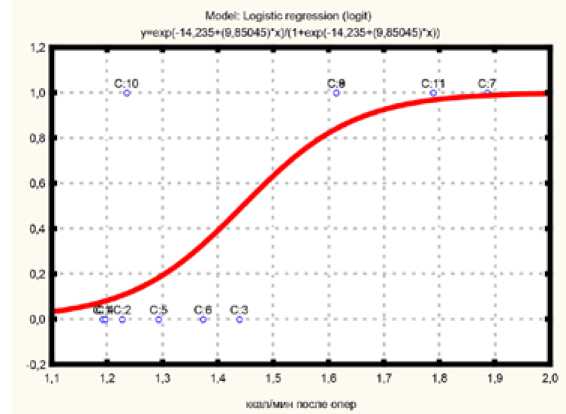
Рис. 3. Связь энергетического обмена и управляемой гемодилюции после оперативного вмешательства необратимой дестабилизации кислородно-энергетического обмена.
Список литературы Анестезиологическое обеспечение тотального эндопротезирования крупных суставов
- Взаимосвязь между клинико-рентгенологической картиной коксартроза, изменениями костной массы шейки бедра и основными параметрами стабилометрии/Г. П. Котельников, И. П. Королюк, А. Г. Шехтман, Л. Я. Мостовой//Вестн. травматологии и ортопедии им. Н.Н. Приорова. 2005. № 1. С. 52-55
- Тотальное эндопротезирование тазобедренного сустава эндопротезами «ЭСИ»/К. С. Сергеев, И.Н. Катрен-ко, Ю.Н. Дорофеев [и др.]//Эндопротезирование тазобедренного сустава отечественным имплантатом: тез. докл. науч.-практ конф. Рязань, 2004. С. 35-36
- Bone density adjacent to press-fit acetabular components: a prospective analysis with quantitative computed tomography/J.M. Wright, P. M. Pellicci, E.A. Salvati [et al.]//J. Bone Joint Surg. Am. 2001. Vol. 83-A (4). P. 529-536
- Казьмин А.И. Беленький B.E., Савельев Л.А. Перспективы использования биомеханической аппаратуры//Ортопедия, травматология и протезирование. 1984. № 11. С. 70-73
- Консервативное лечение больных деформирующим коксартрозом/Н.В. Корнилов, В.А. Шильников, Е.В. Намо-конов, С. О. Давыдов//Травматология и ортопедия России. 2003. № 3. С. 5-9
- Анисимов О. Г., Будяк Ю.В., Короткова А. С, Коряч-кин В. А. Применение продленной эпидуральной аналгезии при лечении дегенеративно-дистрофических заболеваний тазобедренного сустава//Эфферентная терапия. 2010. Т. 16, №1. С. 35-38
- Пригородов М.В. Анестезиологическое обеспечение пациентов высокого анестезиолого-операционного риска: ав-тореф. дис.... д-ра мед. наук. 2009. 38 с.
- Бастрикин С. Ю., Овечкин A.M., Федоровский Н.М. Регионарная анестезия в травматологии и ортопедии//Регионарная анестезия и лечение боли: тем. сб. М. Тверь, 2004. С. 239-246
- Бессонов С. В. Анестезиологическое обеспечение и послеоперационное обезболивание при эндопротезирова-нии крупных суставов нижних конечностей у больных с сердечно-сосудистой патологией: автореф. дис... канд. мед. наук. М., 2005. 36 с.
- Total hip arthroplasty for osteoarthritis in patients aged 80 years or older: influence of co-morbidities on final outcome/E. de Thomasson, I. Caux, O. Guingand [et al.]//Orthop Traumatol. Surg. Res. 2009. Vol. 95 (4). P. 249-253
- Гологорский В.А., Гриненко Т.Ф., Макарова Л.Д. О проблеме адекватности общей анестезии//Анестезиология и реаниматология. 1988. № 2. С. 3-6
- Филатов А. Н., Баллюзек Ф. В. Управляемая гемоди-люция. Л.: Медицина, 1972. 206 с.
- Устройство для определения энергообмена пациента. Классификация по МПК: А61В: пат. на полез, модель № 89358/Пригородов М. В. (RU), Садчиков Д. В. (RU), Пась-ко В.Г. (RU), Вартанян ТС. (RU). Дата публикации: 10 дек. 2009.


