Антагонист бомбезиновых рецепторов BBN/C1-C2 в модели колоректального рака in vitro
Автор: Белобородов Е.А., Юрова Е.В., Сугак Д.Е., Фомин А.Н., Саенко Ю.В.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 1, 2025 года.
Бесплатный доступ
Колоректальный рак является третьим по распространенности и вторым по количеству смертей онкологическим заболеванием в мире. Одна из стратегий лечения колоректального рака заключается в использовании таргетной пептидной терапии, нацеленной на определенные типы рецепторов, сверхэкспрессирующихся на поверхности клеток. Перспективной мишенью является бомбезиновый рецептор GRPR, для которого характерна аномальная экспрессия при колоректальном раке. В данной работе для лечения колоректального рака предлагается использовать молекулу BBN/C1-C2, созданную на основе бомбезина – короткого пептида, тропного к GRPR, и кноттина, который выступает в качестве каркаса для стабилизации молекулы. BBN/C1-C2 выступает в роли антагониста рецептора GRPR, что определяет его роль в выживаемости раковых клеток. Цель. Изучение влияния пептида BBN/C1-C2 на выживаемость клеточной культуры колоректального рака. Материалы и методы. Влияние пептида BBN/C1-C2, полученного с помощью твердофазного синтеза, на выживаемость раковых клеток оценивали в культуре HCT-116 с использованием флуоресцентной микроскопии (апоптоз, некроз) и клеточного анализатора (динамика адгезии клеток) через 3 и 24 ч после воздействия. Результаты. Пептид BBN/C1-C2 в концентрациях от 0,2 до 20 мкМ показал себя как молекулу, способную не только ингибировать пролиферацию клеток, но и вызывать клеточную гибель путем апоптоза уже через три часа после инкубации. Выводы. Таким образом, молекула BBN/C12-C2, созданная на основе агониста GRPR, встроенного в молекулу кноттина, может рассматриваться в качестве прототипа для создания радиофармпрепарата для лечения новообразований толстого кишечника.
Колоректальный рак, бомбезин, таргетная терапия
Короткий адрес: https://sciup.org/14132980
IDR: 14132980 | УДК: 615.849.12;615.277.3 | DOI: 10.34014/2227-1848-2025-1-114-123
Bombesin receptor antagonist BBN/C1-C2 in an in vitro model for colorectal cancer
Colorectal cancer is the third most common cancer and the second most fatal cancer worldwide. One of the strategies for colorectal cancer treatment is targeted peptide therapy that targets certain types of receptors overexpressed on the cell surface. A promising target is a bombesin receptor GRPR, which is abnormally expressed in colorectal cancer. In this paper, we suggest to use BBN/C1-C2 molecule, created on the basis of bombesin, a peptide tropic to GRPR, and knottin, acting as a scaffold to stabilize a molecule, for colorectal cancer treatment. BBN/C1-C2 acts as a GRPR receptor antagonist, which determines BBN/C1-C2 role in the survival of cancer cells. Objective: The aim of the paper is to study the effect of BBN/C1-C2 peptide on colorectal cancer cell survival. Materials and Methods. The effect of BBN/C1-C2 peptide obtained by solid-phase synthesis on cancer cell survival was assessed in HCT-116 culture using fluorescence microscopy (apoptosis, necrosis) and a cell analyzer (cell adhesion dynamics) 3 and 24 hours after exposure. Results: The BBN/C1-C2 peptide (concentrations from 0.2 to 20 μM) was able not only to inhibit cell proliferation, but also to cause cell death (apoptosis) three hours after incubation. Conclusion. BBN/C12-C2 molecule, created on the basis of a GRPR agonist built into a knottin molecule, can be considered as a prototype for a radiopharmaceutical to treat colon tumors.
Текст научной статьи Антагонист бомбезиновых рецепторов BBN/C1-C2 в модели колоректального рака in vitro
Введение. Колоректальный рак, представленный раком толстой или прямой кишки, является третьим по распространенности и вторым по количеству смертей онкологическим заболеванием в мире. В 2020 г. он стал причиной 9,4 % смертей [1]. Стандартным методом лечения колоректального рака является лапароскопическая резекция. Однако существует проблема определения целесообразности данной процедуры [2, 3]. К недостаткам классической химиотерапии можно отнести развитие устойчивости к применяемым препаратам [4]. Важным достижением в области лечения онкопатологии стала таргетная пептид-рецепторная радионуклидная терапия (ПРРТ).
Одна из стратегий ПРРТ колоректального рака заключается в воздействии на сверхэкс- прессирующий фактор роста эндотелия сосудов (VEGF). В качестве препарата может использоваться, например, бевацизумаб, представляющий собой моноклональное антитело, связывающееся с изоформами VEGF [5]. Противоопухолевый эффект бевацизумаба проявляется в противоангиогенном действии, изменении функциональности уже имеющихся в опухоли сосудов, а также непосредственном воздействии на VEGF-рецепторы опухолевых клеток [6]. Еще большим, чем бевацизумаб, сродством к VEGF обладает рекомбинантный белок афлиберцепт, представляющий собой внеклеточный домен VEGFR-1 и VEGFR-2 [7].
Другой стратегией ПРРТ является нацеливание на рецептор эпидермального фактора роста человека (EGFR), сверхэкспрессия кото- рого наблюдается в 65–75 % случаев колоректального рака [8]. Для реализации данного подхода используется цетуксимаб – антитело, которое после конкурентного связывания с внешним доменом рецептора способствует интернализации и разрушению EGFR, что приводит к ингибированию роста клеток, снижению выработки матриксной металлопротеиназы и VEGF, а также к индукции апоптоза [9, 10].
В данной работе для ПРРТ колоректального рака мы предлагаем использовать молекулу BBN/C1-C2, созданную на основе бомбе-зина – короткого пептида, тропного к GRPR, и кноттина, который выступает в качестве каркаса для стабилизации молекулы.
Цель исследования. Обобщить имеющиеся на сегодняшний день данные, касающиеся участия дофамина в регуляции сердечно-сосудистой системы.
Материалы и методы. Синтез BBN/C1-C2. Пептид BBN/C1-C2 получали с помощью твердофазного синтеза на основе Fmoc-химии (все аминокислоты производства Intavis (Германия)) на пептидном синтезаторе ResPep SL (Intavis, Германия) по стандартному протоколу. В качестве активатора использовали HBTU («Кемикал Лайн», Россия). Анализ пептида проводили на хроматографе LC-20AD XR (Shimadzu, Япония) методом обращенно-фазовой хроматографии и на масс-спектрометре MALDI-TOF MS FLEX (Bruker Daltonics, Германия). Очистку проводили на хроматографе
AutoPure25 (Inscinstech, Китай) методом обращенно-фазовой хроматографии.
Клеточная культура и условия эксперимента. В экспериментах использовали клеточную культуру HCT-116 (рак толстого кишечника человека), которую содержали в среде RPMI-1640 («ПанЭко», Россия) с добавлением 10 % фетальной бычьей сыворотки (Global Kang, Китай) и гентамицина. Пассажи проводили каждые 3–4 дня с использованием 0,25 % трипсина.
Перед экспериментом проводили пассаж в 24-луночные планшеты в концентрации 50 000 клеток на лунку. После достижения экспоненциальной стадии к культуре добавляли BBN/C1-C2 в фосфатно-солевом буфере с добавлением 0,1 % бычьего сывороточного альбумина для предотвращения неспецифического связывания и инкубировали 3 ч. После этого буфер заменяли на питательную среду и инкубировали. Для оценки апоптоза и некроза добавляли 20 мкМ пептида, результат фиксировали через 3 и 24 ч. Для анализа клеточного индекса добавляли 0,2, 2 и 20 мкМ BBN/C1-C2.
Флуоресцентная микроскопия . Уровни апоптоза и некроза оценивали с использованием флуоресцентных красителей Yo-Pro 1 (1 мкМ) и PI (1 мкМ), оптической системы Nikon Ti серии S (Nikon, Япония), камеры DS-Qi1MC и соответствующих фильтров. Фиксировали сигнал флуоресценции и обрабатывали информацию с использованием программы ImageJ. После этого получали данные в виде относительных флуоресцентных единиц (сигнал флуоресценции клеток за вычетом сигнала фона) [15].
Клеточный индекс. Анализ динамики адгезии клеток проводили с использованием клеточного анализатора xCellingence RTCA-S16 (ACEA Biosciences, США) [16]. Для этого культуру засеивали в 16-луночные планшеты, предварительно зафиксировав нулевую точку. В режиме реального времени фиксировали изменение клеточного индекса. Далее добавляли BBN/C1-C2, через 3 ч буфер заменяли на среду. Индекс фиксировали при всех манипуляциях.
Статистическая обработка данных. Каждый эксперимент проводили три раза в трех повторах. Статистическую обработку данных проводили с использованием критерия Стьюдента (апоптоз и некроз) и критерия Манна – Уитни (клеточный индекс). Различия считались достоверными при p<0,05.
Результаты. BBN/C1-C2 был получен с помощью твердофазного пептидного синтеза и очищен до 95 %. Далее его инкубировали с культурой HCT-116 3 ч, измеряли динамику клеточного индекса и уровень апоптоза и некроза после 3 и 24 ч восстановления в питательной среде. Данный подход позволяет оценить способность пептида не только непо- средственно вызывать гибель клеток, но и удерживаться на поверхности раковых клеток и обуславливать ингибирование целевого рецептора, что сказывается на динамике роста культуры в период восстановления.
При анализе клеточного индекса, который показывает динамику адгезии клеток как реакцию на внешнее воздействие, видно, что в первые 5 ч эффект BBN/C1-C2 носит дозозависимый характер (рис. 1). При этом действие BBN/C1-C2 в концентрации в 0,2 мкМ неотличимо от контрольных условий.
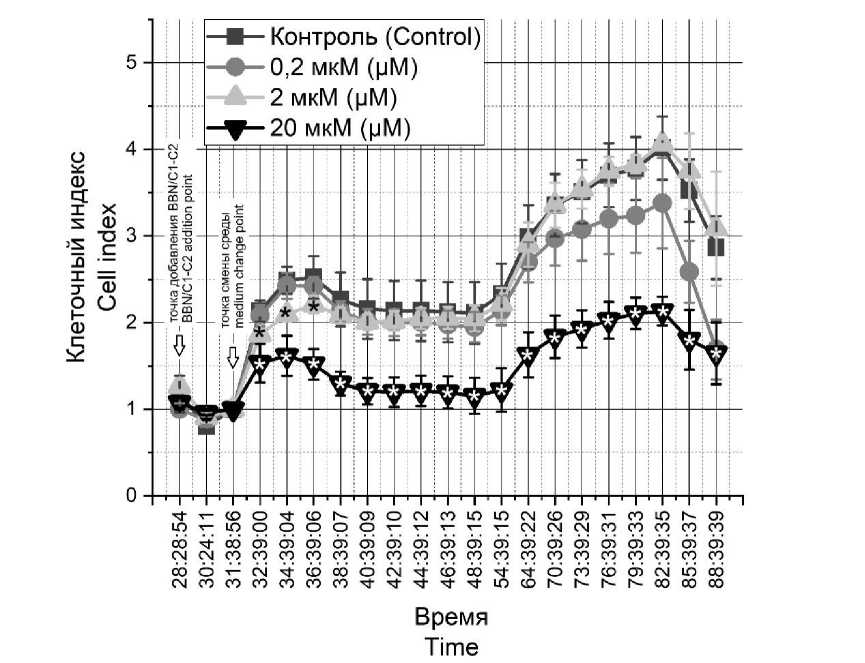
Рис. 1. Дозозависимое изменение клеточного индекса при добавлении к культуре HCT-116 пептида (точка нормализации 31:38:56, * – достоверное отличие от контрольной группы)
Fig. 1 . Dose-dependent change in the cell index while adding different concentrations of BBN/C1-C2 peptide to HCT-116 culture
(normalization point 31:38:56, * – the difference is significant compared with the control)
После воздействия пептида в концентрации 2 мкМ культура восстанавливается до контрольного уровня после 5 ч инкубации в среде. А в концентрации 20 мкМ в это же время продолжает снижаться. Даже несмотря на то что культура постепенно начинает восстанавливаться, клеточный индекс остается пониженным относительно контрольных условий, и со временем культура начинает погибать.
При анализе уровня клеточной гибели, сопровождающей изменение клеточного индекса, отмечается, что в первые 3 ч при инку- бировании культуры в фосфатно-солевом буфере с добавлением бычьего сывороточного альбумина и 20 мкМ BBN/C1-C2 происходит незначительное развитие апоптоза (рис. 2А), при этом уровень некроза остается близким к контролю (рис. 2В).
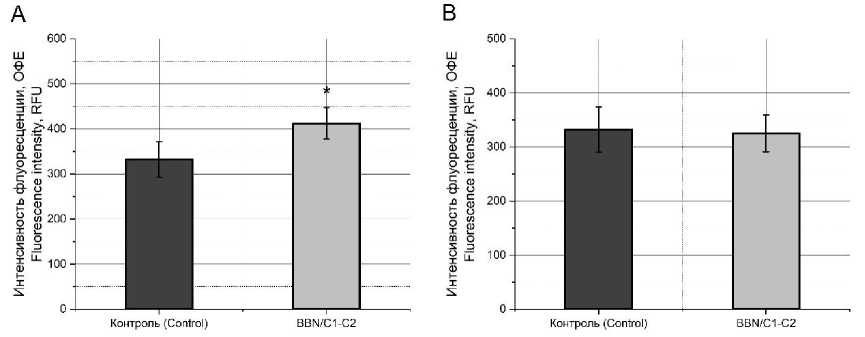
Рис. 2. Уровень апоптоза (А) и некроза (В) в культуре HCT-116 при добавлении BBN/C1-C2 в концентрации 20 мкМ через 3 ч (* – достоверное отличие от контрольной группы)
Fig. 2. Levels of apoptosis (A) and necrosis (B) in HCT-116 culture three hours after adding BBN/C1-C2 peptide (concentration 20 μM)
(* – the difference is significant compared with the control)
Но через 24 ч после смены буфера с BBN/C1-
C2 на питательную среду уровень апоптоза зна- чительно возрастает (рис. 3А), при этом уровень некроза остается прежним (рис. 3В).
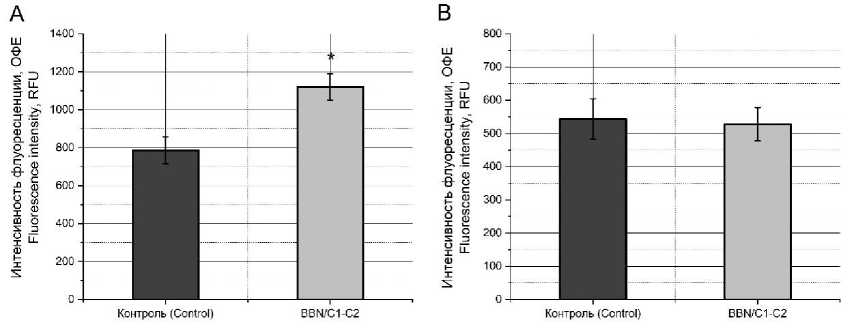
Рис. 3. Уровень апоптоза (А) и некроза (В) в культуре HCT-116 при добавлении BBN/C1-C2 в концентрации 20 мкМ через 24 ч (* – достоверное отличие от контрольной группы)
Fig. 3. Levels of apoptosis (A) and necrosis (B) in HCT-116 culture twenty-four hours after adding BBN/C1-C2 peptide (concentration 20 μM) (* – the difference is significant compared with the control)
Обсуждение. В последние десятилетия разработка радиофармпрепаратов на основе пептидов, нацеленных на бомбезиновые рецепторы, ведется достаточно успешно [17, 18]. Имеется ряд наблюдений, которые позволяют проводить дополнительные модификации пептидов для улучшения их свойств.
Так, в связи с тем, что качестве прототипов для создания радиофармпрепаратов используются пептиды, тропные к рецептору, в данном случае GRPR, эффект их может быть агонистическим, приводящим к биологическому отклику. В таком случае действие пептида на GRPR приведет к усилению трофики новообразования, что значимо скажется на развитии патологии. Ярким примером является агонист бомбезина AMBA (DOTA-Gly-4-аминобензоил-BBN(7–14), применение которого показывает хорошую результативность при визуализации и терапии рака предстательной и молочной желез [19, 20]. Однако у пациентов, прошедших лечением AMBA, наблюдалось его значительное поглощение поджелудочной железой и желудочно-кишечным трактом [21]. Кроме того, исследование фазы I, проведенное у пациентов с метастатическим ка-страционно-резистентным раком простаты, было прекращено из-за серьезных побочных эффектов, вызванных активацией GRPR после инъекции терапевтических доз [22].
Использование антагонистов рецепторов также может значительно изменить ход лечения новообразований. Например, одна из модификаций PD176252, непептидного ингибитора GRPR, обеспечивает значительное снижение скорости роста линий клеток HGC-27 (желудок), HCT-116 (толстый кишечник), PC-3 (простата), A549 (легкие) [23]. Кроме того, RC-3940-II вызывает ингибирование пролиферации клеточных линий рака толстой кишки человека HT-29, HCT-116 и HCT-15 in vitro и in vivo [24].
Нами предлагается создание антагониста на основе пептида бомбезина (агониста рецептора GRPR) с добавлением радиоизотопа, что приведет к развитию двойного эффекта: снижению пролиферации новообразования и ги-белю клеток в результате действия радиоактивности. BBN/C1-C2 был разработан на основе кноттина, содержащего в своем составе ингибиторный цистиновый узел, и короткого пептида – бомбезина, помещенного между первым и вторым остатками цистеина. Подобная структура показывает значительное увеличение стабильности в различных условиях, а также дозозависимое снижение пролиферации линии клеток HCT-116. Динамике клеточного индекса в условиях сразу после инкубации с пептидом в трех концентрациях и в условиях восстановления в питательной среде в течении 24 ч после воздействия свидетельствует о том, что пептид в концентрации 20 мкМ значительно снижает значения индекса, что говорит о нарушении адгезии клеток и неспособности к дальнейшему восстановлению. Данные подтверждаются развитием апоптоза в питательной среде через 3 ч после инкубации с пептидом в той же концентрации и его усилением через 24 ч.
Заключение. Таким образом, молекула BBN/C12-C2, созданная на основе агониста GRPR, встроенного в молекулу кноттина, может рассматриваться в качестве прототипа для создания радиофармпрепарата для лечения новообразований толстого кишечника. Кроме того, повышенная стабильность созданной молекулы позволит ей в полном объеме достигать цели, что снизит нагрузку на организм.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования Российской Федерации (проект № 123020700216 (FEUF-2023-0004)).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Концепция и дизайн исследования: Саенко Ю.В., Фомин А.Н.
Литературный поиск, участие в исследовании, обработка материала: Белобородов Е.А.,
Юрова Е.В., Сугак Д.Е.
Статистическая обработка данных: Белобородов Е.А.
Анализ и интерпретация данных: Юрова Е.В.
Написание и редактирование текста: Белобородов Е.А., Юрова Е.В., Саенко Ю.В.


