Антибактериальное действие лизоцима против возбудителей остеомиелита S. aureus и S. epidermidis
Автор: Шипицына И.В., Осипова Е.В.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.31, 2025 года.
Бесплатный доступ
Введение. Использование лизоцима в качестве бактерицидного агента против ведущих возбудителей хронического остеомиелита может стать альтернативой либо дополнением к существующим антибактериальным препаратам. Цель работы — оценить антибактериальное действие лизоцима в отношении клинических штаммов Staphylococcus aureus и Staphylococcus epidermidis. Материалы и методы. В качестве тест-культур использовали музейные штаммы Staphylococcus aureus (АТСС 25923), Staphylococcus epidermidis (АТСС 14990) и клинические штаммы (n = 48), в том числе MRSA (n = 6) и MRSE (n = 6), изолированные из ран и свищей пациентов с хроническим остеомиелитом. Антибактериальное действие лизоцима оценивали, используя диско-диффузионный метод. Результаты. Лизоцим проявлял бактерицидное действие в отношении музейных штаммов S. aureus и S. epidermidis, зона задержки роста бактерий составляла 11–12 мм. Чувствительны к лизоциму было 87,5 % клинических штаммов S. aureus, диаметр зоны задержки роста составлял 9–13 мм. В отношении трех штаммов S. aureus, в том числе двух MRSA, отмечено отсутствие бактерицидного эффекта, вокруг диска наблюдали сплошной рост бактерий. Среди штаммов S. epidermidis антибактериальное действие лизоцима наблюдали в отношении 79,2 % изолятов, диаметр задержки роста составлял 8–11 мм. Отмечена устойчивость трех штаммов MRSE к лизоциму. Лизоцим усиливал действие ванкомицина и цефокситина против метициллин-чувствительных штаммов стафилококков и норфлоксацина, и ванкомицина — против метициллин-резистентных стафилококков. Обсуждение. Несмотря на обнаруженный ингибирующий эффект, применение только одного лизоцима может быть ограниченно в связи с возможностью его деградации протеазами, а также некоторой иммуногенностью. В литературе имеются работы о синергизме комбинированного действия лизоцима с различными антибиотиками на грамположительные и грамотрицательные бактерии. Полученные в нашем эксперименте данные показали усиление антибактериального эффекта при совместном действии антибиотиков и лизоцима в отношении ведущих возбудителей остеомиелита. Заключение. Установлено, что лизоцим обладает антибактериальным действием в отношении клинических штаммов S. aureus, S. epidermidis, в том числе и MRSA и MRSE, изолированных из ран пациентов с хроническим остеомиелитом. При совместном действии лизоцима с цефотаксимом, норфлоксацином и ванкомицином наблюдается усиление антибактериального эффекта.
Хронический остеомиелит, лизоцим, резистентность, антимикробные пептиды, антибиотики
Короткий адрес: https://sciup.org/142244810
IDR: 142244810 | УДК: [616.718.5/.6-007.24-089.227.84:004.9]-089.168 | DOI: 10.18019/1028-4427-2025-31-3-334-340
Antibacterial action of lysozyme against osteomyelitis agents: S. aureus and S. epidermidis
Introduction The use of lysozyme as a bactericidal agent against the leading pathogens of chronic osteomyelitis can become an alternative or supplement to existing antibacterial drugs. Purpose To study the antibacterial effect of lysozyme against clinical strains of Staphylococcus aureus and Staphylococcus epidermidis Materials and methods Control strains of Staphylococcus aureus (ATCC 25923), Staphylococcus epidermidis (ATCC 14990) and clinical strains (n = 48), including MRSA (n = 6) and MRSE (n = 6), isolated from wounds and fistulas of patients with chronic osteomyelitis were used as test cultures. The antibacterial effect of lysozyme was assessed using the disk diffusion method. Results Lysozyme exhibited bactericidal activity against control strains of S. aureus and S. epidermidis, the growth inhibition zone of bacteria was 11–12 mm. Among clinical strains of S. aureus, 87.5 % were sensitive to lysozyme, the growth inhibition zone diameter was 9–13 mm. No bactericidal effect was observed against three strains of S. aureus, including two MRSAs, and continuous bacterial growth was observed around the disk. Among strains of S. epidermidis, the antibacterial activity of lysozyme was observed against 79.2 % of isolates, the growth inhibition diameter was 8–11 mm. Resistance of three MRSE strains to lysozyme was noted. Lysozyme enhanced the effect of vancomycin and cefoxitin against methicillin-sensitive staphylococci and norfloxacin and vancomycin against methicillin-resistant staphylococci. Discussion Despite the inhibitory effect found, the use of lysozyme alone may be limited due to its possible degradation by proteases, as well as some immunogenicity. There are studies on the synergism of the combined action of lysozyme with various antibiotics on gram-positive and gram-negative bacteria. The data obtained in our experiment showed an increased antibacterial effect by the combined action of antibiotics and lysozyme against the leading causative agents of osteomyelitis. Conclusion It has been established that lysozyme has an antibacterial effect against clinical strains of S. aureus, S. epidermidis, including MRSA and MRSE, isolated from wounds of patients with chronic osteomyelitis. An increased antibacterial effect is observed by a combined action of lysozyme with cefotaxime, norfloxacin and vancomycin.
Текст научной статьи Антибактериальное действие лизоцима против возбудителей остеомиелита S. aureus и S. epidermidis
Чаще всего остеомиелит вызывают бактерии рода Staphylococcus, преимущественно S. aureus и S. epidermidis (включая метициллин-устойчивые штаммы MRSA и MRSE ), которые демонстрируют высокую степень резистентности к традиционным антибиотикам. Это делает лечение пациентов с остеомиелитом сложным и требует поиска новых, более эффективных препаратов [1–4].
Как альтернатива или в дополнении к существующим антибактериальным средствам, актуальным направлением может стать использование лизоцима в качестве бактерицидного агента против ведущих возбудителей хронического остеомиелита. Лизоцим — это антимикробный фермент, который содержится в различных биологических жидкостях, таких как слюна, слезы и грудное молоко [5, 6]. Лизоцимы подразделяются на три основных семейства: куриный тип (c-тип), гусиный тип (g-тип) и беспозвоночный тип (i-тип). Также известны лизоцимы фагового типа, бактериального типа и растительного типа. Куриный и человеческий являются лизоцимами c-типа. Куринный состоит из 129 аминокислотных остатков (14,3 кДа), человеческий — из 130 аминокислотных остатков (14,7 кДа). Между последовательностью человеческих и куриных лизоцимов существует идентичность 59 %, но антибактериальная активность куриного лизоцима в три раза ниже, чем антибактериальная активность человеческого, однако его использование ограничено из-за доступности ресурсов [5, 7, 8].
Поскольку лизоцим является естественным компонентом организма, он обычно хорошо переносится и имеет низкий риск токсичности, поэтому его используют в медицинских целях. Лизоцим разрушает пептидогликаны, которые составляют клеточную стенку бактериальных клеток, что приводит к осмотическому разрушению и гибели бактерий [8]. Комбинация лизоцима с антибактериальными препаратами может усиливать их действие [9, 10]. Лизоцим также способен модулировать иммунный ответ организма [7, 8]. В настоящее время лизоцим уже используется как консервант и антисептик [6, 8]. Перспектива использования лизоцима в качестве антибактериального агента против ведущих возбудителей остеомиелита может расширить область его применения в медицине.
Цель работы — оценить антибактериальное действие лизоцима в отношении клинических штаммов Staphylococcus aureus и Staphylococcus epidermidis .
МАТЕРИАЛЫ И МЕТОДЫ
В качестве тест-культур использовали музейные штаммы Staphylococcus aureus (АТСС 25923), Staphylococcus epidermidis (АТСС 14990) и клинические штаммы ( n = 48), в том числе MRSA ( n = 486) и MRSE ( n = 486), изолированные из ран и свищей пациентов с хроническим остеомиелитом.
Идентификацию бактерий осуществляли на бактериологическом анализаторе BactoScreen (ООО НПФ «Литех»). Чувствительность микроорганизмов к антибактериальным препаратам определяли дискодиффузионным методом. Оценку результатов проводили, используя критерии EUCAST (2017–2022 гг.). Выявление генов метициллин-резистентных стафилококков в биологическом материале осуществляли с использованием набора реагентов для выявления и количественного определения ДНК MSSA и MRSA, MSSE и MRSE методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией «АмплиСенс MRSA-скрин-титр-FL».
Антибактериальное действие лизоцима оценивали, используя диско-диффузионный метод. На поверхность плотной питательной среды (агар Мюллера – Хинтона), засеянной газоном суточной культуры S. aureus или S. epidermidis , помещали диски из картона фильтровального технического (ГОСТ 6722–75) и диски с антибиотиками, пропитанные лизоцимом (CAS–№ 9001-63-2, 20000 U/mg, AppliChem) в концентрации 30 мкг/мл. Чашки Петри с посевами инкубировали в термостате при температуре 37 °С. Через 24 ч. фиксировали результаты, измеряя зону задержки роста вокруг диска. Действие лизоцима на музейные штаммы проводили в шести повторах.
Проанализированы профили резистентности бактерий S. aureus , S. epidermidis к четырем тестируемым АМП (антимикробным препаратам): цефокситин (FOX), гентамицин (GEN), норфлоксацин (NOR), ванкомицин (VAN).
Для статистической обработки полученных данных использовали программы Gnumeric 1.12.17 и электронные таблицы LibreOffice (версия: 5.4.1.2). Проверку выборок на соответствие определённому закону распределения проводили с помощью критерия Андерсона – Дарлинга. Учитывая, что данные в выборках подчинялись нормальному распределению, для проверки гипотезы о равенстве средних значений применяли критерий Стьюдента. Цифровые данные представлены в виде среднего арифметического значения ( М ) и стандартного отклонения (SD). Различия считали значимыми при р < 0,05.
Микробиологические исследования проведены в лаборатории микробиологии НМИЦ ТО имени академика Г.А. Илизарова.
РЕЗУЛЬТАТЫ
Музейные культуры S. aureus и S. epidermidis были чувствительны к действию лизоцима (рис. 1). Среди клинических изолятов бактерий встречались как чувствительные, так и не чувствительные к лизоциму штаммы.
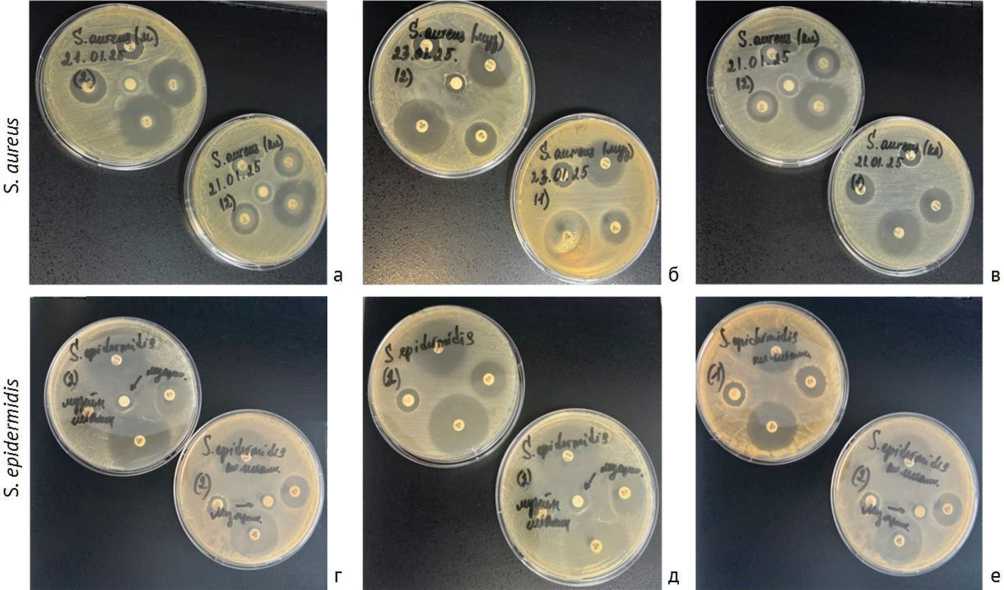
Рис. 1. Антибактериальное действие лизоцима совместно с антибиотиками и без антибиотиков на музейные и клинические штаммы бактерий S. aureus , S. epidermidis : а, г — музейные и клинические штаммы; б, д — музейные штаммы, в, е — клинические штаммы
Значимых различий в диаметре задержки роста между музейными и клиническими штаммами не наблюдали (табл. 1).
Лизоцим в концентрации 30 мкг/мл проявлял бактерицидное действие в отношении музейных штаммов S. aureus и S. epidermidis , зона задержки роста бактерий составляла 11–12 мм. Среди клинических штаммов S. aureus чувствительность к лизоциму выявлена в 87,5 %, диаметр зоны задержки роста составлял 9–13 мм. В отношении
Таблица 1
Зона задержки роста бактерий S. aureus и S. epidermidis после воздействия лизоцима (30 мкг/мл)
|
Микроорганизм |
Диаметр зоны задержки роста, мм |
|
S. aureus АТСС 25923 ( n = 6) |
11,3 ± 0, 47 |
|
S. aureus ( n = 24) |
11,2 ± 1,10 |
|
S. epidermidis АТСС 12228 ( n = 6) |
10,0± 0,43 |
|
S. epidermidis ( n = 24) |
10,5 ± 1,05 |
трех штаммов S. aureus , в том числе двух MRSA , отмечено отсутствие бактерицидного эффекта, вокруг диска наблюдали сплошной рост бактерий.
Среди штаммов S. epidermidis антибактериальное действие лизоцима наблюдали в отношении 79,2 % изолятов, диаметр задержки роста составлял 8–11 мм. Отмечена устойчивость трех штаммов MRSE к лизоциму.
Штаммы S. aureus ( n = 18) и S. epidermidis ( n = 18) были чувствительны к действию тестируемых антибактериальных препаратов. Лизоцим усиливал действие антибиотиков, что выражалось в увеличении зоны задержки роста бактерий вокруг дисков. Значимые отличия наблюдали для ванкомицина и це-фокситина (табл. 2).
В отношении метициллин-резистентных стафилококков лизоцим не усиливал действие цефокситина и гентамицина. Значимые отличия наблюдали только для норфлоксацина и ванкомицина (табл. 3).
Таблица 2
Зона задержки роста метициллин-чувствительных стафилококков, выделенных из ран пациентов с хроническим остеомиелитом под воздействием лизоцима
|
Препарат (мкг) |
Диаметр зоны задержки роста, мм |
|||
|
MSSA , ( n = 18) |
MSSE , ( n = 18) |
|||
|
– |
+ лизоцим (30) |
– |
+ лизоцим (30) |
|
|
Цефокситин (30) |
23,3± 0,47 |
26,5 ± 0,81* p = 0,02476 |
33,3 ± 2,10 |
35,7 ± 1,90 |
|
Норфлоксацин (10) |
29,0 ± 0,82 |
30,0 ± 0,79 |
31,3 ± 0,83 |
32,0 ± 1,40 |
|
Гентамицин (10) |
19,0 ± 1,40 |
19,7 ±1,24 |
20,8 ± 6,60 |
22,3 ± 1,80 |
|
Ванкомицин (5) |
13,7 ± 0,94 |
15,8 ± 0,47* p = 0,0404 |
15,0 ± 0,51 |
17,3 ± 1,10* p = 0,0216 |
Примечание : * — уровень значимости различий между группами, р < 0,05.
Таблица 3
Зона задержки роста метициллин-резистентных стафилококков, выделенных из ран пациентов с хроническим остеомиелитом под воздействием лизоцима
|
Препарат (мкг) |
Диаметр зоны задержки роста, мм |
|||
|
MSSA , ( n = 6) |
MSSE , ( n = 6) |
|||
|
– |
+ лизоцим (30) |
– |
+ лизоцим (30) |
|
|
Цефокситин (30) |
20,3 ± 0,84 |
20,0 ± 0,82 |
19,5 ± 1,10 |
20,0 ±0,80 |
|
Норфлоксацин (10) |
27,3 ± 1,25 |
30,2 ± 0,61* p = 0,0248 |
29,8 ± 1,03 |
32,2 ±0,62* p = 0,0242 |
|
Гентамицин (10) |
18,8 ± 0,24 |
18,5 ± 0,20 |
10,7 ±0,94 |
12,0 ± 0,41 |
|
Ванкомицин (5) |
14,3 ± 0,47 |
14,2 ± 0,62 |
14,7 ±0,47 |
17,5 ± 0,72* p = 0,025 |
Примечание : * — уровень значимости различий между группами, р < 0,05.
ОБСУЖДЕНИЕ
Клинически значимым патогеном при хроническом остеомиелите считается S. аureus , который, взаимодействуя с клетками организма посредством варианта малых колоний (SCV), образованием биопленок и секрецией токсина, индуцирует воспалительную реакцию, вызывая гибель клеток путем апоптоза и некроза [1]. Важная роль в развитии инфекций при хроническом остеомиелите принадлежит и бактериям S. epidermidis [3, 11]. В последнее десятилетие отмечается увеличение числа бактерий с множественной лекарственной устойчивостью, что приводит к неэффективности традиционных подходов в лечении пациентов с хроническим остеомиелитом и определяет необходимость поиска новых препаратов [2, 4].
Перспективным направлением считается использование антимикробных пептидов системы врожденного иммунитета [12]. Известно, что пептиды, полученные в результате расщепления лизоцима, проявляют антимикробную активность, в первую очередь, против грамположительных бактерий [13]. Они могут действовать напрямую (литический эффект) или косвенно (модулировать иммунную систему). Антибактериальный механизм лизоцима обусловлен его мурамидазной активностью, которая гидролизует β -l,4-гликозидную связь пептидогликанов, способностью связываться с нуклеиновыми кислотами микроорганизмов и вызывать мутацию или распад бактериального генетического материала [5, 14, 15].
Из-за различий в механизмах устойчивости бактерий к антибиотикам и антимикробным пептидам клиническое применение лизоцима имеет меньший риск развития резистентности у микроорганизмов. Считается, что устойчивость к пептидогликанразлагающим ферментам у бактерий развивается редко, являясь результатом горизонтального переноса детерминант устойчивости, а не мутацией de novo [16].
По данным литературы, обнаружен ингибирующий эффект лизоцима, полученного из яичного белка, на лекарственно-устойчивые бактерии, в том числе на MRSA [17]. В нашем исследовании 87,5 % MSSA , 79,2 % MSSE и 50 % штаммов MRSA и MRSE были чувствительны к действию лизоцима.
Применение только одного лизоцима может быть ограничено в связи с возможностью его деградации протеазами, присутствующими в жидкостях организма, а также некоторой иммуногенностью, которая при повторном использовании может вызывать иммунные реакции [18, 19]. Вопрос о лизоциме как аллергене остаётся спорным. Одни исследователи считают, что лизоцим, являясь компонентом иммунной системы человека, не вызывает аллергической реакции [20]. В других исследованиях показано, что он действует как слабый аллерген [21, 22]. Кроме того, при нанесении непосредственно на поверхность раны лизоцим может легко смываться экссудатом. В связи с этим разрабатывают новые методы доставки лизоцима в очаг инфекции для повышения эффективности его воздействия и уменьшения побочных эффектов [23]. К ним относятся гидрогели, нанопленки, волокнистые мембраны и композитные системы с модифицированным лизоцимом, что позволит улучшить стабильность лизоцима и снизить его иммуногенность [24, 25].
Одним из видов альтернативного использования пептидов является применение их в сочетании с традиционными антибиотиками для лечения пациентов с остеомиелитом [26]. Полученные в нашем эксперименте данные показали усиление действия антибиотиков в отношении всех чувствительных микроорганизмов, однако значимые различия были установлены для комбинации лизоцима с ванкомицином и цефокситином. В отношении метициллин-резистентных штаммов стафилококков усиление антимикробной активности отмечали только для комбинации лизоцима с ванкомицином и норфлоксацином.
При изучении комбинированного действия лизоцима, полученного из яичного белка, с различными антибиотиками (гентамицин, офлоксацин, оксациллин, рифампицин, полимиксин B, ванкомицин, ципрофлоксацин и тетрациклин) на грамположительные и грамотрицательные бактерии, включая чувствительные и устойчивые к лекарственным препаратам штаммы, установлен синергетический механизм действия, снижающий устойчивость микробов [9, 26, 27]. Антибактериальные пептиды изменяют проницаемость клеточной мембраны, позволяя большему количеству антибиотика проникать в клетку и связываться с внутриклеточными мишенями, усиливая его действия и снижая побочные эффекты высоких концентраций [9, 10].
Исследователями показано, что бактерицидный эффект от совместного действия лизоцима и антибиотика в отношении планктонных клеток и биоплёнок, полученных in vitro , более выражен по сравнению с применением препаратов по отдельности [28].
В то же время, необходимо учитывать тот факт, что у всех бактерий имеются как общие, так и специфические механизмы защиты от факторов врожденного иммунитета. К механизмам устойчивости, используемым грамположительными бактериями, в том числе S. aureus , относятся изменения заряда и состава клеточной стенки. Чувствительность грамположительных бактерий к антимикробным пептидам зависит от: содержания отрицательно заряженных тейхоевых кислот в клеточной стенке, которые связывают лизоцимы и снижают их ферментативную активность [8, 19]; инактивации пептидов за счет связывания их поверхностными или секретируемыми белками и полисахаридами; расщепления антимикробных пептидов бактериальными протеазами; адаптации бактерий к воздействию антимикробных пептидов; вытеснения антимикробных пептидов эффлюксными насосами и транспортными системами [16, 29, 30].
ЗАКЛЮЧЕНИЕ
Установлено, что лизоцим обладает антибактериальным действием в отношении клинических штаммов S. aureus , S. epidermidis , в том числе и MRSA и MRSE , изолированных из ран пациентов с хроническим остеомиелитом. При совместном действии лизоцима с цефотаксимом, норфлоксацином и ванкомицином наблюдается усиление антибактериального эффекта.


