Антибиотикорезистентность штаммов стафилококков, выделенных при заболеваниях мочевыделительной системы у кошек
Автор: Пашинина О.А., Кочкина Е.Е., Сычева М.В., Пашкова Т.М., Морозова Н.В., Карташова О.Л.
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринария и зоотехния
Статья в выпуске: 4 (48), 2022 года.
Бесплатный доступ
Цель исследования - охарактеризовать антибиотикорезистентность штаммов стафилококков, выделенных из мочи кошек с патологией мочевыделительной системы, на уровне фено- и генотипа. Исследуемый материал - стафилококки, выделенные из мочи 22 кошек с заболеваниями мочевыделительной системы путем ее посева на желточно-солевой агар. Вид микроорганизмов оценивали методом MALDI-TOF масс-спектрометрии. Резистентность к 10 антибиотикам (амоксиклав, цефазолин, цефтриаксон, цефепим, цефотаксим, энрофлоксацин, ципрофлоксацин, азитромицин, гентамицин, тилозин) 12 штаммов Staphylococcus aureus, 6 Staphylococcus sciuri, 7 Staphylococcus intermedius определяли диско-диффузионным методом. Гены резистентности к антибиотикам ( mecA ; blaZ ; aac(6')-аph (2'') ; ant(4')-Ia ; аph(3')-IIIa ; gyrA , grlA, ermA, ermB, ermC ) обнаруживали с помощью полимеразной цепной реакции (ПЦР) с использованием подобранных праймеров. Установлена высокая чувствительность стафилококков к цефазолину, цефепиму, амоксиклаву и резистентность к азитромицину. S. aureus и S. intermedius характеризовались умеренной резистентностью к фторхинолонам, а все изученные виды - к тилозину. С помощью ПЦР установлено наличие в геноме изученных штаммов стафилококков генетических детерминант резистентности к пенициллинам и β-лактамам ( mecA ; blaZ ), у S. aureus - к аминогликозидам ( ant (4')-Ia ) и макролидам ( ermA ), у S. intermedius - к фторхинолонам ( gyrA ) . Установленная резистентность к азитромицину штаммов стафилококков разных видов, выделенных из мочи кошек с заболеваниями мочевыделительной системы, свидетельствует о необходимости контроля за его применением. Для эффективной антибактериальной терапии необходимо проводить региональный мониторинг устойчивости микроорганизмов к антибиотикам. В качестве препаратов выбора при эмпирической терапии животных с заболеваниями мочевыделительной системы стафилококковой этиологии могут рассматриваться цефазолин, цефепим, амоксиклав, гентамицин.
Стафилококки, заболевания мочевыделительной системы, кошки, антибиотикорезистентность, молекулярно-генетическое исследование
Короткий адрес: https://sciup.org/142236102
IDR: 142236102 | УДК: 579.62 | DOI: 10.48136/2222-0364_2022_4_156
Antibiotic resistance of staphylococcal strains isolated from diseases of the urinary system in cats
The purpose of the research is to characterize the antibiotic resistance of staphylococcal strains isolated from the urine of cats with pathology of the urinary system, at the level of phenotype and genotype. The studied material was staphylococci isolated from the urine of 22 cats with diseases of the urinary system by inoculation on yolk-salt agar. The type of microorganisms was assessed by MALDI-TOF mass spectrometry. Resistance to 10 antibiotics (amoxiclav, cefazolin, ceftriaxone, cefepime, cefotaxime, enrofloxacin, ciprofloxacin, azithromycin, gentamicin, tylosin) of 12 strains of Staphylococcus aureus , 6 Staphylococcus sciuri , 7 Staphylococcus intermedius was determined by disk diffusion method. Antibiotic resistance genes ( mecA ; blaZ ; aac(6')-aph (2'') ; ant(4')-Ia ; aph(3')-IIIa ; gyrA , grlA, ermA , ermB , ermC ) were detected using polymerase chain reaction (PCR) using selected primers. A high sensitivity of staphylococci to cefazolin, cefepime, amoxiclav and resistance to azithromycin was established. S. aureus and S. intermedius were moderately resistant to fluoroquinolones, and all studied species were resistant to tylosin. Using PCR, the presence in the genome of the studied staphylococcal strains of genetic determinants of resistance to penicillins and β-lactams ( mecA ; blaZ ), in S. aureus to aminoglycosides ( ant(4')-Ia ) and macrolides ( ermA ), and in S. intermedius resistance to fluoroquinolones ( gyrA ). The established resistance to azithromycin of strains of staphylococci of various species isolated from the urine of cats with diseases of the urinary system indicates the need to control its use. For effective antibiotic therapy, it is necessary to conduct regional monitoring of microorganism resistance to antibiotics. Cefazolin, cefepime, amoxiclav, gentamicin can be considered as drugs of choice in the empirical therapy of animals with diseases of the urinary system of staphylococcal etiology.
Текст научной статьи Антибиотикорезистентность штаммов стафилококков, выделенных при заболеваниях мочевыделительной системы у кошек
Патология мочевыделительной системы среди домашних плотоядных является одной из самых часто встречающихся. В течение последних двух десятилетий заболеваемость неуклонно растет [1], ситуация осложняется частыми рецидивами болезни [2].
Лечение пациентов с рецидивирующими заболеваниями мочевыделительной системы является серьезной проблемой, поскольку требует применения противомикроб-ных препаратов в ветеринарии, что способствует развитию резистентности микроорганизмов [3]. Для проведения действенной антибактериальной терапии необходимы достоверные данные об изменении чувствительности патогенов к антибиотикам в каждом регионе. При этом для повышения эффективности лечения мало определить антибио-тикорезистентность бактерий на фенотипическом уровне. Имея одинаковые фенотипы, но реализуя разные механизмы антибиотикорезистентности, микроорганизмы могут существенно отличаться по чувствительности к применяемым антибактериальным препаратам. Для организации тактики эффективного антибактериального лечения на на-
Vestnik of Omsk SAU, 2022, no. 4(48) VETERINARY AND ZOOTECHNY циональном и региональном уровнях нужны данные о распространенности бактериальных генетических детерминант резистентности [4].
Установлено преобладание разных видов стафилококков в составе микрофлоры, выделенной из мочи кошек при заболеваниях мочевыделительной системы [5].
В связи с этим, с одной стороны, представляет интерес фенотипическое исследование антибиотикорезистентности клинических изолятов стафилококков, которые преимущественно инфицируют мочевой пузырь при цистите и мочекаменной болезни, для оценки риска формирования устойчивости к антибактериальным препаратам, а с другой – молекулярно-генетическое исследование антибиотикорезистентности изолятов.
Объекты и методика исследования
В работе были использованы Staphylococcus spp . разных видов, выделенные из мочи 22 кошек с патологией мочевыделительной системы (мочекаменная болезнь и цистит), находящихся на лечении в ветеринарных клиниках г. Оренбурга.
При первичном обследовании пробы мочи из мочевого пузыря с помощью катетера отбирали в стерильные пробирки с соблюдением правил асептики и доставляли в лабораторию в течение одного-двух часов для проведения бактериологического исследования.
Изолировали уроштаммы классическим бактериологическим методом. Для выделения Staphylococcus spp . использовали желточно-солевой агар, куда засевали исследуемый материал. Чашки с посевами культивировали при 37°С в течение 18–24 ч.
Видовую принадлежность микроорганизмов определяли с помощью масс-спектрометра MALDI-TOF серии Microflex (Bruker Daltonics, Германия) с расчетом коэффициента достоверности при использовании программного обеспечения Maldi BioTyper 3,0.
Определение чувствительности микроорганизмов к антибактериальным препаратам осуществляли диско-диффузионным способом согласно [6]. В исследовании применяли стандартные диски промышленного производства, пропитанные следующими антибактериальными препаратами: азитромицин, амоксициллин/клавулановая кислота, цефазолин, цефтриаксон, цефепим, цефотаксим, энрофлоксацин, ципрофлоксацин, гентамицин, тилозин. Учет результатов проводили по диаметру зоны задержки роста тестируемых урокультур.
Молекулярно-генетическому исследованию было подвергнуто 25 штаммов стафилококков: 12 – Staphylococcus aureus, 6 – Staphylococcus sciuri, 7 – Staphylococcus in-termedius .
ДНК экстрагировали из суточной агаровой культуры стафилококков с применением набора реактивов «ДНК-экспресс» («Литех», Россия), согласно рекомендации производителя.
Амплификацию проводили на многоканальном амплификаторе «Терцик МС-2» («ДНК-технология», Россия) по стандартному протоколу. Для выявления генетических детерминант резистентности применяли специфические олигонуклеотидные праймеры, описанные в научных источниках [7; 8] и синтезированные фирмой «Синтол» (Россия) (таблица).
Продукты амплификации анализировали путем электрофоретического разделения (рис. 1).
Vestnik of Omsk SAU, 2022, no. 4(48) VE TE RIN A R Y A ND Z OOTE C HNY
Праймеры, используемые для обнаружения детерминант антибиотикорезистентности микроорганизмов
|
№ |
Антимикробный препарат |
Ген |
Праймер |
Нуклеотидная п осл е д ов а тельнос ть праймеров |
Размер продукта (пн) |
|
1 |
Метициллин (оксациллин), цефалоспорины |
mecA |
mecAQF2 |
GGG A TC A T A GC GTCA TTA T TC C |
163 |
|
mecAQR2 |
C G A TGC C TA TC TC A T A TGC |
||||
|
2 |
Ампициллин, амоксиклав |
blaZ |
blaZ- F |
ACTTCAACACCTGC TGC TT TC |
170 |
|
blaZ-R |
TGACCACTTT TA TC A GCA AC C |
||||
|
3 |
Аминогликозиды: гентамицин тобрамицин, амикацин, канамицин канамицин |
aac(6') aph(2'') |
aac-aph-F |
T TGGGAA G A TGAAGTT T TTA GA |
160 |
|
aac-aph-R |
C C TT TA C TC CAA TAA TT T GGC T |
||||
|
ant(4')-Ia |
ant(4')-1-F |
CAAAC TGC TAAA TC GGTA G AAG C C |
294 |
||
|
ant(4')-1-R |
GG AAA GTTGA C CAG ACAT TA C G AAC T |
||||
|
аph(3')-IIIa |
aph(3')-IIIa-F |
GGC TAAAA TG A G AA T A T CA CC GG |
523 |
||
|
aph(3')-IIIa-R |
C T T TAAAAAA TCA TACA G C TC GC G |
||||
|
4 |
Фторхинолоны |
gyrA |
tnpR-F |
A TGA TT T T TGGC TA TGC T C G |
382 |
|
tnpR-R |
TA A G ACCA G AGT TA GTTCGT TC |
||||
|
grlA |
tnpA-F |
ACAAC TTCT T TCTG TA G AC CAC |
604 |
||
|
tnpA-R |
GTC T T T TA GC CAA G C G AG |
||||
|
5 |
Макролиды |
ermA |
ermAF |
TA TCT TA TC GT TGA G AA G GG A T T |
139 |
|
ermAR |
C TA CAC TTGGC TGA TGAAA |
||||
|
ermB |
ermBF |
C TA TC TGA T TG T TGAA G AA G CA TT |
141 |
||
|
ermBR |
GT T TA C TC T TGG T T TA GG A TCAAA |
||||
|
ermС |
ermCF |
AA TC GTCAA TTC C TGC A TGT |
299 |
||
|
ermCR |
TA A TC GTGGAA T A C G GG T T TG |
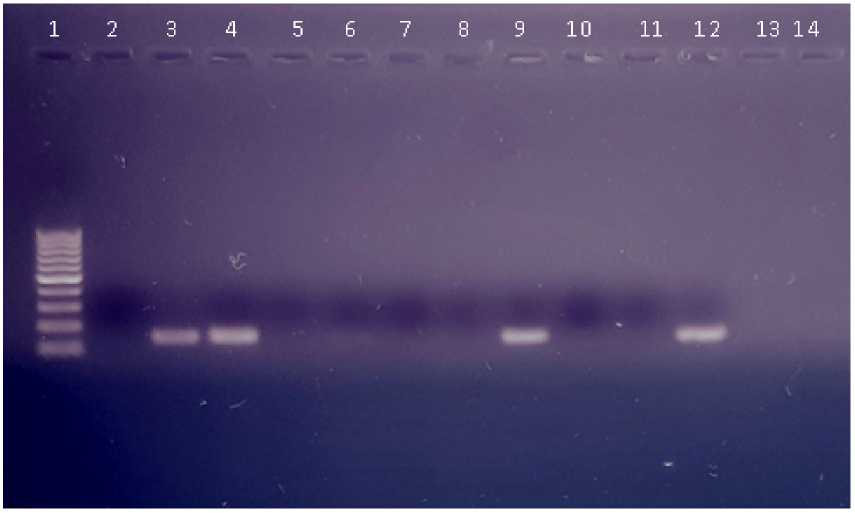
Рис. 1. Электрофореграмма ПЦР-продуктов при определении гена me c A . Дорожки: 1 – маркер молекулярной массы; 2 – от рица тельный контрол ь; 3–14 – тестируемые штаммы
Vestnik of Omsk SAU, 2022, no. 4(48)
VETERINARY AND ZOOTECHNY
Полученные результаты обработаны статистически [9]. Чтобы изучить взаимосвязь между расматриваемыми характеристиками, с помощью программы Microsoft Office Excel 2007 была определена величина коэффициента парной корреляции Пирсона анализируемых величин. Статистически значимым принимали значение коэффициента корреляции более 0,75.
Результаты исследования и обсуждение
При изучении эффективности действия антибактериальных препаратов, относящихся к разным группам по механизму действия, на стафилококки установлена абсо- лютная чувствительность данных микроорганизмов к полусинтетическим пенициллинам, коагулазоположительных штаммов (S. aureus и S. intermedius) – к аминогликозидам, S. intermedius – к цефалоспоринам и S. sciuri – к фторхинолонам и макролидам. По отношению к цефалоспоринам, фторхинолонам и аминогликозидам стафилококки разных видов характеризовались не только чувствительностью, но и умеренной рези-
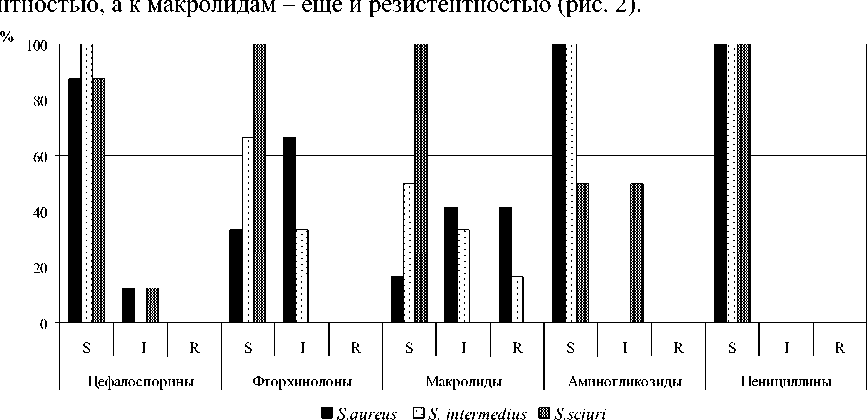
Рис. 2 . Чувствительность стафилококков к антимикробным препаратам разных групп: S – чувствительный; I – умеренно устойчивый; R – резистентный
Спектр чувствительности штаммов S. aureus к отдельным антибиотикам характеризовался следующими особенностями: все изученные культуры были чувствительны к цефазолину, цефепиму, амоксиклаву и гентамицину; умеренно резистентны к ципрофлоксацину и в 66,7 ± 13,6% случаев – к тилозину. Среди изолятов золотистых стафилококков 16,7 ± 10,8% были умеренно резистентны к цефотаксиму; процент умеренно резистентных культур к цефтриаксону и энрофлоксацину был одинаков – 33,3 ± 13,6%. Установлена выраженная резистентность штаммов S. aureus к азитромицину (83,3 ± 10,8%), умеренная резистентность к данному антибактериальному препарату определена в 16,7 ± 10,8% случаев.
Высокий процент чувствительных штаммов S. intermedius и S. sciuri отмечен к цефазолину, цефепиму, амоксиклаву – 100%. Уровень чувствительности изолятов S. intermedius к цефтриаксону, цефотаксиму, гентамицину также составлял 100%, к эн-рофлоксацину, ципрофлоксацину и тилозину – 66,7 ± 17,8%, остальные штаммы были умеренно резистентными к данным антибиотикам. Штаммы S. intermedius по отношению к азитромицину характеризовались чувствительностью, умеренной резистентностью и резистентностью (33,3 ± 17,8%). Все изоляты S. sciuri характеризовались чувст-
Vestnik of Omsk SAU, 2022, no. 4(48)
VETERINARY AND ZOOTECHNY
вительностью к энрофлоксацину, ципрофлоксацину, азитромицину и к антибиотикам, указанным выше; 50 ± 20,4% культур – к цефтриаксону и гентамицину; в 100% случаев были умерено резистентными к тилозину и цефотаксиму.
Тот факт, что имеющиеся генетические детерминанты у микроорганизмов не всегда фенотипически проявляются, дает основание изучить распространение генетических детерминант, кодирующих антибиотикоустойчивость, среди выделенных штаммов Staphylococcus sp ., и сопоставить результаты с фенотипическим профилем уроизо-лятов (рис. 3).
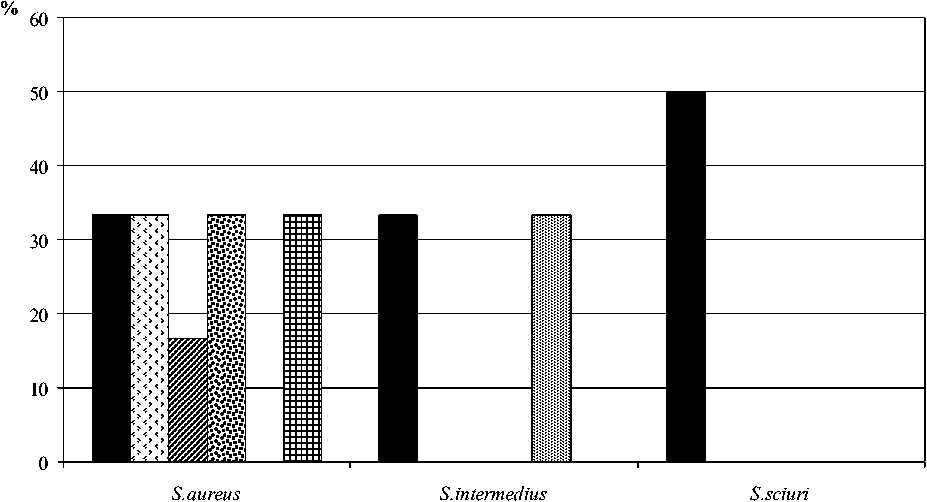
■ mecA и blaZ й aac(6')-аph (2'') и ant (4/)-Ia ЕЛ gyrA В ermC
Рис. 3. Генетическая характеристика антибиотикорезистентности выделенных стафилококков mecA – ген устойчивости к метициллину; blaZ – ген устойчивости к ампициллину;
aac(6')-аph (2'') – ген устойчивости к гентамицину; ant(4')-Ia – ген устойчивости к аминогликозидам (тобрамицину, амикацину и канамицину); gyrA , grlA – гены устойчивости к фторхинолонам;
ermA , ermC – гены устойчивости к макролидам
У всех изученных видов стафилококков регистрировали наличие гена mecA , причем у изолятов S. aureus и S. intermedius в 33,3 ± 17,8% случаев, а у штаммов S. sciuri – в 50 ± 20,4% случаев. Ген gyrA , кодирующий устойчивость к фторхинолонам, выявлен только у изолятов S. intermedius , тогда как гены blaZ , aac(6')-аph (2''), ant(4')-Ia , ermC – только у культур S. aureus . Гены аph(3')-IIIa , grlA , ermA , ermB у изученных штаммов не обнаружены.
У 2 изолятов S. aureus зафиксировано сочетание четырех генов ( mecA , blaZ , ant(4')-Ia , ermC ) и пяти генов ( mecA , blaZ , ant(4')-Ia , aac(6')-аph(2'') , ermC ).
Проведенный корреляционный анализ между исследованными признаками на уровне фено- и генотипа не выявил значимых показателей коэффициента корреляции.
Таким образом, полученные результаты показали высокую чувствительность выделенных стафилококков разных видов к ряду изученных антибиотиков: цефазолину, цефепиму, амоксиклаву. Эффективным в отношении коагулазоположительных стафи-
Vestnik of Omsk SAU, 2022, no. 4(48) VETERINARY AND ZOOTECHNY лококков оказался также гентамицин, несмотря на то, что изучение резистентности к аминогликозидам на генетическом уровне позволило обнаружить у золотистых стафилококков не только ген aac(6')-аph(2'') , но и ген ant(4')-Ia , который обуславливает устойчивость стафилококков к более широкому спектру аминогликозидных препаратов. На несоответствие между генетическими и фенотипическими паттернами устойчивости к аминогликозидам у изолятов стафилококков указывают L.X. Zhu et al. [10].
Особое значение имеет распространение стафилококков, резистентных к метициллину (или к оксациллину) [11]. Некоторые исследователи приводят данные о наличии резистентности к β-лактамным антибиотикам более чем у 50% клинических изоля-тов коагулазонегативных стафилококков [12], что может быть опосредовано экспрессией гена mecA , кодирующего пенициллинсвязывающий белок 2а (PBP2a или PBP2). Необходимо отметить, что полученные нами данные о чувствительности стафилококков, в частности S. sciuri , к амоксиклаву и ряду цефалоспоринов несколько отличались от результатов, опубликованных в некоторых зарубежных и отечественных источниках [13]. Выявленная нами абсолютная чувствительность к амоксиклаву всех изученных штаммов стафилококков, несущих гены mecA и blaZ , объясняется тем, что клаву-лановая кислота является ингибитором и обладает способностью инактивировать широкий спектр β-лактамаз, обычно обнаруживаемых у микроорганизмов, устойчивых к пенициллинам и цефалоспоринам.
Однако исследование генетических детерминант антибиотикорезистентности выявило наличие гена mecA у 33,3 ± 17,8% изолятов S. aureus и S. intermedius , а также у 50,0 ± 20,4% штаммов S. sciuri , что указывает на устойчивость бактерий ко всем β-лактамным антибиотикам (пенициллины, цефалоспорины, карбапенемы) и непредсказуемую клиническую эффективность [14].
Наряду с геном mecA , способствует приобретению и распространению устойчивости бактерий к пенициллинам ген blaZ , кодирующий β-лактамазу и зарегистрированный нами у культур S. aureus .
В настоящее время стафилококки считаются умеренно чувствительными по отношению к фторхинолонам [15]. В нашем исследовании была оценена активность эн-рофлоксацина и ципрофлоксацина и показано, что по отношению к первому проявляли умеренную резистентность 33,3 ± 17,8% S. aureus и S. intermedius , а по отношению к ципрофлоксацину – все штаммы S. aureus и 33,3 ± 17,8% изолятов S. intermedius. Полученные нами результаты и наличие гена устойчивости gyrA у изолята S. intermedius свидетельствуют о том, что фторхинолоны должны использоваться для терапии пациентов с заболеваниями мочевыделительной системы только после определения чувствительности коагулазоположительных стафилококков к антибиотикам данной группы.
Выявленную нами резистентность стафилококков разных видов к азитромицину подтверждают результаты, полученные [16; 17], которые установили продолжающуюся тенденцию повышения устойчивости к данному препарату, что говорит о необходимости контроля за его применением и постоянного мониторинга резистентности клинических штаммов.
Выводы
У выделенных стафилококков установлена резистентность к азитромицину.
Полученные данные свидетельствуют о целесообразности проведения регионального мониторинга антибиотикорезистентности.
При эмпирической терапии животных с заболеваниями мочевыделительной системы стафилококковой этиологии в качестве препаратов выбора могут использоваться цефазолин, цефепим, амоксиклав, гентамицин.
Vestnik of Omsk SAU, 2022, no. 4(48)
Список литературы Антибиотикорезистентность штаммов стафилококков, выделенных при заболеваниях мочевыделительной системы у кошек
- Белозеров Е.С., Четвериков А.В. Инфекционный компонент мочекаменной болезни // Научный медицинский вестник. 2016. № 2(4). С. 17-27.
- Kaul E. et al. Recurrence rate and long-term course of cats with feline lower urinary tract disease. Journal Feline Med. Surg. 2020;22(6):544-556. DOI 10.1177/1098612X19862887.
- Dorsch R., Teichmann-Knorrn S., Lund H.S. et al. Urinary tract infection and subclinical bacteriuria in cats: A clinical update. Journal Feline Med. Surg. 2019;21(11): 1023-1038. DOI 10.1177/1098612X19880435.
- Шкурат М.А., Покудина И.О., Батталов Д.В. Резистентность микроорганизмов к антимикробным препаратам // Живые и биокосные системы. 2014. № 10. URL: http://jbks.ru/archive/issue10/ article-1.
- Морозова Н.В., Сычева М.В., Сорокин В.И. Биопрофиль микроорганизмов, выделенных из мочи кошек при патологии мочевыделительной системы // Вестник Ульяновской государственной сельскохозяйственной академии. 2020. № 3(51). С. 142147. DOI 10.18286/1816-4501-2020-3-142-147.
- Определение чувствительности микроорганизмов к антибактериальным препаратам : методические указания. М. : Федеральный центр Госсанэпиднадзора Минздрава России, 2004. 91 с.
- Gostev V. et al. Molecular epidemiology and antibiotic resistance of methicillin-resistant Staphylococcus aureus circulating in the Russian Federation. Infection, Genetics and Evolution. 2017;53:189-194. DOI 10.1016/j.meegid.2017.06.006.
- Bahraminia F. et al. A high prevalence of ty-losin resistance among Staphylococcus aureus strains isolated from bovine mastitis. Veterinary Research Forum. 2017;8(2):121-125.
- Ашмарин И.П., Воробьев А.А. Статистические методы в микробиологических исследованиях. Л. : Гос. изд-во мед. лит., 1962. 180 с.
- Zhu L.X. et al. Use of a DNA microarray for simultaneous detection of antibiotic resistance genes among staphylococcal clinical isolates. Journal Clin. Microbiol. 2007;45:3514-3521. DOI 10.1128/ JCM.02340-06.
- Шаркова В.А., Лайман Е.Ф., Мазур М.Е. Генетически обусловленная патогенность и анти-биотикорезистентность штаммов Staphylococcus spp. // Тихоокеанский медицинский журнал. 2014. № 3. С. 46-49.
- Chon J.-W. et al. Virulence Characteristics of mecA-Positive Multidrug-Resistant Clinical Coagu-lase-Negative Staphylococci. Microorganisms. 2020; 8(5):659. DOI 10.3390/microorganisms8050659/.
- Becker K., Heilmann C., Peters G. Coagu-lase-negative staphylococci. Clin Microbiol Rev. 2014;27(4):870-926. DOI 10.1128/CMR.00109-13.
- Карпов И.А., Качанко У.Ф. Внебольнич-ные инфекции, обусловленные метициллинрезистентным стафилококком: подходы к антибактериальной терапии // Медицинские новости. 2006. № 10. С. 28-32.
- Яковлев В.П. Антимикробные препараты группы фторхинолонов // Consilium Medicum. 2012. Т. 14. № 4. С. 8-14. URL: https://consihum.orscien-ce.ru/2075-1753/article/view/93558.
- Хараева З.Ф. и др. Антибиотикочувстви-тельность и антилизоцимная активность штаммов Staphylococcus aureus выделенных из крови больных сепсисом // Антибиотики и химиотерапия. 2020. Т. 65. № 11-12. С. 11-15. DOI 10.37489/02352990-2020-65-11-12-11-15.
- Алиева К.Н. и др. Комбинированная терапия как путь к предотвращению антибиотикоре-зистентности бактерий: линезолид-даптомицин против Staphylococcus aureus // Антибиотики и химиотерапия. 2019. Т. 64. № 9-10. С. 8-13. DOI 10.24411/0235-2990-2019-10050.


