Антимикробная активность перевязочного материала, импрегнированного коллоидным серебром
Автор: Серова А.Н., Пехенько В.Г., Тихонова И.Н., Глазкова Е.А., Бакина О.В., Лернер М.И., Псахье С.Г.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 3 т.27, 2012 года.
Бесплатный доступ
Представлены результаты изучения антимикробной активности перевязочного материала на основе полимерной матрицы с иммобилизованными частицами оксигидроксида алюминия, импрегнированного коллоидным серебром. Установлено, что разработанный материал обладает антимикробной активностью в отношении ряда микроорганизмов - E. coli 7935, S. aureus 209, P. aeruginosa 27583 и т.д. Показано, что при многократных пассажах E. coli 7935 с перевязочным материалом не наблюдается изменения свойств микроорганизмов и образования резистентных штаммов.
Перевязочный материал, оксигидроксид алюминия, коллоидное серебро, антимикробная ак# тивность, резистентные штаммы
Короткий адрес: https://sciup.org/14919760
IDR: 14919760 | УДК: 579;
Antimicrobial activity of the dressing material impregnated with colloidal silver
The paper presents the results of the study of microbiological dressing material manufactured based on aluminum oxyhydroxide-containing polymer matrix impregnated with colloidal silver. Our data showed that this material had antimicrobial activity against a number of microorganisms including E. coli 7935, S. aureus 209, P. aeruginosa 27583 and others. Multiple passages of E. coli 7935 with the dressing material did not change the properties of the microorganisms and did not cause the development of resistant strains.
Текст научной статьи Антимикробная активность перевязочного материала, импрегнированного коллоидным серебром
Широкое применение лекарственных препаратов и снижение иммунологического статуса организма привело к тому, что ведущую роль при инфекционно-воспалительных заболеваниях стали играть лекарственно-устойчивые формы патогенных и условно-патогенных микроорганизмов [8]. В связи с этим возникла необходимость создания и внедрения в медицинскую практику антимикробных материалов и изделий из них, не содержащих антибиотики. Сущность этого направления состоит в создании материалов, содержащих антимикробные компоненты пролонгированного действия [10]. Кроме того, получили распространение повязки для ран, импрегни-рованные антимикробными компонентами, такими как серебро, йод, оксид меди и др. [1, 13]. Действие указанных материалов основано на выделении бактерицидных компонентов в рану, что может приводить к патологическим изменениям в тканях.
Более перспективными представляются материалы, действие которых основано на сорбции микроорганизмов из раны и последующей их инактивации в объеме повязки. Одним из таких материалов является сорбционный материал, представляющий собой микроволокни-стую полимерную матрицу с иммобилизованными частицами оксигидроксида алюминия [6]. Перевязочный материал за счет действия оксигидроксида алюминия эффективно сорбирует и удерживает микроорганизмы. Однако частицы оксигидроксида алюминия не оказывают бактерицидного действия, что может привести к размножению микроорганизмов в объеме материала повязки и опасности повторного заражения.
Цель работы: исследование in vitro влияния коллоидного серебра, адсорбированного на частицах оксигидроксида алюминия, на жизнеспособность микроорганизмов в объеме перевязочного материала и изучение возможности возникновения резистентности микроорганизмов к антимикробному агенту, входящему в состав перевязочного материала.
Материал и методы
В качестве объектов исследования использовали образцы перевязочного материала (ПМ) с иммобилизованными частицами оксигидроксида алюминия, импрегни-рованного коллоидным серебром, и образцы ПМ без серебра [3].
Количественную оценку антимикробной активности образцов ПМ с различным содержанием коллоидного серебра проводили на культуре E. coli 7935 in vitro тест-методом AATCC 100–2004 [11]. Содержание оксигидроксида алюминия на всех образцах ПМ составляло 34%. Содержание коллоидного серебра варьировало в пределах от 0,38 до 3,65 мкг/см2. На образцы ПМ диаметром 47 мм наносили 1 мл культуры микроорганизма E. coli 7935 концентрацией 1,0х105 КОЕ/мл до полного поглощения суспензии. Образцы инкубировали при температуре (37±1) °C в течение 24 ч. Затем бактерии с перевязочного материала элюировали встряхиванием во флаконах со 100 мл физиологического раствора (с pH, равным 7,2) и высевали 1 мл суспензии на питательный агар (Эндо ГРМ) в чашки Петри. Посевы инкубировали при температуре (37±1) °C в течение суток, подсчитывали число выросших колоний и рассчитывали процент убыли микроорганизмов в контаминированном образце. В качестве контроля использовали взвесь микроорганизмов в физиологическом растворе.
Для определения антибактериального спектра ПМ использовали штаммы бактерий S. aureus 209, P. vulgaris 4175, E. coli 7935, K. pneumoniae 2482 , P. aeruginosa 27583, С. albicans Y-3108, представляющие споровые и вегетативные, грамположительные и грамотрицательные, кокковые и палочковидные, капсульные и бескапсульные формы микроорганизмов. Для проведения исследования за основу брали метод А.А. Ворошиловой и Е.В. Диановой [4].
Из указанных штаммов бактерий готовили по 5 мл суспензий суточных агаровых культур бактерий в стерильном физиологическом растворе в концентрации 2,0х103 КОЕ/мл (6 опытных пробирок для каждого микроорганизма). В каждую опытную пробирку помещали образец исследуемого стерильного ПМ размером 20х20 мм. В качестве контроля использовали стерильную марлю соответствующего размера и взвесь бактерий в физиологическом растворе. Опытные и контрольные образцы помещали в термостат при температуре (37±1) °C. Через 24 и 48 ч из всех пробирок производили посев 0,1 мл бактериальной взвеси на питательную среду в чашках Петри.
Исследования антимикробного действия ПМ на культурах микроорганизмов E. coli 7935 и S. aureus 209 проводили, взяв за основу метод Кирби–Бауэра [12]. Образцы ПМ диаметром 47 мм помещали на газон растущего соответствующего микроорганизма в чашках Петри и инкубировали в термостате при температуре (37±1) °C. Для получения роста бактерий в виде газона использовали бактериальные суспензии с концентрацией 1,0х107 КОЕ/мл. Через 24 ч инкубации образцы удаляли с поверхности газона, а выросшие под образцами бактерии отбирали с помощью тампонов и засевали на мясопептонный агар (МПА).
Для изучения возможного возникновения резистентности культуры E. coli 7935 при многократном контакте с ПМ [7] использовали образцы с коллоидным серебром и без коллоидного серебра размером 20х20 мм. Стерильные образцы ПМ помещали в пробирки c 5 мл мясопептонного бульона (МПБ), в который инокулировали культуру E. coli 7935 в конечной концентрации 1,0х103 КОЕ/ мл и инкубировали при температуре (37±1) °C. Через сутки пробирки тщательно встряхивали, высевали по 1 мл бульона на питательную среду МПА и инкубировали в те- чение суток при температуре (37±1) °C. На следующий день учитывали количество выросших колоний, готовили из них суспензию с концентрацией бактерий 1,0х103 КОЕ/мл и помещали в приготовленную суспензию новый образец ПМ. Таким образом, проводили 10 последовательных пассажей штамма E. coli 7935 в присутствии образцов ПМ. Далее проводили изучение пассированной культуры кишечной палочки по морфологическим, культуральным и биохимическим свойствам и сравнивали с исходной (до пассажа) культурой E. coli 7935 [7, 9, 14]. В качестве контроля использовали взвесь бактерий без образцов ПМ.
Статистическую обработку результатов осуществляли с применением пакета статистических программ STATISTICA for Windows (версия 5.0) с предварительной оценкой нормальности распределения и использованием t-критерия Стьюдента. Результаты представлены в виде среднего значения (M) и ошибки среднего (m). Для всех видов анализа статистически значимыми считали значения p менее 0,05.
Результаты и обсуждение
Результаты исследования антимикробной активности ПМ (рис. 1) показали, что снижение концентрации бактерий E. coli 7935 зависит от времени контакта образцов ПМ с бактериальной суспензией и содержания коллоидного серебра. При контакте образца ПМ 1 (без серебра) с бактериальной суспензией не наблюдалось изменения концентрации микроорганизмов во всем временном интервале. При содержании коллоидного серебра 0,38 мкг/см2(образец ПМ 2) заметное сокращение количества жизнеспособных микроорганизмов отмечено после 2 ч контакта ПМ с бактериальной суспензией, но полной потери жизнеспособности бактерий не удавалось достичь даже после 24 ч контакта. При увеличении концентрации коллоидного серебра и времени контакта количество жизнеспособных микроорганизмов снижалось, причем полная потеря жизнеспособности микроорганизмов наблюдалась на образцах ПМ, содержащих 0,70 (образец ПМ 3)и 3,65 мкг/см2 серебра (образец ПМ 4) через 24 ч контакта.
Проведенные исследования показали, что в смыве образца ПМ 1 обнаруживаются бактерии в концентрации 1,0х104КОЕ/мл, что свидетельствовало об отсутствии антимикробного действия ПМ без коллоидного серебра. В смыве с образца ПМ 2 присутствовали единичные живые микробные клетки E. coli 7935, что, возможно, обусловлено недостаточной дозой коллоидного серебра для обеспечения полного бактерицидного эффекта. В смыве с образцов ПМ 3 и ПМ 4 жизнеспособных микрооганиз-мов не обнаружено, что могло быть связано с антимикробным действием коллоидного серебра.
Таким образом, минимальное количество коллоидно-
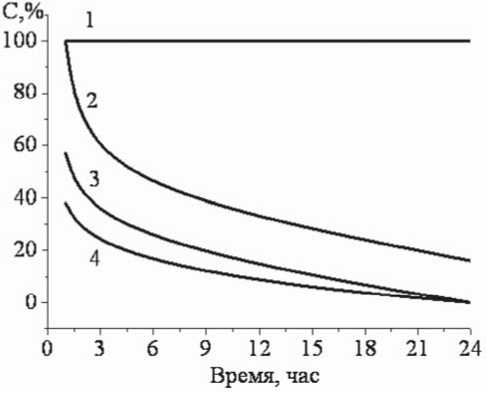
Рис. 1. Антимикробные свойства перевязочного материала в зависимости от содержания коллоидного серебра: 1 – без серебра; 2 – 0,38 мкг/см2; 3 – 0,70 мкг/см2, 4 – 3,65 мкг/см2
Таблица 1
Антимикробный спектр перевязочного материала (образец ПМ 4)
достижения полного бактерицидного эффекта в объеме Эффективность антимикробного действия ПМ с кол-
а) б)

в)

г)
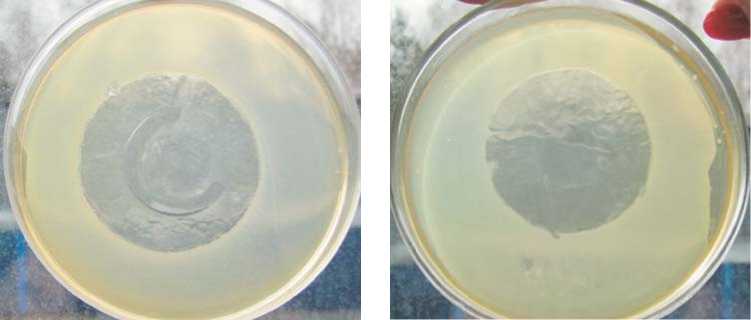
Рис. 2. Состояние газона E. coli 7935 (а, б) и S. aureus 209 (в, г) после удаления диска ПМ: без серебра (а, в), с коллоидным серебром (б, г)
лоидным серебром (табл. 1) зависела от вида микроорганизмов, времени контакта и строения клеточной стенки микроорганизма и снижалось в ряду: Р.vulgaris 4175 – S.aureus 209 – E. coli 7935 – K. pneumoniae 2482 – P. aeruginosa 27583 – C. albicans Y-3108. Наиболее устойчивой к действию коллоидного серебра оказалась культура C. albicans Y-3108, что, вероятно, обусловлено строением клеточной стенки и наличием спор (бластоспор, хламидиоспор).
Изучение антимикробного действия ПМ (концентрация коллоидного серебра – 3,65 мкг/см2) показало, что через сутки на поверхности мясопептонного агара под образцами с серебром концентрация микроорганизмов уменьшилась на три порядка и составила 104КОЕ/ мл, тогда как под образцами без серебра – на два порядка, составив 105 КОЕ/ мл (рис. 2).
Следует отметить, действие материала распространялось только на об-
Таблица 2
Резистентность культуры E.coli 7935 к действию антимикробного агента перевязочного материала
|
Свойства |
E. coli 7935 и ПМ без коллоидного серебра |
E. coli 7935 и ПМ с коллоидным серебром |
E. coli 7935 (исходная культура) |
|
Культуральные Морфологические Биохимические Заключение |
На среде Эндо красные колонии с металлическим блеском, на среде Левина – темнофиолетовые колонии Грамотрицательные палочки, не образуют спор Цитохромоксидаза “–” каталаза “+” уреаза “–” индолообразование “+” образование сероводорода “–” утилизация цитрата Симмонса “–” подвижность “+” ферментация глюкозы и лактозы до кислоты и газа Все свойства соответствуют культуре E. coli 7935 (исходная культура) |
На среде Эндо красные колонии с металлическим блеском, на среде Левина – темнофиолетовые колонии Грамотрицательные палочки, не образуют спор Цитохромоксидаза “–” каталаза “+” уреаза “–” индолообразование “+” образование сероводорода “–” утилизация цитрата Симмонса “–” подвижность “+” ферментация глюкозы и лактозы до кислоты и газа Все свойства соответствуют культуре E. coli 7935 (исходная культура) |
На среде Эндо красные колонии с металлическим блеском, на среде Левина – темнофиолетовые колонии Грамотрицательные палочки, не образуют спор Цитохромоксидаза “–” каталаза “+” уреаза “–” индолообразование “+” образование сероводорода “–” утилизация цитрата Симмонса “–” подвижность “+” ферментация глюкозы и лактозы до кислоты и газа E. coli |
Примечание: “+” – наличие признака, “–” – отсутствие признака.
ласть под образцом, о чем свидетельствовало отсутствие зоны лизиса вокруг дисков ПМ. Следовательно, из образцов ПМ не происходило диффузии антимикробного компонента в агар с тестируемыми микроорганизмами, а действие ПМ обусловлено поглощением и сорбцией микроорганизмов, а также антибактериальным действием коллоидного серебра в объеме ПМ.
Многочисленные исследования подтверждают [2, 5], что микроорганизмы, в силу ряда причин, могут стать резистентными к различным химическим веществам, антибиотикам и т.д., а также изменять свои морфологические, культуральные и биохимические свойства. Полученные результаты (табл. 2) свидетельствуют о том, что все исследуемые показатели многократно пассированной культуры не изменились по сравнению с исходной контрольной культурой бактерий E. coli 7935.
Таким образом, многократное воздействие ПМ с адсорбированным коллоидным серебром в концентрации 3,65 мкг/см2 на суспензию бактерий E. coli 7935 не приводило к изменению свойств тестируемого микроорганизма.
Выводы
-
1. Перевязочный материал на основе микроволокнис-той полимерной матрицы с иммобилизованными частицами оксигидроксида алюминия, импрегнирован-ный коллоидным серебром, обладает антибактериальной активностью и сорбционной способностью. Перевязочный материал без серебра обладает только сорбционной активностью, а адсорбированные микроорганизмы сохраняют жизнеспособность. Коллоидное серебро в концентрации выше 0,70 мкг/см2 придает перевязочному материалу бактерицидные свойства.
-
2. Перевязочный материал, содержащий коллоидное серебро в концентрации 3,65 мкг/см2, обладает широким спектром антимикробной активности, которая зависит от вида микроорганизма и времени его контакта с перевязочным материалом.
-
3. При многократном воздействии антимикробного агента, входящего в структуру перевязочного материала, на микробные клетки E. coli 7935 не происходит изменений их морфологических, культуральных и биохимических свойств, что является одним из показателей безвредности перевязочного материала.
Работа выполнена при финансовой поддержке ГК 14.527.12.0001 и Программы V.37.3.
Список литературы Антимикробная активность перевязочного материала, импрегнированного коллоидным серебром
- Абаев Ю.К. Хирургическая повязка. -Минск: Беларусь, 2005. -150 с.
- Бриан Л.Е. Бактериальная резистентность и чувствительность к химиопрепаратам/пер. с англ. -М.: Медицина, 1984. -272 с.
- Бакина О.В., Глазкова Е.А., Ложкомоев А.С. и др. Модифицирование наноструктурного оксигидроксида алюминия частицами коллоидного серебра//Перспективные материалы. -2011. -№ 6. -С. 47-52.
- Ворошилова А.А., Дианова Е.В. Окисляющие нефть бактерии -показатели интенсивности биологического окисления нефти в природных условиях//Микробиология. -1952. -Т. 21, вып. 4. -С. 408-415.
- Ланчини Д., Паренти Ф. Антибиотики/пер. с англ. -М.: Медицина, 1985. -272 с.
- Лернер М.И., Бакина О.В., Глазкова Е.А. и др. Высокопроизводительный фильтр для очистки воды от коллоидных и микробиологических загрязнений//Экология и промышленность. -2010, сент. -С. 4-7.
- Пяткин К.Д., Кривошеин Ю.С. Микробиология с вирусологией и иммунологией: учебник для мед. ин-тов. -4-е изд., перераб. и доп. -М.: Медицина, 1980. -512 с.
- Руденко А.В., Багдасарова И.В., Брудько А.П. Сорбционное действие Энтеросгеля в отношении различных видов микроорганизмов//Провизор. -2005. -№ 10. -С. 42-43.
- Методы лабораторных исследований и испытаний дезин# фекционных средств для оценки их эффективности и безопасности [Электронный ресурс]: руководство Р 4.2.2643 10//ФМБА России. -2010. -URL: http://ru58.fmbaros.ru/2502/3313/item/2567 (дата обращения 19.04.2012).
- Стрилец О.П., Дикий И.Л., Стрельников Л.С. и др. Изучение антимикробных свойств новой лекарственной формы в виде антисептического перевязочного средства на основе декаметоксина и этакридина лактата//Провизор. -1999. -№ 7. -С. 46-47.
- Antibacterial finishes on textile materials: assessment of developed from American Association of Textile Chemists and Colorists//AATCC Technical Manual. -2006. -P. 149-151.
- Bauer A.W., Kirby W.M.M., Sherris J.C. et al. Antibiotic susceptibility testing by a standartized single disk method//Am. J. Clin. Pathol. -1966. -Vol. 36. -P. 493-496.
- Borkow G., Okon#Levy N., Gabbay J. Copper. Oxide impregnated wound dressing: biocidal and safety studies//Wounds. -2010. -Vol. 22 (12). -P. 301-310.
- Jorgensen J.H., Turnidge J.D. Susceptibility test methods: dilution and disk diffusion methods//Manual of Clinical Microbiology. -9th ed. -Washington: ASM Press, 2007. -P. 1152-1172.


