Антитела к ацетилхолиновому рецептору в оценке эффективности тимэктомии у больных с генерализованной миастенией
Автор: Шевченко Ю.Л., Ветшев П.С., Санадзе А.Г., Аблицов А.Ю., Сиднев Д.В., Дедаев С.И., Магомедов Ба
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.6, 2011 года.
Бесплатный доступ
Впервые в России проведено изучение концентрации антител к АХА у больных генерализованой миастенией, исследована возможность прогнозирования эффекта тимэктомии у этой категории пациентов.
Тимэктомия, антитела, миастения
Короткий адрес: https://sciup.org/140188000
IDR: 140188000 | УДК: 616.438-089.87-097:616.74-009.17
Antibodies to acetylcholine receptors in assessing the effectiveness of thymectomy in patients with generalized myasthenia
For the first time in Russia have been studied the concentration of antibodies to ACHR in patients with generalized myasthenia and investigated the possibility of predicting the effect of thymectomy in these patients.
Текст научной статьи Антитела к ацетилхолиновому рецептору в оценке эффективности тимэктомии у больных с генерализованной миастенией
Известно, что антитела к ацетилхолиновым рецепторам (АХР) постсинаптической мембраны нервно-мышечного соединения выявляются примерно у 80–85% больных с миастенией [3, 5, 10, 18]. Увеличение концентрации антител к АХР, наряду с клиническими проявлениями болезни, электромиографическими феноменами, отражающими нарушения нервно-мышечной передачи, а также положительной реакцией на введение антихолинэстеразных препаратов, являются классическими критериями диагностики аутоиммунной миастении [3, 5, 10, 18]. Вместе с тем, большинство авторов подчеркивает отсутствие корреляции между титром антител к АХР и тяжестью клинических проявлений миастении [3, 5, 10, 12, 18, 19].
Концентрация антител к АХР, как правило, уменьшается на фоне патогенетического лечения, включающего терапию глюкокортикоидными и иммуносупрессорными препаратами, а также после проведения тимэктомии и плазмафереза [4, 7, 8, 9, 12, 17]. Однако и эти данные далеко не однозначны, поскольку улучшение состояния пациента с миастенией может наступить как на фоне неизменного уровня антител, так, даже, на фоне их увеличения [12, 18] и, наоборот, ухудшение состояния может сопровождаться некоторым снижением уровня антител к АХР [13, 19]. Весьма вероятно, что объяснением этому может являться различный временной интервал, в который проводилась оценка клинических и иммунологических изменений после проведенного патогенетического лечения.
В этой связи целью настоящей работы явилось сопоставление изменения концентрации антител к АХР и тяжести клинических проявлений болезни в группах оперированных и неоперированных больных с генерализованной миастенией, на фоне достижения клини- ческого эффекта глюкокортикоидной терапии и через 8–12 месяцев после тимэктомии, с предшествующей предоперационной подготовкой глюкокортикоидными препаратами.
Материал и методы исследования
Обследовано 60 пациентов с миастенией: 15 мужчин и 45 женщин в возрасте от 13 до 56 (средний возраст – 37,1±16,1) лет.
Тимэктомия (тимомтимэктомия) была выполнена у 23 больных: 7 мужчин и 16 женщин в возрасте от 13 до 52 (средний возраст – 27,1±11,1) лет. У 6 больных (5 мужчин и 1 женщина) была выявлена и удалена тимома, а у оставшихся 17 пациентов (2 мужчин и 15 женщин) – удалена гиперплазированная вилочковая железа. Большинство оперативных вмешательств выполнено с применением видеоторакоскопической или эндовидеохирургической робот-ассистированной (Da Vinchi) технологии. Хирургическое лечение было проведено на фоне предварительной предоперационной подготовки больных приемом глюкокортикоидных препаратов.
В качестве контроля обследовано 37 больных: 8 мужчин и 29 женщин в возрасте от 16 до 56 (средний возраст – 36,8±16,9) лет, которым проводилась только глюкокортикоидная терапия (прием внутрь преднизолона или метилпреднизолона по схеме через день).
Диагноз миастении основывался на результатах клинического и иммунологического исследований, а также был подтвержден данными фармакологического теста с подкожным введением раствора прозерина и электро-миографического исследования состояния нервно-мышечной передачи.

Диагноз «тимома» основывался на результатах проведенной МСКТ переднего средостения (при необходимости в сочетании с МРТ) и был верифицирован при оперативном ее удалении.
Тяжесть клинических проявлений миастении оценивалась по Международной клинической классификации MGFA (Barohn R.J., 1996; Jarezki A. et al., 2000):
I – изолированная слабость окулярных мышц любой выраженности;
-
II – легкая слабость других (кроме окулярных или в том числе и окулярных) мышц;
IIa – преобладание легкой слабости мышц туловища, либо проксимальных отделов конечностей, либо того и другого. Также может быть умеренное вовлечение в процесс кранио-бульбарных мышц;
IIb – преобладание слабости кранио-бульбарных и/или дыхательных мышц. Возможно умеренное вовлечение мышц туловища, либо проксимальных отделов конечностей, либо и того и другого;
-
III – средняя слабость других (кроме окулярных) мышц. Также может быть слабость окулярных мышц любой степени тяжести;
IIIa – преобладание средней степени слабости мышц туловища, либо проксимальных отделов конечностей, либо того и другого. Также может быть умеренное вовлечение в процесс кранио-бульбарных мышц.
IIIb – преобладание средней слабости кранио-бульбарных и/или дыхательных мышц. Возможно умеренное вовлечение мышц туловища, либо проксимальных отделов конечностей, либо и того и другого;
-
IV – выраженная слабость других (кроме окулярных) мышц. Также может быть слабость окулярных мышц любой степени тяжести;
IVa – преобладание тяжелой степени слабости мышц туловища, либо проксимальных отделов конечностей, либо того и другого. Также может быть умеренное вовлечение в процесс кранио-бульбарных мышц;
IVb – преобладание тяжелой слабости кранио-бульбарных и/или дыхательных мышц. Возможно умеренное вовлечение мышц туловища, либо проксимальных отделов конечностей, либо и того и другого;
-
V – кризисные состояния (интубация с или без механической вентиляции, использование зондового питания без интубации у пациентов группы IVb).
Концентрацию антител к АХР определяли радио-иммунологическим методом с помощью коммерческой тест-системы (DLD Diagnostika GMBH, Германия). Образцы сыворотки хранили при -20° С. Перед анализом их размораживали, отбирали аликвоты по 5 мкл и помещали в пробирки. К пробам добавляли по 100 мкл 125 I-рецептора ацетилхолина (удельная активность- 342 Ci/ммоль), 50 мкл антител к IgG человека, перемешива- ли и инкубировали в течение 30 мин. при комнатной температуре. Затем добавляли по 1 мл промывочного буфера, центрифугировали при 3000 g в течение 20 мин., надосадочную жидкость удаляли декантацией. Полученный осадок ресуспензировали и повторяли процедуру промывки. Определяли радиоактивность проб и вычисляли концентрацию антител, выражаемую в Нмоль/л по формуле с использованием фактора, учитывающего дату изготовления набора и удельную активность метки, радиоактивность пробы, а также радиоактивность негативного контроля. Повышенным титром антител к АХР являлось значение, превышающее 0,50 Нмоль/л.
Результаты
Распределение всех обследованных больных согласно классификации MGFA до начала лечения представлены в табл. 1.
Как видно из представленных данных, в контрольной группе преобладали пациенты с изначально средней тяжестью (3А, 3В) и тяжелой формой (4А, 4В) миастении – 54% и 29,7% соответственно. Тогда как в группе пациентов, подвергшихся оперативному вмешательству основная масса больных (78,3%) имела исходно среднюю степень тяжести заболевания (3А или 3В) и только один пациент имел тяжелые проявления болезни 4В. Такое несоответствие соотношения больных с тяжелой миастенией в исследуемых группах было связано с наличием определенного риска проведения оперативного вмешательства при выраженных проявлениях заболевания, что делало необходимым предварительное назначение глюкокортикоидных препаратов с целью компенсации состояния тяжелых пациентов перед операцией.
Больные с легкой генерализованной формой в этих группах составили 17,4% и 16,3% соответственно. Изменения тяжести клинических проявлений миастении после проведенного лечения в группах у оперированных и не оперированных пациентов представлены на рис. 1 и 2.
Полученные данные показали, что после проведения оперативного вмешательства (тимэктомия, тимомтимэкто-мия), отчетливое клиническое улучшение наблюдалось у 21
Табл. 1. Тяжесть клинических проявлений миастении до начала лечения
|
Тяжесть клинических проявлений миастении (согласно MGFA) |
Число больных до оперативного вмешательства на тимусе, абс. (%) |
Число больных до терапии стероидами, абс. (%) |
|
2 |
4 (17,4) |
6 (16,3) |
|
2А |
0 |
1 |
|
2В |
4 |
5 |
|
3 |
18 (78,3) |
20 (54) |
|
3А |
6 |
3 |
|
3В |
12 |
17 |
|
4 |
1 (4,3) |
11 (29,7) |
|
4А |
0 |
4 |
|
4В |
1 |
7 |
|
ИТОГО |
23 (100) |
37 (100) |
Распределение пациентов до и после оперативного вмешательства на вилочковой железе
■ до лечения I ■ после лечения
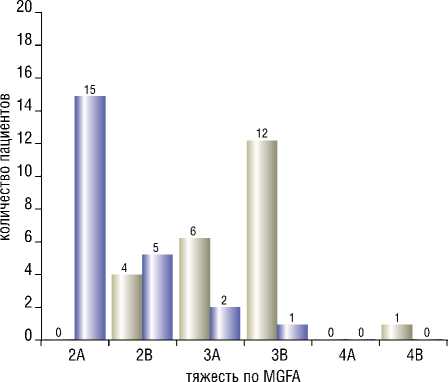
Рис. 1. Изменение тяжести клинических проявлений миастении у тимэк-томированных пациентов после проведения тимэктомии (тимом-тимэктомии)
Обозначения: ось абсцисс – степень выраженности клинических проявлений миастении (согласно MGFA), ось ординат – количество пациентов.
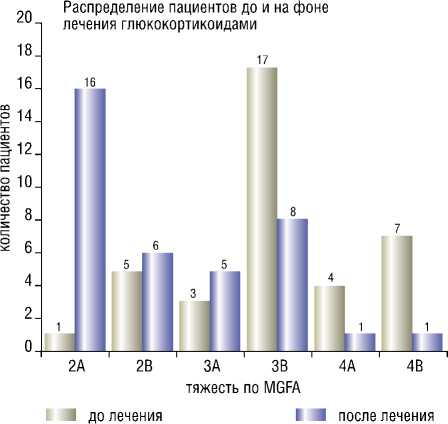
Рис. 2. Изменение тяжести клинических проявлений миастении у нетимэк-томированных пациентов (на фоне терапии глюкокортикоидными препаратами)
Обозначения : ось абсцисс – степень выраженности клинических проявлений миастении (согласно MGFA), ось ординат – количество пациентов.
из 23 (91,3%) пациентов, а у 2 (8,7%) пациентов существенных изменений в течении заболевания отмечено не было.
Из полученных данных видно, что при миастении лечение только глюкокортикоидными препаратами привело к перераспределению больных по степени тяжести в сторону уменьшения их количества в группах, соответ- ствующих средней (3В) и тяжелой (4А; 4В) степени выраженности миастении и увеличения их числа в группах с более легкими проявлениями заболевания. Отчетливое клиническое улучшение на фоне терапии наблюдалось у 26 из 37 (70,3%) пациентов. У 10 (27%) пациентов каких-либо существенных изменений отмечено не было. Состояние 1 пациента ухудшилось, что выражалось в переходе из группы 3В в 4В.
Таким образом, в обеих группах больных с миастенией в большинстве случаев наблюдалось уменьшение тяжести клинических проявлений заболевания, однако в группе прооперированных больных это улучшение более выражено.
Совокупность полученных результатов свидетельствует о том, что комбинация хирургического удаления тимуса в сочетании с предварительным лечением глюкокортикоидами в целях предоперационной компенсации состояния пациента по эффективности превосходит монотерапию глюкокортикоидными препаратами.
Изучение изменения концентрации антител к АХР после проведения тимэктомии (тимомтимэктомии) показало, что у 21 из 23 (91,3%) пациентов оперативное вмешательство привело к снижению титра антител к АХР в среднем на 36,4%±22,8%, с колебаниями от 2,4% до 99,4%.
У 2 (8.7%) больных – титр антител увеличился на 13,0%±0,5% с колебаниями от 12,8% до 13,2%.
Изучение динамики уровня антител к АХР в сыворотке крови больных с миастенией, не подвергшихся тимэктомии показало, что у 25 из 37 (67,6%) пациентов отмечалось снижение концентрации антител к АХР в среднем на 37,1%±23,3%, с колебаниями от 2,4% до 78,6%.
У 12 (32,4%) больных – уровень антител увеличился на 21,7%±19,0% с колебаниями от 1,3% до 55,1%.
Сопоставив изменения клинического параметра в виде динамики выраженности заболевания и иммунологического параметра, выражавшегося в виде флюктуации уровня антител к АХР на фоне проведенного лечения, мы условно выделили ряд возможных клинико-иммунологических вариантов исхода:
-
1) Улучшение состояния, сопровождавшееся снижением уровня антител к АХР.
-
2) Улучшение состояния, без изменений или с увеличением уровня антител к АХР.
-
3) Отсутствие отчетливой положительной клинической динамики, сопровождавшееся снижением уровня антител к АХР.
-
4) Отсутствие отчетливой положительной клинической динамики, в сочетании с отсутствием изменений или повышением уровня антител к АХР.
Полученные результаты свидетельствуют о том, что боле чем в 2/3 наблюдений (70%) уменьшение тяжести клинических проявлений болезни на фоне патогенетического лечения сопровождалось снижением концентрации антител к АХР.

Варианты сочетания изменения клинической картины и динамики уровня антител к АХР
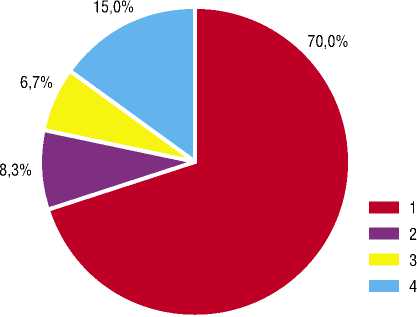
Рис. 3. Сопоставление изменения тяжести клинических проявлений миастении с динамикой концентрации антител к АХР у всех обследованных больных с миастенией на фоне патогенетического лечения
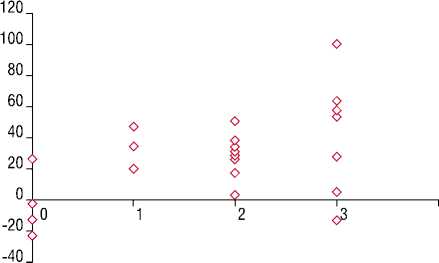
Рис. 4. Степень изменения тяжести клинических проявлений миастении и динамика титра антител к АХР у тимэктомированных больных
По оси ординат – динамика уровня антител к ацетилхолиновым рецепторам (в %).
По оси абцисс – изменение тяжести клинических проявлений миастении: 1- на одну единицу степени тяжести (например, из 4в в 4а); 2- на две единицы степени тяжести (4в-3в); 3- на три единицы степени тяжести (4в-3а); 4- на четыре единицы степени тяжести (4в-2в); 5- на пять единиц степени тяжести (4в-2а).
-
1 – улучшение состояния пациентов сочетающееся со снижением концентрации АТ к АХР.
-
2 – улучшение состояния без изменения или с увеличением концентрации АТ к АХР.
-
3 – без клинических изменений со снижением концентрации АТ.
-
4 – без клинических изменений и без изменений или с увеличением концентрации АТ к АХР.
В 8,3% наблюдений, несмотря на улучшение состояния больных, уровень антител к АХР не изменялся, или даже увеличился.
В 6,7% – у больных выявлялось снижение концентрации антител к АХР без изменения тяжести клинических проявлений миастении;
У 15% обследованных пациентов отсутствие положительной динамики состояния сочеталось с увеличением или с прежней концентрацией антител к АХР.
Проведенное исследование позволило выделить резистентную группу больных, у которых, несмотря на проведенное лечение, наблюдалось отсутствие клинического эффекта, сочетающееся с увеличением концентрации антител к АХР. Эта группа включала в себя двух мужчин и 7 женщин в возрасте от 17 до 42 (28,3±12,6) лет. Тимома была выявлена у двух больных. Проведенный клинический анализ показал, что среди 9 больных, составляющих эту группу, у трех отмечалась тяжелая форма болезни (IV степень), у 5 – средняя степень тяжести (III), и лишь у одного клинические проявления миастении оценивались как легкие (II). Бульбарные нарушения выявлены у 6 пациентов.
Корреляционный анализ изменения тяжести клинических проявлений миастении и динамики концентрации антител к АХР у больных перенесших и не и перенесших тимэктомию (тимомтимэктомию), представлен на рис. 4 и 5.
Как следует из полученных данных, как в группе оперированных больных миастенией, так и в группе
100,00
80,00 _
60,00 _
40,00 _
20,00 _
0.00
-40,00 А
-60,00 _
-80,00 .
О
4 5 6
О
Рис. 5. Степень изменения тяжести клинических проявлений миастении и динамика титра антител к АХР у не оперированных больных
По оси ординат – динамика уровня антител к ацетилхолиновым рецепторам (в %).
По оси абцисс – изменение тяжести клинических проявлений миастении: 1- на одну единицу степени тяжести (например, из 4в в 4а); 2- на две единицы степени тяжести (4в-3в); 3- на три единицы степени тяжести (4в-3а); 4- на четыре единицы степени тяжести (4в-2в); 5- на пять единиц степени тяжести (4в-2а).
неоперированных пациентов выявляется прямая корреляция между уменьшением тяжести клинических проявлений миастении и снижением титра антител к ацетилхолиновым рецепторам – r=0,45, p<0,05; и r=0,50, p<0,05 соответственно.
Обсуждение
Полученные в настоящем исследовании данные показали, что у подавляющего большинства больных на фоне патогенетической терапии глюкокортикоидными

препаратами и после тимэктомии клинический эффект сопровождается уменьшением уровня антител к АХР. Также как и другие исследователи, мы выявили группу больных, у которых улучшение состояния не сочеталось с уменьшением концентрации антител (12, 17). Отсутствие клинического улучшения могло сопровождаться уменьшением уровня антител к АХР, но это снижение не превышало 20%. Schumm J. et al. [14] показали, что улучшение состояния больных на фоне патогенетического лечения отмечено при уменьшении уровня антител к АХР более чем на 20%. Проведенное исследование показало несколько большую эффективность хирургического лечения по сравнению с глюкокортикоидной терапией. Kuкs J. et al. [9] показали, что в группе больных миастенией без тимомы и без приема иммуносупрессорных препаратов тимэктомия приводила к устойчивому снижению уровня антител к АХР на фоне достигнутого в результате операции клинического улучшения. В интервале от 1 до 3,5 лет после тимэктомии у 25 больных, не получавших иммуносупрессорную терапию, уровень антител был достоверно ниже, чем до операции (17). В другом исследовании из 24 больных миастенией после тимэктомии у 6 пациентов (25%) – отмечалась ремиссия, а у 17 (71%) – улучшение состояния, сочетающееся со снижением концентрации антител к АХР (7). Однако ряд исследователей отмечали большую эффективность глюкокортикоидных препаратов или комбинацию преднизолона в сочетании с имму-носупрессантом азатиоприн (8, 11, 14, 16). Из 32 больных миастенией у 17 было отмечено существенное улучшение: из них у 12 концентрация антител к АХР уменьшилась более чем на 50% (15). Плазмаферез и иммуносорбция на фоне клинического улучшения приводят к снижению уровня антител в среднем на 21±5% (4). Отмечен также значительный клинический эффект ритуксимаба, сопровождавшийся достоверным снижением концентрации антител к АХР (6). Совокупность собственных данных и результатов, приведенных в литературе, позволяет считать, что границей ожидаемого улучшения является снижение уровня антител более чем на 20%. Уменьшение концентрации антител более 50%, как правило, ассоциируется с отчетливым клиническим улучшением.
Таким образом, исследование концентрации антител к АХР до и после различных видов патогенетического лечения является важным объективным методом оценки их эффективности. Выявление группы больных, у которых клиническое улучшение ассоциируется с незначительным (менее 20%) снижением уровня антител, с отсутствием изменения или даже увеличением уровня антител к АХР может указывать на неблагополучный прогноз течения болезни с возможным возникновением рецидива или экзацербации миастении.
Список литературы Антитела к ацетилхолиновому рецептору в оценке эффективности тимэктомии у больных с генерализованной миастенией
- Сиднев Д.В., Карганов М.Ю., Щербакова Н.И. и др. Антитела к ацетилхолиновому рецептору у больных с различными клиническими формами миастении и миастеническим синдромом Ламберта-Итона. Журн неврол и психиат 2006;106:1:53-55.
- Сиднев Д.В., Санадзе А.Г., Щербакова Н.И., Ветшев П.С., Кондратьев А.В. Антитела к титину в оценке эффективности тимэктомии у больных с генерализованной миастенией без тимомы//Грудная и сердечно-сосудистая хирургия. -2007. -№ 4. -С. 48-50.
- Ветшев П.С., Санадзе А.Г., Сиднев Д.В., Ипполитов Л.И., Животов В.А., Аблицов А.Ю. Антитела к титину у больных миастенической и немиастенической тимомой//Хирургия. Журнал им. Н.И. Пирогова. -2007. -№ 6. -С. 53-56.
- Dau P.C., Lindsrom J.M., Cassel C.K. et al. Plasmapheresis and immunosuppessive drug therapy in myasthenia gravis. J Neurol Sci 1993; 29: 5: 734-738.
- Drachman D.B., Adams R.N., Josifek L.F., Self S.G. Functional activities of autoantibodies to acetylcholine receptors and the clinical severity of myasthenia gravis. N Engl J Med 1982; 307: 769-773.
- Illa I., Diaz-Manera J., Rojas-Garcia R. et al. Sustained response to rituximab in anti-AChR and anti-MuSK positive myasthenia gravis patients. J Neuroimmunol 2008; 15: 202: 90-94.
- Kagotani K., Monden Y., Nakahara K. et al. Anti-acetylcholine receptor antibody titer with extended thymectomy in myasthenia gravis. J Torac Cardiovasc Surg 1985; 90: 1: 7-12.
- Kennel P.F., Vilquin J.T., Braun S. et al. Myasthenia gravis: comparative autoantibody assays using human muscle, TE671 and glucocorticoid-treated TE671 cells as sources of antigen. Clin Immunol Immunopathol 1995; 74: 293-296.
- Kuks J.B., Oosterhuis H.J., Limburg P.C., The T.H. Anti-acetylcholine receptor antibodies decrease after thymectomy in patients with myasthenia gravis. Clin Correlation J Autoimmun 1991; 4: 2: 197-211.
- Lindstrom J., Shelton D., Fujii Y. Myasthenia gravis. Adv Immunol 1988; 42: 233-284.
- Oosterhuis H.J., Limburg P.C., Hummel-Tapell E., The T.H. Anti-acetylcholine receptor antibodies in myasthenia gravis. Part2. Clinical and serological follow-up of individual patients. J Neurol Sci 1983; 58: 3: 371-385.
- Oosterhuis H.J., Limburg P.C., Hummel-Tapell E. et al. Anti-acetylcholine receptor antibodies in myasthenia gravis. Part3. The effect of thymectomy. J Neurol Sci 1985; 69: 3: 335-343.
- Psaridi-Linardaki L., Trakas N., Mamalaki A., Tzartos S.J. Specific immunoadsorption of the antibodies from myasthenic patients using the extracellular domain of the human muscle acetylcholine receptor alpha-subunit: Development of an antigenspecific therapeutic strategy. Neuroimmunol 2005; 159: 1-2: 183-191.
- Schumm F., Fateh-Moghadam A., Dichgans J. Correlation of acetylcholine receptors antibodies and clinical severity of myasthenia gravis in combined immunosuppessive therapy. Eur Arch Psychiat Neurol Sci 1984; 234: 4: 224-230.
- Seybold M.E., Lindsrom J.M. Patterns of acetylcholine receptor antibody fluctuation in myasthenia gravis. Ann NY Acad Sci 1981; 377: 292-306.
- Shibuya N., Sato T., Osame M. et al. Immunoadsorption therapy for myasthenia gravis. J Neurol Neurosurg Psychiat 1994; 57: 5: 578-581.
- Vincent A., Newsom-Davis J., Newton P., Beck N. Acetylcholine receptor antibody and clinical response to thymectomy in myasthenia gravis. Neurology 1983; 33: 10: 1276-1282.
- Vincent A., Whiting P.J., Schluep M. et al. Antibody heterogeneity and specificity in myasthenia gravis. Ann NY Acad Sci 1987; 505: 106-120.
- Voltz R., Hohlfeld R., Faten-Moghadam A. et al. Myasthenia gravis: measurement of anti-AchR autoantibodies using cell line TE671. Neurol 1991; 41: 1836-1838.
- Barohn R.J. How to administer the quantitative Myasthenia Gravis Foundation of America, Inc. -1996.


