Аортокоронарное шунтирование на работающем сердце в условиях параллельного искусственного кровообращения у больных со сниженной сократительной функцией левого желудочка
Автор: Урюжников Вадим Валерьевич, Сидоров Р.В., Молочков А.В., Чарная М.А., Жбанов И.В., Шабалкин Б.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.5, 2010 года.
Бесплатный доступ
Проведена сравнительная оценка эффективности коронарного шунтирования в условиях параллельного искусственного кровообращения и реваскуляризации миокарда с применением кардиоплегии, изучена динамика метаболических изменений в миокарде в ходе этих операций. Установлено, что гиперлактатемия в крови коронарного синуса, наблюдаемая на протяжении всей операции коронарного шунтирования в условиях кардиоплегии, свидетельствует о длительных структурно-метаболических нарушениях в миокарде вследствие аноксии и реперфузионного синдрома. Коронарное шунтирование на работающем сердце в условиях искусственного кровообращения сопровождается менее выраженными и кратковременными изменениями метаболизма в миокарде. У больных с нормальной сократительной функцией левого желудочка коронарное шунтирование в условиях параллельного искусственного кровообращения не имеет преимуществ перед реваскуляризацией миокарда с применением кардиоплегической остановки сердца. У больных с инвалидизированным миокардом и сниженной сократительной функцией левого желудочка отказ от кардиоплегии и проведение коронарного шунтирования на работающем сердце в условиях искусственного кровообращения приводит к значительному снижению частоты развития острой сердечной недостаточности в периоперационном периоде.
Аортокоронарное шунтирование, параллельное искусственное кровообращение, метаболизм миокарда
Короткий адрес: https://sciup.org/140187864
IDR: 140187864 | УДК: 616.124.2-008.64
On-pump beating heart coronary artery bypass grafting in patients with reduced left ventricular contractility
The article features a comparative evaluation of the effectiveness of on-pump beating heart coronary artery bypass grafting and myocardial revascularization with cardioplegia, the dynamics of metabolic changes in myocardium during these operations. It was found that hyperlactatemia in coronary sinus blood, which is observed throughout the coronary artery bypass surgery with cardioplegia, suggests long-term structural and metabolic disturbances in the myocardium due to anoxia and reperfusion syndrome. On-pump beating heart coronary artery bypass grafting is accompanied by a less pronounced and transient changes in myocardium metabolism. On-pump beating heart coronary artery bypass grafting in patients with normal left ventricular contractility has advantages over myocardial revascularization with cardioplegic. In patients with reduced left ventricular contractility, conducting on-pump beating heart coronary artery bypass grafting leads to a significant reduction in the incidence of acute heart failure in the perioperative period.
Текст научной статьи Аортокоронарное шунтирование на работающем сердце в условиях параллельного искусственного кровообращения у больных со сниженной сократительной функцией левого желудочка
В настоящее время в хирургическом лечении больных ишемической болезнью сердца (ИБС) применяются как традиционное аортокоронарное шунтирование (АКШ) в условиях искусственного кровообращения (ИК) и кардиоплегии (КП), так и реваскуляризация миокарда на работающем сердце без ИК [3, 5]. Накопленный опыт и современное высокотехнологичное обеспечение операций на работающем сердце позволили расширить показания к операциям АКШ у пациентов с высоким риском осложнений, связанных с ИК [4, 10, 6]. Тем не менее, существует категория пациентов с низкой сократительной функцией левого желудочка (ЛЖ), у которых выполнение операции без ИК опасно серьезными гемодинамическими нарушениями, а проведение ИК и КП сопряжено с высоким риском развития синдрома низкого сердечного выброса из-за посткардиоплегической депрессии миокарда. Можно предполагать, что у таких больных оптимальным вариантом операции может быть АКШ на работающем сердце в условиях параллельного ИК. Во-первых, применение ИК во вспомогательном режиме исключает вероятность расстройств центральной гемодинамики во время основного этапа операции. Во-вторых, отказ от КП нивелирует реперфузионный синдром после тотальной аноксии миокарда, что может способствовать восстановлению эффективной сердечной деятельности после окончания ИК. В силу этого целью настоящего исследования является оценка эффективности АКШ на работающем сердце в условиях параллельного ИК у пациентов со сниженной сократительной функцией ЛЖ.
Материал и методы
Исследуемую группу составили 105 пациентов, которым за период с 2004 по 2008 г. последовательно выполнили АКШ на работающем сердце в условиях параллельного ИК. Контрольную группу сформировали методом случайной выборки из 90 больных, оперированных в этот же период времени с ИК и КП.
Пациенты обеих групп не различались по возрасту и полу, исходному клиническому статусу, наличию сопут-

Урюжников В.В., Сидоров Р.В., Молочков А.В., Чарная М.А., Жбанов И.В., Шабалкин Б.В.
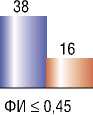
АОРТОКОРОНАРНОЕ ШУНТИРОВАНИЕ НА РАБОТАЮЩЕМ СЕРДЦЕ В УСЛОВИЯХ ПАРАЛЛЕЛЬНОГО ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У БОЛЬНЫХ СО СНИЖЕННОЙ СОКРАТИТЕЛЬНОЙ ФУНКЦИЕЙ ЛЕВОГО ЖЕЛУДОЧКА ствующих заболеваний, характеру и степени поражения коронарных артерий, состоянию сократительной функции ЛЖ, а также объему выполненной реваскуляризации миокарда (табл. 1). Каждая группа была разделена на две подгруппы в соответствии с показателем фракции изгнания ЛЖ. 1 подгруппу составили больные с ФИ > 0,45, 2 подгруппу – с ФИ ≤0,45 (рис. 1).
Операции на работающем сердце в условиях параллельного ИК выполняли в режиме нормотермии с использованием вакуумных стабилизационных систем Acrobat (компания «Giudant», США). В контрольной группе применяли нормотермическое ИК и фармакохолодовую КП внеклеточным раствором «Консол» (компания «Биофарм-94», Россия). У больных обеих групп для шунтирования передней нисходящей артерии (ПНА) использовали левую внутреннюю грудную артерию (ЛВГА), для шунтирования других коронарных артерий – аутовенозные трансплантаты. При параллельном ИК первоначально формировали маммарокоронарный анастомоз между ЛВГА и ПНА, затем шунтировали остальные артерии. В условиях КП маммарокоронарный анастомоз выполняли в последнюю очередь. После этого формировали проксимальные анастомозы.
Для изучения метаболизма миокарда на различных этапах операции определяли концентрацию лактата (ммоль/л) с последующей оценкой разницы между его содержанием в артериальной крови и крови коронарного синуса (КС). До начала ИК, после канюляции восходящей аорты в КС сердца через отдельный кисетный шов правого предсердия вводили катетер для ретроградной КП. Забор крови из КС во время АКШ в условиях параллельного ИК осуществляли перед началом основного этапа, после формирования каждого дистального анастомоза, по завершении проксимальных анастомозов и пуска кровотока по шунтам и перед ушиванием перикарда. Аналогичную процедуру в контрольной группе выполняли до и после пережатия аорты, после формирования проксимальных анастомозов и пуска кровотока по шунтам, а также перед ушиванием перикарда. Одновременно с забором крови из КС осуществляли взятие артериальных проб крови. Исследование провели во время 14 операций в условиях параллельного ИК, и 10 – с использованием ИК и КП.
Для сравнительной оценки ближайших результатов операции АКШ мы провели анализ госпитальной летальности, частоты и причин периоперационных осложнений и в обеих группах больных.
Результаты и обсуждение
Госпитальная летальность в исследуемой и контрольной группах достоверно не различалась и составила, соответственно, 0,95% (1/105) и 1,1% (1/90). Все пациенты обеих групп с ФИ ЛЖ > 0,45 благополучно перенесли хирургическое вмешательство. Различия в этом показателе среди больных с ФИ ≤ 0,45, – соответственно, 2,6% (1/38) против 6,3% (1/16), – статистически не значимы (рис. 2).
В исследуемой группе причиной летального исхода стал периоперационный инфаркт миокарда вследствие тромботической окклюзии аутовенозного шунта к боковой ветви огибающей артерии, видимо, из-за неудовлет-
100 n
I ■ Исследуемая группа Контрольная группа
Табл. 1. Характеристика оперированных пациентов
|
Параметры |
Исследуемая группа (n-105) |
Контрольная группа (n-90) |
|
Возраст |
59,9 ± 9,2 |
59,5 ± 8,1 |
|
Женщины, % |
9,5 |
12,2 |
|
Стенокардия III–IV класса CCS, % |
96,2 |
91,1 |
|
Острый коронарный синдром, % |
15,2 |
12,3 |
|
Ожирение, % |
22,9 |
23,3 |
|
Сахарный диабет % |
11,4 |
8,9 |
|
ХОБЛ, % |
24,8 |
22,2 |
|
Артериальная гипертензия, % |
82,9 |
84,4 |
|
ФИ, % |
49,1 ± 8,5 |
51,6 ± 6,6 |
|
КДО, мл |
140,8 ± 42,4 |
123,7 ± 27,1 |
|
Многососудистое поражение, % |
77,1 |
70,0 |
|
Поражение ствола ЛКА, % |
45,7 |
35,6 |
|
Объём реваскуляризации |
3,2 ± 0,8 |
3,3 ± 0,9 |
|
Повторное АКШ, % |
14,3 |
8,9 |
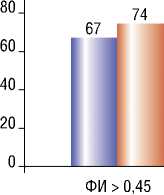
Рис. 1. Распределение пациентов в группах в зависимости от показателя фракции изгнания левого желудочка
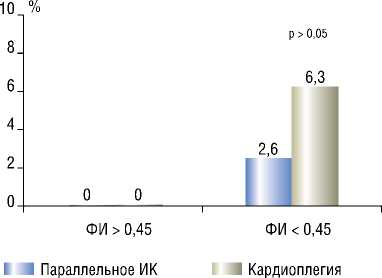
Рис. 2. Госпитальная летальность в исследуемой и контрольной группах при различном показателе фракции изгнания левого желудочка

Урюжников В.В., Сидоров Р.В., Молочков А.В., Чарная М.А., Жбанов И.В., Шабалкин Б.В. АОРТОКОРОНАРНОЕ ШУНТИРОВАНИЕ НА РАБОТАЮЩЕМ СЕРДЦЕ В УСЛОВИЯХ ПАРАЛЛЕЛЬНОГО ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У БОЛЬНЫХ СО СНИЖЕННОЙ СОКРАТИТЕЛЬНОЙ ФУНКЦИЕЙ ЛЕВОГО ЖЕЛУДОЧКА ворительного дистального русла последней. Летальный исход пациента в контрольной группе был обусловлен острой сердечной недостаточностью (ОСН), развившейся в постперфузионном периоде на фоне исходно низких резервов сократительной функции ЛЖ.
Частота развития периоперационного инфаркта миокарда в исследуемой и контрольной группах была одинаковой – соответственно, 0,95% (1/105) и 1,1% (1/95), среди пациентов с ФИ > 0,45 этого осложнения не было, а у больных с более низкой ФИ различия в этом показателе, – соответственно, 2,6% (1/38) против 6,3% (1/16), – были недостоверны (рис. 3).
ОСН, критерием которой считали зависимость центральной гемодинамики от инфузии катехоламинов (допамин в дозе более 5 мкг/кг/мин), наблюдали с одинаковой частотой в исследуемой и контрольной группах, соответственно, в 11,4% (12/105) и 14,4% (13/90) наблюдений. Достоверной межгрупповой разницы в частоте развития ОСН у больных с ФИ > 0,45 ОСН не было – соответственно, 7,5% (5/67) и 6,8% (5/74). Однако у больных с более низкой ФИ это осложнение отметили значительно реже после АКШ на параллельном ИК – у 18,4% (7/38) пациентов против 50,0% (8/16) – после реваскуляризации миокарда в условиях ИК и КП (рис. 4)
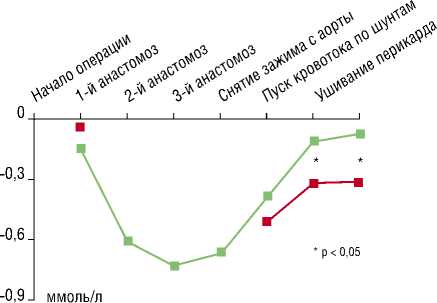
Во время формирования дистальных анастомозов в условиях параллельного ИК мы отметили рост концентрации лактата в крови КС, который является признаком смещения метаболизма в сторону анаэробного гликолиза и, по-видимому, обусловлен локальной ишемией миокарда, развивающейся в ответ на временную окклюзию коронарных артерий при формировании анастомозов (рис. 5). При этом ни у одного пациента мы не наблюдали признаков ишемии миокарда на ЭКГ. Однако, после включения кровотока по шунтам, содержание лактата в крови КС быстро возвращалось к исходному уровню. У больных контрольной группы после снятия зажима с аорты и последующего пуска кровотока по шунтам концентрация лактата в крови КС была достоверно выше, чем на аналогичном этапе у больных исследуемой группы, и оставалась практически неизменной до конечного этапа
-
10 %
8_
6_ о 0 0
ФИ > 0,45
I I Параллельное ИК р > 0,05

ФИ <0,45
Кардиоплегия
Рис. 3. Частота развития периоперационного инфаркта миокарда в исследуемой и контрольной группах при различном показателе фракции изгнания левого желудочка операции. Данный факт свидетельствует о более выраженной гипоксии миокарда, развивающейся во время операции в условиях ИК и КП.
Таким образом, результаты представленного исследования подтверждают негативные последствия аноксии миокарда, которые в той или иной степени свойственны каждой операции, выполняемой в условиях кардиоплегии, и проявляются в активации анаэробного гликолиза и повреждении кардиомиоцитов [9]. Во многом степень таких нарушений определяется видом проводимой кардиоплегии. В частности, доказано, что применение кровяного гиперкалиемического раствора позволяет достичь лучшего уровня защиты миокарда в сравнении с кристаллоидной кардиоплегией [1]. Весьма эффективным является внеклеточный кардиоплегический раствор «Консол», наиболее широко применяемый в нашей клинике (С.Л. Дземешкевич). Протективный эффект любой кардиоплегии находится в обратной пропорциональной зависимости от длительности пережатия аорты [2]. Нарушения метаболизма миокарда усугубляет реперфузионный синдром, развивающийся после пуска кровотока по шунтам [7, 8]. Подтверждением этому служит гипер-
Параллельное ИК -■- Кардиоплегия
Рис. 5. Концентрация лактата в крови коронарного синуса (артериовенозная разница) на различных этапах в исследуемой и контрольной группах
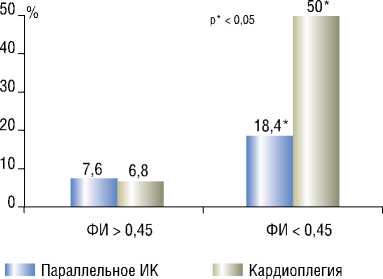
Рис. 4. Частота развития острой сердечной недостаточности в исследуемой и контрольной группах при различном показателе фракции изгнания левого желудочка
Урюжников В.В., Сидоров Р.В., Молочков А.В., Чарная М.А., Жбанов И.В., Шабалкин Б.В.
АОРТОКОРОНАРНОЕ ШУНТИРОВАНИЕ НА РАБОТАЮЩЕМ СЕРДЦЕ В УСЛОВИЯХ ПАРАЛЛЕЛЬНОГО ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ У БОЛЬНЫХ СО СНИЖЕННОЙ СОКРАТИТЕЛЬНОЙ ФУНКЦИЕЙ ЛЕВОГО ЖЕЛУДОЧКА лактатемия, сохраняющаяся до конца операции в крови коронарного синуса. Напротив, при выполнении АКШ на работающем сердце в условиях параллельного ИК концентрация лактата в оттекающей от миокарда крови быстро приходит к исходному уровню, что свидетельствует о восстановлении его нормального метаболизма практически сразу после основного этапа операции.
У пациентов с исходно сохранной сократительной функцией ЛЖ негативные последствия кардиоплегии, как правило, не отражаются на клиническом течении периоперационного периода – результаты операций в условиях КП и параллельного ИК не различаются. Однако, у больных с инвалидизированным миокардом и сниженной ФИ, отказ от применения КП приводит к значимому снижению частоты развития ОСН в ближайшем послеоперационном периоде, что снижает риск хирургического лечения.
Выводы
-
1. Повышенная концентрация лактата в крови коронарного синуса, наблюдаемая на протяжении всей операции аортокоронарного шунтирования в условиях кардиоплегии, свидетельствует о длительном периоде структурно – метаболических нарушений миокарда вследствие его аноксии и последующего реперфузионного синдрома.
-
2. Аортокоронарное шунтирование на работающем сердце в условиях искусственного кровообращения сопровождается менее выраженными и кратковременными метаболическими нарушениями миокарда, нормализация обменных процессов в нем происходит практически сразу по окончании основного этапа операции.
-
3. У больных с нормальной сократительной функцией левого желудочка аортокоронарное шунтирование на работающем сердце в условиях параллельного искусственного кровообращения не имеет преимуществ перед реваскуляризацией миокарда с применением кардиопегической остановки сердца.
-
4. Отказ от кардиоплегии и проведение аортокоронарного шунтирования на работающем сердце в условиях параллельного искусственного кровообращения у больных с инвалидизированным миокардом и сниженной сократительной функцией левого желудочка приводит к значительному снижению частоты развития сердечной недостаточности в периоперационном периоде.
Список литературы Аортокоронарное шунтирование на работающем сердце в условиях параллельного искусственного кровообращения у больных со сниженной сократительной функцией левого желудочка
- Бекназарян Д.Ю. Оценка эффективности различных методов защиты миокарда у больных ИБС//дис. канд. мед. наук. -М, 2008.
- Бунятян А.А., Трекова Н.А. и др. Защита миокарда. Особенности защиты миокарда у кардиохирургических больных.//Руководство по кардиоанестезиологии, 2005. С. 111-112.
- Михеев А.А. Операции на коронарных артериях на работающем сердце без искусственного кровообращения у больных ИБС/А.А. Михеев, В.М. Клюжев, Н.А. Карпун. -М.: Медицина, 2001.
- Шабалкин Б.В. Малоинвазивная реваскуляризация миокарда или аортокоронарное шунтирование без искусственного кровообращения?/Б.В. Шабалкин, И.В. Жбанов//Тезисы докладов V Всероссийского съезда сердечно -сосудистых хирургов. -Новосибирск, 1999. -С. 152.
- Шабалкин Б.В. Реваскуляризация миокарда без искусственного кровообращения/Б. В. Шабалкин//Грудная и серд.-сосуд. хир. -2001. -№ 2. -С. 4-7.
- Ferrari E./On-pump beating heart coronary surgery for high risk patients requiring emergency multiple coronary artery bypass grafting./E. Ferrari, N. Stalder, L. K. von Segesser//J. Cardiothorac Surg. -2008. -Vol. 3. -P. 38.
- Folliguet T.A. Beating heart revascularization with minimal extracorporeal circulation in patients with a poor ejection fraction./T.A. Folliguet, F. Philippe, F. Larrazet et al.//Heart Surg. Forum. -2002. -Vol. 1. -P. 19-23.
- Mohammed Fouda. Coronary Artery Bypass Surgery with On-Pump Beating-Heart Technique./Mohammed Fouda//Asian Cardiovasc. Thorac. Ann. -2007. -Vol. 15. P. 392 -395.
- Rastan A.J. On-pump beating heart versus off-pump coronary artery bypass surgery-evidence of pump-induced myocardial injury./A.J. Rastan, H.B. Bittner, J.F. Gummert//Eur. J. Cardiothorac. Surg. -2005. -Vol. 27. -P. 1057-1064.
- Shinichi M. On-Pump Beating-Heart Coronary Artery Bypass: A Propensity Matched Analysis./M. Shinichi, A. Matsuura, K. Miyahara et al.//Ann Thorac. Surg. -2007. Vol. 83 (6). -P. 1368-1373.


