Апоптоз в опухолевых клетках, подвергнутых сочетанному действию гипертермии и облучения: исследование молекулярных механизмов и мишеней
Автор: Кабаков А.Е., Кудрявцев В.А., Хохлова А.В., Макарова Ю.М., Лебедева Т.В.
Рубрика: Научные статьи
Статья в выпуске: 2 т.27, 2018 года.
Бесплатный доступ
В данной работе мы изучали молекулярную природу радиосенсибилизирующего действия гипертермии на раковые клетки. Исследовались клеточные линии, происходящие из карцином (HeLa, MCF-7), фибросаркомы (НТ 1080) и Т-лимфомы (Jurkat) человека. Культуры клеток выдерживали в условиях гипертермии (42-44 оС) и/или облучали g-фотонами (2-6 Гр), после чего оценивались такие параметры как интенсивность и тип клеточной гибели, клоногенность, количество двунитевых разрывов в ядерной ДНК и динамика их репарации, локализация белков теплового шока (БТШ) и пр. Нами показано, что (1) вызываемое гипертермией усиление пострадиационной гибели клеток в основном обусловлено стимуляцией каспазазависимого апоптоза, (2) запускание такого апоптотического механизма происходит, по-видимому, в результате нарушения клеточной реакции на радиационное повреждение генома, когда белковые компоненты системы репарации ДНК не работают после теплового стресса, (3) экспрессия и распределение белков теплового шока БТШ90, БТШ70 и БТШ27 могут быть важными детерминантами, определяющими дальнейшую судьбу (выживание или «самоубийство») злокачественной клетки, испытавшей воздействие гипертермии и облучения. Обсуждается, что такие факторы как тепловой стресс-ответ, уровень агрегированного клеточного белка и функциональная активность БТШ могут существенно влиять на эффективность радиосенсибилизации опухолей посредством прогревания. Рассматриваются новые подходы и мишени для усиления радиосенсибилизирующего действия гипертермии на раковые клетки.
Радиосенсибилизация, g-излучение, gh2ax фокусы, репарация днк, тепловой стресс, каспаза, белки теплового шока, протеотоксичность, денатурация белков, опухоли, радиобиологические эффекты, лучевая терапия
Короткий адрес: https://sciup.org/170170348
IDR: 170170348 | УДК: 616-006.04-092.18:615.832.8:612.014.482 | DOI: 10.21870/0131-3878-2018-27-2-62-75
Apoptosis in tumor cells subjected to the combined action of hyperthermia and irradiation: a study of the molecular mechanisms and targets
In the present work we investigated the molecular nature of the radiosensitizing action of hyperthermia on various cancer cells. Tumor cell lines derived from human carcinomas (HeLa, MCF-7), fibrosarcoma (HT 1080) and T-lymphoma (Jurkat) were here explored. The cell cultures were exposed to hyperthermic conditions (42-44 оС) and/or irradiated with g-photons (2-6 Gy); then such parameters were assessed as the intensity and type of cell death, clonogenicity, amounts of DNA double strand breaks and their repair dynamics, localization of heat shock proteins etc. We showed that (1) the hyperthermia-induced enhancement of post-radiation cell death is mainly due to stimulation of caspase-dependent apoptosis, (2) triggering of such apoptotic mechanism appears to result in a default of the cellular response to radiation damage to genome, (3) expression and distribution of heat shock proteins HSP90, HSP70 and HSP27 can be the important determinants defining the further fate (survival or “suicide”) of the malignant cell experienced hyperthermia and radiation exposure. It is here discussed that such factors as the heat stress response, level of aggregated cellular protein and functional activities of HSPs can substantially influence on the effectiveness of radiosensitization of tumors by heating. New approaches and targets are considered for the enhancement of radiosensitizing action of hyperthermia on cancer cells.
Текст научной статьи Апоптоз в опухолевых клетках, подвергнутых сочетанному действию гипертермии и облучения: исследование молекулярных механизмов и мишеней
Гипертермическое воздействие используется в клинической онкологии с целью повышения эффективности лучевой и лекарственной терапии [1-4]. Для создания локальной гипертермии в зоне опухолевого роста в основном применяются наведённые электромагнитные поля сверхвысокочастотного, ультравысокочастотного или высокочастотного диапазона [4]. Несмотря на определённые проблемы, иногда осложняющие проведение гипертермии у больных, в различных клиниках накоплено достаточно большое количество данных, свидетельствующих о пользе применения этого метода в комбинированной противоопухолевой терапии [2-6]. Эти же данные одновременно указывают на необходимость дальнейшего изучения биологических эффектов гипертермии, что способствовало бы разработке новых подходов в лечении пациентов с различными злокачественными новообразованиями.
Хотя противоопухолевое действие гипертермии известно уже давно, и его молекулярные механизмы довольно подробно изучались [7, 8], терморезистентность и радиорезистентность некоторых опухолей по-прежнему остаются актуальными проблемами для терапии, поэтому важной задачей является поиск клинически применимых способов термо- и радиосенсибилиза-
Кабаков А.Е.* – зав. лаб., к.б.н.; Кудрявцев В.А . – научн. сотр.; Хохлова А.В. – мл. научн. сотр.; Макарова Ю.М. – научн. сотр.;
Лебедева Т.В. – в.н.с., к.б.н. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
ции таких опухолей. В данном исследовании мы старались прояснить некоторые критические моменты в тепловом стресс-ответе раковых клеток и выявить взаимосвязь между клеточными реакциями на гипертермию и облучение.
Материалы и методы
Были использованы 4 охарактеризованные клеточные линии, происходящие из карцином молочной железы (MCF-7) или шейки матки (HeLa), фибросаркомы (НТ 1080) и Т-лимфомы (Jurkat) человека. Клетки выращивали в среде DMEM с 10% телячьей фетальной сывороткой, 2 моль/л L-глютамином и 10000 IU/мл пенициллин/стрептомицином (Hyclone, США) в инкубаторе с 5% СО 2 при 37 °C.
Гипертермическую обработку проводили, погружая герметично закрытые чашки Петри с клеточными культурами в термостатированную водяную баню с заданной температурой (42, 43, или 44 оС) на 20, 30 или 60 мин.
Пластиковые чашки Петри с клетками подвергали прямому воздействию γ-излучения на радиотерапевтической установке «Луч-1» (Латвия) с γ-источником 60Со и интенсивностью 0,9-1 Гр/мин.
Фракции апоптотических и некротических клеток определяли на проточном цитофлуориметре «FACS Vantage» (Becton Dickinson, США) после окрашивания ФИТЦ-меченным аннекси-ном V и йодистым пропидием [9]. Параллельно, интенсивность апоптоза оценивали иммуноблоттингом, выявляя активацию каспаз в образцах клеток [9] с помощью антител к каспазе-3, антител к поли-АДФ-рибоза полимеразе (ПАРП), вторых антител, конъюгированных с пероксидазой, и реагентов для проявления методом усиленной хемилюминесценции (Amersham, Великобритания). Выживание облучённых опухолевых клеток оценивали по вырастанию клеточных колоний (тест на клоногенность) [9].
Сайты фосфорилирования H2AX гистона (так называемые «γH2AX фокусы») выявляли с помощью антител к γH2AX и вторых антител с флуорохромом alexa-fluor 488 (Millipor, США) [10]. Препараты окрашенных клеток анализировали на конфокальном микроскопе (Leica TCS SPE, Германия).
Протеотоксические (т.е. приводящие к повреждению клеточных белков) эффекты гипертермии оценивали двумя разными способами: 1) по изменённой динамике ренатурации фермента люциферазы, инактивированного в прогретых клетках [11]; 2) по спровоцированному стрессом увеличению уровня агрегированного (неэкстрагируемого Тритоном Х-100) клеточного белка [12, 13].
Изменения содержания БТШ90, БТШ70 и БТШ27 в цитозольной и ядерно-цитоскелетной (Тритон Х-100-нерастворимой) фракциях оценивали с помощью иммуноблоттинга после сканирования проявленных блотов [11-13].
Все количественные результаты представлены как усреднённые данные (± разброс) 4-6 независимых экспериментов с 3-мя параллелями для каждой точки. Статистическую обработку результатов проводили по критерию Манна-Уитни с помощью программы «Statistica 6.0» («Microcal Softcare, Inc.»). Различия между усреднёнными величинами считались значимыми при р<0,05.
Результаты и обсуждение
Радиосенсибилизирующая гипертермия стимулирует каспазазависимый апоптоз в облучённых опухолевых клетках. Наши эксперименты показали, что гипертермическая обработка, которая сама по себе не убивала опухолевые клетки, может значительно усилить их апоптотическую гибель, если применяется в сочетании с облучением γ-фотонами (рис. 1-3, табл. 1). Во всех 4-х исследованных опухолевых линиях такое сочетанное воздействие стимулировало «классический» апоптоз с ранней транслокацией аннексин V-тропного лиганда (фосфатидилсерин) на клеточную поверхность (рис. 1 и [9]) и летальной активацией прокаспазы-3 в терминальной фазе (рис. 2 и [9]).
Контроль (37 оС, 0 Гр)
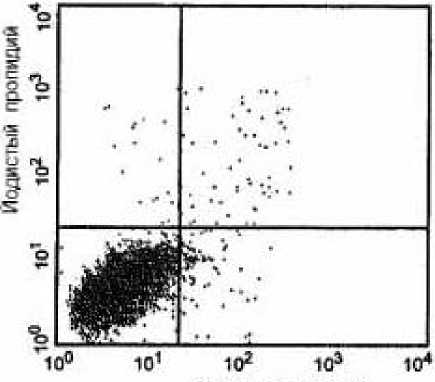
ФИТЦ-аннексим V
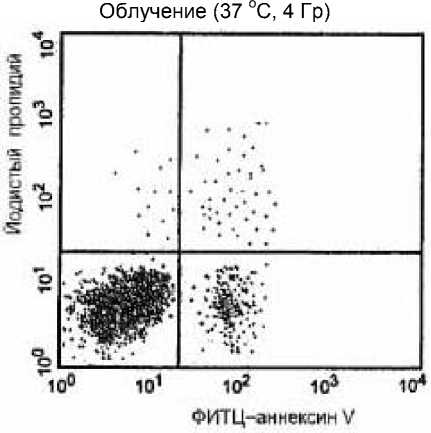
44 оС + 4 Гр
43 оС + 4 Гр
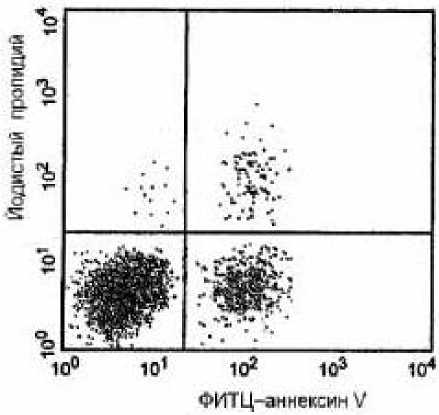
Рис. 1. Усиление апоптоза в клетках Т-лимфомы Jurkat, испытавших действие гипертермии перед облучением. Клетки прогревали при 43 оС или 44 оС в течение 60 или 30 мин соответственно, и затем облучали (4 Гр). Здесь хорошо заметно увеличение апоптотической фракции в прогретых образцах. Похожие результаты получали и на других опухолевых культурах (см. рис. 3 и табл. 1).
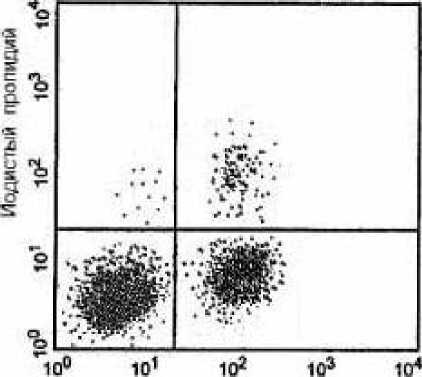
ФИТЦ-анмексин V
Интенсивность этого апоптоза ожидаемо коррелировала с температурой прогрева и падением выживаемости и клоногенности прогретых клеток (рис. 1-3, табл. 1). Увеличение временного периода между гипертермией и облучением приводило к снижению цитотоксичности комбинированного воздействия (данные не приводятся). Таким образом, усиление апоптотиче-ской гибели в прогретых и облучённых опухолевых клетках, как и снижение их клоногенности, является проявлением радиосенсибилизирующего действия гипертермии.
A
12 3 4
gg^ Прокаспаза-3 (32 кДа)
17 кДа фрагмент
12 кДа фрагмент

(116 кДа)
Рис. 2. Иммуноблоттинг, показывающий усиленную активацию каспазы-3 в опухолевых клетках MCF-7, облучённых после гипертермии.
А: (1) только неактивная прокаспаза-3 (85 кДа) присутствует в контроле; (2) активные фрагменты каспазы-3 (17 кДа и 12 кДа) появляются после облучения при дозе 4 Гр; (3 и 4) гиперактивация каспазы-3 происходит в клетках, которые перед облучением прогревались 60 мин при 43 оС (3) или 30 мин при 44 оС (4). Б: в результате активации каспазы-3 происходит сайт-специфичный протеолиз её терминального субстрата – ПАРП (116 кДа), легко определяемый по появлению характерного фрагмента с массой 85 кДа. Более интенсивные полосы 85 кДа в образцах 3 и 4 свидетельствуют об усилении пострадиационного апоптоза в прогретых клетках. Похожие результаты получали с культурами HeLa, HT 1080 и Jurkat (данные не приводятся).
85 кДа фрагмент
То, что относительно мягкий тепловой стресс стимулирует апоптоз в облучённых клетках фибросаркомы (НТ 1080) и карцином (MCF-7, HeLa), на наш взгляд, заслуживает внимания. Не удивительно, когда апоптотическая гибель усиливается в прогретых перед облучением клетках лимфомы Jurkat, поскольку именно каспазазависимый апоптоз является типичной и основной формой клеточной гибели в опухолях лимфатической системы. Однако известно, что апоптоз не характерен для облучённых клеток сарком и карцином, которые погибают в основном из-за митотической катастрофы или некроза [14, 15]. Судя по нашим результатам, использование гипертермии в комбинации с облучением иногда позволяет не только усиливать радиационный ответ опухоли-мишени, но и кардинально изменять сам механизм пострадиационной гибели злокачественных клеток. Стоит отметить, что in vivo массивная некротическая гибель клеток часто сопровождается литическим разрушением окружающих тканей, развитием острого воспаления и другими опасными осложнениями, негативно влияющими на организм пациента. Напротив, апоптотическое «самоубийство» повреждённых клеток происходит без сопутствующих патологических реакций, и потому апоптоз считается наиболее предпочтительным способом элиминации раковых клеток в процессе цитотоксической терапии [16]. Мы установили, что комбинация гипертермии и облучения даёт возможность реализовать этот желательный механизм (апоптоз) даже в тех типах опухолей, которым он обычно не свойственен (т.е. в карциномах и саркомах).
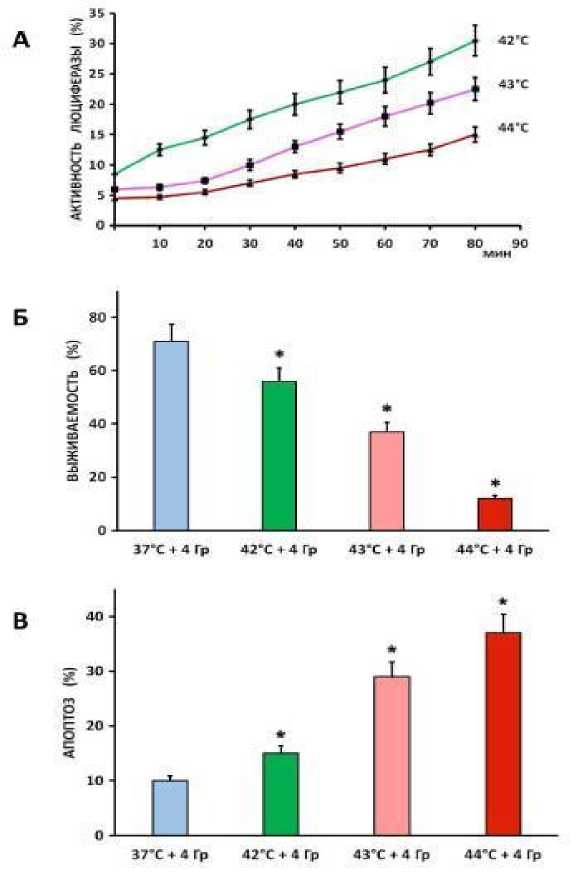
Рис. 3. Корреляция между температурой гипертермии, её протеотоксичностью, определённой по замедлению реактивации денатурированной люциферазы (А), и её радиосенсибилизирующими эффектами, снижающими выживаемость (Б) и усиливающими апоптоз (В) в облучённых клетках HeLa (см. табл. 1). * – значимое отличие от значений, полученных при 37 оС, p<0,05.
Таблица 1
Усиление пострадиационного апоптоза и увеличение значений ФИД в культуре опухолевых клеток HeLa, подвергнутых гипертермии и облучению
|
Условия обработки |
% апоптоза |
ФИД |
|
37 оС (контроль) |
1 – 4 |
-- |
|
37 оС + 4 Гр |
10 – 12 |
-- |
|
42 оС, 90 мин + 4 Гр |
15 – 18 |
1,48 |
|
43 оС, 60 мин + 4 Гр |
20 – 24 |
1,72 |
|
44 оС, 20 мин + 4 Гр |
26 – 29 |
2,05 |
Примечание: ФИД – фактор изменения дозы.
Гипертермия нарушает реакцию облучённых опухолевых клеток на повреждение ядерной ДНК. Принято считать, что на молекулярном уровне радиосенсибилизирующие эффекты гипертермии обусловлены усилением повреждения ДНК и денатурацией термолабильных клеточных белков, которые нужны для восстановления облучённых клеток; в первую очередь, к таким белкам относятся ферменты, участвующие в процессах репарации радиационных повреждений ДНК [8]. А
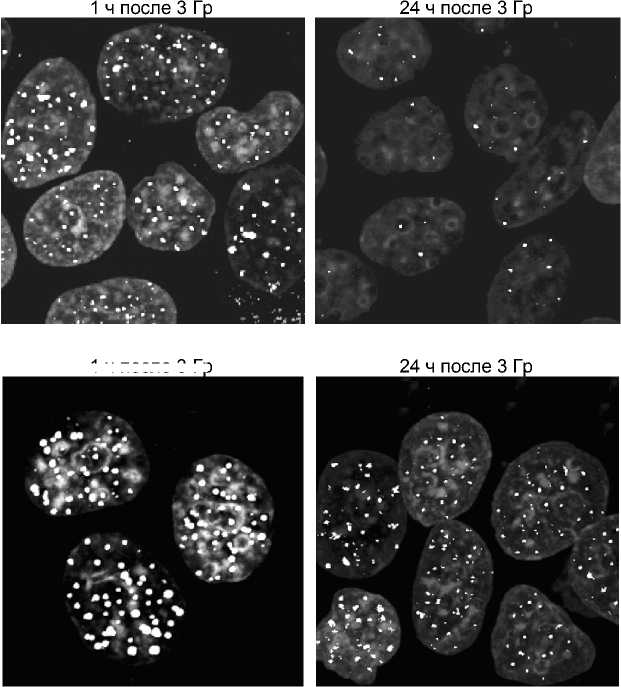
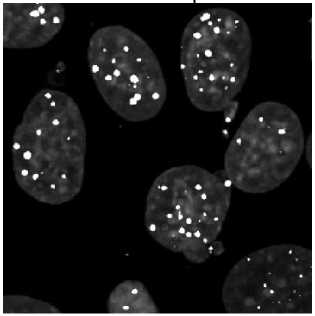
Рис. 4. Вызванное гипертермией изменение динамики формирования и исчезновения γH2AX фокусов в ядрах облучённых клеток MCF-7.
А: нормальный радиационный ответ непрогретых (растущих при 37 оС) клеток, показывающий завершение репарации двойных разрывов ядерной ДНК за 22-24 ч после облучения (3 Гр). Б: эффект гипертермической предобработки (43 оС, 60 мин), приводящий к нарушению процесса репарации разрывов ядерной ДНК (см. текст и табл. 2).
37 оС 0 Г

Б
43 оС 0 Г
1 ч после 3 Гр
Мы анализировали динамику образования и исчезновения фосфо-гистоновых (γH2AX) фокусов в ядрах карциномных MCF-7 клеток после их облучения (рис. 4, табл. 2), что отражало эффективность репарации двунитевых разрывов ДНК [10]. Согласно нашим наблюдениям, предварительный прогрев (43 оС, 60 мин) МСF-7 клеток вызывал образование ядерных γH2AX фокусов ещё до облучения (рис. 4Б, табл. 2). На ранних сроках (1-2 ч) после облучения ядра прогретых клеток содержали заметно больше γH2AX фокусов по сравнению с ядрами непрогре-тых облучённых клеток. В непрогретых образцах через 24 ч после облучения уровень γH2AX фокусов возвращался к контрольному, что означает завершение репарации двойных разрывов ядерной ДНК (рис. 4А, табл. 2). Напротив, через 24 ч после облучения в ядрах прогретых клеток всё ещё оставались γH2AX фокусы (рис. 4Б, табл. 2) – это свидетельствует о нарушении радиационного ответа и замедлении (или блокировке) пострадиационной репарации ядерной ДНК.
Таблица 2
Среднее количество фокусов γH2AX на ядро в культуре опухолевых клеток MCF-7, подвергнутых гипертермии и облучению
|
Градусы, время |
Среднее количество фокусов γ H2AX на ядро клетки |
||
|
до облучения |
через 1 ч после облучения (3 Гр) |
через 24 ч после облучения (3 Гр) |
|
|
37 оС (контроль) |
3 ± 2 |
27 ± 6,2 |
4,3 ± 2,5 |
|
42 оС, 90 мин |
14,5 ± 4,1* |
44 ± 9* |
22 ± 5,6** |
|
43 оС, 60 мин |
17 ± 4,6* |
49 ± 11* |
26,4 ± 6** |
|
44 оС, 20 мин |
23,2 ± 5,5** |
54,5 ± 12,1* |
30,2 ± 7** |
* – значимое отличие от соответствующего контроля (37 оС), p<0,05;
** – значимое отличие от соответствующего контроля (37 оС), p<0,01.
Следовательно, незаконченная вовремя репарация ДНК в прогретых и облучённых опухолевых клетках может быть причиной стимуляции их апоптотической гибели, поскольку запускание «самоубийственного» (р53-зависимого) механизма апоптоза является естественным клеточным ответом на сильное повреждение генома [17]. Важный вопрос: как тепловой стресс препятствует нормальной пострадиационной репарации ДНК? Появление γH2AX фокусов в ядрах прогретых клеток ещё до облучения можно объяснить, например, тем, что гипертермия сама вызывает разрывы ДНК (это возможно в условиях сильного прогрева клеток [18]), или тем, что тепловой стресс приводит к аномальной активации киназы АТМ, которая из-за этого начинает фосфорилировать H2AX гистоны также и в тех местах, где нет двунитевых разрывов ДНК, таким образом, увеличивая число «ложных» фокусов (такой механизм тоже описан [18]). Очевидно, что всё это будет замедлять процесс пострадиационной репарации ДНК. Кроме того, согласно опубликованным данным, в опухолевых клетках гипертермия инактивирует основанную на гомологической рекомбинации систему репарации разрывов ДНК, вызывая падение экспрессии и деградацию такого ключевого компонента этой системы как BRCA2 [19].
По нашим наблюдениям, сочетание прогрева и невысоких доз (2-4 Гр) γ-излучения не убивало абсолютно все обработанные клетки, и даже после сильной (44 оС) и продолжительной гипертермии иногда выживало несколько колоний. Это говорит о том, что существует и термо-резистентая система репарации ДНК, которая даёт шанс прогретой и облучённой опухолевой клетке избежать гибели и восстановить пролиферативную активность. Мы полагаем, что такую действующую в злокачественных клетках терморезистентную систему репарации стоит рассматривать как важную терапевтическую мишень, поскольку её ингибирование помогло бы усилить противоопухолевые эффекты гипертермии и облучения. Недавние сообщения других исследователей, где с целью большего воздействия на опухоль предлагается комбинировать гипертермию с ингибиторами участвующих в репарации разрывов ДНК ферментов RAD51, ПАРП [20] и DNA-PKcs [21], говорят в пользу нашего предположения.
Протеотоксичность радиосенсибилизирующей гипертермии коррелирует с интенсивностью пострадиационного апоптоза. Разумеется, помимо инактивации ферментов, непосредственно вовлечённых в репарацию ДНК, гипертермическая обработка клеток вызывает денатурацию и агрегацию самых разных белков в цитоплазме, ядре и органеллах, что сопровождается угнетением клеточного метаболизма, разборкой цитоскелета, ионным дисбалансом, нарушением транспорта биомолекул и пр. [7, 8, 12]. С целью выявления причинноследственных связей в исследуемом феномене мы старались оценить степень протеотоксич-ности при разных условиях прогрева клеток и проверить, как это соотносится с пострадиационным апоптозом.
Для оценки протеотоксичности нами использовался хорошо известный метод с восстановлением активности (ренатурацией) люциферазы в клетках, испытавших тепловой стресс. По относительной скорости ренатурации люциферазы в восстанавливающихся клетках можно судить о степени протеотоксичности применённого теплового воздействия [11]. Рис. 3А демонстрирует ожидаемую корреляцию между температурой гипертермии и замедлением ренатурации люциферазы в клетках HeLa. Также можно заметить существование позитивной корреляции между уровнями протеотоксичности (рис. 3А) и цитотоксичности, когда падение выживаемости (рис. 3Б) и апоптоз (рис. 3В) тоже усиливаются с увеличением температуры прогрева клеток. Похожие результаты получались и на культурах MCF-7 и HT 1080 (не показано). Принято считать, что, хотя люцифераза не влияет на жизнеспособность трансфектантов, динамика ренату-рации этого фермента должна отражать процесс рефолдинга многих термолабильных внутриклеточных белков, среди которых есть и те, что необходимы для выживания стрессированной клетки [11]. Соответственно, тепловая денатурация таких белков и недостаточно быстрая их реактивация при нормальной температуре могут быть факторами, стимулирующими апоптоз в прогретых и облучённых клетках.
В параллельных экспериментах мы оценивали протеотоксические эффекты гипертермии по увеличению уровня агрегированного клеточного белка (табл. 3). Ещё в 90-е годы [12, 13] было обнаружено, что характерной реакцией клеток на тепловой шок и многие другие стрессы является значительное повышение содержания белка в Тритон Х-100-нерастворимой (т.е. ядер-но-цитоскелетной) фракции. Это происходит из-за образования седиментирующих белковых агрегатов и неспецифической ассоциации денатурированных цитозольных белков с нерастворимыми структурами цитоскелета и ядра. На основе этого феномена были разработаны количественные методики, позволяющие определить протеотоксичность того или иного стресса по приросту Тритон Х-100-нерастворимого клеточного белка [12, 13]. Из результатов, приведённых в табл. 3, видно, что уровень агрегированного белка в прогретых клетках возрастал с повышением градусов гипертермии; аналогичная корреляция имела место при увеличении продолжительности тепловой обработки клеток (данные не приводятся). Кроме того, уровень агрегированного клеточного белка коррелировал с интенсивностью апоптоза и падением клоногенного потенциала (табл. 3). Поскольку агрегаты денатурированных белков в цитоплазме и ядре негативно влияют на жизнеспособность стрессированной клетки и наверняка затрудняют её пострадиационное восстановление, мы полагаем, что вызванная гипертермией агрегация цитозольных и ядерных белков должна быть мощным стимулом к запусканию апоптотического механизма.
Здесь важно подчеркнуть, что агрегацию белков в прогреваемой клетке можно дополнительно усилить, изменяя рН или подавляя энергетический метаболизм [12, 13], а также используя специальные фармакологические агенты, такие как ингибиторы активности и экспрессии БТШ [11]. Кроме того, представляется реальным заблокировать клеточные механизмы избавления от денатурированных белков, применяя ингибиторы деградации белковых молекул в лизосомах и протеасомах, и это тоже приведёт к увеличению уровня агрегированного белка в ци- топлазме. Вероятно, такая искусственная стимуляция белковой агрегации в прогретых опухолях будет усиливать радиосенсибилизирующие эффекты гипертермии, и в будущем мы планируем проверить это экспериментально.
Таблица 3
Агрегация цитозольного белка и вовлечение в нее БТШ90, БТШ70 и БТШ27 в опухолевых клетках HeLa, испытавших гипертермическую обработку
|
Градусы, время |
Относительное содержание белка и отдельных БТШ в Тритон Х-100-нерастворимой фракции |
|||
|
тотальный белок |
БТШ90 |
БТШ70 |
БТШ27 |
|
|
37 оС (контроль) |
1 |
1 |
1 |
1 |
|
42 оС, 90 мин |
1,35 ± 0,07* |
1,65 ± 0,09* |
1,5 ± 0,08* |
1,6 ± 0,08* |
|
43 оС, 60 мин |
1,5 ± 0,09* |
2,8 ± 0,2** |
2,65 ± 0,2** |
2,4 ± 0,18** |
|
4 4 оС, 20 мин |
1,85 ± 0,1** |
3,5 ± 0,28** |
3,1 ± 0,25** |
3,2 ± 0,27** |
* – значимое отличие от соответствующего контроля (37 оС), p<0,05;
** – значимое отличие от соответствующего контроля (37 оС), p<0,01.
Гипертермия, стимулирующая пострадиационный апоптоз, истощает цитозольный пул молекулярных шаперонов. Хорошо известно, что основные молекулярные шапероны эукариот – БТШ90, БТШ70 и БТШ27 – являются эндогенными супрессорами апоптоза, причём эта активность обусловлена, главным образом, их способностью специфически взаимодействовать с компонентами апоптотического сигнального каскада и, тем самым, прерывать его [22]. С другой стороны, БТШ играют ключевую роль в клеточном ответе на протеотоксиче-ский стресс. Соответственно, мы постарались исследовать реакцию БТШ90, БТШ70 и БТШ27 в опухолевых клетках, подвергнутых радиосенсибилизирующей гипертермии.
37 о С 42 о С 43 о С 44 о С
БТШ90
цитозольная фракция ядро/цитоскелет/агрегаты
37 о С 42 о С 43 о С 44 о С
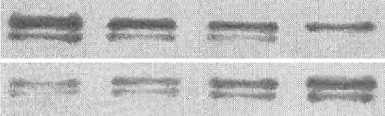
БТШ70
цитозольная фракция ядро/цитоскелет/агрегаты
37 о С 42 о С 43 о С 44 о С
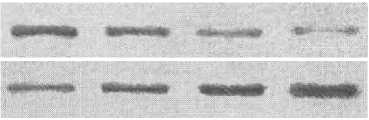
БТШ27
цитозольная фракция ядро/цитоскелет/агрегаты
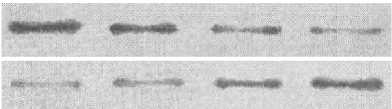
Рис. 5. Фрагменты блотов, показывающие взаимосвязь между температурой гипертермической обработки клеток HeLa и истощением цитозольного пула БТШ90, БТШ70 и БТШ27 из-за их транслокации в ядерно-цитоскелетные компартменты и соагрегации с денатурированными белками. Клетки подвергали 30-минутному прогреву при указанной температуре, после чего фракционировали с помощью Тритон Х-100-содержащего буфера и центрифугирования для последующего анализа иммуноблоттингом (см. также табл. 3).
Данные, приведённые на рис. 5 и в табл. 3, показывают, что гипертермическая обработка клеток приводит к истощению пула шаперонов в цитозольной (Тритон Х-100-экстрагируемой) фракции и соответствующему увеличению их содержания в ядерно-цитоскелетной (Тритон Х-100-неэкстрагируемой) клеточной фракции, где оказываются все крупные белковые агрегаты. Очевидно, это происходит из-за связывания (и соагрегации) шаперонов с их естественными субстратами – термоденатурированными клеточными белками в цитоплазме, ядре и цитоске-летных структурах. По нашим наблюдениям, степень истощения цитозольного пула БТШ90, БТШ70 и БТШ27 (т.е. их «инсолюбилизация») в прогреваемых опухолевых клетках заметно увеличивалась с повышением температуры и позитивно коррелировала с приростом агрегированного белка и интенсивностью пострадиационного апоптоза (рис. 5, табл. 3 и табл. 1). В совокупности, полученные данные дают нам основания рассматривать цитозольный уровень шаперонов как важную детерминанту, от которой может зависеть дальнейшая судьба (выживание или гибель) стрессированной клетки.
Возникают интересные вопросы: почему спровоцированный гипертермией дефицит молекулярных шаперонов в цитозоле способствует пострадиационному апоптозу и возможно ли целенаправленно повлиять на субклеточную локализацию БТШ, чтобы усилить апоптотическую гибель прогретых и облучённых опухолевых клеток? Мы предполагаем, что в испытавшей тепловой стресс клетке возникает своего рода конкуренция между субстратами за связывание с шаперонами. В условиях гипертермии, когда происходит денатурация многих клеточных белков, большая часть шаперонов (БТШ) оказывается рекрутирована в комплексы и агрегаты с этими термоденатурированными белками и, таким образом, уходит из цитозоля. Соответственно, при возникшем дефиците шаперонов их не хватает, чтобы нейтрализовать эффекторы апоптотиче-ского сигнального каскада (например, Apaf-1 или цитохром Ц [22]) и блокировать каспазазави-симый апоптоз, который запускается в облучённой клетке в ответ на повреждения ДНК.
Что касается возможности влияния на уровень цитозольных шаперонов, этот вопрос заслуживает отдельного серьёзного изучения. Ранее, в качестве одного из потенциальных подходов мы описали комбинирование гипертермии с ингибиторами шаперонной активности БТШ90 и ингибиторами индукции БТШ [11]. Наверное, существуют и другие перспективные комбинации, например, с агентами, блокирующими деградацию клеточных белков или усиливающими их агрегацию (см. предыдущий раздел), что приведёт к ещё большей «занятости» цитозольных шаперонов другими субстратами и, следовательно, к снятию БТШ-опосредованной блокады с каскада проапоптотических сигналов. На наш взгляд, всю АТФ-зависимую шаперонную машине-рию злокачественной клетки следует рассматривать как комплексную мишень для противораковой терапии, и необходимы дальнейшие системные и сфокусированные исследования, чтобы разработать клинически применимые способы инактивации опухолевых БТШ.
Заключение
Используя экспериментальные модели с 4-мя линиями опухолевых клеток разного происхождения, мы показали, что (1) радиосенсибилизирующие эффекты гипертермии обусловлены стимуляцией каспазазависимого апоптоза, что наблюдалось даже в карциномных и саркомных клетках, для которых апоптоз не является характерной формой пострадиационной гибели;
-
(2 ) триггером такого апоптотического механизма становится, по-видимому, спровоцированное гипертермией нарушение клеточной реакции на разрывы ядерной ДНК; (3) вызываемая гипертермией агрегация внутриклеточных белков и связанное с этим истощение цитозольного пула БТШ90, БТШ70 и БТШ27 представляются критическими событиями для выживания облучённой раковой клетки.
На основе полученных нами данных и фактов, описанных другими исследователями, мы наметили потенциальные подходы и молекулярные мишени, которые позволили бы усилить радиосенсибилизирующие эффекты гипертермии. По нашему мнению, терморезистентные ферменты репарации ДНК, клеточные системы деградации белков, БТШ и другие компоненты шаперонной машины заслуживают пристального внимания в качестве перспективных мишеней для дополнительного терапевтического воздействия на злокачественную опухоль.
Данная работа проводилась в рамках выполнения тем государственного задания МРНЦ им. А.Ф. Цыба - филиала ФГБУ «НМИЦ радиологии» Минздрава России за 2015-2016 гг. и первую половину 2017 г., промежуточные итоги выполнения которых нашли отражение в обобщающей публикации [23].
Список литературы Апоптоз в опухолевых клетках, подвергнутых сочетанному действию гипертермии и облучения: исследование молекулярных механизмов и мишеней
- Курпешев О.К. Возможности и перспективы использования гипертермии в медицине//Клиническая медицина. 1996. № 1. С. 14-16.
- Курпешев О.К., Андреев В.Г., Панкратов В.А., Гулидов И.А., Орлова А.В. Сравнительные результаты консервативной химиолучевой и термохимиолучевой терапии местно-распространённого рака гортани//Вопросы онкологии. 2014. Т. 60, № 5. С. 602-606.
- Datta N.R., Ordonez S.G., Gaipl U.S., Paulides M.M., Crezee H., Gellermann J., Marder D., Puric E., Bodis S. Local hyperthermia combined with radiotherapy and-/or chemotherapy: recent advances and promises for the future//Cancer Treat. Rev. 2015. V. 41, N 9. P. 742-753.
- Курпешев О.K., van der Zee J. Локорегионарная гипертермия злокачественных опухолей: методики, термометрия, аппаратура//Медицинская радиология и радиационная безопасность. 2017. № 5. С. 52-63.
- Ohguri T. Current status of clinical evidence for electromagnetic hyperthermia on prospective trials//Thermal Med. 2015. V. 31, N 2. P. 5-12.
- Курпешев О.К., Рагулин Ю.А., Мозеров С.А., Орлова А.В., Лебедева Т.В. Возможности локальной гипертермии при лечении больных отёчной формой рака молочной железы//Вопросы онкологии. 2016. № 5. С. 680-687.
- Курпешев О.К. Закономерности радиосенсибилизирующего и повреждающего эффектов гипертермии на нормальные и опухолевые ткани (экспериментально-клиническое исследование): автореф. дис. … докт. мед. наук. Обнинск, 1989. 35 с.
- Hyperthermic oncology from bench to bedside/Eds.: S. Kokura, T. Yoshikawa, T. Ohnishi. Springer, 2016. 444 p.
- Kabakov A.E., Gabai V.L. Cell death and survival assays//Methods Mol. Biol. 2018. V. 1709. P. 107-127.
- Sharma A., Singh K., Almasan A. Histone H2AX phosphorylation: a marker for DNA damage//Methods Mol. Biol. 2012. V. 920. P. 613-626.
- Кудрявцев В.А., Макарова Ю.М., Кабаков А.Е. Термосенсибилизация опухолевых клеток ингибиторами активности и экспрессии шаперонов//Биомедицинская химия. 2012. Т. 58, № 6. С. 662-672.
- Kabakov A.E., Gabai V.L. Protein aggregation as primary and characteristic cell reaction to various stresses//Experientia. 1993. V. 49, N 8. P. 706-713.
- Kabakov A.E., Gabai V.L. Stress-induced insolubilization of certain proteins in ascites tumor cells//Arch. Biochem. Biophys. 1994. V. 309, N 2. P. 247-253.
- Schmitt C.A. Cellular senescence and cancer treatment//Biochimica et Biophysica Acta (BBA) -Reviews on Cancer. 2007. V. 1775. P. 5-20.
- O’Callaghan-Sunol C., Gabai V.L. Involvement of heat shock proteins in protection of tumor cells from genotoxic stresses. A chapter in: Heat shock proteins in cancer/Eds.: S.K. Calderwood, M.Y. Sherman, D.R. Ciocca. Springer, 2007. P. 169-189.
- Koff J.L., Ramachandiran S., Bernal-Mizrachi L. A time to kill: targeting apoptosis in cancer//Int. J. Mol. Sci. 2015. V. 16. P. 2942-2955.
- Balcer-Kubiczek E.K. Apoptosis in radiation therapy: a double-edged sword//Exp. Oncol. 2012. V. 34, N 3. P. 277-285.
- Pandita T.K., Pandita S., Bhaumik S.R. Molecular parameters of hyperthermia for radiosensitization//Crit. Rev. Eukaryot. Gene Expr. 2009. V. 19, N 3. P. 235-251.
- van den Tempel N., Laffeber C., Odijk H., van Cappelen W.A., van Rhoon G.C., Franckena M., Kanaar R. The effect of thermal dose on hyperthermia-mediated inhibition of DNA repair through homologous recombination//Oncotarget. 2017 DOI: 10.18632/oncotarget.17861
- Takahashi A., Mori E., Nakagawa Y., Kajihara A., Kirita T., Pittman D.L., Hasegawa M., Ohnishi T. Homologous recombination preferentially repairs heat-induced DNA double-strand breaks in mammalian cells//Int. J. Hyperthermia. 2017 DOI: 10.1080/02656736.2016.1252989
- van Oorschot B., Granata G., Di Franco S., Ten Cate R., Rodermond H.M., Todaro M., Medema J.P., Franken N.A. Targeting DNA double strand break repair with hyperthermia and DNA-PKcs inhibition to enhance the effect of radiation treatment//Oncotarget. 2016. V. 7, N 40. P. 65504-65513.
- Kennedy D., Jager R., Mosser D.D., Samali A. Regulation of apoptosis by heat shock proteins//IUBMB Life. 2014. V. 66, N 5. P. 327-338.
- Каприн А.Д., Галкин В.Н., Жаворонков Л.П., Иванов В.К., Иванов С.А., Романко Ю.С. Синтез фундаментальных и прикладных исследований -основа обеспечения высокого уровня научных результатов и внедрения их в медицинскую практику//Радиация и риск. 2017. Т. 26. № 2. С. 26-40.


