Аргоноплазменная коагуляция в лечении пациентов с хроническим лучевым проктитом, осложненным кровотечением
Автор: Кольцов В.А., Мусинов И.М., Алиева И.Р.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.19, 2024 года.
Бесплатный доступ
Обоснование: хронический лучевой проктит является осложнением дистанционной лучевой терапии, применяемой для лечения злокачественных новообразований малого таза, и часто осложняется развитием ректальных кровотечений. Аргоноплазменная коагуляция является одним из доступных эндоскопических методов их лечения, однако эффективность её применения нуждается в изучении.Цель: Оценить эффективность применения эндоскопической аргоноплазменной коагуляции для устранения телангиоэктазий прямой кишки у пациентов с хроническим лучевым проктитом, осложненным кровотечением, и представить посекторальную классификацию поражения слизистой оболочки прямой кишки телангиоэктазиями.Материалы и методы: представлены результаты лечения 18 пациентов с хроническим лучевым проктитом, которым была выполнена аргоноплазменная коагуляция телангиоэктазий слизистой оболочки прямой кишки с целью остановки кровотечений и профилактики их возникновения. Для оценки эффективности лечения была применена посекторальная классификация поражения прямой кишки.Результаты: после проведенной аргоноплазменной коагуляции телангиоэктазий слизистой оболочки прямой кишки у всех пациентов отсутствовали прямокишечные кровотечения в течение 6 месяцев. У 13 (72%) больных отмечалось резкое снижение частоты выделения крови при дефекации, у остальных 5 (28%) пациентов отсутствовало выделение крови из прямой кишки. В послеоперационном периоде наблюдали два рецидива кровотечения из места обработки на вторые и седьмые сутки послеоперационного периода, что потребовало повторного применения аргоноплазменной коагуляции.Заключение: Проведение эндоскопической аргоноплазменной коагуляции эффективно для устранения телангиоэктазий у пациентов с хроническим лучевым проктитом, осложненным кровотечением. Представленная посекторальная классификация поражения прямой кишки при хроническом лучевом проктите удобна в применении и способствует оценке изменений слизистой оболочки прямой кишки в динамике.
Хронический лучевой проктит, аргоноплазменная коагуляция, ректальные кровотечение, телангиоэктазии, лучевая терапия
Короткий адрес: https://sciup.org/140308256
IDR: 140308256 | DOI: 10.25881/20728255_2024_19_4_58
Argonoplasmic coagulation in the treatment of chronic radiation proctitis complicated by bleeding
Rationale: Chronic radiation proctitis is a complication of remote radiation therapy used to treat malignant neoplasms of the pelvis, and is often complicated by the development of rectal bleeding. Argonoplasmic coagulation is one of the available endoscopic methods of their treatment, but the effectiveness of its use needs to be studied.Objective: To evaluate the effectiveness of endoscopic argonoplasmic coagulation to eliminate telangiectasias of the rectal mucosa in patients with chronic radiation proctitis complicated by bleeding, and to present a sectoral classification of lesions of the rectal mucosa with telangiectasias.Methods: The article presents the results of treatment of 18 patients with chronic radiation proctitis who underwent argonoplasmic coagulation of telangiectasias of the mucous membrane of the rectum in order to stop bleeding and prevent their occurrence. To assess the effectiveness of treatment, a sectoral classification of the rectal lesion was applied.Results: After argonoplasmic coagulation of telangiectasia of the rectal mucosa, all patients had no rectal bleeding for 6 months. In 13 (72%) patients, there was a sharp decrease in the frequency of blood excretion during defecation, in the remaining 5 (28%) patients there was no blood excretion from the rectum. In the postoperative period, two recurrence of bleeding from the treatment site was observed on the second and seventh days of the postoperative period, which required repeated application of argonoplasmic coagulation.Conclusion: Endoscopic argonoplasmic coagulation is effective in eliminating telangiectasia in patients with chronic radiation proctitis complicated by bleeding. The presented sectoral classification of rectal lesions in chronic radiation proctitis is convenient to use and contributes to the assessment of changes in the mucous membrane of the rectum in dynamics.
Текст научной статьи Аргоноплазменная коагуляция в лечении пациентов с хроническим лучевым проктитом, осложненным кровотечением
Количество пациентов, получающих дистанционную лучевую терапию, брахитерапию или их сочетание является эффективным методом лечения злокачественных образований малого таза [1]. Лучевая терапия у этих больных сопровождается риском развития осложнений, возникновение которых зависит от суммарной общей дозы излучения (СОД), полученной при лечении [2; 3]. Одним из осложнений лучевой терапии является лучевой проктит, протекающий в острой или в хронической форме. Острый лучевой проктит, как правило, требует симптоматического лечения и самостоятельно проходит после окончания лучевой терапии. Хроническая форма лучевого проктита (ХЛП) встречается в 5–20% случаев, сопровождается развитием стриктур, образованием свищей, выделением крови при дефекации, часто осложняется кровотечением и приводит к анемии различной степени тяжести [4; 5]. Медикаментозное лечение его не всегда эффективно, так как не устраняет телангиоэкта-зии слизистой оболочки, которые являются субстратом кровотечений [6; 7].
Цель исследования: оценить эффективность применения эндоскопической аргоноплазменной коагуляции (АПК) для устранения телангиоэктазий прямой кишки у пациентов с ХЛП, осложненным кровотечением, и представить посекторальную классификацию поражения слизистой оболочки прямой кишки телан-гиоэктазиями.

Материалы и методы
АПК выполнена 18 больным с ХЛП, осложненным кровотечением, которые находились на лечении в СПб ГБУЗ «Городская больница №9» в 2023 и 2024 гг.
У 6 (33%) больных АПК была проведена по поводу активного кровотечения, у 12 (67%) пациентов – с ректальным кровотечением в анамнезе с целью их профилактики. Средний возраст больных составил 73±6,5 года. Мужчин было 13 (72%) человек, женщин – 5 (28%) человек. Показаниями к лучевой терапии были: рак предстательной железы – 12 (67%) случаев, рак влагалища – 3 (17%) случая, рак шейки матки – 2 (11%) случая и в одном случае рак прямой кишки. СОД облучения была от 46 Гр до 80 Гр (65 Гр±11,5). Первые эпизоды кровотечения отмечались через 7–13 месяцев после проведения лучевой терапии. Контрольный эндоскопический осмотр прямой кишки проводился через 3 месяца после первичной АПК. У 4 (22%) больных АПК проведена повторно для устранения оставшихся ангиоэктазий в плановом порядке через 3 месяца.
Для более точной локализации поражения прямой кишки использовали собственную посекторальную оценку телангиоэктазий прямой кишки, включающую количество телангиоэктазий и наличие сливных телангиоэктазий на сектор слизистой прямой кишки. Преимущество классификации в том, что есть возможность понять локализацию и площадь поражения телангиоэктазиями слизистой прямой кишки, а также спрогнозировать объем обработки слизистой оболочки и оценить результаты лечения при динамическом наблюдении.
Исследование проводилось на левом боку. Окружность прямой кишки условно делили на 4 сектора с буквенными обозначениями, где передняя стенка (A), левая стенка (B), задняя стенка (C), правая стенка (D). Каждый сектор оценивается по трем степеням поражения, где 0 степень соответствует отсутствию телангиоэктазий, 1 степень – до 6 телангиоэктазий, не сливающихся между собой, 2 степень – более 6 те-лангиоэктазий или наличие одного участка сливных телангиоэктазий, 3 степень – более 10 телангиоэктазий или 2–3 сливных участка. При отсутствии изменений на слизистой оболочке данный сектор не выносился в заключение (Рис. 1; 2).
Перед плановой операцией назначались препараты 5-ацетилсалициловой кислоты (5-АСК) ректально для снижения воспалительных изменений прямой кишки. У 5 (28%) больных оперативное вмешательство проводили под внутривенной анестезией, у остальных пациентов без нее. Во время операции применяли инсуфляцию углекислого газа. Для работы использовали эндоскопы Olympus 180/190 серии и электрохирургическую установку Erbe 300D с режимом Forced APC 36–38 W и потоком аргона 1,0–1,2 л/мин. Для ко-
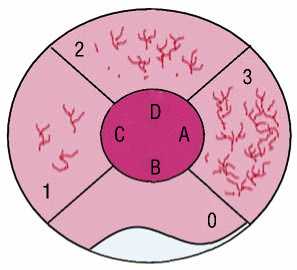
Рис. 1. Cхема посекторальной классификации ХЛП.
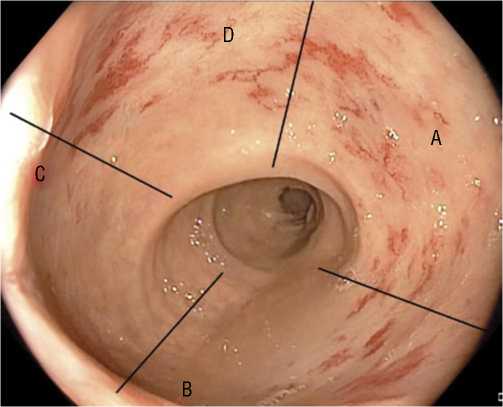
Рис. 2. Эндоскопическая фотография. Слизистая прямой кишки поражена на 3 степень по передней стенке, на 2 степень по левой стенке и на 2 степень по правой стенке. Заключение: ХЛП (A3B2D2).
агуляции применяли зонд APC прямого или бокового типов. На эндоскоп всегда монтировали прозрачный дистальный колпачок. При болевых ощущениях у пациента использовали инъекцию 0,9% изотонического раствора натрия хлорида в подслизистый слой прямой кишки. АПК телангиоэктазий проводили с максимальным сохранением неизмененной слизистой оболочки, не оставляя при обработке дистальные ветви телангиоэктазий. У пациентов с первой и второй степенью поражения стремились обработать телангиоэктазии в максимальном объеме (Рис. 3). При третьей степени обрабатывали только крупные телангиоэктазии и явный источник активного или состоявшегося кровотечения.
После операции пациентам назначались свечи 5-АСК и свечи Метилурацил сроком на 3 месяца, порошок Му-кофальк сроком на 1 месяц.

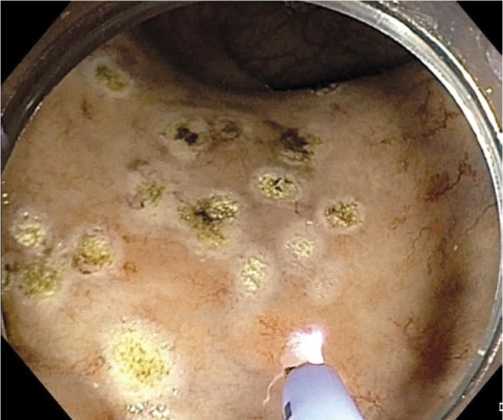
Рис. 3. Эндоскопическая фотография. Телангиоэктазии после обработки АПК.
Табл. 1. Степень поражения прямой кишки при первичном осмотре и через 3 месяца после проведенной АПК
|
Стенка |
Степень |
До лечения |
Через 3 месяца |
|
А |
1 |
5 (28%) |
3 (17%) |
|
2 |
6 (33%) |
7 (39%) |
|
|
3 |
7(39%) |
4 (22%) |
|
|
всего |
18 (100%) |
14 (78%) |
|
|
B |
1 |
7 (39%) |
4 (22%) |
|
2 |
6 (33%) |
4 (22%) |
|
|
3 |
3 (17%) |
2 (11%) |
|
|
всего |
16 (89%) |
10 (55%) |
|
|
C |
1 |
6 (33%) |
3 (17%) |
|
2 |
– |
1 (5%) |
|
|
3 |
3 (17%) |
2 (11%) |
|
|
всего |
9 (50%) |
6 (33 %) |
|
|
D |
1 |
4 (22%) |
2 (11%) |
|
2 |
3 (17%) |
3 (17%) |
|
|
3 |
5 (28%) |
3 (17%) |
|
|
всего |
12 (67%) |
8 (45%) |
Результаты и обсуждение
После проведенной АПК у всех пациентов отсутствовали прямокишечные кровотечения в течение 6 месяцев. У 13 (72%) больных отмечалось резкое снижение частоты выделения крови при дефекации, у остальных 5 (28%) пациентов отсутствовало выделение крови из прямой кишки. У пролеченных пациентов передняя стенка поражалась в 100% случаев, левая – в 89% случаев, задняя – в 50% случаев, правая – в 67% случаев. В раннем послеоперационном периоде после проведенной АПК наблюдали два рецидива кровотечения из места обработки на вторые и седьмые сутки послеоперационного периода, что потребовало повторного применения АПК. Других осложнений в послеоперационном периоде не наблюдалось.
При повторном эндоскопическом осмотре через 3 месяца оценивали результат лечения, применяя посек-торальную классификацию. Отмечалась положительная динамика с уменьшением степени поражения, что позволяет сделать вывод об эффективности применения АПК в лечении ХЛП (табл. 1).
При контрольных осмотрах после применения АПК определялись оставшиеся телангиоэктазии, рубцовая деформация и грануляционная ткань слизистой оболочки обработанных участков, а также единичные поверхностные эпителизирующиеся дефекты слизистой оболочки (Рис. 4).
Результаты исследования позволяют считать режим Forced APC 36–38 W с потоком 1,0–1,2 л/мин. безопасным для обработки телеангиоэктазий прямой кишки. При этом целесообразно использовать селективную обработку телангиоэктазий, без повреждения неизмененной слизистой оболочки прямой кишки.
Важно обработать конечные ветви телангиоэктазий, которые могут явиться источником повторного кро-
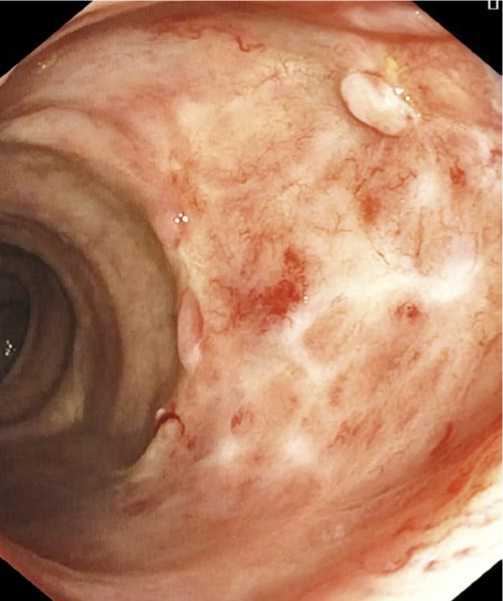
Рис. 4. Эндоскопическая фотография, больной С. ХЛП (А2). Слизистая через 3 месяца после проведенной АРС.
вотечения. В зависимости от оставшегося поражения телангиоэктазиями слизистой прямой кишки решается вопрос о проведение повторной операции через 3–6 месяцев. При тяжелом поражении телангиоэктазиями прямой кишки (A3B3C3D3) предпочтительно провести поэтапное лечение с помощью АПК, начиная с крупных телангиоэктазий.
Заключение
Проведение эндоскопической АПК эффективно для устранения телеангиоэктазий у пациентов с ХЛП, осложненным кровотечением. Представленная посек-торальная классификация поражения прямой кишки при ХЛП удобна в применении и способствует оценке изменений слизистой оболочки прямой кишки в динамике.
Список литературы Аргоноплазменная коагуляция в лечении пациентов с хроническим лучевым проктитом, осложненным кровотечением
- Dahiya DS, Kichloo A, Tuma F, Albosta M, Wani F. Radiation Proctitis and Management Strategies. Clin Endosc. 2022; 55(1): 22-32. DOI: 10.5946/ce.2020.288 EDN: ICWEWQ
- Корытов О.В. Влияние поздних лучевых осложнений на качество жизни и отдаленную выживаемость пациентов, получавших облучение органов малого таза // Российский биотерапевтический журнал. - 2022. - Т.21. - №2. - С.67-72. DOI: 10.17650/1726-9784-2022-21-2-67-72 EDN: AHSPII
- Im CM, Cho IJ, Yu HJ, et al. Clinical outcome and risk factors of chronic radiation proctitis following pelvic radiation therapy. Anticancer Res. 2022; 42(12): 5951-5959. DOI: 10.21873/anticanres.16105 EDN: EOKTMP
- Weiner JP, Wong AT, Schwartz D, et al. Endoscopic and non-endoscopic approaches for the management of radiation-induced rectal bleeding. World J. Gastrointest. Endosc. 2016; 22(31): 6972-6986. 10.3748/ wjg.v22.i31.6972. DOI: 10.3748/wjg.v22.i31.6972 EDN: TROMHY
- Yuan ZX, Qin QY, Zhu MM, et al. Diverting colostomy is an effective and reversible option for severe hemorrhagic radiation proctopathy. World J Gastroenterol. 2020; 26(8): 850-864. DOI: 10.3748/wjg.v26.i8.850 EDN: UIMBNM
- Lee JK, Agrawal D, Thosani N, et al. ASGE guideline on the role of endoscopy for bleeding from chronic radiation proctopathy. Gastroinest. Endosc. 2019; 90(2): 171-182. DOI: 10.1016/j.gie.2019.04.234
- Ramakrishnaiah NV, Krishnamachar S. Chronic haemorrhagic radiation proctitis: A review. World J. Gastrointest. Surg. 2016; 8(7): 483-491. DOI: 10.4240/wjgs.v8.i7.483


