Артериальная реваскуляризация миокарда с использованием y-композитных конструкций и in situ кондуитов внутренних грудных артерий: непосредственные результаты
Автор: Сабетов Азат Керимбекович, Сирота Д.А., Хван Д.С., Жульков М.О., Чернявский А.М.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ишемическая болезнь сердца
Статья в выпуске: 4 т.24, 2020 года.
Бесплатный доступ
Цель. Изучить непосредственные результаты аутоартериальной реваскуляризации с использованием Y-композитных и in situ кондуитов внутренних грудных артерий. Методы. В исследование включено 76 пациентов с ишемической болезнью сердца, которым было выполнено коронарное шунтирование с марта 2018 г. по март 2020 г. Были отобраны 2 группы пациентов: в первой группе использовали аутоартериальные кондуиты из внутренней грудной артерии по методике in situ (n = 39); во второй группе использовали аутоартериальные кондуиты с формированием Y-композитной конструкции из внутренних грудных артерий (n = 37). Результаты. Общая характеристика и частота встречаемости послеоперационных осложнений по большинству событий были сопоставимы в обеих группах. В первой группе применение искусственного кровообращения было достоверно чаще, чем во второй- 28,2 и 3,0 % соответственно, p
Аутоартериальная реваскуляризация миокарда, бимаммарное коронарное шунтирование, ишемическая болезнь сердца
Короткий адрес: https://sciup.org/142230768
IDR: 142230768 | DOI: 10.21688/1681-3472-2020-4-63-71
Arterial revascularisation using in situ or Y-composite conduits of internal thoracic arteries: early results
Aim. This study aimed to research the early results of arterial revascularisation using in situ or Y-composite conduits of internal thoracic arteries. Methods. The study included 76 patients with coronary heart disease who underwent coronary artery bypass surgery between March 2018 and March 2020. Two groups of patients were selected. In the first group, autoarterial conduits from the internal thoracic arteries were used according to the in situ technique (n = 39). In the second group, autoarterial conduits were used with the formation of a Y-composite structure from the internal thoracic arteries (n = 37). Results. The general characteristics and frequency of postoperative complications for most events were comparable in both groups. The usage of on-pump coronary artery bypass graft was significantly more frequent in the in situ group than in the Y-composite group (28.2 and 3.0 %, respectively; p
Текст научной статьи Артериальная реваскуляризация миокарда с использованием y-композитных конструкций и in situ кондуитов внутренних грудных артерий: непосредственные результаты
Сабетов А.К., Сирота Д.А., Хван Д.С., Жульков М.О., Чернявский А.М. Артериальная реваскуляризация миокарда с использованием Y-композитных конструкций и in situ кондуитов внутренних грудных артерий: непосредственные результаты. Патология кровообращения и кардиохирургия. 2020;24(4): 63-71. http:// org/10.21688/1681-3472-2020-4-63-71
Д.А. Сирота, https://orcid.
Д.С. Хван,
М.О. Жульков, 0000-0001-7976-596X
А.М. Чернявский, https://orcid.
org/0000-0001-9818-8678
М.О. Жульков, А.М. Чернявский, 2020
Статья открытого доступа, распространяется по лицензии Creative Commons Attribution 4.0 .
А.К. Сабетов, Д.А. Сирота, Д.С. Хван, М.О. Жульков, А.М. Чернявский
Федеральное государственное бюджетное учреждение
«Национальный медицинский исследовательский центр имени академика Е.Н. Мешалкина» Министерства здравоохранения Российской Федерации, Новосибирск, Российская Федерация
Цель. Изучить непосредственные результаты аутоартериальной реваскуляризации с использованием Y-композитных и in situ кондуитов внутренних грудных артерий.
Методы. В исследование включено 76 пациентов с ишемической болезнью сердца, которым было выполнено коронарное шунтирование с марта 2018 г. по март 2020 г. Были отобраны 2 группы пациентов: в первой группе использовали аутоартериальные кондуиты из внутренней грудной артерии по методике in situ (n = 39); во второй группе использовали аутоартериальные кондуиты с формированием Y-композитной конструкции из внутренних грудных артерий (n = 37).
Результаты. Общая характеристика и частота встречаемости послеоперационных осложнений по большинству событий были сопоставимы в обеих группах. В первой группе применение искус-ственногокровообращениябылодостоверночаще,чемвовторой— 28,2 и 3,0 % соответственно, p < 0,003. Продолжительность инотропной поддержки была значительно меньше в первой группе и составила 3,72 ± 8,60 против 8,0 ± 9,6 во второй, p < 0,007. По основным неблагоприятным сердечным и мозговым событиям достоверной разницы не получено в госпитальном периоде наблюдения. Заключение. Низкая частота периоперационных осложнений, отсутствие периоперационных инфарктов миокарда и госпитальной летальности демонстрируют безопасность бимаммарного коронарного шунтирования. Несмотря на отсутствие разницы в раннем послеоперационном периоде мы ожидаем, что в отдаленном периоде будет статистически значимая разница по основным неблагоприятным сердечно-сосудистым событиям между Y-композитными конструкциями и in situ кондуитов из внутренних грудных артерий.
Актуальность
Несмотря на достижения современной медицины, внедрение новых лекарственных средств и хирургических методов лечения, сердечно-сосудистые заболевания являются основной причиной смертности в США, Европе и странах СНГ. По данным Всемирной организации здравоохранения, смертность от сердечно-сосудистых заболеваний составляет 31 % и является наиболее частой причиной смертельных исходов во всем мире. На территории Российской Федерации этот показатель составляет 57,1 %, из которых на долю ишемической болезни сердца выпадает более половины всех случаев (28,9 %), что составляет 385,6 на 100 тыс. населения в год. Для сравнения: смертность от той же причины на территории Евросоюза составляет 95,9 на 100 тыс. населения в год, что в 4 раза меньше, чем в нашей стране [1].
Аортокоронарное шунтирование является одной из самых распространенных операций по всему миру с доказанной отдаленной эффективностью при лечении ишемической болезни сердца [2; 3]. Тем не менее стандартное коронарное шунтирование с использованием аутовенозных кондуитов имеет ряд существенных недостатков, таких как неудовлетворительная отдаленная проходимость аутовенозных кондуитов, свобода от больших неблагоприятных сердечно-сосудистых событий и повторных коронарных вмешательств, выживаемость [4; 5].
Так, при использовании аутовенозных кондуитов 10-летняя проходимость шунтов не превышает 40–50 %, что требует выполнения повторных вмешательств, приводит к потере трудоспособности и снижению качества жизни [6]. Применение аутоартериальных кондуитов, в особенности внутренней грудной артерии (ВГА), позволяет снизить эти риски, поскольку доказанная отдаленная проходимость через 10–15 лет составляет в среднем 95 % [7].
Это обусловлено тем фактом, что ВГА редко подвергается атеросклеротическому поражению. Такая толерантность к развитию атеросклероза обусловлена наличием непрерывной внутренней эластической мембраны, которая препятствует миграции гладкомышечных клеток из медии в интиму. Еще одна причина длительного функционирования ВГА — это повышенное продуцирование эндотелием простациклина и оксида азота, сильных вазодилататоров и ингибиторов функциональ- ной активности тромбоцитов [8; 9]. Кроме того, при прогрессировании атеросклероза в нативных коронарных артериях шунты из ВГА in situ способны адаптироваться к условиям коронарного кровотока, что также улучшает отдаленный прогноз [10].
Использование данного аутоартериального кондуита является «золотым стандартом» в коронарной хирургии. Тотальное аутоартериальное шунтирование получает все большее распространение, в том числе бимаммарное шунтирование, однако выполняется лишь в небольшом количестве сердечно-сосудистых центров. Его распространенность ограничивается опасениями некоторых хирургов по поводу более высокого количества осложнений со стороны операционной раны, длительности операции и количества периоперационных осложнений [5; 11]. Кроме того, факторами являются техническая сложность выполнения артериальных конструкций и отсутствие достаточной доказательной базы по основным подходам к аутоартериальному шунтированию.
Цель — изучить непосредственные результаты аутоартериальной реваскуляризации с использованием Y-композитных и in situ кондуитов внутренних грудных артерий.
Методы
Было организовано простое слепое проспективное рандомизированное исследование по изучению аутоартериальной реваскуляризации с использованием Y-композитных и in situ кондуитов. В исследование включили 76 пациентов с ишемической болезнью сердца, которым было выполнено коронарное шунтирование с марта 2018 г. по март 2020 г. Пациентов рандомизировали при помощи метода конвертов на 2 группы: в первой группе использовали аутоартериальные кондуиты из ВГА по методике in situ (n = 39); во второй группе использовали аутоартериальные кондуиты с формированием Y-композитной конструкции из внутренних грудных артерий (n = 37) (рисунок) .
При изучении непосредственных результатов лечения за основные конечные точки исследования брали кардиоваскулярную смерть, острый инфаркт миокарда, инсульт и повторную реваскуляризацию до выписки из стационара.
Критерии включения: возраст 25–70 лет, многососудистое поражение коронарных артерий с поражением бассейна левой коронарной арте-
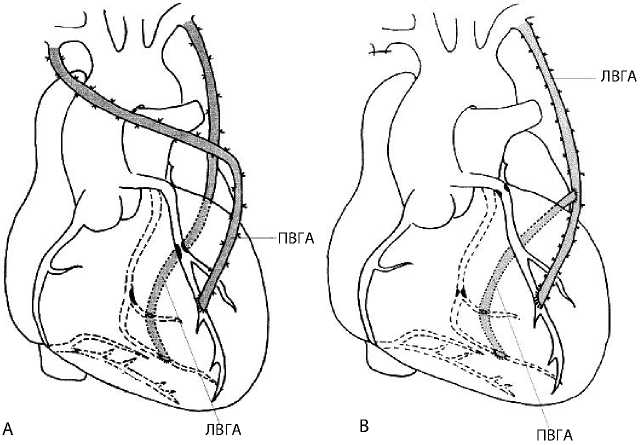
Схема использования внутренних грудных артерий методом in situ (А) или Y-композитной конструкции (В)
Примечание.
ПВГА — правая внутренняя грудная артерия;
ЛВГА — левая внутренняя грудная артерия
рии, стабильная стенокардия напряжения II–IV функционального класса по классификации Канадского сердечно-сосудистого общества (англ. Canadian Cardiovascular Society, CCS), атеросклеротическое поражение коронарной артерии с подтвержденной ишемией миокарда, согласие пациента на исследование.
Критерии исключения: необходимость экстренной реваскуляризации при остром инфаркте миокарда или остром коронарном синдроме, диаметр целевых артерий для кондуитов ВГА менее 1 мм, гемодинамически значимый атеросклероз подключичных артерий в первом сегменте, сопутствующая кардиоваскулярная патология, требующая дополнительной одновременной хирургической коррекции, тяжелая сопутствующая патология, ограничивающая продолжительность жизни (например, инкурабельное онкологическое заболевание).
Оперативное лечение проводили в объеме изолированного коронарного шунтирования с использованием или без искусственного кровообращения, выполнили все хирургические процедуры через срединную стернотомию. В качестве кондуитов для коронарного шунтирования использовали внутренние грудные артерии. Выделяли кондуиты от устья до бифуркации (скелетизацией или полускелетизацией, без фасции и мышечного лоскута). После выделения кондуитов вводили расчетную дозу гепарина, после чего отсекали ВГА на уровне бифуркации, правую ВГА — дистально и прокси- мально при шунтировании по методике Y-композитной конструкции. Коронарное шунтирование выполняли с учетом рандомизации по методике in situ или Y-композитной конструкции внутренних грудных артерий. Бассейн правой коронарной артерии при необходимости реваскуляризировали с помощью аутовены или лучевой артерии.
Все пациенты дали письменное информированное согласие до включения в исследование. Протокол исследования одобрен и утвержден экспертным советом НМИЦ им. ак. Е.Н. Мешалки-на. Соответствие исследования принципам Хельсинкской декларации рассмотрено и согласовано с этическим комитетом НМИЦ им. ак. Е.Н. Мешал-кина согласно внутреннему протоколу (№ 001 от 05.04.2018 г.).
Статистический анализ
Все статистические анализы проводились в программе SPSS Statistics 22.0 (IBM Corporation, Армонк, США). Достоверность различий между сравниваемыми группами (p) для непрерывных данных рассчитывалась с использованием непараметрического критерия Манна – Уитни, для категориальных данных — с помощью таблиц сопряжения с применением точного теста Фишера. Уровень значимости между сравниваемыми группами считался достоверным при p < 0,05, что соответствует критериям, принятым в медико-биологических исследованиях.
Табл. 1. Предоперационная сравнительная характеристика по основным клиническим параметрам
|
Показатель |
Первая группа, n = 39 |
Вторая группа, n = 37 |
p |
|
Возраст, годы |
60,8 ± 6,4 |
60,6 ± 6,3 |
0,86 |
|
Пол, n (%) |
31 (79,4) |
28 (76) |
0,78 |
|
Рост, см |
169,3 ± 6,1 |
168,8 ± 7,6 |
0,56 |
|
Вес, кг |
82,7 ± 11,5 |
82,9 ± 13,6 |
0,64 |
|
Индекс массы тела |
28,8 ± 3,6 |
29,0 ± 3,9 |
0,99 |
|
Курение, n (%) |
10 (26) |
10 (27) |
0,99 |
|
Хроническая обструктивная болезнь легких , n (%) |
1 (2,56) |
0 (0) |
0,99 |
|
Фракция выброса левого желудочка, % |
60,1 ± 8,4 |
61,0 ± 6,3 |
0,63 |
|
Шкала EuroScore II, баллов |
1,2 ± 0,6 |
1,4 ± 0,9 |
0,98 |
|
Атеросклероз брахиоцефальных артерий , n (%) |
9 (23) |
9 (24) |
0,99 |
|
Сахарный диабет, n (%) |
13 (33,3) |
7 (19) |
0,19 |
|
Стенокардия напряжения, I–IV ФК , безболевая форма, n |
3 (2; 3) |
2 (2; 3) |
0,002 |
|
Хроническая сердечная недостаточность, I–III ФК по классификации NYHA, n |
2 (2; 3) |
2 (2; 3) |
0,14 |
|
Артериальная гипертония, n (%) |
37 (94,8) |
35 (95) |
0,99 |
|
Нарушения ритма сердца до операции, n (%) |
5 (12,8) |
3 (8) |
0,71 |
|
Острое нарушение мозгового кровообращения в анамнезе, n (%) |
7 (17,9) |
3 (8) |
0,31 |
|
Атеросклероз артерий нижних конечностей, n (%) |
4 (10,2) |
5 (14) |
0,73 |
Примечание. ФК — функциональный класс, NYHA — Нью-Йоркская ассоциация сердца (англ. New York Heart Association).
Результаты
При предоперационной сравнительной характеристике пациентов по основным клинико-демографическим параметрам в обеих группах достоверного различия между группами не выявлено (табл. 1).
Интра- и послеоперационные данные представлены в табл. 2. Общая характеристика и частота встречаемости послеоперационных осложнений по большинству событий были сопоставимы в обеих группах. В первой группе применение искусственного кровообращения было достоверно чаще, чем во второй — 28,2 и 3,0 % соответственно, p < 0,003. Продолжительность инотропной поддержки была значительно меньше в первой группе и составила 3,72 ± 8,60 против 8,0 ± 9,6 во второй группе, p < 0,007. Инотропная поддержка в высоких дозах не применялись ни у одного пациента. По основным неблагоприятным сердечным и мозговым событиям достоверная разница не получена в госпитальном периоде наблюдения.
Обсуждение
Аутоартериальная реваскуляризация с использованием Y-композитных и in situ кондуитов ВГА улучшает клинические результаты после коронарного шунтирования. Однако применение тотального аутоартериального шунтирования не получило широкого распространения ввиду отсутствия однозначных убедительных данных в преимуществах такого подхода.
В 2016 г. опубликована работа D. Glineur о тотальном аутоартериальном шунтировании по типу Y-композитных и in situ кондуитов [12]. В данном исследовании на 304 пациентах показано отсутствие разницы в проходимости аутоартериальных шунтов между двумя методиками через 3 года, однако большие неблагоприятные события в 7-летний период возникали чаще в группе in situ . Одной из главных причин такого результата, на наш взгляд, являлся метод выполнения in situ , при котором шунтирование передней нисходящей артерии выполнялось
Табл. 2. Интра- и послеоперационные данные пациентов
|
Показатель |
Первая группа, n = 39 |
Вторая группа, n = 37 |
p |
|
Искусственное кровообращение, n (%) |
11 (28,2) |
1 (3) |
0,003 |
|
Периоперационный инфаркт миокарда, n (%) |
0 (0) |
0 (0) |
0,99 |
|
Периоперационный инсульт, n (%) |
1 (2,5) |
0 (0) |
0,99 |
|
Повторная реваскуляризация, n (%) |
0 (0) |
0 (0) |
0,99 |
|
Пребывание в реанимации, дни |
1,3 ± 0,4 |
1,4 ± 0,6 |
0,42 |
|
Инотропная поддержка, ч |
3,7 ± 8,6 |
0,007 |
|
|
Искусственная вентиляция легких, ч |
4,0 ± 1,9 |
4,7 ± 2,1 |
0,18 |
|
Впервые возникшее нарушение ритма после операции, n (%) |
9 (23) |
4 (11) |
0,22 |
|
Острое почечное повреждение (согласно критериям международного консорциума KDIGO), n (%) |
1 (2,56) |
0 (0) |
0,99 |
|
Заместительная почечная терапия, n (%) |
0 (0) |
0 (0) |
0,99 |
|
Фракция выброса левого желудочка, % |
58,3 ± 6,6 |
58 ± 6 |
0,77 |
|
Летальный исход, n (%) |
0 (0) |
0 (0) |
0 |
|
Длительность госпитализации, дни |
12,9 ± 3,5 |
13,2 ± 3,1 |
0,46 |
|
Инфекционные осложнения, n (%) |
0 (0) |
0 (0) |
0 |
|
Время операции, мин |
227,9 ± 47,6 |
242,8 ± 46,6 |
0,15 |
|
Основные неблагоприятные сердечно-сосудистые события, n (%) |
1 (2,56) |
0 (0) |
0,99 |
Примечание. KDIGO — Заболевание почек: улучшение глобальных результатов (англ. Kidney Disease: Improving Global Outcomes).
левой ВГА, а ветви тупого края — правой ВГА, проведенной через поперечный синус. Также стоит отметить разницу в количестве шунтируемых артерий сердца: при Y-композитной конструкции достигалась более полная реваскуляризация миокарда.
В то же время в работе O. Lev-Ran об аутоартериальной реваскуляризации миокарда с использованием двух ВГА по типу in situ и Y- или T-композитным графтом, выявлены возрастание частоты рецидива стенокардии и снижение выживаемости в среднесрочном наблюдении у пациентов с композитным графтом [13]. На послеоперационной коронаро-шунтографии определена более низкая проходимость композитных трансплантатов, чем в группе in situ . Вероятно, это связано с техническими ошибками из-за сложности выполнения Y-композитных конструкций.
В свою очередь G. Nasso с соавт. оценили 204 пациентов, получавших Y-композитную конструкцию, и 202 — in situ [14]. В результате исследования не выявлено существенных различий между группа- ми по основным неблагоприятным сердечно-сосудистым событиям (англ. Major Adverse Cardiac and Cerebrovascular Events, MACCE) при 2-летнем наблюдении.
Однако, несмотря на противоречивые данные, в метаанализе B. Yanagawa с соавт. не выявлено разницы между методиками шунтирования с Y-композитными и in situ кондуитами, что означает более высокую вероятность действительного отсутствия разницы между двумя методиками [15].
В нашем исследовании выполнение методики in situ заключается в том, что левой ВГА шунтировали ветвь огибающей артерии, правой ВГА in situ — переднюю межжелудочковую артерию. В данной методике не применяется «золотой стандарт» левая ВГА – передняя межжелудочковая артерия, что, впрочем, не является препятствием для длительного функционирования кондуита. Так, S. Ogawa с соавт. сравнили различные конфигурации использования ВГА (правой и левой) к передней межжелудочковой артерии и изучили ранние и поздние результаты [16]. При анализе отдаленных результатов выявлено, что случаи смерти, повторной реваскуляризации и инфаркта миокарда были значительно выше в группе левая ВГА – передняя межжелудочковая артерия. Среднесрочная проходимость правой ВГА при шунтировании передней межжелудочковой артерии составила 96,2 %, а анализ Каплана – Майера показал, что случаи смерти, повторной реваскуляризации и инфаркта миокарда были значительно выше в группе левая ВГА – передняя межжелудочковая артерия. Однако следует отметить другое исследование, в котором J. Trent Magruder и соавт. провели сравнение различных конфигураций использования правой и левой ВГА к передней межжелудочковой артерии. При анализе не обнаружено существенных различий с точки зрения долгосрочной выживаемости и свободы от повторной реваскуляризации [17].
В нашем исследовании непосредственные результаты аутоартериальной реваскуляризации с использованием Y-композитных и in situ кондуитов ВГА показывают низкую частоту периоперационных осложнений и отсутствие различий между исследуемыми группами. Мы сравнили длительность операций, в которых выполняли коронарное шунтирование с использованием аутоартериальных in situ и Y-композитных кондуитов из ВГА. В первой группе длительность операции составляла 227,9 ± 47,6 мин, во второй — 242,8 ± 46,6 мин, то есть методика Y-композитных конструкций удлиняла операцию на 14,4 мин, но это разница не достигала статистической значимости, p = 0,15. Из предоставленных данных можно отметить, что есть тенденция к сокращению длительности операции по методике in situ , однако для получения достоверных результатов, вероятно, потребуется дальнейшее наблюдение и большее количество пациентов.
Оперативное лечение проводилось в объеме изолированного коронарного шунтирования с использованием или без искусственного кровообращения в зависимости от предпочтений хирурга. Наши результаты показывают, что, несмотря на разницу в группах по искусственному кровообращению, по послеоперационным осложнениям нет разницы, однако она может проявиться при дальнейшем наблюдении. По мнению ряда авто- ров, проведение коронарного шунтирования в условиях искусственного кровообращения сопряжено с высоким риском развития ранних послеоперационных осложнений: острой дыхательной недостаточности, острой почечной недостаточности, требующей проведения гемодиализа, острого нарушения мозгового кровоснабжения после операции. Проанализировав результаты исследования на 1 339 пациентах с ишемической болезнью сердца и многососудистым поражением коронарных артерий, А.А. Меликулов с соавт. отметили более высокое (р < 0,05) количество церебральных и почечных осложнений в послеоперационном периоде у пациентов, перенесших аортокоронарное шунтирование в условиях искусственного кровообращения [18]. Аналогичные результаты были получены и в исследовании, включившем 4 819 пациентов с нормальной функцией почек до операции, которое показало частоту острых почечных травм в группе аортокоронарного шунтирования с искусственным кровообращением 4 %, а частоту возникновения необходимости использования диализа 2,4 % [19]. D.P. Taggart с соавт. считают, что выполнение коронарного шунтирования более безопасно, в то же время не найдено достоверного различия в частоте развития рецидива стенокардии, острого инфаркта миокарда и послеоперационных осложнений между группами аортокоронарного шунтирования в условиях искусственного кровообращения и на работающем сердце [20]. Тем не менее M. Polomsky и соавт. в метаанализе на 876 081 пациенте показали, что операции на работающем сердце, выполненные в клиниках, обладающих большим опытом, связаны с достоверным уменьшением рисков смерти, инсульта, острой почечной недостаточности, длительности послеоперационного пребывания в стационаре [21]. Еще один показатель с достоверной разницей — это увеличение продолжительности инотропной поддержки во второй группе (8,0 ± 9,6 ч в назначении малых доз инотропных препаратов), — возможно, связан с длительностью вмешательства.
Необходимо отметить отсутствие стернальных осложнений в обеих группах. Мы не можем полностью согласиться с авторами, указывающими на более частое развитие таких осложнений у больных после бимаммарного коронарного шунтирования. Конечно, мы не отрицаем прогностически неблагоприятное сочетание таких факторов, как избыточная масса тела и сахарный диабет. В то же время прецизионное скелетизированное выделение обеих ВГА сводит к минимуму раневую инфекцию со стороны грудины. Наиболее показательны в этом плане данные исследования по оценке кровоснабжения и остеобластической активности ткани грудины после маммарокоронарного шунтирования [22]. Пациентам на госпитальном этапе проводилась однофотонная эмиссионная компьютерная томография. Отмечались ухудшение кровоснабжения и уменьшение остеобластической активности грудины при лоскутном заборе ВГА, а выделение методом скелетизации не приводило к статистически значимому изменению перфузии грудины. Наряду с общеизвестными профилактическими мероприятиями это позволяло существенно снизить риск стернальных осложнений.
Внедрение оптимального метода коронарного шунтирования в виде аутоартериальной реваскуляризации позволит улучшить показатели функционирования аортокоронарных шунтов в отдаленном периоде, следовательно, снизить отдаленную смертность и уменьшить количество незапланированных госпитализаций и больших неблагоприятных сердечно-сосудистых осложнений.
Ограничения
Ограничением исследования является недостаточное количество пациентов.
Заключение
Низкая частота периоперационных осложнений, отсутствие периоперационных инфарктов миокарда и госпитальной летальности демонстрируют безопасность бимаммарного коронарного шунтирования. Несмотря на отсутствие разницы в раннем послеоперационном периоде, мы ожидаем, что в отдаленном периоде будет статистически значимая разница по неблагоприятным сердечнососудистым событиям между группами Y-композитных конструкций и in situ кондуитов из внутренних грудных артерий.
Список литературы Артериальная реваскуляризация миокарда с использованием y-композитных конструкций и in situ кондуитов внутренних грудных артерий: непосредственные результаты
- Gansera B., Schmidtler F., Angelis I., Kiask T., Kemkes B.M., Botzenhardt F. Patency of internal thoracic artery compared to vein grafts - postoperative angiographic findings in 1189 symptomatic patients in 12 years. Thorac Cardiovasc Surg. 2007;55(7):412-417. PMID: 17902061. http://dx.doi. org/10.1055/s-2007-965372
- YusufS., Zucker D., Peduzzi P., Fisher L.D.,TakaroT., Kennedy J.W., Davis K., Killip T., Passamani E., Norris R., Morris C., Mathur V., Varnauskas E., Chalmers T.C. Effect of coronary artery bypass graft surgery on survival: overview of 10-year results from randomised trials by the Coronary Artery Bypass Graft Surgery Trialists Collaboration. Lancet. 1994;344(8922):563-570. PMID: 7914958. http://dx.doi.org/10.1016/s0140-6736i94191963-1
- Taggart D.P. Thomas B. Ferguson Lecture. Coronary artery bypass grafting is still the best treatment for multivessel and left main disease, but patients need to know. Ann Thorac Surg. 2006;82(6):1966-1975. PMID: 17126093. http://dx.doi. org/10.1016/j.athoracsur.2006.06.035
- Aldea G.S., Bakaeen F.G., Pal J., Fremes S., Head S.J., Sabik J., Rosengart T., Kappetein A.P., Thourani V.H., Firestone S., Mitchell J.D., Society of Thoracic Surgeons. The Society of Thoracic Surgeons clinical practice guidelines on arterial conduits for coronary artery bypass grafting. Ann Thorac Surg. 2016;101 (2):801 -809. PMID: 26680310. http://dx.doi. org/10.1016/j.athoracsur.2015.09.100
- Gaudino M., Taggart D., Suma H., Puskas J.D., Crea F., Massetti M. The choice of conduits in coronary artery bypass surgery. J Am Coll Cardiol. 2015;66(15):1729-1737. PMID: 26449144. http://dx.doi.org/10.1016/Uacc.2015.08.395
- Tatoulis J. Total arterial coronary revascularization-patient selection, stenoses, conduits, targets. Ann Cardiothorac Surg. 2013;2(4):499-506. PMID: 23977629, PMCID: PMC3741872. http://dx.doi.org/10.3978Aissn.2225-319X.2013.07.02
- Taggart D.P. Current status of arterial grafts for coronary artery bypass grafting. Ann Cardiothorac Surg. 2013;2(4):427-430. PMID: 23977618, PMCID: PMC3741887. http://dx.doi. org/10.3978/j.issn.2225-319X.2013.07.21
- Семагин А.П., Кузнецов Д.В., Поляков П.В., Николаева Е.Н., Семагин А.А. Использование большой подкожной вены у больных ишемической болезнью сердца при коронарном шунтировании: новые возможности. Кардиология и сердечно-сосудистая хирургия. 2011;4(2):4-6. [Semagin A.P., Kuznetsov D.V., Poliakov P.V., Nikolaeva E.N., Semagin A.A. Application of great saphenous vein in patients with coronary heart disease undergoing coronary bypass grafting: new possibilities. Russian Journal of Cardiology and Cardiovascular Surgery = Kardiologiya i serdechno-sosudistaya khirurgiya. 2011;4(2):4-6. (In Russ.)]
- He G.-W. Arterial grafts: clinical classification and pharmacological management. Ann Cardiothorac Surg. 2013;2(4):507-518. PMID: 23977630, PMCID: PMC3741890. http://dx.doi.org/10.3978/Ussn.2225-319X.2013.07.12
- Buxton B.F., Hayward P.A.R., Newcomb A.E., Moten S., Seevanayagam S., Gordon I. Choice of conduits for coronary artery bypass grafting: craft or science? Eur J Cardiothorac Surg. 2009;35(4):658-670. PMID: 19231230. http://dx.doi. org/10.1016/j.ejcts.2008.10.058
- LoopF.D., Lytle B.W.,Cosgrove D.M.,Stewart R.W., GoormasticM., Williams G.W., Golding L.A., Gill C.C., Taylor P.C., Sheldon W.C., Proudfit W.L. Influence of the internal-mammary-artery graft on 10-year survival and other cardiac events. N Engl J Med. 1986;314( 1 ):1 -6. PMID: 3484393. http://dx.doi.org/10.1056/ NEJM198601023140101
- Glineur D., Boodhwani M., Hanet C., de Kerchove L., Navarra E., Astarci P., Noirhomme P., El Khoury G. Bilateral internal thoracic artery configuration for coronary artery bypass surgery: A prospective randomized trial. Circ Cardiovasc Interv. 2016;9(7):e003518. PMID: 27406988, PMCID: PMC4949001. http://dx.doi.org/10.1161/CIRCINTERVENTI0NS.115.003518
- Lev-Ran O., Paz Y., Pevni D., Kramer A., Shapira I., Locker C., Mohr R. Bilateral internal thoracic artery grafting: midterm results of composite versus in situ crossover graft. Ann Thorac Surg. 2002;74(3):704-711. PMID: 12238828. http://dx.doi. org/10.1016/s0003-4975(02)03791-8
- Nasso G., Coppola R., Bonifazi R., Piancone F., Bozzetti G., Speziale G. Arterial revascularization in primary coronary artery bypass grafting: direct comparison of 4 strategies-results of the Stand-in-Y Mammary Study. J Thorac Cardiovasc Surg. 2009;137(5):1093-1100. PMID: 19379973. http://dx.doi. org/10.1016/j.jtcvs.2008.10.029
- Yanagawa B., Verma S., Jüni P., Tam D.Y., Mazine A., Puskas J.D., Friedrich J.O. A systematic review and meta-analysis of in situ versus composite bilateral internal thoracic artery grafting. J Thorac Cardiovasc Surg. 2017;153(5):1108-1116.e16. PMID: 28017369. http://dx.doi.org/10.1016/utcvs.2016.11.027
- Ogawa S., Tsunekawa T., Hosoba S., Goto Y., Kato T., Kitamura H., Tomita S., Okawa Y. Bilateral internal thoracic artery grafting: propensity analysis of the left internal thoracic artery versus the right internal thoracic artery as a bypass graft to the left anterior descending artery. Eur J Cardiothorac Surg. 2020;57(4):701-708. PMID: 31638700. http://dx.doi. org/10.1093/ejcts/ezz290
- Magruder J.T., Young A., Grimm J.C., Conte J.V., Shah A.S., Mandal K., Sciortino C.M., Zehr K.J., Cameron D.E., Price J. Bilateral internal thoracic artery grafting: Does graft configuration affect outcome? J Thorac Cardiovasc Surg. 2016;152( 1 ):120-127. PMID: 27343909. http://dx.doi. org/10.1016/j.jtcvs.2016.03.022
- Меликулов А.А., Мерзляков В.Ю., Ключников И.В., Скопин А.И., Мамедова С.К., Жалилов А.К., Ахмедова М.Ф., Байчурин Р.К., Саломов М.А. Непосредственные результаты коронарного шунтирования на работающем сердце у пациентов высокого хирургического риска. Анналы хирургии. 2017;22(6):353-360. [Melikulov A.A., Merzlyakov V.Yu., Klyuchnikov I.V., Skopin A.I., Mamedova S.K., Zhalilov A.K., Akhmedova M.F., Baychurin R.K., Salomov M.A. The immediate results of beating heart coronary artery bypass grafting in high-risk patients. Russian Journal of Surgery = Annaly Khirurgii. 2017;22(6):353-360. (In Russ.)] http://dx.doi.org/10.18821/1560-9502-2017-22-6-353-360
- Wang J., Gu C., Gao M., Yu W., Li H., Zhang F., Yu Y. Comparison of the incidence of postoperative neurologic complications after on-pump versus off-pump coronary artery bypass grafting in high-risk patients: a meta-analysis of 11 studies. Int J Cardiol. 2015;185:195-197. PMID: 25797677. http://dx.doi. org/10.1016/j.ijcard.2015.03.115
- Taggart D.P., Altman D.G., Gray A.M., Lees B., Nugara F., Yu L.-M., Flather M., ART Investigators. Effects of on-pump and off-pump surgery in the Arterial Revascularization Trial. Eur J Cardiothorac Surg. 2015;47(6):1059-1065. PMID: 25217501. http://dx.doi.org/10.1093/ejcts/ezu349
- Polomsky M., He X., O'Brien S.M., Puskas J.D. Outcomes of off-pump versus on-pump coronary artery bypass grafting: Impact of preoperative risk. J Thorac Cardiovasc Surg. 2013;145(5):1193-1198. PMID: 23597624. http://dx.doi. org/10.1016/j.jtcvs.2013.02.002
- Григорян Г.Р. Артериальная реваскуляризация миокарда у больных с ИБС. Обзор литературы [дата обращения:]. Режим доступа: http://www.medlib.am/ articles/Grigoryan(VX08-2).pdf. [Grigoryan G.R. Arterial revascularization of the myocardium in patients with coronary artery disease. A review of the literature] Available from: http://www.medlib.am/articles/Grigoryan(VX08-2).pdf (In Russ.)]


