IFN-индуцированные дендритные клетки у больных множественной миеломой
Автор: Леплина О.Ю., Насонова Г.В., Тихонова М.А., Крючкова И.В., Лисуков И.А., Останин А.А., Черных Е.Р.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 6 (36), 2009 года.
Бесплатный доступ
Проведено сравнительное исследование фенотипических и функциональных свойств дендритных клеток (ДК), генери- рованных in vitro в присутствии GM-CSF и IFN-α, у здоровых доноров (n=34) и больных множественной миеломой (n=12). Показано, что по своему составу (количеству зрелых/незрелых ДК и клеток промежуточной степени зрелости) популяция ДК больных в целом была сопоставима с ДК здоровых доноров. ДК больных множественной миеломой (ММ) не отличались от ДК доноров по уровню продукции IFN-γ и TNF-α. В то же время ДК больных характеризовались более низким содержанием активированных CD25+клеток в сочетании с повышенной продукцией IL-10, что, по-видимому, обусловливало ослабление их стимуляторной активности в СКЛ. Тем не менее ДК больных ММ сохраняли свою способность к запуску Th1-ответа, что проявлялось 5-кратным увеличением количества CD3+IFN-γ+ Т-клеток. Полученные данные аргументируют возмож- ность клинического применения ДК у больных ММ в качестве клеточных вакцин (особенно в сочетании с адъювантной цитокинотерапией) с целью повышения эффективности противоопухолевого иммунного ответа.
Множественная миелома, дендритные клетки, th1/th2 цитокины, скл
Короткий адрес: https://sciup.org/14055197
IDR: 14055197 | УДК: 616-006.448:612.017.1
IFN-induced dendritic cels in patients with multiple myeloma
The phenotypical and functional properties of dendritic cells (DCs), generated in vitro with GM-CS and IFN-α, were studied in the healthy donors (n=34) and patients with multiple myeloma (MM, n=12). The normal quantity of mature/non-mature and semi-mature cells was found in DCs population, generated in patients with MM. The level of IFN-γ and TNF-α production by DCs of patients was comparable with healthy donors. However, DCs of patients with MM were characterized by low percentage of activated CD25+cells coupled with enhance IL-10 production, which obviously cause the decrease of DCs stimulatory activity in mixed lymphocyte culture (MLC). Nevertheless, DCs of patients were able to induce Th1 response that was accompanied by 5-fold increase of CD3+IFN-γ+ Т-cells relative number in MLC. Our data argue the possibility of clinical application of DCs in patients with MM (in the form of cellular vaccines, particularly, in combination with adjuvant cytokine therapy) with the aim to enhance the efficiency of anti-tumor immune response.
Текст научной статьи IFN-индуцированные дендритные клетки у больных множественной миеломой
Множественная миелома (ММ) является В-клеточным лимфопролиферативным заболеванием, которое характеризуется клональной пролиферацией в костном мозге (реже – в экстрамедуллярных очагах) атипичных плазматических клеток, продуцирующих моноклональный иммуноглобулин и/или свободные моноклональные легкие цепи иммуноглобулинов (к или λ). В структуре гемобластозов доля ММ составляет 10%, при этом в России ежегодно погибает более 10 000 больных с данной патологией. Современные подходы в лечении ММ предполагают использование высокодозной полихимиотерапии (ПХТ) мелфаланом с последующей аутотрансплантацией периферических стволовых кроветворных клеток (СКК). Другой подход заключается в проведении повторных курсов ПХТ с трансплантацией аутологичных СКК после каждого курса химиотерапии («тандемная» трансплантация). Но даже такая комплексная терапия не предотвращает развитие рецидивов.
С целью контроля минимальной остаточной болезни и для поддержания ремиссии после ВДХ назначается интерферон- α (IFN- α ). Несмотря на то, что поддерживающая терапия позволяет в ряде случаев увеличивать продолжительность ремиссии, достичь увеличения продолжительности жизни при этом не удается. Общий прогноз при множественной миеломе неблагоприятный.
Это делает актуальным поиск новых подходов к лечению данного заболевания.
Известно, что ключевую роль в распознавании опухолевого антигена и презентации его специфическим цитотоксическим Т-клеткам играют дендритные клетки (ДК), способные инициировать иммунный ответ [5, 13]. Соответственно, создание лечебных вакцин на основе ДК рассматривается в качестве одного из новых подходов в комплексной терапии опухолевых заболеваний [3, 4, 9, 20].
Как правило, ДК получают in vitro из прилипающей фракции мононуклеарных клеток (МНК) периферической крови. Классическим считается протокол генерации ДК путем культивирования моноцитов крови в присутствии GM-CSF и IL-4 в течение 5–7 дней (незрелые ДК) с последующей стимуляцией их созревания в течение 24–48 ч с различными факторами (зрелые ДК) [18]. В последние годы в литературе появились данные о возможности быстрой генерации частично зрелых ДК с помощью GM-CSF и IFN- α [16]. Отличительными особенностями данного типа ДК (IFN-ДК) являются высокая способность к захвату антигена; высокая миграционная активность за счет экспрессии хемокинового рецептора ССR7; функциональная стабильность в отсутствие ростовых факторов; способность индуцировать как Th1-, так и Th2-ответ; а также секретировать IFN- α , обладающий противовирусной и противоопухолевой активностью [11]. Тем не менее исследование возможности генерации и характеристика IFN-ДК при ММ ранее не проводилось. Исходя из этого, целью работы явилось изучение фенотипических и функциональных свойств IFN α -индуцированных ДК у больных множественной миеломой.
Материал и методы
МНК выделяли из гепаринизированной венозной крови центрифугированием в градиенте плотности фиколла-верографина. Моноциты выделяли на чашках Петри (Nuclon, Дания) путем прилипания к пластику МНК (2–5×106 клеток/мл) в присутствии 10 % сыворотки крови АВ (IV) группы. Для генерации ДК моноциты культивировали во флаконах (BD Biosciences Falcon, Великобритания) в течение 3 сут в среде RPMI-1640 (Sigma-Aldrich, США), дополненной 0,3 мг/мл L-глутамина, 5мМ HEPES-буфера, 100 мкг/мл гентамицина и 5 % сыворотки плодов коровы («БиоЛот», СПб.), в присутствии GM-CSF (40 нг/мл, Sigma-Aldrich, США) и INF-α (1000 Ед/мл, Роферон-А, Roche, Швейцария) с последующим дозреванием с липополисахаридом (10 мкг/мл, LPS E. coli 0114:В4, Sigma-Aldrich, США) в течение 24 ч.
Фенотипический анализ ДК проводили методом одноцветной или двуцветной проточной цитофлюориметрии (FACSCalibur, Becton Dickinson, США) с использованием FITS- или PE-меченных моноклональных антител (CD83, CD1a, CD11c, CD14, CD25, CD123; PharMingen, США). Аллостимуляторную активность ДК оценивали в смешанной культуре лимфоцитов (СКЛ). В качестве отвечающих клеток использовались МНК доноров (0,1×106/лунку), которые культивировали в 96-луночных круглодонных планшетах для иммунологических исследований в среде RPMI-1640 (как описано выше) с 10 % инактивированной сыворотки крови АВ (IV) группы при 37°С в СО2-инкубаторе. Стимуляторами служили аллогенные IFN-ДК здоровых доноров или больных ММ в соотношении МНК:ДК = 10:1. Пролиферативный ответ в СКЛ оценивали на 5 сут радиометрически по включению 3H-тимидина (1 мкКю/лунку), вносимого за 18 ч до окончания культивирования.
В культуральных супернатантах, генерированных IFN-ДК, определяли концентрацию IFN-γ, IL-4, IL-10 и TNF-α с помощью соответствующих тест-систем для иммуноферментного
Клиническая и гематологическая характеристика больных ММ
Таблица 1
|
№ пациента |
Пол |
Возраст |
Изотип парапротеина |
Плазматические клетки в костном мозге, % |
Стадия |
Состояние здоровья |
Терапия |
|
1 |
Ж |
67 |
65 |
III |
Ремиссия |
Cy/Dexa+Велкейд |
|
|
2 |
Ж |
61 |
30 |
IIIБ |
Ремиссия |
Велкейд |
|
|
3 |
М |
49 |
IgG |
11,5 |
IIIА |
Ремиссия |
PAD |
|
4 |
Ж |
50 |
IgG |
31 |
II |
Ремиссия |
Нет |
|
5 |
Ж |
69 |
76 |
III |
Прогрессия |
Зомета |
|
|
6 |
М |
49 |
IgG |
10 |
III |
Ремиссия |
Велкейд |
|
7 |
Ж |
50 |
2 |
III |
Частичная ремиссия |
Нет |
|
|
8 |
М |
63 |
IgA |
48 |
III |
Частичная ремиссия |
Нет |
|
9 |
М |
46 |
IgA |
27 |
III |
Частичная ремиссия |
Нет |
|
10 |
М |
56 |
IgA |
6 |
III |
Частичная ремиссия |
Нет |
|
11 |
Ж |
67 |
IgG |
29,5 |
IIIБ |
Прогрессия |
VMmP |
|
12 |
Ж |
48 |
IgG |
8 |
III |
Прогрессия |
Нет |
анализа в соответствии с инструкцией фирмы-производителя («Вектор-Бест», Новосибирск).
Оценку экспрессии внутриклеточных цитокинов в популяции CD3+Т-лимфоцитов, стимулированных ДК, проводили методом трехцветной проточной цитометрии (FACSCalibur, «Becton Dickinson», США). Для этого МНК, истощенные от моноцитов, культивировали в 96-луночных планшетах в полной культуральной среде с 10 % сыворотки плодов коровы в отсутствие (контроль) и в присутствии (опыт) ДК в соотношении 10:1 в течение 72 ч. За 18 ч до конца инкубации в культуру добавляли брефел-дин (10 мкг/мл, «IСN», США), затем клетки отмывали и инкубировали 15 мин при комнатной температуре с APC-меченными моноклональными анти-CD3-антителами (Becton Dickinson, США). Далее проводили пермеабилизацию клеток с помощью 0,2 % раствора Твин-20 и инкубировали их с моноклональными FITC-конъюгированными анти-INF-γ антителами и PE-меченными анти-IL-4 (Becton Dickinson, США). В культурах МНК, истощенных от моноцитов (МНК0) и активированных ДК (МНК + ДК) здоровых доноров и больных ММ, определяли относительное содержание CD3+Т-клеток с внутриклеточной экспрессией IFN-γ и IL-4, при этом рассчитывали соответствующие индексы влияния ДК (ИВДК) на количество Т-клеток, экспрессирующих IFN-γ и IL-4, по формуле ИВДК = опыт/контроль.
Математическую обработку полученных результатов проводили с помощью пакета программ Statistica 6.0.
Результаты и обсуждение
Популяция прилипающих к пластику клеток у больных ММ, так же как и у здоровых доноров, была представлена преимущественно CD14+ моноцитами (77,6 ± 1,9 и 81,3 ± 2,3 % соответственно). В результате культивирования моноцитов с GM-CSF и IFN-α в течение 3–4 сут клетки теряли способность прилипать к пластику и приобретали типичные морфологические черты дендритных клеток. Сравнительный фенотипический анализ показал (табл. 2), что в группе больных ММ среди генерируемых IFN-ДК отмечается повышенное содержание CD14+моноцитов. Тем не менее общее количество миелоидных CD11с+ДК у больных было достоверно выше, чем у доноров, при этом относительное число зрелых CD83+ДК сохранялось на уровне нормы. Однако в популяции генерируемых IFN-ДК больных отмечалось
|
статистически значимое снижение содержания активированных ДК, экспрессирующих CD25 (рецептор к α-цепи IL-2). Таблица 2 Фенотипическая характеристика IFN-ДК здоровых доноров и больных ММ |
||
|
Маркеры |
Доноры (n=18), % |
Больные ММ (n=12), % |
|
CD14 |
8,7 ± 1,4 |
17,7 ± 2,1* |
|
CD1a |
10,4 ± 2,0 |
7,1 ± 1,35 |
|
CD11c |
28,7 ± 2,2 |
48,0 ± 6,5* |
|
CD123 |
24,9 ± 2,6 |
23,8 ± 4,9 |
|
СD83 |
22,4 ± 2,4 |
22,5 ± 5,9 |
|
CD25 |
25,1 ± 3,5 |
7,7 ± 2,1* |
|
CD83 +CD1a- |
17,9 ± 2,5 |
18,3 ± 5,8 |
|
CD83 +CD1a+ |
4,6 ± 0,8 |
4,2 ± 0,8 |
|
CD83 -CD1a+ |
5,3 ± 1,7 |
3,0 ± 1,5 |
|
CD11с+CD123- |
19,8 ± 4,3 |
34,3 ± 5,3* |
|
CD11с+CD123+ |
7,3 ± 1,3 |
13,8 ± 3,2* |
|
CD11с-CD123+ |
14,3 ± 2,3 |
8,6 ± 1,6 |
Примечание: * – различия статистически значимые по сравнению с донорами (pU<0,05, U критерий Вилкоксона–Манна–Уитни).
Поскольку маркеры CD83 и CD1a характеризуют различные стадии созревания миелоидных ДК, дополнительно была проанализирована коэкспрессия CD83 и CD1а молекул на IFN-ДК. Популяция генерируемых ДК больных ММ была сопоставима с ДК здоровых доноров по количеству терминально дифференцированных ДК с фенотипом CD83+CD1а-, а также по числу незрелых CD83-CD1а+ДК и CD83+CD1а+клеток промежуточной степени зрелости.
Одной из особенностей IFN-ДК является наличие на них рецептора к IL-3 (CD123). Данный маркер высоко экспрессируется на плазмаци-тоидных ДК и практически отсутствует на ДК, генерируемых в присутствии GM-CSF и IL-4 [17]. ДК больных ММ не отличались от ДК доноров по относительному количеству СD123+ клеток (табл. 2). Результаты двуцветной цитофлюорометрии показали, что у доноров большая часть CD123+ клеток сосредоточена в популяции CD11c-негативных клеток, что позволяет отнести их к классу плазмацитоидноподобных ДК. В то же время у больных ММ CD123 маркер чаще обнаруживался среди миелоидных CD11c+ДК. Соответственно, у больных относительное количество CD11+CD123+-клеток практически в 2 раза превышало аналогичный показатель здоровых доноров (13,8 ± 3,2 % и 7,3 ± 1,3 %; pU<0,05).
Как известно, популяция IFN-ДК является гетерогенной в отношении степени зрелости клеток , из которых только 25–30 % экспрессируют маркеры зрелых и активированных ДК (CD83 и CD25 соответственно) [11], что соответствует полученным нами данным в группе здоровых доноров. По группе обследованных нами больных ММ можно заключить, что при данной патологии в культуре in vitro генерируется популяция ДК, в целом сопоставимая с аналогичной популяцией здоровых доноров. Несмотря на то, что среди ДК больных оставалось повышенным относительное количество CD14+моноцитов, а доля активированных CD25+ДК была достоверно ниже, тем не менее у больных генерировалось большее количество миелоидных CD11c+ДК (48,0 ± 6,5 % против 28,7 ± 2,2% у доноров, pU<0,05), при этом среди них сохранялись нормальные пропорции зрелых CD83+ДК, включая терминально дифференцированные CD83+CD1а-клетки, и незрелых CD83-CD1а+ДК, а также CD83+CD1а+ клеток промежуточной степени зрелости.
Особенностью ДК, генерируемых у больных ММ, является увеличение относительного количества миелоидных CD11c+клеток ко-экспрессирующих CD123 (рецептор к IL-3). Поскольку известно, что IFN-α способен блокировать снижение экспрессии CD123 на моноцитах по мере их дифференцировки в ДК, то увеличение CD11c+CD123+ клеток может быть связано с функциональными особенностями моноцитов больных ММ. Кроме того, нельзя исключить наличие среди прилипающих к пластику клеток предшественников плазмацитоидных ДК. Однако в отличие от здоровых доноров у больных ММ CD123+ клетки преимущественно локализованы среди CD11c+ДК, что в сочетании с более низким числом плазмацитоидноподоб-ных CD11с-CD123+ДК снижает вероятность высказанного предположения.
Учитывая потенциальную возможность использования IFN-ДК в качестве клеточной основы при создании терапевтических вакцин для лечения гемобластозов, представлялось важным оценить функциональную активность
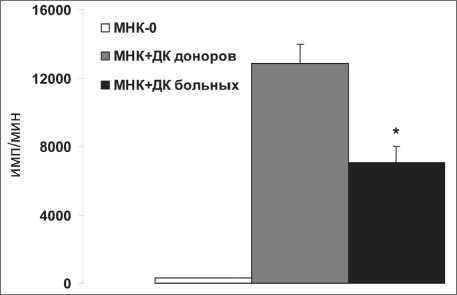
Рис. 1. Аллостимуляторная активность ДК здоровых доноров и больных ММ.
МНК доноров (0,1×106/лунку) культивировали в течение
5 сут в отсутствие (МНК-0) или в присутствии аллогенных ДК здоровых доноров (n=34) или больных ММ (n=12) в соотношении 10:1.
Примечание: интенсивность пролиферации (имп/мин) в СКЛ представлена в виде M ± S.E. * – различия статистически значимы по сравнению с ДК доноров (рU <0,05)
ДК, генерируемых у больных ММ. С этой целью был проведен сравнительный анализ аллости-муляторной активности ДК здоровых доноров и больных ММ в СКЛ (рис. 1). Было выявлено умеренное, но статистически значимое снижение уровня пролиферативного ответа в СКЛ в присутствии ДК больных (7093 ± 913 против 12880 ± 1100 имп/мин у доноров, pU<0,05). Полученные результаты свидетельствуют о нарушении антигенпрезентирующей функции IFN-ДК, полученных от больных ММ.
Поскольку способность ДК активировать
Т-клетки во многом связана со спектром и уровнем продуцируемых ими цитокинов, дополнительно была исследована продукция Th1/ про- (IFN-γ/TNF-α) и Th2/противовоспалитель-ных (IL-4/IL-10) цитокинов в культуральных супернатантах IFN-ДК (рис. 2). Оказалось, что ДК больных ММ активно секретировали IFN-γ и TNF-α на достаточно высоком уровне, сопоставимом со средними значениями здоровых доноров. Продукция IL-4 была минимальной и в обеих анализируемых группах находилась на нижней границе чувствительности иммунофер-ментных тест-систем (<5 пг/мл). В то же время ДК больных ММ характеризовались повышенной способностью секретировать IL-10 (110 ± 36 против 82 ± 13 пг/мл у доноров, pU<0,05). При этом у 50 % обследованных больных ММ (6/12) индивидуальные значения продукции IL-10 выходили за верхнюю границу квартильного диапазона нормы (>93 пг/мл). Можно полагать, что выявленное ранее снижение аллостимуляторной активности ДК больных в СКЛ обусловлено не столько дефектом их антигенпрезентирующей функции, сколько повышенной супрессорной активностью, которая опосредуется через синтез IL-10.
Следует отметить, что пролиферативный ответ МНК в присутствии ДК больных ММ был снижен в среднем на 45 % по сравнению с уровнем ответа в присутствии ДК здоровых доноров. Иными словами, примерно половина Т-клеток все-таки пролиферировала в ответ на аллоантигены, представленные дендритными клетками больных. Чтобы выяснить, какой тип
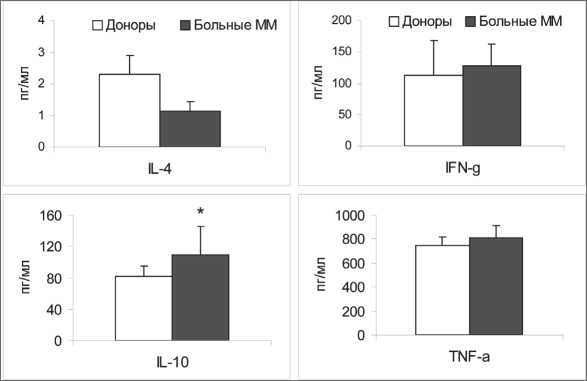
Рис. 2. Концентрация цитокинов в культуральных супернатантах ДК здоровых доноров и больных ММ. Содержание IFN-γ, IL-4, IL-10 и TNF-α (пг/мл, M ± S.E.) измеряли в супернатантах генерируемых культур IFN-ДК здоровых доноров (n=17) и больных ММ (n=12). Примечание: * – различия статистически значимы по сравнению с ДК доноров (рU<0,05)
Влияние ДК здоровых доноров и больных ММ на внутриклеточную экспрессию Т-клетками IFN-γ и IL-4
Таблица 3
|
Источник ДК |
CD3+ IFN-γ+ Т-клетки, % |
CD3+ IL-4+ Т-клетки, % |
||||
|
МНК0 |
МНК + ДК |
ИВДК |
МНК0 |
МНК + ДК |
ИВДК |
|
|
Доноры (n=18) |
1,83 ± 0,3 |
6,35 ± 0,61 |
5,4 ± 1,1 |
1,3 ± 0,2 |
1,6 ± 0,3 |
1,6 ± 0,3 |
|
Больные (n=12) |
1,36 ± 0,1 |
6,11 ± 0,58 |
5,5 ± 1,4 |
1,9 ± 0,1 |
2,3 ± 1,1 |
2,0 ± 0,2 |
Примечание: ИВДК – индекс влияния ДК на количество Т-клеток, экспрессирующих IFN-γ и IL-4.
Т-лимфоцитов преимущественно активируется в присутствии IFN-ДК, была исследована внутриклеточная экспрессия Т-клетками IFN-γ и IL-4 в СКЛ (табл. 3). Видно, что стимуляция МНК дендритными клетками здоровых доноров приводила к четкому усилению внутриклеточной продукции IFN-γ в популяции Т-лимфоцитов, что проявлялось 5-кратным увеличением количества CD3+IFN-γ+ Т-клеток. В то же время активация внутриклеточной продукции IL-4 в популяции CD3+Т-клеток была слабовыражен-ной (ИВ=1,6 ± 0,3). ДК больных ММ обладали сходной с донорами стимулирующей активностью в отношении внутриклеточной продукции IFN-γ (ИВДК 5,5 ± 1,4 против 5,4±1,1 расч.ед. у доноров) и такой же низкой Th2-поляризующей активностью (ИВДК в отношении CD3+IL-4+Т-клеток составил 2,0 ± 0,2 расч.ед.). Таким образом, IFN-ДК больных, так же как и ДК доноров, активируют преимущественно Th1 ответ.
В литературе имеются противоречивые данные о количестве и функциональной активности ДК у больных ММ. Так, в отдельных работах показано, что пациенты с ММ характеризуются пониженным содержанием и/или функциональной дефектностью дендритных клеток [10, 15]. В то же время ряд других исследователей отмечают только функциональные (но не количественные) нарушения ДК [7, 8], тогда как, по данным N. Raje et al., ДК, генерированные из МНК костного мозга или периферической крови больных ММ, вообще являются фенотипически и функционально нормальными [14]. Не менее противоречивыми являются данные относительно экспрессии маркеров зрелости и аллостимуляторной активности ДК при множественной миеломе [7, 8, 10, 14, 15].
Следует отметить, что в большинстве на- учных работ, в том числе посвященных ММ, исследуются ДК, генерированные in vitro по «классическому» протоколу с использованием GM-CSF и IL-4 [18]. Однако является ли данный путь генерации ДК физиологичным, остается спорным вопросом, поскольку продукция большого количества IL-4 в естественных условиях представляется маловероятной. Кроме того, имеются данные, что ДК, полученные с помощью GM-CSF/IL-4, характеризуются in vivo слабой миграционной активностью и низкой стабильностью в отсутствие цитокинов [19]. С этой точки зрения большой интерес представляют ДК, генерируемые в присутствии GM-CSF и IFN-α. Как известно, помимо антивирусной активности, IFN-α обладает выраженным стимулирующим эффектом на клеточный и гуморальный иммунитет и индуцирует быструю дифференцировку моноцитов в ДК с высокой миграционной активностью. Кроме того, IFN-α продуцируется в больших количествах в ответ на стимуляцию инфекционными антигенами и провоспалительными цитокинами, и, следовательно, активация системы интерферонов, возможно, отражает ранний и более физиологичный путь генерации ДК in vivo в ответ на инфекцию и опухолевую прогрессию [6, 17].
Задержка созревания и нарушение функций ДК являются характерным проявлением опухолевой иммуносупрессии при многих онкологических заболеваниях [12]. Дисфункции ДК являются, очевидно, одним из критических механизмов ускользания опухоли от иммунного ответа. Нарушение созревания ДК при опухолевом росте обычно связывают с изменением цитокинового микроокружения, в частности снижением уровня цитокинов, стимулирующих дифференцировку ДК, и увеличением кон- центрации факторов, ингибирующих данный процесс. Кроме того, дефект ДК у больных гемобластозами может быть обусловлен также изменением функциональных свойств моноцитов, которые являются источником генерации ДК. Так, согласно полученным нами ранее данным, проведение ПХТ у больных лимфомами индуцирует супрессорную активность моноцитов, в том числе за счет увеличения продукции ИЛ-10 [1, 2]. В то же время хорошо известно, что дифференцировка ДК в присутствии IL-10 существенно ингибируется, а генерируемые ДК характеризуются толерогенными свойствами.
В целом проведенные нами исследования продемонстрировали возможность генерации у больных миеломной болезнью IFN-ДК, которые обладают определенными фенотипическими и функциональными особенностями. По своему составу (количеству зрелых/незрелых ДК и клеток промежуточной степени зрелости) популяция ДК больных в целом была сопоставима с ДК здоровых доноров. Отличия заключались в более низком содержании активированных CD25+клеток в сочетании с повышенной продукцией IL-10, что, по-видимому, и приводит к ослаблению их стимуляторной активности в СКЛ. Тем не менее ДК больных ММ сохраняют свою способность к запуску Th1-ответа, что демонстрирует принципиальную возможность их клинического применения в качестве лечебных, клеточных вакцин с целью индукции противоопухолевого иммунного ответа. Можно полагать, что действие дендритноклеточных вакцин у больных ММ может быть более эффективным в комбинации с адъювантной цитокинотерапией (например, с использованием препаратов рекомбинантного IL-2 и/или интерферона-α), которая позволит нивелировать иммуносупрессорные эффекты IL-10 и активировать in vivo дополнительное количество ДК и цитотоксических Т-лимфоцитов, участвующих в запуске и развитии противоопухолевого иммунного ответа.


