Микроскопический контроль процесса остеоинтеграции имплантатов
Автор: Тимченко Павел Евгеньевич, Захаров Валерий Павлович, Волова Лариса Теодоровна, Болтовская Виолетта Викторовна, Тимченко Елена Владимировна
Журнал: Компьютерная оптика @computer-optics
Рубрика: Наномасштабные изображения
Статья в выпуске: 2 т.35, 2011 года.
Бесплатный доступ
Экспериментально показано, что метод конфокальной флуоресцентной микроскопии обеспечивает динамический контроль процесса интеграции различных типов клеток в костный имплантат с разрешением не хуже 400 нм. Предложена оптическая методика оценки качества костных имплантатов и технологии их изготовления.
Конфокальная микроскопия, флуоресценция, остеоинтеграция, контраст, разрешение
Короткий адрес: https://sciup.org/14059003
IDR: 14059003
Diagnostics of bone implantat and control of their process osteointegration with of a method confocal microscopy
Applicability confocal microscopy for the dynamic control of process integration of various types of cells in bone implant with wave length of 400 nanometers is shown. The quality estimation optical method of bone implant and their manufacturing technology is offered.
Текст научной статьи Микроскопический контроль процесса остеоинтеграции имплантатов
Заместительное восстановление (регенерация) органо-тканевых участков в поражённой области организма является одной из важных проблем современной медицины [1]. Она затрагивает практически все области костной хирургии: травматологию, челюстно-лицевую хирургию, хирургическую стоматологию, ортопедию, оториноларингологию и нейрохирургию, - где необходимо восстановить утраченную структуру и/или функцию органа методами остеосинтеза или костной пластики [2]. Однако активное практическое применение имплантатов породило новую проблему. Внедрение синтезированных материалов в поражённую область организма приводит к нарушению гомеостаза, последствием которого является плохая интеграция эксплантата и даже его отторжение, неспособность длительного функционирования внедряемой синтетической матрицы. Вероятность развития данных эффектов связана как с методикой остеоинтеграции имплантата, так и корректным определением завершённости данного процесса.
Данные явления сложно прогнозировать на этапе изготовления имплантата, следовательно, для обеспечения качества операции трансплантации необходим динамический контроль процесса остеоинтеграции, который, в свою очередь, должен быть неразрушающим и обеспечивать разрешение на клеточном уровне [3]. Традиционные методы электромиографии и ультрасонографии не обладают требуемым разрешением [4], необходим переход к оптическим методам. Учитывая, что биологическая ткань является сильно рассеивающей средой, методы широкопольной микроскопии оказываются неэффективными [5]. Данную проблему можно преодолеть, переходя к методу конфокальной микроскопии, который обеспечивает увеличение контраста изображения за счёт применения сфокусированного излучения и диафрагмирования рассеянного излучения в плоскости наблюдения. Такое увеличение контрастности приводит к возможности разрешения объектов, имеющих разницу в интенсивности до 200: 1, и их локализации как в плоскости объекта, так и вдоль оптической оси. Дальнейшее увеличение контраста возможно за счёт эффекта флуоресценции, используя либо естественные флуорофоры биологической ткани, либо специ- альные окрашивающие вещества. Следует отметить, что метод флуоресцентной микроскопии обладает более низким разрешением по сравнению с электронной или атомно-силовой микроскопией. Однако в отличие от последних он позволяет наблюдать за внутренней микроструктурой живых клеток и даже небольшими организмами. Благодаря этому флуоресцентная микроскопия оказалась оптимальным методом для изучения механизмов функционирования организмов на клеточном, субклеточном и молекулярном уровнях [6- 8].
Действительно, изменение клеточных характеристик под действием различных факторов как негативного (например, повышение температуры при хирургическом вмешательстве), так и позитивного характера (покрытия имплантатов, стимулирующие остеоинтеграцию, шероховатость) сопровождается изменением оптических характеристик тканей, что позволяет использовать данный факт для контроля динамики их состояния.
Целью работы является диагностика костных имплантатов и контроль процесса их остеоинтеграции с помощью метода конфокальной флуоресцентной микроскопии.
Материалы и методы исследования
В качестве объектов исследования были выбраны лиофилизированные биоимплантаты, изготовленные на сублимационной установке ALPHA2-4LSC из соединительных тканей человека по технологии «Лио-пласт»®, согласно ТУ-9398-001-01963143-2004. Данные имплантаты сохраняют свои первоначальные качества от 3 до 5 лет и удобны для транспортировки и хранения.
Экспериментальный стенд [9] был реализован на базе конфокального оптического микроскопа и лазерного комбайна фирмы ANDOR (скорость сканирования до 25 слоёв в секунду). На рис. 1 приведена блок-схема установки. Стенд обеспечивал два режима микросъёмки: режим конфокальной микроскопии в видимом свете и режим лазерной флуоресценции. В первом случае в качестве источника излучения использовался широкополосный источник (галогеновая лампа), а во втором – лазерные излучатели мощностью 100 мВт на длинах волн 488 нм и 561 нм.
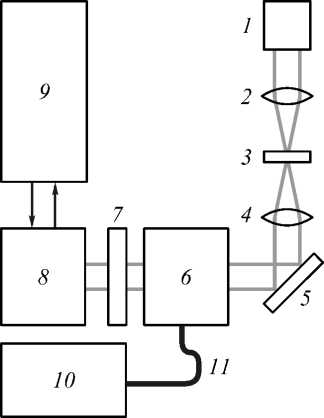
Рис. 1. Установка флуоресцентной конфокальной микроскопии: 1 – источник видимого света (галогеновая лампа), 2 – коллиматор, 3 – объект, 4 – объектив, 5 – поворотное зеркало, 6 – конфокальный сканирующий блок, 7 – блок фильтров, 8 – камера, 9 – компьютер, 10 – лазерный блок, 11 – волоконный ввод
В режиме конфокальной микроскопии свет от галогеновой лампы 1 (видимый диапазон) через блок фильтров поступает на систему фокусировки 2, которая фокусирует излучение на объекте 3. Прошедшее через объект (рассеянное вперед) излучение собирается объективом (20× или 40×) 4 и через систему зеркал и призм 5 вводится в сканирующий конфокальный блок 6. Сканирующий конфокальный блок построен по принципу Нипкова [10]: вращающиеся диски с микродиафрагмами, реализующими конфокальный метод. Перемещение фокальной плоскости (выделение анализируемого слоя ткани) осуществляется за счёт управляемого с компьютера пьезоэлектрического z-микросканера с установленным на нём объектом исследования. Спектральная фильтрация излучения осуществляется в блоке 7, реализованном в виде системы сменных фильтров, установленных на вращающейся турели. Спектральная фильтрация позволяет повысить контрастность регистрируемого изображения. После блока 7 излучение вводится в камеру 8 (1024×1024, время экспозиции 40 мс - 10 мин.). Для снижения темновых токов (в среднем на 3 порядка) матрица камеры охлаждается до температуры –75oC.
В режиме флуоресценции галогеновая лампа выключена. Вместо неё используется либо 4-модульный блок лазеров 10 (в настоящей работе использовались каналы излучения с длинами волн 488 нм и 561 нм), либо ртутная лампа. В обоих случаях используется волоконный ввод 11, а мощность каждого источника независимо управляется с компьютера (с шагом 0,1%). Фокусировка и согласование падающего излучения осуществляется в блоке 6 при помощи вращающегося диска с микролинзами, синхронизованного с диском Нипкова.
Результаты исследований
Динамика развития остеобластов была исследована в модельной среде (в чашке Петри). Наблюдения проводились в течение нескольких суток с регистрацией изображений (в том числе серийных) в режиме конфокальной микроскопии. Характерный микроснимок остеобластов в модельной среде представлен на рис. 2. Размер микроснимка 370×370 мкм, достигнутое разрешение составляет 400 нм на пиксель.
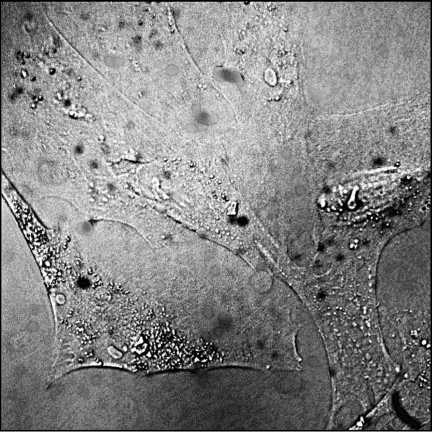
Рис. 2. Остеобласты в модельной среде в чашки Петри (размер снимка 370×370мкм)
Полученные результаты позволили детально описать динамику развития остеобластов в модельной среде: через 2 часа после пересева большая часть их пристаёт ко дну чашки Петри и распластывается по нему; через сутки формируется неполный равномерный монослой, в котором клетки соединены своими отростками; на вторые сутки количество клеток увеличивается, отростками клетки соединяются друг с другом (рис. 2); дальнейший рост количества клеток приводит к формированию равномерного монослоя; на 6 сутки образуется полный монослой, а на 7 сутки происходит насыщение и процесс переходит в стационарную фазу. Развитие остеобластов в модельной среде характеризуется своими особенностями: клетки имеют значительно большую длину (50– 100 мкм) и площадь сечения, чем в естественной среде, и образуют монослой. Вследствие этого изображение имеет низкую величину контраста – не более 0,2-0,3. Основное рассеяние даёт мембрана клетки и её ворсинки, что не позволяет должным образом визуализировать внутреннюю структуру клетки.
Переход в режим флуоресценции позволяет выделять не только клетки, но обеспечить и визуализацию ядра и органелл клетки. Для реализации режима флуоресценции нами был использован флуорофор, который при введении в среду концентрировался в цитоплазме клеток и возбуждался на длине волны 561 нм (рис. 3). В силу того, что флуорофор концен- трируется преимущественно в клетках, интенсивность фонового излучения на длине волны флуоресценции минимальна и контрастность изображения превышает 0,9. Хорошо видны отростки клеток, ядра, а также деление клеток (показано стрелкой). В отличие от красителей, традиционно используемых в гистологии, данный флуорофор не токсичен и позволяет детально исследовать динамику процессов. Так, для случая развития остеобластов в модельной среде измеренная скорость движения остеобластов составила 7- 8 мкм/час .
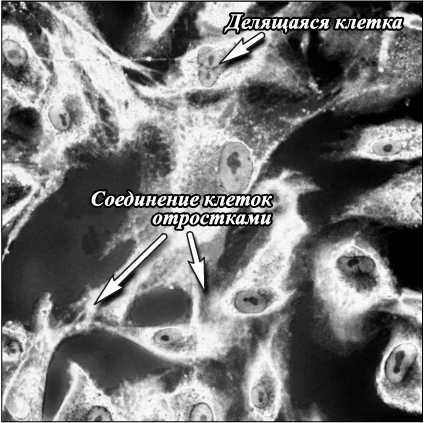
Рис. 3. Остеобласты в модельной среде в чашки Петри, 4 день (флюоресценция, размер снимка 370×370 мкм)
Отработанные на модельных средах режимы позволили перейти к исследованию интеграции остеобластов в костном имплантате. На рис. 4 представлен характерный микроснимок имплантата с остеобластами, полученный в режиме флуоресценции. Имплантат благодаря своей пористости тоже впитывает флуорофор, однако, несмотря на это, контраст изображения остаётся достаточно высоким (порядка 0,5 - 0,6) для уверенной визуализации остеобластов.
Анализ полученных микроснимков позволяет сделать вывод, что остеобласты активно интегрируют в костный имплантат (рис . 4), расселяясь преимущественно по его поверхности и формируя «колонии» вблизи выхода пор имплантата на его поверхность. Уже на восьмой день плотность активных остеобластов составляет 500-700 клеток/мм2.
Несомненным достоинством данного метода является возможность выявления именно активных остеобластов и возможность оценки скорости заселения остеобластами различных имплантатов в реальном масштабе времени. Это позволяет использовать данный метод для контроля и оптимизации условий изготовления и применения имплантатов.
Заключение
Показано, что метод конфокальной микроскопии позволяет осуществлять динамический контроль процесса интеграции различных типов клеток в костный имплантат с разрешением не хуже 400 нм. Данный метод позволит проводить дооперационное тестирование и контроль различных имплантатов с прогнозирования его качества.
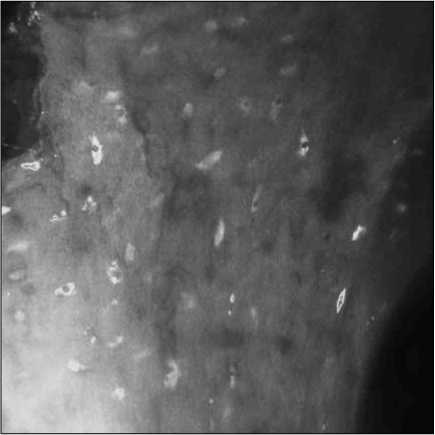
Рис. 4. Микроснимки интеграции остеобластов в костный имплантат спустя 8 дней (флуоресценция, размер снимка 370×370 мкм)
Работа выполнена при поддержке федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на 2009 - 2013 годы .


