Разработка элементов методики апомиктического размножения селекционно ценных образцов капусты кочанной
Автор: Кондратенко С.И., Чернышенко Т.В., Артемьева А.М.
Журнал: Овощи России @vegetables
Рубрика: Теория и практика селекции овощных культур
Статья в выпуске: 2 (11), 2011 года.
Бесплатный доступ
Выявлены экзогенные факторы, влияющие на проявление апомиксиса у капусты кочанной. Апомиктическое развитие семенных зародышей было получено у трех сортов капусты белокочанной - Яна, Лазурная и Леся украинской селекции. Удалось индуцировать незавершенный органогенез партеногенетических семян у четырех сортов капусты кочанной. Проявление нерегулярного апомиксиса было вызвано синергическим действием фитогормональных регуляторов и чужеродной пыльцы при условии одновременного нанесения водной смеси гиббереллина и ци-токинина на основание пестика, а чужеродной пыльцы (китайской редьки Лоба) - на рыльца пестиков кастрированных бутонов капусты за 2-3 суток до их раскрытия.
Капуста кочанная, апомиксис, экзогенные факторы
Короткий адрес: https://sciup.org/14024880
IDR: 14024880 | УДК: 582.683.2:581.1:631.811.982
Elaboration of elements of methods for apomictic propagation of valuable accessions of white head cabbage
Exogenous factors affecting on the expression of apomixis in cabbage have been identified. Apomictic seeds developed into embryoids were observed in three cabbage varieties such as Jana, Lazurnaya and Lesia (Ukraine). Thus, it was possible to induce an incomplete organogenesis of parthenogenesis seeds originated from these four varieties of cabbage. The occurrence of apomixis was provoked by the synergitic effect of plant growth regulators and alien pollen applied simultaneously as an aqueous mixture of gibberellins and cytokinin applied on the base of the pistil, while the alien pollen (Chinese radish - Loba) was placed on the stigma of castrated cabbage buds 2-3 days before they disclose.
Текст научной статьи Разработка элементов методики апомиктического размножения селекционно ценных образцов капусты кочанной
Апомиксис – природное явление, заключающееся в развитии зародыша из яйцеклетки или другой клетки зародышевого мешка при отсутствии опыления. Такой тип апомиксиса называется партеногенезом или апогамией и встречается в природе с достаточно низкой частотой проявления (10-6) [1]. В последнее время исследователями предпринимаются попытки индуцировать нерегулярный апомиксис у важнейших сельскохозяйственных растений. К сожалению, у большинства из них почти полностью отсутствует способность к апогамии. Согласно литературным данным у капусты кочанной удалось получить пар- теногенетические семена после экзогенной обработки неоплодотво-ренных завязей фитогормонами или их синтетическими аналогами, дей- ствие которых заключалось в стимуляции митотического деления и удвоения числа хромосом неоплодот-воренных яйцеклеток [2, 3]. Этими же авторами было показано, что на фенотипическое проявление партеногенеза в значительной степени влияет генотип растения, фаза развития зародышевого мешка, вид фитогормонов, их весовые соотношения в апомиктическом агенте для обработки и нормы расхода данного агента на одну неоплодотворенную яйцеклетку [2-4]. Учитывая литературные данные, в задачу наших исследований входила эксперимен- тальная проверка уже предложенных методик индуцирования нерегулярного апомиксиса капусты кочанной и возможная их оптимизация в случае получения отрицательного результата при использовании на наших растительных объектах.
Материалы и методы
Для получения апомиктических семян капусты кочанной использовались элементы методик, предложенные в работах [2, 4]. В качестве объектов исследований были использованы семенники капусты белокочанной сортов Лазурная, Лика, Леся, Белоснежка, Яна, Харьковская зимняя и капусты краснокочанной сорта Палета. В опыте изучались семенники капусты на начальном периоде фазы цветения (распускание цветков на главном стебле и осях первого порядка верхнего яруса). Для получения апомиктических семян первоначально проводилась процедура кастрации бутонов полностью сформированных цветков за 2-3 суток до их раскрытия. Кастрированные бутоны обрабатывали модифицированными вариантами апомиктического агента (АГ), в основе которого было обязательное присутствие водной смеси регуляторов роста – гиббереллина (ГК3) и цитокинина (БАП) с добавлением других биологически-активных веществ. Перед нанесением АГ у кастрированных бутонов обрабатывали рыльца и пестики 96%-водным раствором этилового спирта для удаления на их поверхности случайно попавшей пыльцы капусты. Затем с помощью микропипетки на основание пестиков наносили 10 мкл АГ. Процедуру кастрации проводили в утренние часы суток (7-10 ч.). Обработанные, таким образом, репродуктивные побеги с кастрированными бутонами изолировали от остальных пергаментными изоляторами до времени полной потери восприимчивости рыльца к пыльце капусты на
8-10 суток. На семенниках, с обработанными АГ бутонами, оставляли стебли, на которых проходило свободное опыление цветков капусты насекомыми. После удаления изоляторов проводили фенологические наблюдения за ростом стручков и формированием апомиктических семенных зародышей в течение всего периода роста семенников до полного вызревания семян капусты, которые образовывались в результате свободного внутрисортового опыления.
Результаты и их обсуждение
В 2006 году были начаты исследования по индукции нерегулярного апомиксиса на экспериментальной базе Института овощеводства и бахчеводства НААН. При использовании методических рекомендаций по обработке АГ кастрированных бутонов цветков, предложенных в работах [2, 4], по истечении срока вызревания семенников в наших опытах наблюдали формирование только бессемянных стручков у всех изученных сортов капусты кочанной. Согласно данных вышеуказанных литературных источников на капусте белокочанной удалось получить патреногенетические семе-
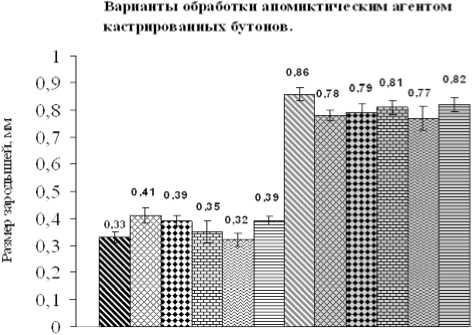
Рис. 1. Результаты биометрических измерений (в световом поле бинокуляра) длины 10 рендомизировано отобранных апомиктических зародышей капусты кочан-
ной разных сортов, проведенные в конце периода созревания семенников (дан-
ные 2007 года).
123456789 10 11 12
на при обработке АГ, содержащем водный раствор гиббереллина (ГК3) [2] или гиббереллина (ГК3) и цитокинина (БАП) [4].
В 2007 году был расширены поисковые работы по оптимизации компонентного состава АГ. В отличие от предыдущего года в работе использовали следующие варианты обработки кастрированных бутонов:
-
1) АГ № 1 – водная смесь ГК3 и
- БАП (контроль);
-
2) АГ № 2 – водная смесь ГК3, БАП и препарата Марс-El;
-
3) АГ № 1 с дополнительным одновременным нанесением на рыльце инородной пыльцы несовместимых с капустой кочанной видов растений семейства крестоцветные;
-
4) АГ № 2 с дополнительным одновременным нанесением на рыльца инородной пыльцы несовместимых с капустой кочанной видов растений семейства крестоцветные.
В результате проведенных исследований были выделены, как наиболее перспективные для дальнейшей работы 3-й и 4-й варианты обработки, при использовании которых был обнаружен эффект кратковременного роста апомиктических семенных
Сорта капусты кочанной.
-
к I Лазурная < вар 1)
-
Q 2. Тика (вар 1)
-
0 5. X зимняя (вар !)
В 3 Белоснежка (ва)) 1)
В 4 Яна (вар 1)
-
9 6 Палета (вар 1)
я7 Лазурная (вар.З)
S 8 Лика (вар 3)
Q 9. Белоснежка (вар 3)
S 10 Яна (вар.З)
-
§ 11 X зимняя (вар 3)
-
в 12 Палета (вар.З)
зародышей в стручках всех задействованных в эксперименте сортовых генотипов капусты кочанной. После эмпирического перебора был обнаружен вид растения семейства Brassicaceae – подвид китайской редьки Лоба (Convar lobo Sazon) вида Raphanus sativus L., пыльца с растений которой обеспечивала вышеуказанный прирост. В частности, в наших экспериментах использовали сорт Трояндовая селекции ИОБ НААН вышеуказанного подвида редьки.
На рис. 1 представлены результаты биометрических измерений длины семенных апомиктических зародышей у сортов капусты кочанной, которые были задействованы в 1-м и 3-м вариантах опыта. Из полученных данных следует, что синергическая обработка АГ № 1 и пыльцой редьки Лоба (3-й вариант) стимулирует частичный рост зародышей, увеличивая их размер в 1,8-2 раза, по сравнению с обработкой только АГ № 1 (1-й вариант). На рис. 2 показаны фотографии сформированных стручков с недоразвитыми зародышами, которые были получены во 2м и 4-м вариантах обработки семенников сорта капусты краснокочанной Палета.
В общем, если использовали для обработки АГ № 1 или АГ № 2 (1-й и 2-й варианты обработки), то при этом наблюдали исключительно пар-тенокарпический рост стручков без роста зародышей. Использование препарата Марс-El в смеси с фито-гормональными регуляторами было обусловлено его функциональной особенностью, как пленкообразующего и водоудерживающего вещества для сохранения на более длительное время на поверхности пестика капли водной смеси ГК3 и БАП [5]. Однако в дальнейших опытах было обнаружено негативное действие данного препарата на органогенез семенных зародышей, поэтому он был исключен из работы.
В 2008 году использовали следу- ющие варианты обработки кастрированных бутонов:
-
1) АГ № 1 – водная смесь ГК3 и
- БАП (контроль);
-
2) АГ № 2 – АГ №1 с дополнительным одновременным нанесением на рыльце пыльцы редьки сорта Трояндовая;
-
3) АГ № 3 – водная смесь ГК3, БАП и регулятора ДГ-475(12) с дополнительным одновременным нанесением на рыльце пыльцы редьки сорта Трояндовая.
При использовании 1-го варианта обработки мы наблюдали только партенокарпический рост стручков. По результативности выделили 2-й и 3-й варианты обработки. Как и в опыте 2007 года, при применении 2-го варианта у сортов Лика, Белоснежка, Яна, Харьковская зимняя обнаружен эффект кратковременного роста апомиктических зародышей. В отличие от предыдущих лет исследований были увеличены репрезентативные выборки бутонов по каждому сорту капусты кочанной (на одном семеннике 10-15 образцов в
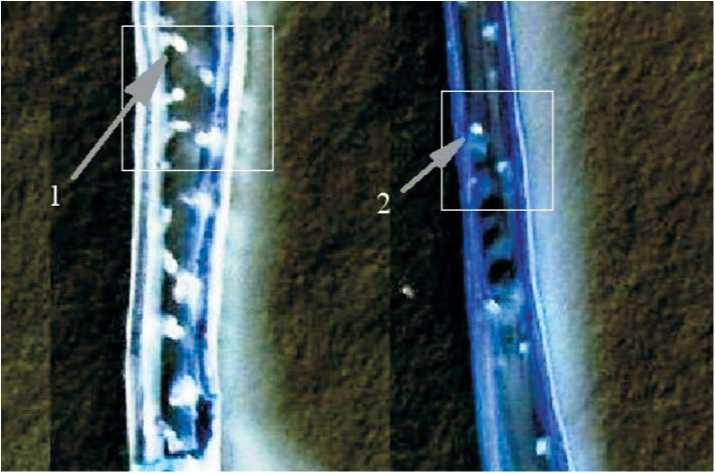
Рис. 2. Временная стимуляция формирования апомиктических зародышей в 4-м варианте и ее отсутствие во 2-м варианте опыта по индукции нерегулярного апомиксиса (растения репродуктивной фазы развития сорта капусты краснокочанной Палета, данные 2007 года):
1) 4-й вариант обработки (нанесение на пестики АГ № 2 и пыльцы дикой редьки на рыльца кастрированных бутонов);
2) 2-й вариант обработки (нанесение на пестики АГ № 2).
2006-2007 годах и 50-70 образцов в 2008 году). В результате во 2-м варианте обработки у сорта капусты белокочанной Леся было обнаружено формирование апомиктических семян (14 образцов, частота образования 25,6 %) и у сорта Лазурная – 2 образца (частота образования 2,9 %). Применение АГ № 3, также, оказалось эффективным на сорте капусты краснокочанной Палета (прирост семенных зародышей в 3-3,5 раза больший по сравнению с вариантом обработки АГ № 1). Данный экспериментальный факт свидетельствует о довольно существенном влиянии генотипа сорта на фитогормональный состав АГ, обнаружено избирательное позитивное действие на данный сорт капусты препарата ДГ-475 (12), который является химическим соединением, производным пиридина. ДГ-475 (12) ранее использовали мы в опытах по культуре протопластов капусты белокочанной in vitro, как регулятор, инициирующий и поддерживающий митотическую активность соматических клеток [6]. Аналогично предыдущим годам исследований, в 2008 году АГ № 1 не обнаружил высокой стимулирующей активности, поэтому в дальнейшем был исключен из работы.
В 2009 году использовали такие же модификации компонентного состава АГ, как и в 2008 году (только 2й и 3-й варианты обработки). Получены партеногенетические семена сорта капусты белокочанной – Яна (4 семени, частота образования 3,2 %). Позитивное регуляторное действие на формирование апомиктических семян имела синергическая обработка кастрированных бутонов АГ №3 и пыльцой растений редьки сорта Трояндовая.
Опыты 2010 года оказались неудачными вследствие неблагоприятных климатических условий, которые сложились в период вызревания семенников капусты. В течение мая-июня месяца были отмечены высокие дневные температуры воздуха до 40оС. При такой высокой температуре пыльца китайской редьки Ло-ба теряла свою фертильность, что негативно сказалось на завязывании партеногенетических семян капусты кочанной.
Как правило, полностью сформированные партеногенетические семена завязывались в проксимальной части (по отношению к столбику) за- вязи в количестве 1-2 экземпляров на стручок (рис. 3.). Все апомиктические семена показали 100 % всхожесть в лабораторных условиях при проращивании в чашках Петри на влажных фильтровальных мостиках.
Рис. 3. Сформированное партеногенетическое семя в проксимальной части завязи
(сорт капусты белокочанной Лазурная, опыт 2008 года)

Заключение и выводы
В результате проведенных исследований выявлены экзогенные факторы, влияющие на проявление нерегулярного апомиксиса у капусты кочанной. Из семи изученных сортов партеногенетические семена были получены у трех сортов капусты кочанной – Яна, Лазурная и Леся с разной частотой формирования в зависимости от генотипа сорта. Действием экзогенных факторов удалось индуцировать незавершенный органогенез партеногенетических семян у всех остальных сортов капусты кочанной. Проявление нерегулярного апомиксиса было вызвано синергическим воздействием фито-гормональных регуляторов и чужеродной пыльцы при условии одновременного нанесения водной смеси гиббереллина и цитокинина на основание пестика, а чужеродной пыльцы (китайской редьки Ло-ба) – на рыльца пестиков кастрированных бутонов капусты за 2-3 суток до их раскрытия.
Список литературы Разработка элементов методики апомиктического размножения селекционно ценных образцов капусты кочанной
- Тырнов В.С. Гаплоидия у растений: научное и прикладное значение//М.:Наука.-1998.-53с.
- Eenink A.H. Matromorphy in Brassica oleracea L. IV. Formation of homozygous and heterozygous diploid products of gametogenesis and qualitative genetical research on matromorphic plants//Euphytica -1974. -V. 23. -P. 719-724.
- Бабицкий А. Эволюция и репродуктивная память//Reports and Abstracts of the VIII Geneticist's and Breeder's Congress of Moldova «Genetics and breeding of Plants, Animals and Microorganisms». -Chishinau (Moldova), 2005. -С 696-701.
- Способ получения гомозиготных диплоидов сельскохозяйственных культур: Патент. Российская Федерация. A01H 1/04, A 01N 43/40, 61/00/В.Г. Курбатов -№ 2035134; Заявл. 23.01.91; Опубл. 20.05.95, Бюл. № 14.
- Кондратенко С.И., Чернишенко Т.В., Баштан Н.А., Дульнєв П.Г. оценка регуляторного эффекта биологично-активных соединений, производных пиридина и полиэтиленгликоля на вегетирующих растениях капусты белокочанной//овощеводство и бахчеводство. -Харьков: ИОБ УААН. -2005. -Вып. 50. -С. 342-351.
- Kondratenko S.I. Effect of plant extract and new synthetical substitutes of phytohormones on plant regeneration from protoplasts of cabbage (Brassica oleracea var. capitata)//Horticulture and Vegetable Growing. -Babtai: Lithuanian Institute of Horticulture. -2001. -V.20(3), №1. -P. 343-349.


