Автоматизированная лазерная коагуляция сетчатки: реализация принципа обратной связи в условиях in vitro
Автор: Бойко Э.В., Суетов А.А., Докторова Т.А., Измайлов А.С., Иванов А.А., Пищелин А.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.18, 2023 года.
Бесплатный доступ
Обоснование. Лазерная коагуляция остается важным методом лечения ряда заболеваний сетчатки, при этом в зависимости от патологии требуется различное по интенсивности воздействие. Разработка лазерных систем с автоматическим контролем формируемых коагулятов может повысить эффективность проводимого лазерного лечения.
Сетчатка, лазерная коагуляция, автоматизированная лазерная система, обратная связь
Короткий адрес: https://sciup.org/140302485
IDR: 140302485 | DOI: 10.25881/20728255_2023_18_4_S1_9
Automated laser coagulation of the retina: implementation of the feedback principle in vitro
Background. Laser photocoagulation is an important treatment method for the various retinal diseases. The development of laser systems with automatic control of the resulting coagulates will improve the effectiveness of laser treatment.
Текст научной статьи Автоматизированная лазерная коагуляция сетчатки: реализация принципа обратной связи в условиях in vitro
Обоснование
Лазерная коагуляция остается важным методом лечения таких заболеваний сетчатки, как например, периферические разрывы и регматогенные дегенерации сетчатки, диабетическая и постокклюзионная ретинопатия, экстрафовеальная хориоидальная неоваскулярная мембрана или центральная серозная хориоретинопатия с идентифицированной точкой просачивания [1; 2]. При

этом параметры лазерного воздействия зависят от клинической ситуации и основываются, главным образом, на глубине (характеризующейся как степень) получаемого ожога на глазном дне и площади как единичного ожога, так и группы ожогов [3; 4]. При традиционной лазерной коагуляции параметры воздействия, как правило, в разных участках сетчатки постоянны, что может приводить к ее неодинаковому термическому повреждению. Слабая пигментация глазного дна и снижение прозрачности оптических сред не позволяют точно оценить степень формируемого коагулята. В результате, чрезмерное или недостаточное воздействие может снижать эффективность проводимого лазерного лечения. С другой стороны, используемая градация интенсивности лазерного воздействия по F.A. L’Esperance [4] не учитывает особенности пигментации глазного дна, является субъективной и недостаточно точна, но все еще остается общепринятой практикой.
Ранее были описаны ряд лазерных систем, реализующих принцип обратной связи для контроля интенсивности коагуляционного воздействия на сетчатку. В одних из них в оптическую систему интегрировали рефлектометр для контроля лазерного воздействия, в других воздействие контролировалось компьютерной программой посредством видеокамеры, интегрированной в оптическую систему мидриатической фундус-камеры [5; 6]. Также описана лазерная система с автоматическим контролем коагуляции тканей на основе оптоакустического эффекта [7; 8].
Описанные в литературе системы являются экспериментальными, при этом использованные подходы имеют свои ограничения. Тем не менее, разработка лазерных систем с автоматическим контролем яркости формируемых коагулятов может повысить эффективность проводимого лазерного лечения, сделав его более безопасным, воспроизводимым и быстрым.
Цель
Изучить в условиях in vitro возможность проведения дозируемой лазерной коагуляции с помощью автоматизированной лазерной системы, работающей по принципу обратной связи.
Материалы и методы
Прототип разработанной системы автоматизированной управляемой лазерной коагуляции включает в себя лазерный модуль АЛОД-01 с длиной волны генерируемого лазерного излучения (ЛИ) 0,81 мкм (Алком Медика, Россия), лазерную приставку для транспупиллярной коагуляции ПФК-2 (Алком Медика, Россия) и видеоадаптер с видеокамерой ToupcamMicro U3CMOS03100KPA (Touptek, КНР), смонтированные на щелевой лампе Takagi SM-2N (Takagi, Япония). Лазерный модуль и видеокамера подключены к персональному компьютеру (ПК), на котором с помощью программного обеспечения происходит управление процессом лазерного воздействия.
Настройки видеокамеры и щелевой лампы обеспечивают видеозахват с частотой 60 Гц, при этом в каждом кадре управляющая программа последовательно анализирует средний уровень яркости пикселей в участке изображения, соответствующем пятну планируемого лазерного воздействия, и сравнивает их с окружающей пятно областью. Во время воздействия ЛИ происходит формирование коагулята, отличающегося по яркости от окружающего фона, и как только достигается заданный уровень яркости, программа отключает лазер. В программе предусмотрен выбор диаметра пятна, соответствующего зоне самого лазерного воздействия, диаметра зоны, служащей для сравнения, при этом программа автоматически отслеживает положение метки пилотного лазера (0,65 мкм), перемещая в него указанные зоны. Во время лазерного воздействия пилотный лазер отключается, исключая его влияние на анализ видеопотока, фиксируемые при видеозахвате блики и засветы (артефакты) программа исключает из анализа.
Лазерный модуль работает в режиме непрерывной генерации ЛИ, при этом длительность воздействия в выбранной точке зависит от предустановленной мощности ЛИ и выбранного порога коагуляции, определяемого как соотношение получаемой при коагуляции и фоновой яркости (в % от порогового значения).
Для экспериментов in vitro использовали оригинальную модель глазного дна, представляющую собой заключенный между двумя покровными стеклами блок из копировальной бумаги (акцептор ЛИ, имитирующий пигментный эпителий сетчатки), покрытый слоем яичного альбумина (модель нейроретины). Во время воздействия ЛИ поглощается копировальной бумагой, при это выделяется тепло, обеспечивающее коагуляцию альбумина. Глубина коагуляции и, соответственно, яркость ожога, зависят от мощности и длительности воздействия ЛИ в выбранной точке.
Лазерное воздействие производили через трех-зер-кальную линзу Гольдмана с контактным гелем (Визитил), при этом диаметр пятна ЛИ на поверхности модели составил 200 мкм. В работе исследовали время формирования и однородность получаемых коагулятов по яркости, соответствие планируемой и фактической яркости коагулята при мощности ЛИ 100, 140, 180, 200 и 300 мВт и яркости, превышающей значение пороговой яркости на 5, 10, 15, 20, 25, 30, 35, 40, 50 и 70%.
Статистическая обработка результатов исследования проводилась методами параметрического и непараметрического анализа с использованием программы Statistica 12.0 (StatSoft Inc., США). Статистически значимыми считали результаты с уровнем значимости p<0,05.
Результаты
На Рис.1 представлен пример проведения дозируемой лазерной коагуляции с помощью автоматизированной лазерной системы, работающей по принципу обратной связи, в условиях модели глазного дна.
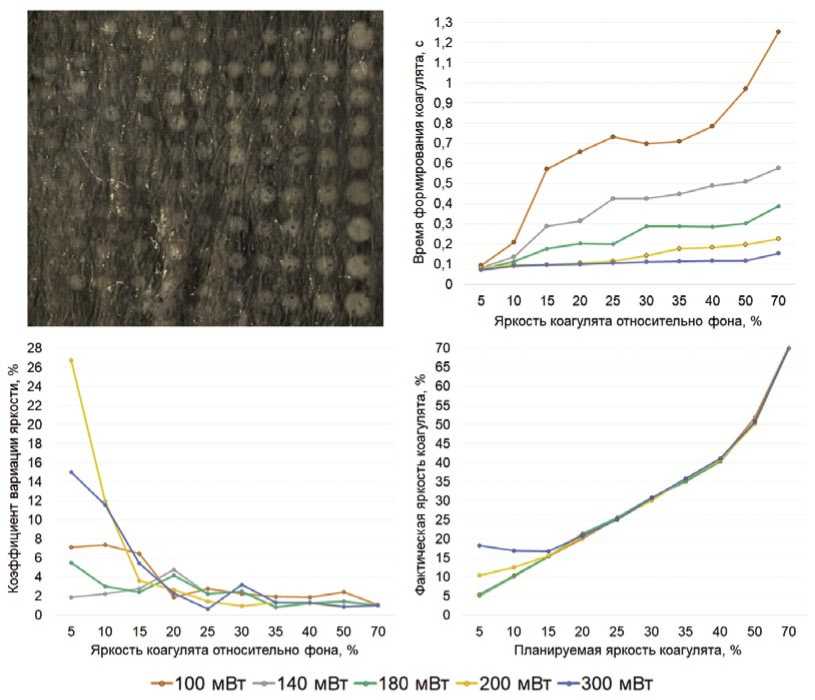
Рис. 1. Пример проведения дозируемой лазерной коагуляции с помощью автоматизированной лазерной системы, работающей по принципу обратной связи, в условиях модели глазного дна и анализ формируемых лазерных коагулятов по времени формирования, однородности и соответствию получаемых планируемым коагулятам (пояснения в тексте).
Время формирования коагулятов зависело от выбранных уровня мощности ЛИ и требуемой яркости коагулята. При мощности 200 и 300 мВт время формирования коагулята не превышало 200 мс независимо от требуемой яркости, в то время, как при мощности 100 мВт и планируемой яркости коагулята 15% и более от уровня фона необходимое для формирования коагулята время составило более 500 мс (Рис. 1). Наиболее оптимальный уровень мощности ЛИ 180 мВт, при котором даже на уровне яркости 50-70%, соответствующем 3 степени ожога по F.A. L’Esperance, время формирования коагулята не превышало 400 мс, что сопоставимо с длительностью импульса при традиционной коагуляции сетчатки.
Однородность получаемых коагулятов по яркости также отличалась в зависимости от мощности ЛИ и требуемой яркости коагулята.
Наибольшие значения коэффициента вариации яркости коагулятов (26,7 и 15%, Рис. 1) были отмечены при мощности воздействующего ЛИ 200 и 300 мВт с планируемой яркостью коагулятов, близкой к пороговой – 5% от уровня фона, что было обусловлено недостаточной скоростью видеозахвата для последующего своевременного отключения лазера в условиях более высокой мощности
ЛИ. Одновременно, при яркости коагулята более 15% от фона независимо от мощности ЛИ коэффициент вариации не превышал 7%, что позволяет говорить о высокой однородности коагулятов, получаемых в автоматическом режиме.
Планируемая и фактическая яркость формируемого коагулята в наибольшей степени совпадали при использовании мощности ЛИ в диапазоне 100–180 мВт для всех значений яркости от 5 до 70% (Рис. 1). При использовании мощности ЛИ 200 и 300 мВт фактическая яркость превышала планируемую в диапазоне яркости менее 15% от фона, то есть при формируемых коагулятах 1 степени по F.A. L’Esperance.
Проведенное исследование in vitro показало возможность проведения в автоматическом режиме дозируемой лазерной коагуляции, при этом получаемые коагуляты обладают высокой степенью однородности по яркости, и их фактическая яркость соответствует запланированной практически во всем протестированном диапазоне яркости и мощности. Полученные результаты свидетельствуют, что параметры лазерной системы ограничивают ее работу при необходимости получения близких к пороговым значениям коагулятов.

Заключение
В условиях in vitro новая автоматизированная лазерная система, работающая на принципе обратной связи, позволяет получить однородные воспроизводимые лазерные коагуляты в автоматическом режиме, при этом в наибольшей степени соответствие фактической и планируемой яркости коагулятов достигается при выходной мощности лазерного излучения в диапазоне 140–180 мВт.
Источник финансирования: исследовательская работа проведена на личные средства авторского коллектива.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Автоматизированная лазерная коагуляция сетчатки: реализация принципа обратной связи в условиях in vitro
- Бойко Э.В. Лазеры в офтальмохирургии: теоретические и практические основы. СПб: ВМедА им.С.М.Кирова; 2003.
- Boiko E.V. Lazery v oftal'mohirurgii: teoreticheskie i prakticheskie osnovy. SPb: VMedA im.S.M.Kirova; 2003].
- Фёдоров С.Н. Лазерные методы лечения заболеваний глаз. Москва: Медицина; 1990.
- Fyodorov SN. Lazernye metody lecheniya zabolevanij glaz. Moskva: Medicina; 1990].
- Ardamakova AV, Bol'shunov AV, Ilyina TS, Fedoruk NA, Siplivyl VI. Transpupillary laser photocoagulation of ocular fundus: history, the present, and the future. Vestnik Oftalmologii. 2017;133(1):81-87. (In Russ.). DOI: 10.17116/oftalma2017133181-87 EDN: YFMPYJ
- L'Esperance FA. Ophthalmic Lasers. Photocoagulation, Photoradiation and Surgery. St. Louis: Mosby; 1989.
- Inderfurth JHC, Ferguson RD, Frish MB, Birngruber R. Dynamic reflectometer for control of laser photocoagulation on the retina. Lasers Surg Med 1994;15:54-61. DOI: 10.1002/lsm.1900150108
- Jerath MR, Chundru R, Barrett SF, Rylander HG, Welch AJ. Reflectance Feedback Control of Photocoagulation in Vivo. Arch Ophthalmol 1993;111: 531-4. DOI: 10.1001/archopht.1993.01090040123045
- Schlott K, Koinzer S, Ptaszynski L, Bever M, Baade A, Roider J, et al. Automatic temperature controlled retinal photocoagulation. J Biomed Opt 2012;17:061223. DOI: 10.1117/1.JBO.17.6.061223
- Серебряков В.А., Бойко Э.В., Ян А.В. Оптико-акустический мониторинг температуры сетчатки при лазерной терапии в режиме реального времени. Оптический журнал. 2014;81(6):14-16. EDN: TQQKIP
- Serebryakov VA, Boiko fiV, Yan AV. Real-time optoacoustic monitoring of the temperature of the retina during laser therapy. J. Opt. Technol. 2014;81(6):14-16. (In Russ.). DOI: 10.1364/JOT.81.000312 EDN: TQQKIP


