Бактерицидные и фунгицидные свойства ацетиленовых четвертичных аммониевых солей
Автор: Андреев Владимир Петрович, Зачиняева Анна Владимировна, Ремизова Людмила Александровна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Медицинские науки
Статья в выпуске: 4 (125), 2012 года.
Бесплатный доступ
Диско-диффузионным методом показано, что моноацетиленовые четвертичные аммониевые соли обладают более слабым, но более избирательным бактерицидным и фунгицидным действием по отношению к микроорганизмам Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 25922, Proteus vulgaris, Proteus mirabilis, Penicillium spp. и Bacillus cereus, чем не содержащий тройной связи триоктилметиламмоний иодид и диацетиленовый диоктилди(гепт-2-инил)аммоний бромид. Только триоктил(гепт-2-инил)аммоний иодид активен по отношению к Saccharomyces cerevisiae.
Ацетиленовые четвертичные аммониевые соли, противомикробные, бактерицидные, фунгицидные свойства, дезинфекция
Короткий адрес: https://sciup.org/14750153
IDR: 14750153 | УДК: 547.333.4+579.23+579.25+579.66
Bactericidal and fungicidal properties of acetylenic quaternary ammonium salts
Disco-diffusion method revealed that monoacetylenic quaternary ammonium salts have weaker but more selective bactericidal and fungicidal activity against Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 25922, Proteus vulgaris, Proteus mirabilis, Penicillium spp. and Bacillus cereus microorganisms than trioctylmethylammonium iodide and diacetylenic dioctyldi(hept-2-ynyl) ammonium bromide, which do not contain a triple bond. Only trioctyl (hept-2-ynyl) ammonium iodide is active against Saccharomyces cerevisiae.
Текст научной статьи Бактерицидные и фунгицидные свойства ацетиленовых четвертичных аммониевых солей
Среди четвертичных аммониевых соединений (ЧАС, [R 1 R 2 R 3 R 4 N] + X - ) наибольшее практическое значение имеют алкилбензилди-метиламмонийхлорид, смесь равных частей ал-килбензилдиметиламмонийхлорида с алкилди-метилбензиламмоний хлоридом, диоктилдиме-тиламмонийхлорид, дидецилдиметиламмоний хлорид, смесь октилдецилдиметиламонийхло-рида (50 %) с диоктилдиметил-аммоний-хлори-дом (25 %) и дидецилдиметиламмоний хлоридом (25 %), которые входят в состав большинства современных дезинфекционных и антисептических средств [7]. Действующим веществом в средстве «ДЕЗЭФЕКТ-САНИТ» является смесь 6 четвертичных аммониевых солей, суммарное содержание которых составляет 3,8 %. В состав смеси этих ЧАС входят октилдецилдиметилам-моний хлорид (30,0 %), тетрадецилдиметил бен-зиламмоний хлорид (20,0 %), додецилдиметил бензиламмоний хлорид (16,0 %), диоктилдиме-тиламмоний хлорид (15,0 %), дидецилдимети-ламмоний хлорид (15,0 %) и гексадецилдиметил бензиламмоний хлорид (4,0 %) [11].
Согласно [12], среднегодовые темпы роста спроса на дезинфекционные и антисептические средства из группы ЧАС в промышленно развитых странах составляют 6–7 %, причем в настоящее время наблюдается отчетливая тенденция возрастания объемов потребления препаратов, в состав которых они входят в смеси с другими активно действующими веществами (АДВ) аль
дегидами, производными гуанидина, алкилами-нами, пероксисоединениями, спиртами и др.
Первым комплексным препаратом широкого спектра действия стало дезинфицирующее средство «Лизафин», зарегистрированное в РФ в 1999 году. Оно обладает антимикробной активностью в отношении Гр + и Гр - бактерий (в том числе возбудителей внутрибольничных инфекций, микобактерий туберкулеза, чумы и холеры), грибов рода Candida и Trichophyton, вирусов – возбудителей гепатита, полиомиелита и других энтеровирусных, аденовирусных инфекций, вирусов группы Herpesviridea, ВИЧ-ассоциированных инфекций. В качестве действующих веществ в состав препарата были введены алкилдиметилбензиламмоний хлорид, глутаровый альдегид и глиоксаль. Основными достоинствами альдегидов являются щадящее действие на объекты и наличие антимикробной активности в отношении всех видов микроорганизмов за счет алкилирования амино-, карбоксильных и сульфгидрильных групп протеинов и других органических соединений и подавления синтеза последних.
ЧАС проявляют сравнительно узкий спектр противомикробной активности: они эффективны в отношении возбудителей кишечных и воздушно-капельных инфекций бактериальной этиологии, грибов, некоторых вирусов, однако недостаточно активны в отношении культур Proteus vulgaris, Proteus morganii, Proteus mirabilis, что существенно ограничивает возможности их применения для профилактики нозокомиальных инфекций. По данным [30], около 89,5 % госпитальных штаммов микроорганизмов рода Proteus резистентны к ЧАС. Имеют место случаи нозокомиальных инфекций (сепсис с высоким процентом летальности), которые связаны с использованием в клинике растворов ЧАС, контаминированных культурами Proteus mirabilis [29]. Большинство препаратов этой группы не активны в отношении вирусов, споровых форм бактерий и микобактерий туберкулеза [7], [25], [32]. В экспериментальных и клинических условиях установлена гетерогенность чувствительности популяций бактерий к ЧАС. В частности, бактериальные клетки одного штамма Escherichia coli, находящиеся на разных стадиях онтогенетического развития, проявляют неодинаковую чувствительность к препаратам этой группы. Переход культуры из экспоненциальной к стационарной фазе роста сопровождается уменьшением гидрофобности и повышением содержания липополисахаридов во внешней мембране клеток, которые защищают цитоплазматическую мембрану от дезорганизации под влиянием ЧАС [10]. Экспоненциальные клетки Гр+ микроорганизмов (B. cereus), наоборот, уступают в чувствительности к ЧАС клеткам, которые находятся в стационарной фазе роста [7].
Учитывая сравнительно узкий спектр про-тивомикробной активности, дезинфекционные средства из группы ЧАС применяют для дезинфекции ограниченного круга объектов в учреждениях здравоохранения – поверхностей помещения (стены, пол, окна, двери, оконные стекла), предметов обстановки, медицинских приборов, оборудования и аппаратов с лакокрасочным, гальваническим и полимерным покрытием, предметов ухода за больными, нательного и постельного белья, однако их не используют для дезинфекции хирургического и стоматологического инструментария вследствие ограниченного спектра противомикробной активности ЧАС [27]. Многочисленные экспериментальные исследования и клинические наблюдения свидетельствуют о быстром формировании и распространении резистентных к ЧАС бактерий в учреждениях здравоохранения и окружающей среде. Например, чувствительность клинических изолянтов Staphylococcus aureus к препаратам из группы бис-четвертичных аммониевых соединений (декаметоксин, этоний) на протяжении 10-летнего периода снизилась в 2–10 раз [7]. Это обусловлено недостаточно обоснованным применением одних и тех же препаратов из группы ЧАС в учреждениях здравоохранения, ветеринарии, пищевой и перерабатывающей промышленности, в быту. Дезинфекцию объектов (емкости, коммуникации, трубопроводы и др.) в таких отраслях пищевой промышленности, как пиво-безалкогольная, молочная, кондитерская, выполняют объемным способом – заполняют их рабочим раствором дезинфекционного средства с последующим сбросом в канализационную систему. Такой способ дезинфекции обусловливает поступление значительных количеств ЧАС в объекты внешней среды (вода водоемов, почва) и селекцию устойчивых к ним вариантов микроорганизмов.
Таким образом, существующий ассортимент средств дезинфекции из группы ЧАС не полностью отвечает современным требованиям к свойствам препаратов этой группы по таким критериям, как универсальность (применяют для дезинфекции сравнительно узкого круга объектов), узкий спектр противомикробной активности, сравнительно быстрое формирование и распространение резистентных к ЧАС видов микроорганизмов .
Целью данной работы явился поиск новых типов ЧАС, у которых отсутствуют отмеченные недостатки.
Хорошо известно, что к основным элементам структуры, обусловливающим противомикроб-ные свойства ЧАС, относятся гидрофильные полярные четвертичные аммониевые группы и гидрофобные углеводородные радикалы [7]. Соединения, содержащие короткоцепочечные углеводородные радикалы у атома четвертичного азота, проявляют умеренные противо-микробные свойства или лишены их. Увеличение количества атомов углерода в радикале до восьми приводит к появлению поверхностной активности и вместе с ней противомикробных свойств. Активность повышается при введении в структуру ЧАС ненасыщенных углеводородных радикалов [28], асимметричного атома азота [15], простых эфирных связей [7]. Среди моночетвертичных аммониевых солей максимальную активность, как правило, проявляют соединения, которые содержат 12–16 атомов углерода в радикале [14], [17]. Дальнейшее удлинение углеродной цепи приводит к снижению активности [22]. Согласно [8], противомикробные свойства ЧАС коррелируют с поверхностной активностью. Эти соединения концентрируются на поверхности раздела фаз «раствор : поверхность клетки бактерий», встраиваются в цитоплазматическую мембрану с последующими изменениями конформации мембранных липидов, что приводит к повышению проницаемости цитоплазматической мембраны.
Токсичность ЧАС, наоборот, находится в обратно пропорциональной зависимости от длины углеродной цепи – уменьшается по мере того, как увеличивается количество атомов углерода в радикале. Кроме того, алифатические ЧАС менее токсичны, чем циклические [21], а ацетиленовые соединения менее токсичны, чем олефиновые, и особенно алифатические [1].
В литературе отмечаются особые свойства четвертичных аммониевых солей, содержащих длинноцепной ацетиленовый радикал, в частности их повышенная бактерицидная активность [16]. Поэтому мы поставили задачу выяснить влияние длины и числа алкильных и алкинильных групп в ЧАС на бактерицидные и фунгицидные свойства этих веществ.
В качестве обьектов исследования были выбраны следующие соединения:
[(C8H17)3NCH2C CH] Br [(C10H21)3NCH2C CC6H13] Br [(C 8 H 17 ) 3 NCH 2 C CC4H9 ] I
[(C8H17)2N(CH2C CC4H9)2] Br
[(C 8 H 17 ) 3 NCH 3 ]I
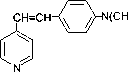
I
O
Следует отметить, что ЧАС (1–4) могут быть легко синтезированы по разработанной нами методике кватернизацией триоктиламина, тридециламина и диоктил(ди-2-гептинил)амина соответствующими галогенидами пропаргильного типа в очень мягких условиях [1], [3]. Реакция между этими реагентами при комнатной температуре заканчивается в ацетонитриле за 1–2 часа, а в пентане за 1–2 суток с выходами ЧАС, близкими к количественным. Указанные моно- и диацетиленовые ЧАС содержат от 27 до 39 атомов углерода, в качестве стандарта использован алифатический аналог (5) с 25 атомами углерода.
N-оксид транс-4-(4-диметиламиностирил) пиридина (4-DPyO) был получен согласно методике [2]. Последнее соединение было выбрано нами для исследований, поскольку стирильные производные вида
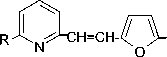
NO2
R = CH2OCONHAc, CH2Cl, CH2I, CH2OP(O)(OH)2, CH2NRR' и др.
обладают противомикробной, противодерма-тозной и противопротозойной активностью [13], а 4-DPyO – апоптогенной активностью [5].
Экспериментальные данные относительно чувствительности микроорганизмов к химиотерапевтическим препаратам, полученные нами диско-диффузионным методом, даны в таблице, в которой представлены все классы микроорганизмов (бактерии и грибы), имеющие эпидемиологическое значение.
К сожалению, стирильное производное N-оксида пиридина (6) оказалось неактивным по отношению ко всем видам микроорганизмов, в то время как ЧАС в зависимости от строения проявляют избирательное биологическое действие.
Следует отметить (см. таблицу), что Proteus vulgaris (тест-культура № 3) резистентна ко всем образцам ЧАС, а рост Saccharomyces cerevisiae (№ 7) подавляется только триоктилгепт-2-инил-аммонийиодидом (3).
Диаметр зоны подавления роста микроорганизмов химиотерапевтическим препаратом (4-DPyO, предельные, моно- и диацетиленовые ЧАС)
|
Четвертичные аммониевые соли и DPyO (формула и номер согласно схеме) |
Тест-культура* Диаметр зоны подавления роста микроорганизмов, мм |
||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
|
[(C8H17)3NCH2C≡CH]Br (1) |
0 |
0 |
0 |
0 |
20 |
25 |
0 |
|
[(C10H21)3NCH2C≡CC6H13]Br (2) |
15 |
15 |
0 |
0 |
0 |
0 |
0 |
|
[(C8H17)3NCH2C≡CC4H9]I (3) |
0 |
0 |
0 |
15 |
10 |
12 |
10 |
|
[(C8H17)2N(CH2C≡CC4H9)2]Br (4) |
20 |
20 |
0 |
20 |
30 |
17 |
0 |
|
[(C8H17)3NCH3]I (5) |
30 |
20 |
0 |
20 |
30 |
17 |
0 |
|
транс- (CH3)2NC6H4CH=CHC5H4N→O (6) |
0 |
0 |
0 |
0 |
0 |
0 |
0 |
* Staphylococcus aureus – № 1, Escherichia coli – № 2, Proteus vulgaris – № 3, Proteus mirabilis – № 4, Penicilliu m spp. – № 5, Bacillus cereus – № 6, Saccharomyces cerevisiae – № 7.
По отношению к культурам 1–5 (триоктилп-ропаргиламмоний бромид (1) на Bacillus cereus (№ 6) оказывает более сильное химиотерапевтическое воздействие) триоктилметиламмонийио-дид с алкильными группами (5) и диацетиленовый диоктилдил-2-гептиниламмонийбромид (4) проявляют одинаковое (за исключением культуры № 1), более сильное подавление роста культур, чем моноацетиленовые ЧАС (1–3). В то же время избирательность биологического действия последних соединений (1 – № 5, 6; 2 – № 1, 2; 3 – № 4–7) теоретически может позволить избирательно уничтожать некоторые виды микроорганизмов, не влияя на жизнеспособность других.
Особенно важным может оказаться тот факт, что ЧАС (3) подавляют рост культуры № 7, на которую не воздействуют другие исследованные в данной статье химиотерапевтические препараты. Это соединение можно было бы использовать как добавку к применяемым в настоящее время мягким дезинфицирующим средствам.
Кроме того, ввиду сравнительно быстрого формирования и распространения резистентных к ЧАС видов микроорганизмов применение ацетиленовых ЧАС, с которыми они пока не сталкивались, может привести к разработке новых эффективных бактерицидных и фунгицидных средств.
Целью нашей дальнейшей работы является синтез и исследование противомикробной активности более доступных ацетиленовых ЧАС меньшей молекулярной массы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Ацетиленовые четвертичные аммониевые соли
Синтез 1-бром-2-пропина (бромистого пропаргила)
В трехгорлую колбу, снабженную мешалкой, капельной воронкой, обратным холодильником и охлажденную до -5 °С льдом с солью, вноси- ли 36,5 г (0,65 моль) перегнанного пропаргилового спирта и 6 мл пиридина. К этой смеси при перемешивании по каплям прибавляли 61,6 г (0,23 моля) PBr3 в 2 мл пиридина. Температуру реакционной смеси постепенно в течение одного часа доводили до комнатной и смесь кипятили один час на водяной бане. Затем обратный холодильник заменяли на нисходящий и отгоня-
ли бромистый пропаргил в приемник на сухой поташ. Через некоторый промежуток времени
бромистый пропаргил перегоняли еще раз. Вы- ход – 43,3 г (56 %). Т 1,4920 [1].
84 ° С / 760 мм рт. ст., n D20
кип
Синтез метилпропаргилового эфира
В трехгорлую колбу на 1 л, снабженную мешалкой, обратным холодильником и капельной воронкой, охлажденную смесью льда с солью, вносили 84 г (1,5 моля) пропаргилового спирта, 201 г (1,65 моля) диметилсульфата, 60 мл воды и прибавляли по каплям раствор едкого натра (82 г NaOH в 82 мл воды) с такой скоростью, чтобы температура реакционной смеси не превышала -15 ° С. Затем продолжали перемешивание в течение 2 часов. Органический слой отделяли от водного и сушили безводным CaCl2. После перегонки получали 84 г (80 %) метилпропаргилового эфира. Т 61-62 ° С / 760 мм рт. ст., n D20 1,3965. Литературные данные: Т 61-62 ° С / 760 мм рт. ст., nD 20 1,3975 [31]. кип
Синтез 1-метокси-2-гептина [19]
В трехгорлую колбу на 1 л, снабженную мешалкой, обратным холодильником и капельной воронкой, охлажденную до -50 ° С твердой углекислотой в эфире, наливали около 500 мл жидкого аммиака и при перемешивании вносили 500 мг Fe(NO)3∙9H2O (катализатор) и 1 г металлического натрия. После перехода окраски из синей в серую в колбу вносили 23 г (1 гатом) мелконарезанного натрия и продолжали перемешивание в течение 2 часов. Образование густой темно-серой взвеси указывает на конец превращения. Охладив колбу до -60 ° С, по каплям прибавляли 70 г (1 моль) метилпропаргилового эфира, растворенного в 100 мл абсолютного эфира, и продолжали перемешивание еще в течение 1,5–2 часов. Далее охлаждали колбу до -70-75 ° С и добавляли раствор 137 г (1 моль) бромистого бутила в 110 мл абсолютного эфира. Реакционную смесь оставляли на ночь для испарения аммиака и на следующий день в колбу последовательно добавляли 200 мл сухого эфира, 5 г NH4Cl и 100 мл воды. Эфирный слой отделяли от водного, водный слой несколько раз экстрагировали эфиром, эфирные вытяжки обь-единяли и пропускали через них CO2 из аппарата Кипа до нейтральной реакции. Эфирный раствор сушили безводным MgSO4. После удаления растворителя остаток перегоняли в вакууме. Из одного синтеза получали в среднем 81 г (65 %) 1-метокси-2-гептина. Т 50-51 ° С /10 мм рт. ст., n D20 1,4320. Литературные данные: Ткип 53-54 ° С /
11 мм рт. ст., n D20 1,4300 [26], Т кип 56-57 ° С /12 мм рт. ст., nD 20 1,4320 [19].
Синтез 1-бром-2-гептина
В трехгорлую колбу на 100 мл, снабженную мешалкой, обратным холодильником и капельной воронкой, помещали 16 г (0,13 моля) бромистого ацетила и 0,25 г безводного ZnCl2 (катализатор), по каплям при интенсивном перемешивании прибавляли 16,5 г (0,13 моля) 1-ме-токси-2-гептина. Реакционную смесь нагревали на водяной бане при температуре 50 ° С. После прибавления эфира температуру бани поднимали до 70 ° С и продолжали перемешивание в течение 1,5 часа. Далее реакционную смесь выливали в ледяную воду, органический слой отделяли, водный слой экстрагировали несколько раз эфиром. Эфирный раствор сушили безводным MgSO4 и после отгонки растворителя остаток перегоняли в вакууме. Из одного синтеза получали 18 г (79 %) 1-бром-2-гептина.
Ткип 69 ° С / 10 мм рт. ст., nD 25 1,4895. Литературные данные: Ткип 71-73 ° С / 12 мм рт. ст., n D25 1,4890 [26], Ткип 88,7 ° С / 27 мм рт. ст., n D20 1,4898 [24].
Синтез бромистого ди-н-октил-ди-(2-гептинил) аммония
Реакционную смесь, содержащую 0,034 моля 1-ди-н-октиламино-2-гептина, 0,03 моля 1-бром-2-гептина и 10 мл ацетонитрила, перемешивали при комнатной температуре в течение 3–4 часов. Ацетонитрил отмывали водой. Выделившееся масло промывали пентаном, растворяли в эфире и сушили безводным MgSO4. Эфир удаляли в вакууме. Выход продукта – 50 %.
Остальные ЧАС получали аналогично. В ацетофеноне реакционную смесь оставляли на ночь, в пентане реакцию проводили в течение 3–4 дней (в последнем случае нерастворимые ЧАС промывали пентаном и растворитель удаляли в вакууме).
Определение чувствительности микроорганизмов к химиотерапевтическим препаратам проводили диско-диффузионным методом [18], [20].
Для исследования использовали стандартные питательные среды: АГВ – для определения чувствительности бактерий к химиотерапевтическим препаратам, Мюллер–Хинтон с добавлением метиленового синего и глюкозы – для определения чувствительности грибов к химиотерапевтическим препаратам.
На поверхность подсушенной питательной среды в чашке Петри наносили 1 мл исследуемой культуры (18–20-часовой бульонной культуры или стомиллионной агаровой суспензии из агаровой культуры). Диски, пропитанные насыщенными растворами исследуемых ЧАС и N-оксида в ДМСО, накладывали пинцетом на равном расстоянии друг от друга и на 2 см от края чашки. Чашки с посевами бактерий инкубировали при 35-37 °С в течение 18-20 часов. Чашки с посевами грибов инкубировали при 22-25 °С в течение 7–10 суток.
Для учета результатов с помощью линейки измеряли диаметр зон подавления роста вокруг дисков с точностью до 1 мм.
Тест-культуры: Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 25922, Proteus vulgaris , Proteus mirabilis , Penicillium spp. , Bacillus cereus , Saccharomyces cerevisiae .
Список литературы Бактерицидные и фунгицидные свойства ацетиленовых четвертичных аммониевых солей
- Андреев В. П. Молекулярные комплексы гетероароматических N-оксидов и ацетиленовых аминов с v-акцепторами как модель исследования нуклеофильности и основности соединений с пространственно доступными реакционными центрами: Дисс.... д-ра хим. наук. Петрозаводск, 2007. 427 с.
- Андреев В. П., Батоцыренова Е. Г., Рыжаков А. В., Родина Л. Л. Процессы внутримолекулярного переноса заряда в ряду стирильных производных N-оксидов пиридина и хинолина//ХГС. 1998. № 8. C. 1093-1102.
- Андреев В. П., Вукс Е. М., Кочеткова Е. В., Ремизова Л. А., Фаворская И. А. Кватернизация ацетиленовых аминов 2-пропинил-и алкилгалогенидами//ЖОрХ. 1979. Т. 5. Вып. 3. С. 464-467.
- Волкова С. В., Клементенок Е. В., Ефремова М. И. Оптимизация состава современного дезинфицирующего средства на примере препарата «Лизафин» [Электронный ресурс]. Режим доступа: http://www.petrospirt.ru/articles/1/index.html
- Волкова Т. О., Немова Н. Н. Молекулярные механизмы апоптоза лейкозной клетки. М.: Наука, 2006. 205 с.
- Гудзь О. В. Влияние этония на процесс дегидрирования метаболитов цикла трикарбоновых кислот культурами клетки Escherichia coli и Pseudomonas aeruginosa//Микробиологический журнал. 1985. Т. 47. № 2. С. 60-63 [Электронный ресурс]. Режим доступа: http://www.provisor.com.ua/archive/1998/N12/klin_dez.htm
- Гудзь О. В. Итоги и перспективы клинического применения дезинфекционных средств из группы четвертичных аммониевых соединений. Совет по регламентации применения и внедрения дезинфекционных средств Минздрава Украины (г. Киев)//Провизор. 1998. Вып. 12.
- Гудзь О. В., Писько Г. Т. Молекулярные аспекты действия поверхностно-активных веществ на микроорганизмы//Фармакология и токсикология: Республ. междувед. сборник. Киев: Здоров’я, 1983. С. 106-111.
- Гудзь О. В., Писько Г. Т. Влияние четвертичных аммониевых соединений на функциональное состояние цитоплазматической мембраны Escherichia coli//Микробиологический журнал. 1988. Т. 50. № 3. С. 75-78.
- Иванов А. Ю., Фомченков В. М. Зависимость повреждающего действия поверхностно-активных веществ на клетки Escherichia coli от фазы роста культуры//Микробиология. 1989. Т. 58. Вып. 6. С. 969-975.
- Инструкция по применению средства дезинфицирующего «ДЕЗЭФЕКТ-САНИТ» на предприятиях мясной промышленности [Электронный ресурс]. Режим доступа: http://www.dezefekt.ru/san_meat_instruction.doc
- Йоффе Б. С., Бабаян Е. П., Злотник Р. Е. Синтез и применение катионных ПАВ//Хлорная промышленность. М.: НИИТЕХИМ, 1988. 42 с.
- Колямшин О. А., Кормачев В. В., Митрасов Ю. Р., Братилов Б. И. N-окиси пиридина. Чебоксары: Чувашский ГУ, 1987. 95 с.
- Крученок Т. Б. Научные основы направленного поиска новых дезинфицирующих средств и изучение механизма их действия//Проблемы дезинфекции и стерилизации. М., 1985. С. 6-13.
- Лиманов М. О., Иванов С. Б., Крученок Т. Б. Синтез и бактерицидная активность катионных поверхностноактивных веществ, содержащих асимметричный атом азота//Хим.-фарм. журн. 1984. № 6. С. 703-706.
- Лиманов В. Е., Эпштейн А. Е., Скворцова Е. К., Арефьева Л. И. 5-я всесоюзная конференция по химии ацетилена. Тбилиси, 1975.
- Ляпунов Н. А., Бобылева Л. Г., Иванов Л. В., Грецкий В. М., Чуева И. Н., Рудько А. П. Исследование катионных поверхностно-активных веществ -солей алкиламидопропилдиметилбензиламмония//Фармация. 1984. Т. ХХХШ. № 3. С. 26-30.
- Медицинская микробиология/Под. ред. А. М. Королюка, В. Б. Сбойчакова. СПб., 1999. 272 с.
- Мкрян Г. М., Гаспарян С. М., Волнина Э. А., Капланян Э. Е. Исследование в области соединений ацетиленового ряда. V. Присоединение алкилхлорметиловых эфиров к однозамещенным ацетиленовым углеводородам. Синтез алкин-2-илалкиловых эфиров//Арм. хим. журнал. 1970. Т. 23. № 5. С. 419-424.
- МУК 4.12.1890-04. Определение чувствительности микроорганизмов к антибактериальным препаратам. М.: Минздрав России, 2004.
- Писько Г. Т., Гудзь О. В. Зависимость между строением катиона и биологической активностью катионных поверхностно-активных веществ//Фармакология и токсикология. 1980. № 5. С. 210-215.
- Писько Г. Т., Овчинников В. Г., Гудзь О. В., Смирнова Н. А., Тарасенко В. С. Противомикробные свойства производных гексаметилендиамина, содержащих остатки высокомолекулярных спиртов//Физиологически активные вещества. 1984. Вып. 16. С. 54-57.
- Чернявская М. А., Павлова И. Б. Структурно-функциональные изменения клеток сферопластов эшерихий при воздействии катионного поверхностно-активного вещества//Журнал микробиологии, эпидемиологии и иммунобиологии. 1983. № 2. С. 62-66.
- Bartlett P. D., Rosen L. J. An acetylenic analog of neopentyl bromide; evidence that the hindrance to displacement reactions in neopentyl halides is steric in nature//J. Am. Chem. Soc. 1962. Vol. 64. № 3. P. 542-546.
- Best M., Sattar S. A., Springthorpe V. S., Kennedy M. E. Efficacies of selected disinfectants against Mycobacterium tuberculosis//J. Clin. Microbiol. 1990. № 10. Р. 2234-2239.
- Couffignal R., Gaudemar M., Perriot P. Sur la preparation des bromures propargyliques du type R-C=C-CH2-Br (note de laboratoire)//Bull. Soc. Chim. Fr. 1967. № 10. P. 3909-3910.
- Desinfektionsmittel-Liste der DGHM. Wiesbaden, 1997.
- Kabara J. J., Mckillip W. J., Sedor E. A. Ammimides. 1. Antimicrobial tffect of some long chain fatty acid derivatives//J. Amer. Oilchem. Soc. 1975. № 8. Р 316-317.
- Frank M. J., Schaffner W. Contaminated Aqueous Benzalkonium Chloride an Unnecessary Hospital Infection Hazard//J. Amer. Med. ABS. 1976. Vol. 236. № 21. Р 2418-2419.
- Girardo P., Reverdy M. E., Martra A., Fleurette J. Determsnation de la concentration minimale bactericide de trois antiseptiques et un desinfectant sur S 80 soudes de bacilles gram negatife d,origine hospitaliere//Pathol. Biol. 1989. № 5 bis. P. 605-611.
- Perriot P., Gaudemar M. Sur la preparation des estersd’alcools a-acetyleniques y-halogenes//Bull. Soc. Chim. Fr. 1968. F. 8. P. 3239-3244.
- Russell A. D. Bactarial spores and chemical sporicidal agents//Clin. Mcrobiol. Rev. 1990. № 2. Р. 99-119.


