Бактерии-деструкторы полихлорированных бифенилов из почв с различным уровнем загрязнения
Автор: Егорова Д.О., Шестакова Е.А., Первова М.Г., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2014 года.
Бесплатный доступ
Наличие в почвах специфического загрязнения, в частности присутствие галогенароматиче-ских соединений, привело к формированию в микробном сообществе бактерий, способных разрушать вещества группы «стойкие органические загрязнители» (СОЗ): штаммы Rhodococ-cus sp. Ch628, Microbacterium oxydans B51 и Rhodococcus erytropolis B7a эффективно разлагали как индивидуальные ПХБ, так и их промышленные смеси. В то же время, в почвах, отобранных в экологически чистом районе (Республика Бурятия), не были выявлены активные штаммы-деструкторы токсичных соединений.
Полихлорированные бифенилы, соз, почва, загрязнение, штаммы-деструкторы
Короткий адрес: https://sciup.org/147204697
IDR: 147204697 | УДК: 579.87
Bacteria destructors of polychlorinated biphenyls from the soil with various level of pollution
The presence of a specific soil pollution, in particular the presence of halogenated aromatic compounds, led to the formation in the microbial communities of bacteria that can effectively decompose the substance of the "persistent organic pollutants" (POPs): strains of Rhodococcus sp. Ch628, Microbacterium oxydans B51 and Rhodococcus erytropolis B7a effectively degraded as individual PCBs, as well as their industrial mixtures. At the same time, in the soils sampled in an ecologically clean area (Republic of Buryatia), have not been identified active strains-destructors toxic compounds.
Текст научной статьи Бактерии-деструкторы полихлорированных бифенилов из почв с различным уровнем загрязнения
Процессы естественной селекции бактерий с теми или иными свойствами протекают в почвах непрерывно. При этом направление отбора зависит от спектра и количества химических соединений, присутствующих в почве.
В настоящее время остро стоит проблема поиска бактериальных штаммов, обладающих высокой деструктивной активностью по отношению к стойким органическим загрязнителям (СОЗ). В группу СОЗ включены хлорароматические соединения, в частности полихлорированные бифенилы (ПХБ), линдан, гексахлорбензол, особо устойчивые к воздействию физических, химических и биологических факторов .
Анализ научных публикаций и собственные исследования показали, что бактериальная деструкция – это один из оптимальных способов утилизации данных соединений как с экологических, так и с экономических позиций [Unterman, 1996; Зана-вескин, Аверьянов, 1998; Pieper, 2005; Васильева, Стрижакова, 2007; Хоменков и др., 2008; Егорова и др., 2010; Егорова, Демаков, Плотникова, 2011; Егорова, Плотникова, 2011]. Однако для очистки обширных территорий от ПХБ и других СОЗ, перспективно применение штаммов, деструктивные свойства которых являются результатом естественного отбора в природных эконишах.
Цель работы – выделение и исследование штаммов-деструкторов хлорароматических веществ из районов с разной техногенной нагрузкой.
Материалы и методы исследования
Образцы почв. Почвы отбирали в районах, находящихся на значительном расстоянии друг от друга и отличающихся уровнем экологического благополучия:
-
1. Образцы под шифром SSE были получены с территории, прилегающей к оз. Сульфатное Селен-гинского р-на республики Бурятия. 51°22'N106°35'E
-
2. Образцы под шифром SBE – с территории, прилегающей к оз. Белое Иволгинского р-на республики Бурятия. 51°32'N107°1'E
-
3. Образцы BP – с территории г. Березники, прилегающей к промышленным предприятиям, Пермский край. 59°28'N56°46'E
-
4. Образцы СH – с территории предприятия ОАО СВЗХ, г. Чапаевск, Самарской обл.
52°59'N49°41'E
Формат координат: Ddd градусов mm минут ss.s секунд.
Все образцы отобраны по методу «конверта» с соблюдением правил асептики в радиусе 100 м от указанной точки. Для дальнейшего анализа брали усредненную пробу.
Анализ почв на загрязнение. Обработку проб почвы проводили по «Методике выполнения измерений массовой концентрации полихлорбифенилов в воздухе рабочей зоны, промвыбросах, природных и сточных водах и почвах методом газожидкостной хроматографии» № 88-16358-25-2000. Условия хроматографирования.
ГХ-ПИД условия : газовый хроматограф «Shimadzu GC 2010», с пламенно-ионизационным детектором, кварцевой капиллярной колонкой ZB-5 длиной 30 м, диаметром 0.25 мм, толщина пленки 0.25 мкм. Начальная температура колонки 40°С (выдержка 3 мин.), далее нагрев со скоростью 10°С/мин. до 280°С (выдержка 30 мин.). Температура испарителя 250°С, детектора 300°С. Газ-носитель – азот, деление потока 1:30, расход через колонку 1.0 мл/мин. Вводили 1.0 мкл.
ГХ-ЭЗД условия : газовый хроматограф «Shi-madzu GC 2010Plus», с электроно-захватным детектором, кварцевой капиллярной колонкой GsBP-5MS длиной 30 м, диаметром 0.25 мм, толщина пленки 0.25 мкм. Начальная температура колонки 40°С (выдержка 3 мин.), далее нагрев со скоростью 10°С/мин., до 280°С (выдержка 30 мин.). Температура испарителя 250°С, детектора 300°С. Газ-носитель – азот, деление потока 1:30, расход через колонку 1.0 мл/мин. Вводили 1.0 мкл.
ГХ-МСД условия: газовый хроматограф-масс-спектрометр «Agilent GC 7890A MS 5975C Inert XL EI/CI» с квадрупольным масс-спектрометрическим детектором, кварцевой капиллярной колонкой HP-5MS длиной 30 м, диаметром 0.25 мм, толщина пленки 0.25 мкм.; электронная ионизация (70 эВ); сканирование по полному ионному току в интервале m/z 20–1000 Da; газ-носитель – гелий, деление потока 1:50, расход через колонку 1.0 мл/мин.; температура колонки – начальная 40°С (выдержка 3 мин.), программирование со скоростью 10°С/мин. до 290°С (выдержка 30 мин.), температура испарителя – 250°С, температура источника – 230°С, квадруполя – 150°С, переходной камеры – 280°С. Вводили 1.0 мкл.
Идентификацию компонентов проводили на основании базы масс-спектров NIST05 и калибровочных хроматограмм ГСО 7821-2000 «Совол».
Штаммы-деструкторы. В работе использованы штаммы, осуществляющие разложение одного или нескольких хлорароматических соединений: Microbacterium oxydans B51 [Рыбкина и др., 2003],
Rhodococcus erytropolis B7a [Егорова и др., 2010], Rhodococcus sp. Ch628 и Pseudomonas sp. SBE14a (настоящее исследование).
Выделение штаммов-деструкторов проводили двумя методами: методом накопительного культивирования, как описано [Рыбкина и др., 2003], и прямого высева на минеральную среду с бифенилом, в качестве источника углерода и энергии. Для выделения и роста бактерий-деструкторов из образцов BP и CH использовали минеральную среду К1 [Зайцев, Карасевич, 1981], для образцов SSE и SSВ – минеральную среду АММ [Заварзина и др., 2006].
Для получения агаризованной среды добавляли агар до конечной концентрации 1.5%. При выращивании бактерий на агаризованных средах бифенил добавляли на крышку чашки Петри.
Определение таксономического положения изолированных штаммов. Морфологические признаки микроорганизмов изучали по общепринятым методикам [Методы…, 1983; Методы…, 1991]. Амплификацию генов 16S рРНК проводили с использованием бактериальных праймеров 27F и 1492R [Tiirola et al., 2002]. Секвенирование продуктов амплификации осуществляли с помощью набора реактивов DYEnamic ET Dye Terminator Cycle sequencing Kit на автоматическом секвенаторе Genetic analyser 3500XL (Applied Biosystems, США) согласно рекомендациям производителя. Полученные нуклеотидные последовательности анализировали с использованием программ CLUSTAL W [Thompson, Higgins, Gibson, 1994], TREECON [van de Peer, DeWachter, 1994], BLAST . Поиск гомологичных последовательностей производили по базам данных GenBank и EzTaxon .
Ростовые характеристики штаммов изучались в жидкой минеральной среде К1 [Zaitsev et al., 1991] или АММ [Заварзина и др., 2006]. Штаммы выращивали в колбах Эрленмейера объемом 250 мл в 100 мл минеральной среды при температуре 28оС и аэрации на шейкере со скоростью 220 об/мин. В качестве субстрата использовали бифенил в концентрации 1 г/л. Рост контролировали по изменению оптической плотности среды, измерение проводили на спектрофотометре Shimadzu BioSpec-mini («Shimadzu», Япония) при длине волны 600 нм.
Деструкцию соединений группы СОЗ проводили, как описано [Егорова и др., 2010].
Продукты деградации хлорбифенилов (ХБ) определяли спектрофотометрически (спектрофотометр Shimadzu BioSpec-mini) и методом высокоэффективной жидкостной хроматографии (ВЭЖХ) (хроматограф Shimadzu LC-20A, детектор Shima- dzu RF-20A, колонка Discovery C18 (150 x 4.6 мм) («Supelco», «Sigma-Aldrich», США)), как описано [Егорова и др., 2011]. Эксперименты с «отмытыми клетками» проводили аналогично экспериментам Д.О. Рыбкиной и др. [Рыбкина и др., 2003].
Статистическая обработка результатов. Все эксперименты проводили в трехкратной повторности. Полученные данные обрабатывали с использованием стандартных пакетов компьютерных программ Microsoft Excel.
Результаты и их обсуждение
Анализ почв, отобранных на территории г. Березники делены и описаны активные штаммы-деструкторы полихлорированных бифенилов и хлорбензойных кислот – Microbacterium oxydans B51 [Рыбкина и др., 2003] и Rhodococcus erytropolis B7a [Егорова и др., 2010]. Способность данных штаммов к разложению веществ группы СОЗ, в частности полихлорированных бифенилов, позволила предположить, что естественная селекция данных штаммов протекала в условиях специфического химического загрязнения.
Анализ образцов почв в условиях газовой хроматографии с применением различных детекторов показал наличие широкого спектра галогенированных ароматических и циклических соединений, а также алифатических углеводородов (рис. 1, табл. 1).
В результате ранее проведенных исследований
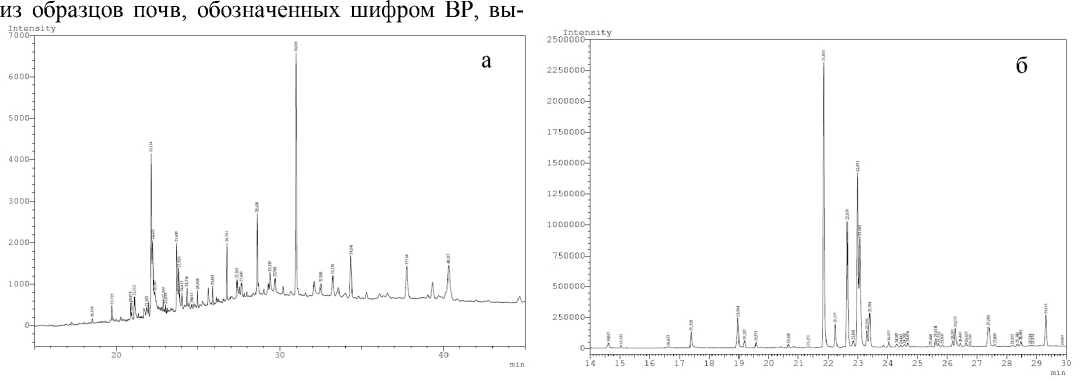
Рис. 1 . Хроматограммы усредненного образца почвы ВР с применением различных детекторов:
а – условия ГХ-ПИД, б – условия ГХ-ЭЗД
Таблица 1
Основные загрязнители, выявленные в усредненном образце почвы ВР 4
|
Время удерживания, мин |
Название |
Брутто-формула |
Молек. масса |
Структура |
|
|
ПИД |
ЭЗД |
||||
|
18.524 |
18.964 |
Pentadecane Benzene, tribromo- |
C15H32 C6H3Br3 |
212 312 |
Br Br Br |
|
19.725 |
Hexadecane |
C16H34 |
226 |
Линейный углеводород |
|
|
20.874 |
21.853 |
Thiophene, tetrabromo- |
C4Br4S |
396 |
Br S Br Br Br |
|
20.941 |
Heptadecane, |
C17H36 |
230 |
Линейный углеводород |
|
|
21.112 |
22.237 |
Dibromobenzo(b)thiophene |
C8H4Br2S |
290 |
S Br |
|
21.853 |
22.639 |
Benzene, tetrabromo- |
C6H2Br4 |
390 |
Br Br Br Br |
|
22.134 |
22.991 |
Naphthalene, dibromo- |
C10H6Br2 |
284 |
Br Br |
Окончание табл. 1
|
Время удерживания, мин |
Название |
Брутто-формула |
Молек. масса |
Структура |
|
|
ПИД |
ЭЗД |
||||
|
22.221 |
23.061 |
Naphthalene, dibromo- |
C10H6Br2 |
284 |
Br Br |
|
23.299 |
Naphthalene, dibromo- |
C10H6Br2 |
284 |
Br Br |
|
|
22.869 |
23.394 |
Benzene, tetrabromo- |
C6H2Br4 |
390 |
Br Br Br Br |
|
23.014 |
Nonadecane |
C19H40 |
268 |
Линейный углеводород |
|
|
23.689 |
24.307 |
Dibutyl phthalate |
C16H22O4 |
278 |
O OO O |
|
24.013 |
Eicosane |
C20H42 |
282 |
Линейный углеводород |
|
|
24.316 |
18-Norabietane |
C19H34 |
262 |
||
|
25.614 |
1,1'-Biphenyl, dibromo- |
C12H8Br2 |
310 |
Br ^оуУ(5у- Br |
|
|
24.968 |
Heneicosane |
C21H44 |
296 |
Линейный углеводород |
|
|
25.883 |
Docosane |
C22H46 |
310 |
Линейный углеводород |
|
|
27.380 |
DDE - Benzene, 1,1'-(dichloroethenylidene)bis[4-chloro- 2,4,6-Tribromobiphenyl |
C14H8Cl4 C12H7Br3 |
316 388 |
Cl Cl ууу Cl Cl Br Br Br Br |
|
|
26.761 |
Tricosane |
C23H48 |
324 |
Линейный углеводород |
|
|
27.385 |
29.315 |
p,p'-DDT |
C14H9Cl5 |
352 |
Cl Cl IC^JOJ Cl Cl Cl |
|
27.643 |
Tetracosane |
C24H50 |
338 |
Линейный углеводород |
|
|
28.610 |
Pentacosane |
C25H52 |
352 |
Линейный углеводород |
|
|
29.387 |
Di-n-octyl phthalate |
C24H38O4 |
390 |
O OO O |
|
|
29.708 |
Hexacosane |
C26H54 |
366 |
Линейный углеводород |
|
|
30.985 |
Heptacosane |
C27H56 |
380 |
Линейный углеводород |
|
|
32.500 |
Octacosane |
C28H58 |
394 |
Линейный углеводород |
|
Штаммы Microbacterium oxydans B51 и Rhodococcus erytropolis B7a осуществляли разложение моноароматических соединений, таких как бензол, толуол и ряд других, отличающихся типом и количеством заместителей в кольце [Рыбкина и др., 2003, Егорова и др., 2010]. Как видно из полученных данных, в почве присутствуют производ- ные бензола и фталевой кислоты (табл. 1). Таким образом, наличие данных соединений способствовало естественной селекции штаммов, обладающих ферментными системами окисления ароматических веществ.
Среди выявленных в ВР-образцах загрязнителей высока доля соединений, состоящих из двух ароматических колец. Известно, что разложение таких веществ происходит в результате ферментативного окисления кольца молекулы [Pieper, 2005, Solyanikova et al., 2008]. При этом в случае присутствия нескольких соединений, близких по структуре, в клетках бактерий могут активироваться уникальные сочетания ферментативных путей. Следует отметить, что штаммы Microbacterium oxydans B51 и Rhodococcus erytropolis B7a характеризуются высокой деструктивной активностью по отношению к полихлорированным бифенилам и их химически модифицированным производным, а также обладают уникальным сочетанием ферментов, обусловливающих окисление сложных ароматических соединений [Рыбкина и др., 2003, Егорова и др., 2010; Егорова, Демаков, Плотникова, 2011; Егорова, Плотникова, 2011].
Для дальнейших исследований были отобраны образцы почв на двух территориях, отличающихся по уровню экологического благополучия.
Анализ образцов почв с территории республики Бурятия
Районы оз. Сульфатное и Белое республики Бурятия являются экологически благополучными.
Газохроматографический анализ с применением трех возможных детекторов не выявил загрязнения в почвах Селенгинского р-на (образцы SSE). В образцах SBE из Иволгинского р-на обнаружены в следовых количествах гексахлорбензол и линдан, входящие в группу СОЗ и являющиеся инсектицидами (табл. 2).
Таблица 2
Основные загрязнители, выявленные в почвах образцов SBE
|
Время удерживания, мин. |
Название |
Брутто-формула |
Молек. масса |
Структура |
|
|
ПИД |
ЭЗД |
||||
|
21.499 |
22.278 |
Benzene, hexachloro- |
C6Cl6 |
282 |
Cl Cl Cl Cl Cl |
|
22.680 |
22.786 |
Lindane |
C6H6Cl6 |
288 |
Cl Cl Cl Cl Cl Cl |
Выделение штаммов-деструкторов из образцов почв с территории республики Бурятия
Из образцов почв SSE ни одним из использованных способов не удалось получить штаммы, способные расти на минеральной среде с бифенилом в качестве единственного источника углерода и энергии.
Методом накопительного культивирования в минеральной среде с бифенилом с последующим рассевом до единичных колоний из образцов SВE получено 1.5 х 10 6 КОЕ/г почвы. Все колонии были разделены на 2 морфотипа:
-
а) колонии округлые диаметром 3 мм, поверхность гладкая, блестящая, профиль выпуклый, прозрачные, бесцветные, край ровный, структура однородная;
-
б) колонии округлые диаметром 2–3 мм, поверхность гладкая, блестящая, профиль выпуклый, прозрачные, цвет бледно-желтый, ровный край, однородная структура.
Представители морфогрупп были идентифицированы на основе анализа нуклеотидных последовательностей гена 16S рРНК. Показано, что среди обнаруженных бактерий присутствуют представи- тели родов Achromobacter, Pseudomonas и Halomonas.
Для дальнейших исследований был отобран штамм SBE14а. У данного штамма определена нуклеотидная последовательность гена 16S рРНК длиной 1412 п.н. и проведено сравнение с гомологичными последовательностями, имеющимися в международных базах данных GenBank/EMBL/DDBJ и на сервере EzTaxon . Выявлена филогенетическая близость исследуемого штамма с типовым штаммом Pseudomonas stutzeri CCUG11256T (GenBank U26262). На настоящем этапе исследования штамм идентифицирован как Pseudomonas sp.
Исследование ростовых характеристик показало, что штамм Pseudomonas sp. SBE14а активно растет в жидкой минеральной среде (максимальная оптическая плотность составляла ОП 600 =0.78 оп.ед.) и использует незамещенный бифенил как источник углерода и энергии. Однако штамм не проявлял деградативной активности к хлорированным бифенилам.
Таким образом, из почв с низким уровнем загрязнения хлорароматическими соединениями не удалось выделить активных штаммов-деструкторов.
Анализ образцов почв с территории г. Чапаевск
Город Чапаевск с 1999 г. признан зоной экологического бедствия . На его территории находятся предприятия, на которых длительное время производили вещества хлорароматического ряда.
В ходе данной работы проведен анализ почвы, отобранной на территории предприятия, производившего широкий спектр химических соединений (рис. 2, табл. 3).
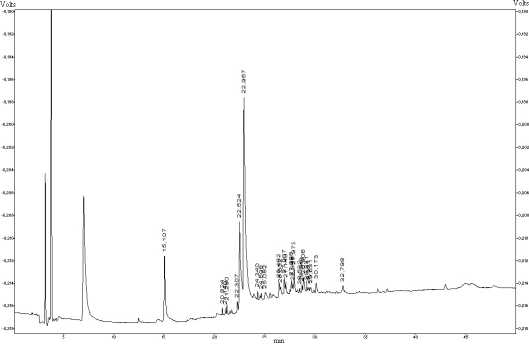
Рис. 2 . Хроматограмма усредненной пробы почв образцов СН
Таблица 3
Основные загрязнители, выявленные в усредненной пробе образцов СН
|
Время удерживания, мин. |
Название |
Брутто-формула |
Молек. масса |
Структура |
|
|
ПИД |
ЭЗД |
||||
|
21.499 |
22.278 |
Benzene, hexachloro- |
C6Cl6 |
282 |
Cl Cl Cl Cl Cl |
|
22.680 |
22.786 |
Lindane |
C6H6Cl6 |
288 |
Cl Cl Cl Cl Cl Cl |
|
26.482 – 32.798 |
Polychlorobiphenyl (mix) |
C 12 H n Cl m |
Cl Cl Cl Cl Cl Cl Cl дод Cl Cl Cl |
||
При анализе в условиях ГХ-ПИД на хроматограммах образцов почвы регистрируется пики соединений, соответствующие смеси углеводородов С 17 -С 25 , дибутил- и диоктилфталатам. При регистрации в условиях ГХ-ЭЗД на хроматограммах регистрируются пики ПХБ, гексахлорбензола и линдана (γ-гексахлор-циклогексан).
Количественная оценка показала, что содержание данных веществ в почве превышает допустимые нормы (табл. 4).
Таблица 4
Содержание веществ группы СОЗ в образце почвы СН
|
Соединение |
ПДК, мг/кг |
В образце СН, мг/кг |
|
гексахлорбензол |
0.03 |
0.816 |
|
линдан |
0.1 |
5.468 |
|
смесь ПХБ |
0.06 |
0.408 |
Выделение штаммов-деструкторов из образцов почв г. Чапаевска
Методом прямого высева установлено, что в образцах почвы СН в значительном количестве присутствуют бактерии, способные расти на мине- ральной среде с бифенилом (8.6 х 106 КОЕ/г почвы).
Методом накопительного культивирования с последующим рассевом до единичных колоний из образцов СН получено 25.9 х 106 КОЕ/г почвы, способных использовать бифенил в качестве ростового субстрата. Выделено две доминирующие группы бактерий, отличающихся морфологией колоний. Анализ нуклеотидных последовательностей гена 16S рРНК показал принадлежность основных представителей данных морфогрупп к родам Pseudomonas и Rhodococcus.
Для дальнейшего исследования отобран штамм Сh628. Анализ нуклеотидной последовательности гена 16S рРНК длиной 1390 п.н. и сравнение с гомологичными последовательностями выявил филогенетическую близость исследуемого штамма с типовым штаммом Rhodococcus wratislaviensis NCIMB 13082T (GenBank Z37138).
При культивировании штамма Сh628 в жидкой минеральной среде с бифенилом установлено, что максимальная оптическая плотность культуры составляет ОП 600 =0.299 оп.ед. и достигается за 72 ч.
Установлено, что штамм Rhodococcus sp. Ch628 проявляет высокую активность к хлорированным бифенилам (табл. 5).
Штамм Ch628 осуществляет почти 100%-ное разложение моно- и дихлорированных бифенилов за 48 ч. Несколько ниже показатель при разложении трихлорированных бифенилов. Следует отметить, что исследуемый штамм разрушает не только отдельные хлорбифенилы, но и их промышленные смеси (табл. 5). Подобная деградативная активность описана для ограниченного круга бактериальных штаммов-деструкторов [Pieper, 2005; Ade-busoye et al., 2007; Егорова и др., 2010].
Таблица 5
Разложение хлорированных бифенилов и их промышленных смесей штаммом Rhodococcus sp. Ch628
|
ПХБ |
Время деструкции, сут |
Концентрация ПХБ, мг/л |
Промежуточные продукты |
||
|
ГОФДК, ОП 397 |
ХБК, мг/л |
(ОН)БК, мг/л |
|||
|
0 |
18.9±0.02 |
Н.О. |
Н.О. |
Н.О. |
|
|
2ХБ |
1 |
0.51±0.02 |
Н.О. |
0.41±0.02 |
2.79±0.02 |
|
2 |
0.05* ±0.01 |
Н.О. |
0.46±0.01 |
2.77±0.01 |
|
|
0 |
18.9±0.03 |
Н.О. |
Н.О. |
Н.О. |
|
|
4ХБ |
1 |
0.936±0.02 |
Н.О. |
0.09±0.02 |
0.08±0.01 |
|
2 |
0.59±0.01 |
Н.О. |
0.11±0.01 |
0.16±0.01 |
|
|
0 |
22.3±0.02 |
Н.О. |
Н.О. |
Н.О. |
|
|
2,4'-ХБ |
1 |
2.29±0.04 |
0.612±0.002 |
0.01±0.03 |
0.42±0.02 |
|
2 |
0.17±0.01 |
0.465±0.001 |
0.02±0.01 |
0.57±0.03 |
|
|
0 |
12.9±0.03 |
Н.О. |
Н.О. |
Н.О. |
|
|
2,4,4'-ХБ |
1 |
4.79±0.02 |
0.289±0.001 |
0.001±0.0002 |
0.11±0.01 |
|
2 |
2.88±0.01 |
Н.О. |
0.002±0.0001 |
0.08±0.01 |
|
|
0 |
12.9±0.02 |
Н.О. |
Н.О. |
Н.О. |
|
|
2,4,2'-ХБ |
1 |
5.77±0.04 |
Н.О. |
0.003±0.0003 |
0.12±0.01 |
|
2 |
5.16±0.01 |
Н.О. |
0.005±0.0001 |
0.11±0.01 |
|
|
0 |
0.13±0.03 |
Н.О. |
Н.О. |
Н.О. |
|
|
«Делор 103» |
5 |
0.034 ±0.02 |
0.869±0.001 |
0.09±0.02 |
0.03±0.01 |
|
8 |
0.003 ±0.01 |
1.167±0.002 |
0.12±0.01 |
0.06±0.01 |
|
|
0 |
0.55±0.02 |
Н.О. |
Н.О. |
Н.О. |
|
|
«Совол» |
5 |
0.016 ±0.04 |
Н.О. |
0.14±0.03 |
Н.О. |
|
8 |
0.005 ±0.01 |
0.270±0.001 |
0.31±0.01 |
Н.О. |
|
Примечание. Н.О. – не обнаружено, «*» - жирным шрифтом выделены концентрации ниже значения ПДК.
Показано, что штамм Rhodococcus sp. Ch628 способен разлагать и ряд других соединений группы СОЗ (табл. 6). Так как данные вещества особо устойчивые как к химическому, так и к биологическому разложению, то уровень деструкции, показанный данным штаммом, несомненно, является значимым.
Таблица 6
Разложение соединений группы СОЗ штаммом Rhodococcus sp. Ch628
|
Вещество |
Начальная концентрация, мкг/мл |
Концентрация через 4 сут., мкг/мл |
Деструкция, % |
|
Хлорбензол |
10±0.1 |
0 |
100 |
|
Линдан |
0.2±0.01 |
0.15±0.01 |
20.7 |
|
ГХБ |
2.5±0.02 |
1.95±0.01 |
21.8 |
|
ДДТ |
0.2±0.01 |
0.13±0.01 |
30.5 |
Таким образом, штамм Rhodococcus sp. Ch628 обладает уникальным сочетанием деградативных свойств в отношении ряда соединений группы СОЗ.
Заключение
Загрязнение галогенароматическими углеводородами различных территорий является важным фактором в процессах естественного отбора групп бактерий, способных к разложению одного или нескольких веществ группы СОЗ.
В результате проведенных исследований установлено, что наиболее активные штаммы-деструкторы полихлорированных бифенилов, обладающие уникальным сочетанием ферментативных путей, выделены из почв, длительное время загрязненных галогенароматическими углеводородами. Показано, что штамм Rhodococcus sp. Ch628, способный эффективно разлагать смеси ПХБ и ряд других СОЗ, выделен из почв с высоким уровнем загрязнения данными веществами, а штаммы Microbacterium oxydans B51 [Рыбкина и др., 2003] и Rhodococcus erytropolis B7a [Егорова и др., 2010] – из почвы, загрязненной различными галогенароматическими и алифатическимим углеводородами. Напротив, в почвах из экологически чистого района не удалось обнаружить бактериальные штаммы с искомыми свойствами.
Работа поддержана грантом РФФИ-Урал №14-04-96021р_урал_а.
Список литературы Бактерии-деструкторы полихлорированных бифенилов из почв с различным уровнем загрязнения
- Васильева Г.К., Стрижакова Е.П. Биоремедиация почв и седиментов, загрязненных полихлори-рованными бифенилами//Микробиология. 2007. Т.76, №6. С. 725-741.
- Егорова Д.О. и др. Разложение хлорированных бифенилов и продуктов их биоконверсии штаммом Rhodococcus sp. В7а//Прикладная биохимия и микробиология. 2010. Т. 46, № 6. С. 644 -650.
- Егорова Д.О., Демаков В.А., Плотникова Е.Г. Разложение смеси (три-гекса)хлорированных би-фенилов штаммами рода Rhodococcus//Прикладная биохимия и микробиология. 2011. Т. 47, № 6. С. 655-662.
- Егорова Д.О., Плотникова Е.Г. Разложение смеси хлорированных бифенилов с преобладанием тетразамещенных конгенеров штаммом Microbacterium sp. B51//Вестник Уральской медицинской академической науки. 2011. № 4.1. С. 172-173.
- Заварзина Д.Г. и др. GEOALKALIBACTER FER-RIHYDRITICUS GEN. NOV., SP. NOV., первый алкалофильный представитель семейства GEOBACTERACEAE, выделенный из содового озера//Микробиология. 2006. Т. 75, № 6. С. 775-785
- Зайцев Г.М., Карасевич Ю.Н. Подготовительный метаболизм 4-хлорбензойной кислоты у Arthrobacter globiformis//Микробиология. 1981. T.50. C. 423-428.
- Занавескин Л.Н., Аверьянов В.А. Полихлорбифенилы: проблемы загрязнения окружающей среды и технологические методы обезвреживания//Успехи химии. 1998. Т. 67, № 8. С. 788-800.
- Методы общей бактериологии/под ред. Ф. Гер-хардт и др. М.: Мир, 1983. Т. 1-3.
- Методы почвенной микробиологии и биохимии: учеб. пособие/под ред. Д.Г. Звягинцева. М.: Изд-во МГУ, 1991. 304 с.
- Рыбкина Д. О. и др. Новый аэробный грамположительный микроорганизм с уникальными свойствами деструкции орто-и пара-хлорированных бифенилов//Микробиология. 2003. Т. 72, № 6. С. 759-765.
- Хоменков В.Г. и др. Организация метаболических путей и молекулярно-генетические механизмы биодеградации ксенобиотиков у микроорганизмов//Прикладная биохимия и микробиология. 2008. Т. 44, № 2. С. 133-152.
- Adebusoye A.S. et al. Growth on dichlorobipnenyls with chlorine substitution on each ring by bacteria isolated from contaminated African soils//Appl. Microbial. Biotechnol. 2007. Vol. 74. P. 484-492.
- Pieper D.H. Aerobic degradation of polychlorinated biphenyls//Appl. Microbiol. Biotechnol. 2005. Vol. 67. P. 170-191.
- Solyanikova I.P. et al. Varyability of enzyme system of Nocardioform bacteria as a basis of their metabolic activity//J. Environmental Science and Health. Part B. 2008. Vol. 43. P. 241-252.
- Thompson J.D., Higgins D.G., Gibson T.J. CLUSTAL W: improving the sensitivity of progressive multiple sequence alignment son///Nucleic. Acids. Res. 1994. Vol. 22. P. 4673-4680.
- Tiirola M.A. et al. Isolation and characterization of Novosphingobium sp. Strain MT1, a dominant polychlorophenol-dagrading strain in a groundwa-ter bioremediation system//Appl. Environ. Mi-crobiol. 2002. Vol. 68. P. 173-180.
- Unterman R. A history of PCB biodegradation//Bio-remediation. Principles and Applications/Eds. Crawford R.L., Crawford D.L. Cambridge Univarsity Press: New York, 1996. P. 209-253.
- Van de Peer Y., DeWachter R. TREECON for Windows a software package for the construction and drawing of evolutionary trees for the Microsoft Windows environment//Comput. Appl. Biosci. 1994. Vol. 10. P. 569-570.
- Zaitsev G.M. et al. Genetic control of degradation of chlorinated benzoic acids in Arthrobacter globiformis, Corynebacterium sepedonicum and Pseu-domonas cepacia strains//FEMS Microbiol. Lett. 1991. Vol. 81. P. 171-176.


