Баллонная ангиопластика рестенозов коронарных стентов в качестве "моста" к экстренному коронарному шунтированию при остром коронарном синдроме без подъема сегмента ST высокого риска
Автор: Нишонов А.Б., Гусев С.М., Тарасов Р.С.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 2 т.37, 2022 года.
Бесплатный доступ
Данный клинический случай демонстрирует возможность применения баллонной ангиопластики у пациентов с острым коронарным синдромом без подъема сегмента ST (ОКСбпST) и рестенозом ранее имплантированных коронарных стентов в качестве меры, позволяющей временно стабилизировать коронарный кровоток и состояние пациента для предоперационной подготовки к последующему экстренному коронарному шунтированию (КШ).
Баллонная ангиопластика, рестеноз коронарных стентов, экстренное коронарное шунтирование, острый коронарный синдром без подъема сегмента st, многососудистое поражение
Короткий адрес: https://sciup.org/149140491
IDR: 149140491 | УДК: 616.132.2-007.272-036.11-089.197.4:616.132.2-089.86 | DOI: 10.29001/2073-8552-2022-37-2-118-123
Balloon angioplasty for restenosis of coronary stents as a “bridge” to emergency coronary bypass grafting in non-ST segment elevation acute coronary syndrome
This case demonstrates the possibility of using balloon angioplasty in patients with non-ST segment elevation acute coronary syndrome and restenosis of previously implanted coronary stents as a measure to temporary stabilize coronary blood flow and the patient’s condition for preoperative preparation for subsequent emergency coronary bypass grafting.
Текст научной статьи Баллонная ангиопластика рестенозов коронарных стентов в качестве "моста" к экстренному коронарному шунтированию при остром коронарном синдроме без подъема сегмента ST высокого риска
Острый коронарный синдром без подъема сегмента ST (ОКСбпST) является одной из форм ишемической болезни сердца, субстратом которого принято считать нестабильную бляшку в коронарной артерии. Также известно, что пациенты данной группы характеризуются значимым коморбидным фоном в силу более старшего возраста в сравнении с когортой пациентов с ОКС с подъемом сегмента ST [1]. Крайняя клинико-демографическая и анатомо-ангиографическая неоднородность пациентов с ОКСбпST создает существенные трудности в вопросах выбора стратегии дальнейшего лечения пациентов. Наиболее остро это касается пациентов с ОКСбпST высокого риска, когда на выбор и реализацию дальнейшего метода реваскуляризации отводится 24 ч. В силу временных рамок, ограниченных 24 ч, в большинстве случаев пациентам с ОКСбпST высокого риска выполняется чрескожное коронарное вмешательство (ЧКВ). В силу своей доступности и малотравматичности оно представляется методом выбора по сравнению с коронарным шунтированием (КШ). Однако необходимо помнить и о таких недостатках ЧКВ, как рестенозы стентов и повторные вмешательства в будущем, меньшие возможности по достижению полной реваскуляризации в сравнении с КШ [2]. Вместе с тем, поражение ствола левой коронарной артерии (CтЛКА) встречается у 10% пациентов, а летальность через 5 лет у данных пациентов достигает 50% [3]. Несмотря на совершенствование эндоваскулярных техник на СтЛКА, оптимальная стратегия остается предметом споров, особенно учитывая большой объем и техническую сложность ЧКВ в ситуациях, когда стенозу СтЛКА сопутствует многососудистое поражение. В приведенном ниже клиническом случае продемонстрирована возможность применения баллонной ангиопластики (БА) у пациента с рестенозом стента в СтЛКА в качестве «моста» к ранней хирургической реваскуляризации при ОКСбпST высокого риска.
Клинический случай
Пациентка в возрасте 71 года поступила в клинику 08.06.2021 г. для выполнения плановой коронароангиогра-фии (КАГ). Из анамнеза известно о том, что 23.04.2020 г. в рамках ОКС выполнено стентирование СтЛКА, передней нисходящей артерии (ПНА) и огибающей артерии (ОА) стентами с лекарственным покрытием (DES). После вмешательства клиника стенокардии не прослеживалась, однако в сентябре 2021 г. отмечалось возобновление стенокардии в пределах II функционального класса. Пациентка наблюдалась у кардиолога по месту жительства, направлена на плановую КАГ 08.06.2021 г. При поступлении по электрокардиограмме (ЭКГ) регистрируется синусовый ритм, ишемические изменения не определяются. На момент поступления двойную антитромбоцитарную терапию (ДАТ) не получала. По результатам проведенной плановой КАГ правая и левая коронарные артерии отходили от правого коронарного синуса. Выявлены субтотальные рестенозы стентов в СтЛКА, ПНА и ОА, а также стенозы ПНА 70% и ОА 90% дистальнее стентов, устьевой значимый стеноз артерии острого края (АОК), рисунок 1.
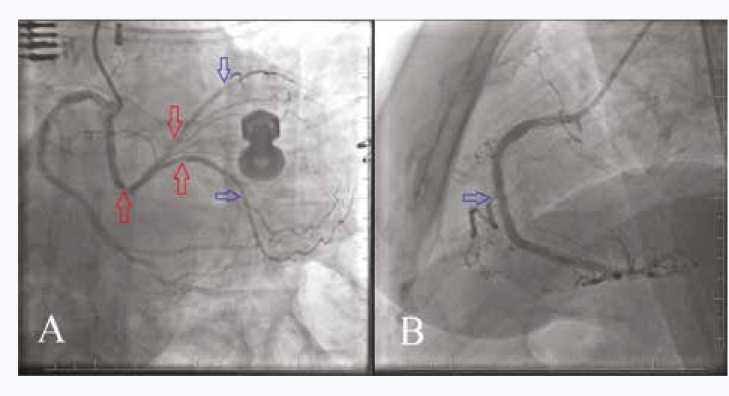
Рис. 1. А – левая косая каудальная проекция. Красными стрелками указаны рестенозы в стентах в СтЛКА, ПНА и ОА, синими – значимые стенозы дистальнее стентов в ПНА и ОА. В – правая косая каудальная проекция. Стрелкой указан устьевой стеноз артерии острого края Fig. 1. A – left oblique caudal projection. Red arrows indicate restenoses in the stents; blue arrows indicate significant stenoses distal to the stents. B – right oblique caudal projection. The arrow indicates the ostial stenosis of аcute marginal artery
Состояние пациентки обсуждено кардиокомандой (кардиолог, рентгенэндоваскулярный хирург и сердечно-сосудистый хирург). Рискометрия тяжести поражения коронарного русла по Syntax score составила 44 балла (тяжелое поражение с крайне высоким риском неблагоприятных событий при выполнении ЧКВ), принято решение в пользу КШ в срочном порядке. Рекомендовано дообследование: тромбоэластография, цветное дуплексное сканирование брахиоцефальных артерий (ЦДС БЦА), компьютерная томография (КТ) без контрастиро- вания восходящего отдела аорты на предмет выявления кальциноза. Пациентка для предоперационной подготовки переведена в отделение реанимации под мониторное наблюдение. В первый час пребывания в отделении реанимации у пациентки регистрировался кратковременный ангинозный приступ, купируемый нитратами. Тропонин Т < 0,05 нг/мл. Однако, по данным ЭКГ, отмечалась депрессия ST в отведениях I, AVL, V2-V3, признаки умеренной субэндокардиальной ишемии миокарда левого желудочка (рис. 2).
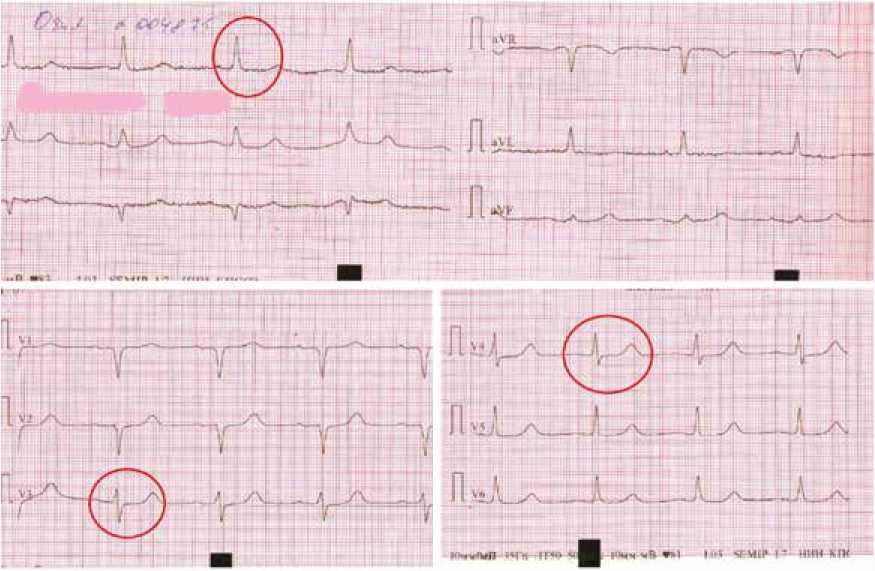
Рис. 2. Электрокардиограмма до вмешательства. Выделена депрессия ST
Fig. 2. Electrocardiogram before intervention. Highlighted ST depression
По данным эхокардиографии (ЭхоКГ), фракция выброса (ФВ) левого желудочка составила 62%, нарушения локальной сократимости миокарда отсутствуют, имеются склеротические изменения на митральном клапане, регургитация 0–I степени. Учитывая повторяющиеся ангинозные приступы в состоянии покоя, отрицательную динамику по ЭКГ в дневное время 09.06.2021 г. и характер поражения коронарного русла, принято решение о повторной КАГ и последующем обсуждении состояния пациентки с ОКСбпST высокого риска. По данным повторной КАГ, отрицательной динамики не выявлено. Кардиокомандой рекомендована установка внутриаортальной баллонной контрпульсации (ВАБК) с последующей БА рестенозов стентов. Через общую бедренную артерию справа установлен ВАБК, затем выполнена успешная БА рестенозов с СтЛКА, ПНА и ОА. Результат успешной БА представлен на рисунке 3.
С учетом отсутствия имплантации коронарных стентов и планируемой операции КШ ДАТ не назначалась. Продолжена предоперационная подготовка пациентки к оперативному лечению.
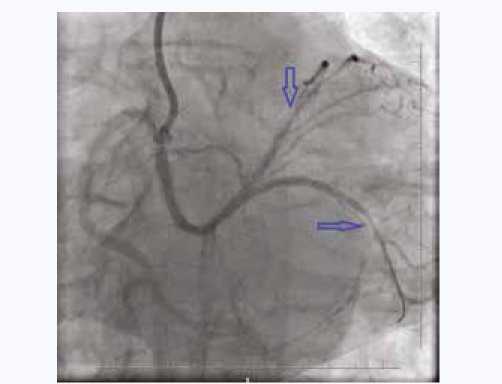
Рис. 3. Левая косая каудальная проекция. Результат баллонной ангиопластики. Остаточные стенозы указаны синей стрелкой
Fig. 3. Left oblique caudal projection. The result of balloon angioplasty.
Residual stenoses are indicated by blue arrows
По данным тромбэластографии, значимых отклонений от референсных значений не выявлено (R = 6,8 мин, К = 1,2 мин, Angle = 72 deg, MA = 69,1 мм), что свидетельствует о нормоагрегации тромбоцитов. По ЦДС БЦА выявлены гемодинамически незначимые стенозы внутренних сонных артерий, окклюзия левой позвоночной артерии.
КТ восходящего отдела аорты позволила установить локальные кальцинаты надклапанной части аорты, данных за кальциноз восходящего отдела аорты не выявлено (рис. 4).
В динамике после проведенной БА рестенозов стентов состояние пациентки оставалось стабильным, ЭКГ картина прежняя, тропонин в пределах референсных значений. В утренние часы 10.06.2021 г. больная доставлена в операционную на фоне продолжающейся ВАБК. Доступ, выделение кондуитов и основной этап операции прошли без технических особенностей. В условиях искусственного кровообращения (ИК) выполнено аутовенозное аортокоронарное шунтирование ветви острого края (ВОК) и 1 ветви тупого края, маммарокоронарное шунтирование ПНА. Время ИК составило 92 мин, время пережатия аорты – 64 мин. В клинике проведена рутинная флоуметрия (MEDISTIM VeriQ™) для контроля функции шунтов. Поток по маммарному шунту составил 40 мл/мин, пульсовой индекс (ПИ) – 2, на аутовенозных шунтах к АОК и ветви тупого края (ВТК) – 70 мл/мин, ПИ 2,5 и 30 мл/мин, ПИ – 3 соответственно. Проведены хирургический гемостаз и послойное ушивание раны. Осуществлено отлучение от ВАБК. Пациентка доставлена в отделение реанимации. Через 4 ч проведена плановая экстубация пациентки, установлена стабильная гемодинамика без инотропной поддержки. За первые сутки послеоперационного периода дренажные потери по страховочным дренажам составили 250 мл, тропонин Т = 0,17 нг/мл, пациентка переведена в блок интенсивной терапии кардиохирургического отделения, где ей назначена ДАТ. Закономерное течение послеоперационного периода. На вторые сутки после операции по ЭКГ отмечается течение послеоперационного перикардита, очаговых изменений нет (рис. 5).
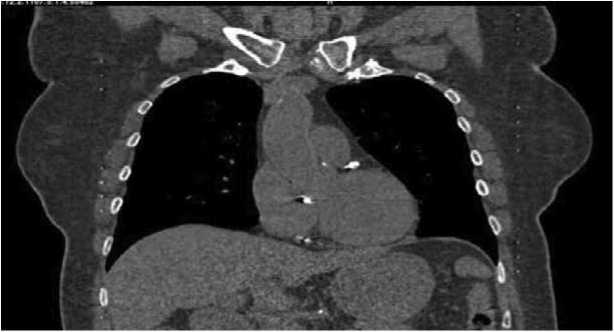
Рис. 4. Компьютерная томография восходящей аорты. Фронтальная проекция Fig. 4. CT of the ascending aorta. Frontal projection
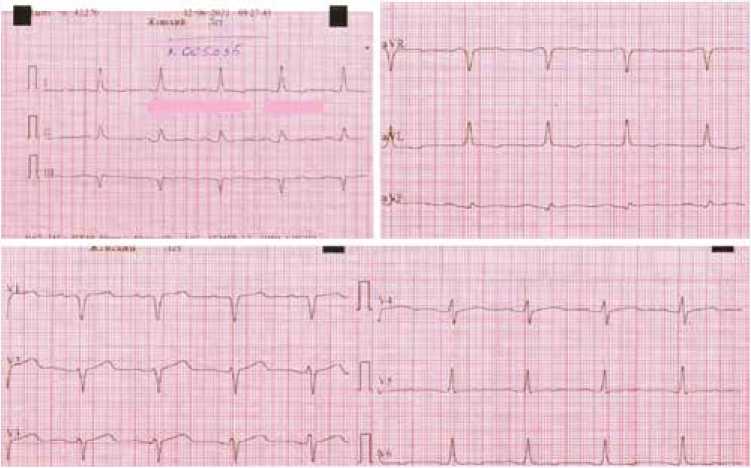
Рис. 5. Электрокардиограмма после коронарного шунтирования Fig. 5. Electrocardiogram after coronary artery bypass grafting
Плановое удаление временных электродов и центрального катетера на 5-е сут. По данным ЭхоКГ, ФВ составляет 66%, свободной жидкости в полости перикарда не обнаружено. Пациентка в удовлетворительном состоянии выписана на 13-е сут послеоперационного периода. В последующем (время наблюдения 5 мес. после операции) пациентка не отмечает рецидивов ангинозных приступов.
Обсуждение
В современной литературе не описаны случаи использования БА в качестве меры, позволяющей устранить критические рестенозы для профилактики развития сердечно-сосудистой катастрофы при подготовке пациента на экстренную хирургическую реваскуляризацию миокарда. В целом оптимальная стратегия при рестенозе стента в настоящее время широко обсуждается [4]. Актуальные рекомендации предписывают выполнение БА, имплантацию стентов с лекарственным покрытием (ЛП), а также выполнение БА баллоном с ЛП [5, 6]. В настоящее время уделяется повышенный интерес к последнему подходу. Так, в метаанализе W. Mamuti и соавт. систематизированы исследования, посвященные проблематике лечения рестеноза стента DES простым баллоном и баллоном с ЛП. В исследование включено 5 рандомизированных исследований с суммарной выборкой, составляющей 964 пациента (468 вмешательств с простым баллоном + DES, 396 – с баллоном с ЛП). Показано, что частота MACE при применении баллона с ЛП существенно ниже, чем при применении простого баллона или повторной имплантации DES (19,7 против 32,5%, р = 0,012). Другими авторами представлены сопоставимые результаты применения баллона с ЛП и повторной имплантации DES [7, 8]. Тем не менее в данном клиническом случае предпочтение отдано КШ, учитывая рестеноз стентов с ЛП через 14 мес., наличие значимых стенозов ПНА и ОА дистальнее рестенозированных стентов, значимый устьевой стеноз
АОК, удовлетворительное дистальное русло, а также 44 балла по Syntax score, указывающее на предпочтительность КШ.
Современные исследования демонстрируют обнадеживающие результаты КШ по сравнению с ЧКВ. Показано, что выполнение КШ у пациентов с ОКС позволяет снизить частоту нефатальных инфарктов миокарда, а также снижает риск повторных вмешательств [9, 10]. Согласно данным американских коллег (S.H. Patlolla и соавт.), доля пациентов с ОКСбпST в когорте пациентов, которым проведено КШ в экстренном порядке, с 2000 по 2017 гг увеличилась с 56 до 80% ( p < 0,001) [11]. Тем не менее, частота экстренного КШ из всех пациентов, госпитализированных с острым инфарктом миокарда ( n = 11 622 528), составила 9,7% ( n = 1 071 156). Авторы отмечают снижение летальности в данной группе пациентов с 5,2 до 3,5% за период наблюдения. Таким образом, у пациентов с ОКСбпST с многососудистым поражением выполнение КШ представляется методом выбора. Применение БА в представленном случае позволило предупредить окклюзию стентов в области субтотальных стенозов, что, в свою очередь, в сочетании с ВАБК сделало возможным выполнение дообследования на фоне стабилизации состояния и подготовку пациента к неотложному хирургическому вмешательству. Наличие значимых стенозов дистальнее стентов позволило избежать конкурентного кровотока по нативной артерии, что было подтверждено данными интраоперационной флоуметрии.
Выводы
Применение БА у пациентов с субтотальным рестенозом стентов при ОКСбпST высокого риска и многососудистом поражении позволяет снизить риск окклюзии рестенозированных стентов и подготовить пациента к экстренной хирургической реваскуляризации миокарда, не назначая ДАТ.
Список литературы Баллонная ангиопластика рестенозов коронарных стентов в качестве "моста" к экстренному коронарному шунтированию при остром коронарном синдроме без подъема сегмента ST высокого риска
- Lemor A., Hernandez G.A., Patel N., Blumer V., Sud K., Cohen M.G. et al. Predictors and etiologies of 30-day readmissions in patients with non-ST-elevation acute coronary syndrome. Catheter. Cardiovasc. Interv.2019;93(3):373-379. https://doi.org/10.1002/ccd.27838.
- Ram E., Sternik L., Klempfner R., Iakobishvili Z., Peled Y., Shlomo N. et al. Outcomes of different revascularization strategies among patients presenting with acute coronary syndromes without ST elevation. J. Thorac. Cardiovasc. Surg. 2020;160(4):926-935.e6. https://doi.org/10.1016/j.jtcvs.2019.08.130.
- Tam D.Y., Bakaeen F., Feldman D.N., Kolh P., Lanza G.A., Ruel M. et al. Modality selection for the revascularization of left main disease. Can. J. Cardiol. 2019;35(8):983-992. https://doi.org/10.1016/j.cjca.2018.12.017.
- Стельмашок В.И., Полонецкий О.Л., Зотова О.В., Стриго Н.П., Зацепин А.О., Захаревич А.Н. и др. Эффективность рентгеноэндоваскулярной коррекции внутристентовых рестенозов после успешно выполненной реканализации хронических тотальных окклюзий коронарных артерий. Комплексные проблемы сердечно-сосудистых заболеваний. 2019;8(2):37-48. https://doi.org/10.17802/2306-1278-2019-8-2-37-48.
- Sousa-Uva M., Neumann F., Ahlsson A., Alfonso F., Banning A., Benedetto U. et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur. J. Cardiothorac. Surg. 2019;55(1):4-90. https://doi.org/10.1093/ejcts/ezy289.
- Levine G.N., Bates E.R., Blankenship J.C., Bailey S.R., Bittl J.A., Cercek B. et al. 2011 ACCF/AHA/ SCAI Guideline for percutaneous coronary intervention: A report of the American College of Cardiology Foundation/ American Heart Association Task Force on Practice Guidelines and the Society for Cardiovascular Angiography and Interventions. Circulation. 2011;124(23):e574-651. https://doi.org/10.1161/CIR.0b013e31823ba622.
- Giacoppo D., Alfonso F., Xu B., Claessen B.E.P.M., Adriaenssens T., Jensen C. et al. Drug-coated balloon angioplasty versus drug-eluting stent implantation in patients with coronary stent restenosis. J. Am. Coll. Cardiol. 2020;75(21):2664-2678. https://doi.org/10.1016/j.jacc.2020.04.006.
- Lin Y., Sun X., Liu H., Pang X., Dong S. Drug-coated balloon versus drug-eluting stent for treating de novo coronary lesions in large vessels: A meta-analysis of clinical trials. Herz. 2021;46(3):269-276. https://doi.org/10.1007/s00059-020-04938-8.
- Neumann A., Vöhringer L., Fischer J., Mustafi M., Schneider W., Krüger T. et al. Off-pump coronary artery bypass grafting in acute coronary syndrome: Focus on safety and completeness of revascularization. Thorac. Cardiovasc. Surg. 2020;68(8):679-686. https://doi.org/10.1055/s-0039-1677834.
- Huckaby L.V., Sultan I., Mulukutla S., Kliner D., Gleason T.G., Wang Y. et al. Revascularization following non-ST elevation myocardial 34 infarction in multivessel coronary disease. J. Card. Surg. 2020;35(6):1195-1201. https://doi.org/10.1111/jocs.14539.
- Patlolla S.H., Kanwar A., Cheungpasitporn W., Doshi R.P., Stulak J.M., Holmes D.R. Jr. et al. Temporal trends, clinical characteristics, and outcomes of emergent coronary artery bypass grafting for acute myocardial infarction in the United States. J. Am. Heart Assoc. 2021;10(15):e020517. https://doi.org/10.1161/JAHA.120.020517.


