Барий как раскислитель и модификатор жидкой стали
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна, Выдрин Дмитрий Александрович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 1 т.13, 2013 года.
Бесплатный доступ
Выполнен анализ термодинамических функций реакций раскисления барием жидкой стали. Построены поверхности растворимости для условий раскисления жидкой стали сплавами бария с кремнием и алюминием. Показано, что реально возможно описание закономерностей раскисления барием только в том случае, если константа раскисления барием составляет ~ 10 -4-10 -5. Вследствие малой растворимости и большой молекулярной массы барий не может быть эффективным раскислителем. Из имеющихся в литературе рекомендаций по подбору модификаторов, поверхностных свойств бария в металле показано, что введенный в сталь барий на заключительном этапе рафинирования способен уменьшать размеры неметаллических включений и измельчать первичное зерно литого металла. Сделан вывод о том, что барий не является эффективным раскислителем, но может играть роль модификатора.
Барий, раскислитель, модификатор, сталь
Короткий адрес: https://sciup.org/147156806
IDR: 147156806 | УДК: 669.18.054:669.893+669.141.33
Barium as deoxidant and modifier of liquid steel
Thermodynamic functions of reactions of deoxidation by barium of liquid steel are analyzed. Solubility surfaces for conditions of deoxidation of liquid steel by barium alloys with silicon and aluminium are drawn. It is shown that the description of regularities of deoxidation by barium is really possible only if the constant of deoxidation by barium is about 10 -4-10 -5. Owing to small solubility and great molecular weight barium cannot be an effective deoxidant. From recommendations available in literature about the selection of modifiers and surface properties of barium in metal it is shown that the barium entered into steel at the final stage of refinement is capable to reduce the amount of nonmetallic inclusions and to refine the primary grain of cast metal. The conclusion is drawn that barium is not an effective deoxidant but can play the role of a modifier.
Текст научной статьи Барий как раскислитель и модификатор жидкой стали
В настоящее время раскислительная и рафинирующая способность сплавов, смесевых раскислителей и лигатур определяется в основном по кривым раскислительной способности отдельных элементов: алюминия, кремния, кальция и других путем нанесения термодинамических данных по разным системам на общие диаграммы, построенные в координатах [O, %] – элементы-раскислители [R, %], причем по оси абсцисс откладываются концентрации всех перечисленных выше раскислителей. На основании этих упрощенных построений делаются выводы об относительной раскисли-тельной и рафинирующей способности отдельных элементов и возможности их комплексного применения. Эта концепция изложена в учебной и монографической литературе по металлургии стали и теории металлургических процессов. Следует отметить, что вышеперечисленные кривые раскис-лительной способности могут характеризовать только конкретную систему. Например, раскисли-тельная способность алюминия (изотерма раскисления) характеризует ситуацию в системе Fe–Al–O, изотерма раскислительной способности кремния – систему Fe–Si–O и т. д. Если необходимо установить, при каких концентрациях и температурах, скажем, в качестве индивидуальных раскислителей или комплексно выступают кремний и алюминий, необходимо рассматривать систему Fe–Si–Al–O. А в присутствии углерода – необходимо уже рассматривать систему Fe–Si–Al–С–O. Особенные трудности в понимании проблемы рафинирования реального металла возникают при изучении взаимодействия высокоактивных элементов – Ca, Mg, Ba, растворенных в стали, с неметаллическими примесями O, C, N, S. Если кальций и магний под- тверждают эффективность своего участия в процессах рафинирования присутствием в составе неметаллических включений в стали, то введенный в сталь барий ведет себя неоднозначно. Исследователи отмечают, что после введения бария в металл его в нем не находят или практически не находят ни в металле, ни в неметаллических включениях [1]. В то время как кальций, обладающий по приблизительным анализам меньшей раскисли-тельной способностью, обнаруживается и в шлаковых глобулях, и в силикатах, и в алюминатах.
По фазовому составу включений во многих работах утверждается следующее: в конечном счете, при раскислении силикобарием состав неметаллических включений подобен раскислению кремнием, при раскислении алюмобарием – состав неметаллических включений через 1–2 мин аналогичен тому, что получается при раскислении алюминием. В пробах, отобранных через 1–2 мин после введения лигатур с барием, в неметаллических включениях не обнаруживается оксид бария, затем оксиды бария в течение нескольких минут встречаются в единичных включениях комплексов алюминатов и силикатов. Далее в отобранных пробах барий не обнаруживается.
Результаты раскисления стали сплавом Ca– Si–Al–Ba показывают, что образовавшиеся в стали неметаллические включения принадлежат системе CaO–SiO 2 –Al 2 O 3 . Оксид бария в этих оксидах не обнаруживается [2].
Для того чтобы разобраться с механизмом влияния сплавов с барием на глубину раскисления металла и формирование неметаллических включений, необходимо провести тщательный термодинамический анализ процессов раскисления ба- рием. Мы предлагаем установить концентрационные области составов металла, равновесных со всеми возможными неметаллическими фазами, используя при этом аппарат химической термодинамики и имеющиеся экспериментальные данные по растворимости компонентов жидкого металла. Этот метод мы назвали методом построения поверхностей растворимости компонентов в металле (метод построения ПРКМ). Для этого также необходима термодинамическая интерпретация сопряженных с металлическими фазами диаграмм состояния неметаллических систем, т. е. необходимо знать активности компонентов или их соединений в жидком состоянии, активности компонентов, как в неметаллических, так и в металлических фазах переменных составов.
Исходя из тройной диаграммы состояния FeO - BaO - SiO2 (рис. 1) можно считать, что на изотермических сечениях ПРКМ системы Fe–Si– Ba–O–C должны существовать области составов металла, равновесного с оксидным расплавом переменного состава, твердыми оксидами бария и кремния, силикатами бария ( 2BaO ⋅ SiO2 и при T < 1873 К BaO ⋅ SiO2). В присутствии углерода возможно образование и газовой фазы, состоящей из CO и CO2 .
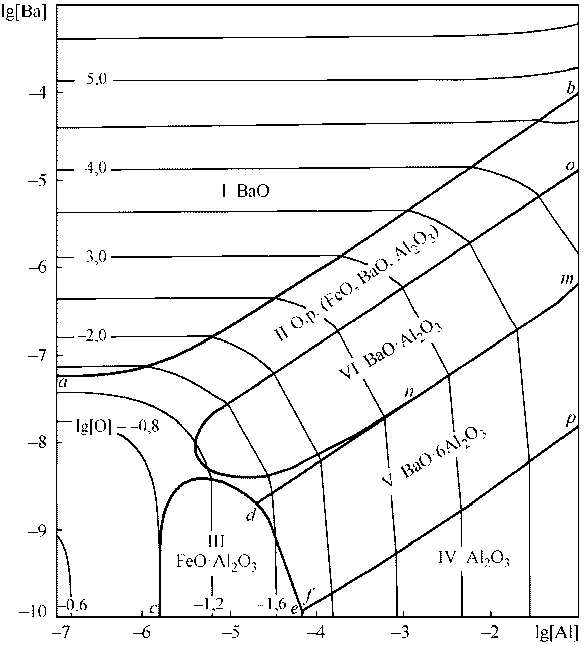
На рис. 2 приведена диаграмма состояний системы FeO - BaO - Al2O3 , из которой следует, что в равновесии с жидким металлом при раскислении сплавом Ba и Al могут находиться корунд (Al2O3 ), оксид бария ВаО, алюминаты бария (BaO⋅6Al2O3, BaO⋅Al2O3 и при T < 1873 К 3BaO ⋅ Al2O3 ) и оксидный расплав переменного состава ( FeO, BaO, Al2O3 ).
Термодинамические данные, использованные при расчете координат ПРКМ, приведены в табл. 1–4.
Первые три позиции в табл. 1 получены путем термодинамических расчетов с использованием термохимических данных. Ю.А. Агеев и С.А. Ар-чугов получили сведения из своих экспериментальных данных. В работе [7] данные получены путем сопоставления составов промышленного металла и расчета координат поверхности ликвидус диаграммы FeO - BaO - Al2O3 (см. рис. 2).
При проведении расчетов координат ПРКМ активности компонентов металлических расплавов рассчитывали с использованием параметров взаимодействия (см. табл. 4). Оксидные расплавы полагались субрегулярными растворами. Энергетические параметры этих растворов представлены в табл. 3. Методика расчетов подробно изложена в работе [8]. После проведения расчетов было проведено сравнение ПРКМ. Рассматривались рис. 3, а, б, а так же рис. 4, а, б.
Если учесть данные работы [4], то при концентрации кремния в металле 0,1 мас. % уже при
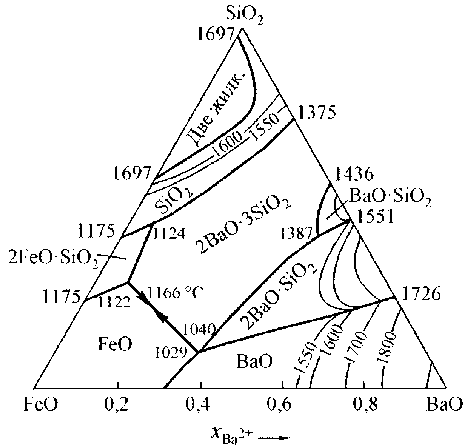
Рис. 1. Диаграмма состояния системы FeO–BaO–SiO 2
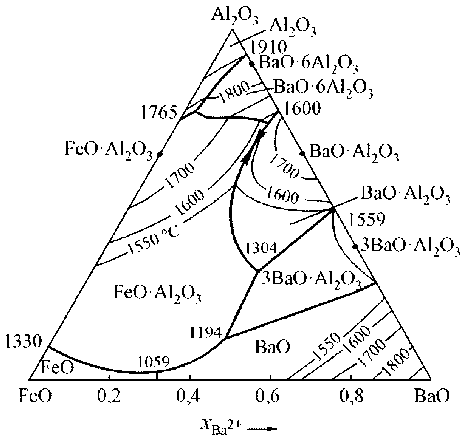
Рис. 2. Диаграмма состояния системы FeO–BaO–Al 2 O 3
Таблица 1
Зависимость констант равновесия для реакции раскисления стали барием |BaO| = [Ba] + [O]
|
№ |
lg K = – A / T + B |
K 1873 |
Авторы |
|
1 |
–31 830/ Т + 7,65 |
7,4·10–11 |
Куликов И.С. [3] |
|
2 |
–32 433/ Т + 7,87 |
7,0·10–9 |
Бужек З. [4] |
|
3 |
–30 416/ Т + 11,86 |
2,6·10–8 |
Камардин В.А. [5] |
|
4 |
–37 734/ Т + 9,43 |
3,12·10–11 |
Арчугов С.А., Агеев Ю.А. [6] |
|
5 |
–4,109 |
7,78·10–5 |
Михайлов Г.Г., Вильгельм Е.М. [7] |
Таблица 2
Зависимость констант равновесия от температуры
|
Реакция |
lg K = – A / T + B |
|
|
A |
B |
|
|
(FeO) = [Fe] + [O] |
6320 |
4,734 |
|
(Al 2 O 3 ) = 2[Al] + 3[O] |
58 320 |
18,02 |
|
(BaO) = [Ba] + [O] |
20 384 |
7,36 |
|
(SiO 2 ) = [Si] + 2[O] |
30 225 |
11,56 |
|
|Al 2 O 3 | = 2[Al] + 3[O] |
64 000 |
20,48 |
|
|BaO| = [Ba] + [O] |
23 400 |
8,73 |
|
|SiO 2 | = [Si] + 2[O] |
31 100 |
12,0 |
|
I ВаО^А1 2 О з | = [Ba] + 2[Al] + 4[O] |
84 000 |
25,76 |
|
I BaO^6A№ | = [Ba] + 12[Al] + 19[O] |
402 350 |
125,99 |
|
I 3BaO^A№ | = 3[Ba] + 2[A1] + 6[O] |
127 800 |
40,95 |
|
| 2BaO^SiO 2 | = 2[Ba] + [Si] + 4[O] |
77 718 |
27,385 |
|
| BaO^SiO 2 | = [Ba] + [Si] + 3[O] |
54 129 |
19,048 |
|
{CO} = [C] + [O] |
1168 |
–2,07 |
|
{CO 2 } = [C] + 2[O] |
9616 |
2,51 |
Таблица 3
Энергетические параметры теории субрегулярных ионных растворов для оксидных расплавов FeO–BaO–SiO 2 и FeO–BaO–Al 2 O 3
|
Система |
Параметры теории Qijkl , кал/моль |
||
|
Q iiij |
Q iijj |
Q ikkk |
|
|
FeO–BaO |
–5000 |
–10 000 |
–5000 |
|
FeO–SiO 2 |
229 |
–8162 |
12 088 |
|
FeO–Al 2 O 3 |
661 |
–16329 |
–4917 |
|
BaO–SiO 2 |
–8346 |
–65 493 |
–5485 |
|
BaO–Al 2 O 3 |
–21 194 |
–10 073 |
–32 395 |
|
SiO 2 –Al 2 O 3 |
6175 |
11 565 |
928 |
|
Система |
Q iijk |
Q ijjk |
Q ijkk |
|
FeO–BaO–SiO 2 |
–40 000 |
–50 000 |
–70 000 |
|
FeO–BaO–Al 2 O 3 |
–10 000 |
–20 000 |
–30 000 |
Таблица 4
Параметры взаимодействия компонентов eij в жидком металле при T = 1873 К
Независимо от того, какое количество бария вводилось в металл (до 0,2 кг/т), через несколько минут барий ни в металле, ни во включениях не обнаруживался [2]. Что при этом происходит с введенным в металл барием? В какой-то степени ситуацию может прояснить эксперимент, в котором был проведен баланс расхода бария. Надо учесть, что барий – поверхностно-активный элемент по отношению к железу и поэтому стремится выйти на любую межфазную границу: жидкого металла с футеровкой, шлаком, неметаллическими включениями, газовой фазой [9]. При проведении балан- совых лабораторных плавок было установлено, что из всего введенного в металл бария в среднем около 12 % ВаО находится в оксидной пленке на поверхности слиточка, 17 % на боковой и донной части слиточка, 66 % – в прилегающих стенках тигля с образованием алюминатов 3BaO ⋅ Al2O3 и
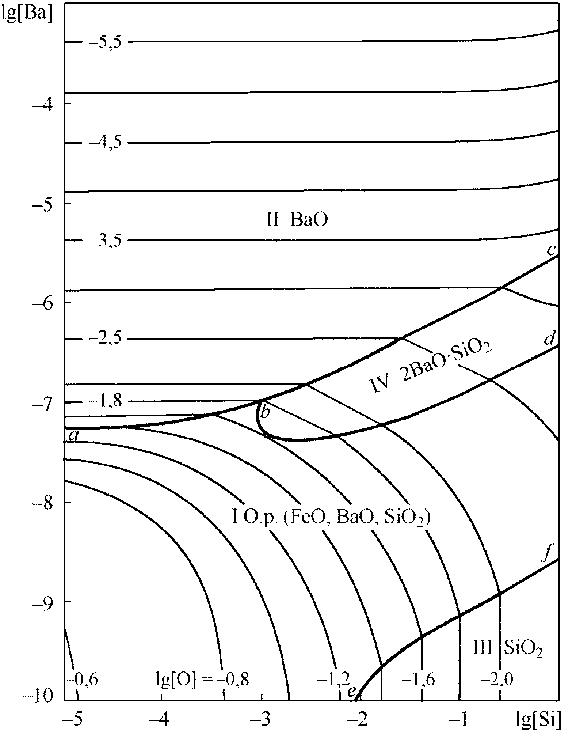
а)
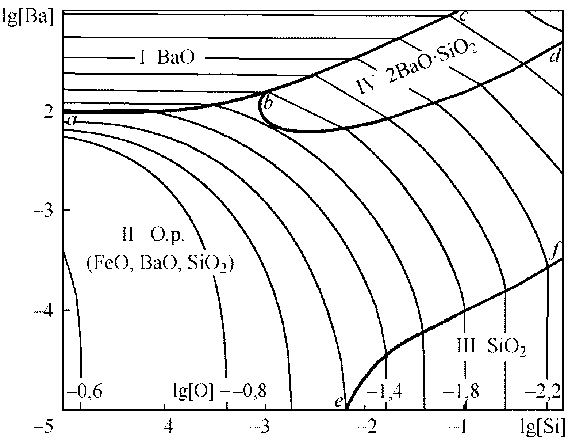
б)
Рис. 3. ПРКМ системы Fe–Ba–Si –O (1873 К) по данным [4] (а) и [7] (б)
а)
б)
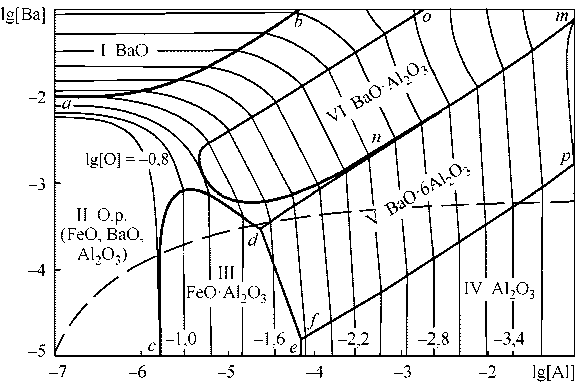
Рис. 4. ПРКМ системы Fe–Ba–Al–O (1873 К) по данным [4] (а) и [7] (б)
BaO ■ Al 2 O 3 ; 1,5-2 % ВаО было обнаружено в возгонах на крышке тигля. То же самое, скорее всего, происходит и в промышленном металле. Лишь незначительная часть бария участвует в образовании неметаллических включений. Из проведенного термодинамического анализа следует, что вклад бария в раскисление ничтожен. Если при концентрации насыщения содержание бария составит 0,001 мас. % и весь барий израсходуется на связывание кислорода, то концентрация кислорода в стали уменьшится на 0,001 % —— = 0,00011, т. е.
MBa на неуловимую величину.
На рис. 4, б показан возможный ход процесса раскисления стали при введении алюмобариевой лигатуры, нанесенный на ПРКМ штриховой линией. Вначале, при малых концентрациях бария и алюминия, возможно участие бария в образовании жидких неметаллических включений. Затем, по мере роста концентрации алюминия, возможно образование алюминатов бария и далее корунда [2]. При этом достигается предельная возможная концентрация бария в стали и несмотря на дальнейшее введение в сталь он лишь в малых количествах может остаться в жидком металле. По-види-мому, барий может модифицировать металл и влиять на размеры неметаллических включений.
Действительно, в промышленном металле отмечается модифицирующее действие бария [10]. Обычно модифицирующее действие оценивается по влиянию на размеры неметаллических включений, на размеры первичного зерна в литом металле, технологическую пластичность и на эксплуатационные свойства металла. При производстве конструкционного и транспортного металла после введения комплексных сплавов с барием отмечается измельчение неметаллических включений (но барий в них не определяется), уменьшение первичного зерна, снижение анизотропии механических свойств и повышение пластичности литого металла. Анализ свойств эффективных модификаторов показывает, что обычно они отличаются малой растворимостью в стали, высокой химической активностью (большим сродством к кислороду, сере, азоту, углероду) и краткосрочностью действия, сопровождаемого длительным повышением свойств стали. В этом отношении барий подходит под все требования и может быть эффективным модификатором. Так отсутствие крупных включений после введения бария в сталь может быть связано с высокой поверхностной активностью бария. Присутствующий в металле барий понижает межфазное натяжение между зарождающимся включением и жидким металлом и тем самым уменьшает критический радиус зародыша и пересыщение по компонентам металла. В результате получится большое количество мелких включений, которые несущественно влияют на механические свойства стали.
Другой модифицирующий фактор может быть связан со взаимодействием микроколичеств бария с кластерными образованиями в жидком металле. О микрокристаллической неоднородности жидкого металла известно из работ В.И. Архарова, И.А. Новохатского, Н.А. Ватолина, Б.А. Баума, Г.В. Тягунова [11]. Гомогенизации металлического расплава, как это следует из работ Б.А. Баума и Г.В. Тягунова, можно добиться в результате высокотемпературной обработки металлических расплавов. В работах И.А. Новохатского [12] и А.А Дерябина [13] утверждается, что гомогенизация металлического расплава возможна после введения в жидкий металл поверхностно-активных веществ, которые сворачивают процесс кластерообразова-ния, понижают температуру начала кристаллизации и таким образом понижают температуру гомогенизации стали. Это приводит к измельчению первичного зерна в литом металле, повышению технологической пластичности стали и снижению показателей анизотропии.
Заключение
-
1. В силу малой растворимости в жидком металле и высокой поверхностной активности барий не может быть эффективным раскислителем стали.
-
2. Высокая поверхностная активность бария позволяет рассматривать барий как достаточно эффективный модификатор. Использование бария в лигатурах приводит к измельчению неметаллических включений, гомогенизации жидкого металла, понижению температуры ликвидус, измельчению первичного зерна литой стали, увеличению технологической пластичности. Все перечисленные эффекты получены на промышленных плавках стали.
Список литературы Барий как раскислитель и модификатор жидкой стали
- Deoxidation and Desulphyrization of liquid iron with barium and barium bearing calcium alloys/Y. Kataura, T. Shoji, K. Topawa, T. Takahashi//Transaction Iron and Steel Institute Japan. -1980. -Vol. 20, no. 12. -P. 801.
- Природа неметаллических включений в основной подшипниковой стали, обрабатываемой в ковше порошками щелочноземельных металлов/Е.Ф. Мазуров, А.М. Евграшин, О.С. Тучкина, Г.Г. Михайлов//Неметаллические включения в сталях: темат. отраслевой сб. -М.: Металлургия, 1983. -С. 67-76.
- Куликов, И.С. Раскисление металлов/И.С. Куликов. -М.: Металлургия, 1975.-504 с.
- Bužek, Z. Základní termodynamické údaje o metalurgických reakcích a o interakcích prvků v sous-tavách významných pro hutnickou teorii a praxi/Z. Bužek//Hutn. actual. -1979. -Vol. 20, no. 1-2. -S. 111.
- Камардин, В.А. Термодинамика реакций щелочноземельных металлов при рафинировании легированных сталей фторидно-оксидными расплавами/В.А. Камардин, Г.М. Никитин//Теория металлургических процессов: сб. науч. тр. -М.: Металлургия, 1975. -№ 3. -С. 168-177.
- Агеев, Ю.А. Исследование растворимости ЩЗМ в железе, чугуне, сталях и ферросплавах/Ю.А. Агеев, С.А. Арчугов//Научно-технический отчет. Челябинский НИИМ -Челябинск, 1984. -95 с.
- Михайлов, Г.Г. Термодинамический анализ процессов раскисления коррозионностойкой стали Х18Н10Т кальцием и барием/Г.Г. Михайлов, Л.А. Чернова//Известия вузов. Черная металлургия. -1991. -№ 12. -С. 37-40.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю. С. Кузнецов. -М.: Издат. Дом МИСиС, 2009. -520 с.
- Михайлов, Г.Г. Влияние бария на контактное взаимодействие стали Х18Н10Т с оксидными материалами/Г.Г. Михайлов, И.Ю. Пашкеев, Л.А. Чернова//Высокотемпературные расплавы. -1996. -№ 1. -С. 17-22.
- Перспективное применение барийсодер жащих лигатур для раскисления и модифицирования транспортного металла/К.В. Григорович, К.Ю. Демин, А.И. Арсенкин и др.//Металлы. -2011. -№ 5. -С. 146-156.
- Термовременная обработка расплава -основа развития нанотехнологий/В.С. Цепелев, Б.А. Баум, Г.В.Тягунов и др.//Современные проблемы электрометаллургии стали: материалы XIII Междунар. конф./под ред. В.Е. Рощина. -Челябинск: Изд-во ЮУрГУ, 2007. -Ч. 1. -С. 33-34.
- Новохатский, И.А. О механизме влияния различных добавок на переохлаждение жидкого железа/И.А. Новохатский, А.И. Погорелов, B.З. Кисунько//Изв. АН СССР. -1969. -Т. 185. -C. 1069.
- Влияние модифицирования рельсовой стали барием и кальцием на свойства рельсов/А.А. Дерябин, В.В. Могильный, Л.А. Годик и др.//Влияние свойств металлической матрицы на эксплуатационную стойкость рельсов: сб. науч. тр. -Екатеринбург: ГНЦ РФ ОАО УИМ, 2006. -С. 18-36.


