Биметаллические Комплексы со связями Ag-Sb: особенности синтеза и строения
Автор: Шарутина О.К., Шарутин В.В., Ефремов А.Н.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 2 т.17, 2025 года.
Бесплатный доступ
Три(пара-толил)сурьма реагирует с нитратом серебра в смеси метанол/ацетонитрил при комнатной температуре как в мольном соотношении 3:1, так и 4:1 с образованием ионного комплекса [(p-Tol3Sb)4Ag][NO3] (1). Продуктом реакции трифенилсурьмы с нитратом серебра в тех же условиях является нитратотрис(трифенилстибин)серебро (Ph3Sb)3AgNO3 (2) независимо от их мольного соотношения. Попытка заместить в комплексе (Ph3Sb)3AgNO3 нитратный лиганд на карбоксилатный при действии 2-метоксибензойной кислоты (мольное соотношение 1:1) и добавлении триэтиламина привела к кристаллизации из реакционной смеси аддукта состава (Ph3Sb)3AgOC(O)C6H4OMe-2×(Ph3Sb)3AgNO3×2СН3ОН (3) с выходом 84 %. Комплексы 1-3 охарактеризованы методами ИК-спектроскопии и рентгеноструктурного анализа (РСА). По данным РСА, атомы Ag и Sb в 1-3 имеют искаженную в разной степени тетраэдрическую координацию с углами между связями, отклоняющимися от теоретического значения 109,5°. Средние расстояния Ag-Sb в 1-3 составляют 2,747, 2,732, 2,726 Å соответственно. Связи Sb-C варьируют в интервалах 2,128(3)-2,145(3) Å (1), 2,127(5)-2,147(5) Å (2), 2,124(6)-2,156(6) Å (3). В ионном соединении 1 нитрат-анион плоский с наличием оси симметрии С2, совпадающей с одной из связей N-O; связи O-N равны 1,148(6) и 2 × 1,164(4) Å, валентные углы составляют 110,4(7)° и 2 × 124,8(4)°. В 2 расстояние Ag-О равно 2,306(13) Å. В кристалле 3 присутствует два одинаковых фрагмента (Ph3Sb)3Ag, в которых группы OC(O)C6H4OMe-2 и NO3 имеют заселенность 50 %. Расстояния Ag-О с нитратной и карбоксилатной группами равны 2,263(14) и 2,352(18) Å соответственно. На каждый фрагмент приходится по одной молекуле сольватного метанола.
Триарилсурьма, нитрат серебра, комплексы присоединения, 2-метоксибензойная кислота, замещение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248079
IDR: 147248079 | УДК: 546.175+546.571+546.863+547.53.024+548.312.4 | DOI: 10.14529/chem250207
Bimetallic complexes with the Ag-Sb bonds: synthesis and structure features
Tri(para-tolyl)antimony reacts with silver nitrate in a methanol/acetonitrile mixture at room temperature in both 3:1 and 4:1 molar ratios to form the ionic complex [(p-Tol3Sb)4Ag][NO3] (1). The reaction product of triphenylantimony with silver nitrate under the same conditions is nitratotris(triphenylstibine)silver (Ph3Sb)3AgNO3 (2), regardless of their molar ratio. An attempt to replace the nitrate ligand in the (Ph3Sb)3AgNO3 complex with a carboxylate ligand under the action of 2-methoxybenzoic acid (molar ratio 1:1) and the addition of triethylamine resulted in the crystallization of the adduct of the composition (Ph3Sb)3AgOC(O)C6H4OMe-2·(Ph3Sb)3AgNO3·2СН3ОН (3) from the reaction mixture with a yield of 84 %. Complexes 1-3 were characterized by IR spectroscopy and X-ray diffraction analysis (XRD). According to XRD data, the Ag and Sb atoms in 1-3 have a tetrahedral coordination distorted to varying degrees with the angles between the bonds deviating from the theoretical value of 109.5°. The average Ag-Sb distances in 1-3 are 2.747, 2.732, 2.726 Å, respectively. The Sb-C bonds vary in the ranges of 2.128(3)-2.145(3) Å (1), 2.127(5)-2.147(5) Å (2), 2.124(6)-2.156(6) Å (3). In ionic compound 1, the nitrate anion is planar and includes the C2 symmetry axis coinciding with one of the N-O bonds; the O-N bonds are 1.148(6) and 2×1.164(4) Å, the bond angles are 110.4(7)° and 2×124.8(4)°. In 2 the Ag-O distance is 2.306(13) Å. In crystal 3 there are two identical fragments of (Ph3Sb)3Ag, in which the OC(O)C6H4OMe-2 and NO3 groups have an occupancy of 50%. The Ag-O distances with the nitrate and carboxylate groups are 2.263(14) and 2.352(18) Å, respectively. Each fragment contains one molecule of solvate methanol.
Текст научной статьи Биметаллические Комплексы со связями Ag-Sb: особенности синтеза и строения
В медицинской химии все чаще используются препараты, содержащие различные металлы. Так, усилиями ученых постоянно расширяется терапевтический потенциал соединений серебра. Установлено, что они могут использоваться как антисептики [1], антибактериальные [2] и нестероидные противовоспалительные [3] средства. Комплексы серебра(I) с различными типами лигандов, таких как карбоновые кислоты, аминокислоты, n -донорные лиганды с атомами азота, фосфора или серы, проявляют селективность в отношении различных раковых клеток [4–10]. Результаты исследований антипролиферативной и противоопухолевой активности комплексов се-ребра(I) рассмотрены в обзоре [11].
Исследования в области металлотерапии по разработке новых эффективных и безопасных лекарственных препаратов продолжаются. Одно из направлений исследований – создание биметаллических комплексов, сочетающих в себе элементы различного фармакологического действия. Например, соединения серебра обладают противомикробными свойствами, производные сурьмы являются хорошими антиоксидантами и препятствуют распространению инфекций в организме. Было показано, что комплексы, содержащие связи Ag–Sb и биологически активные лиганды, способны повышать защитные функции организма, снижать воспаления, лечить острые хронические заболевания, могут выступать как селективные противораковые агенты [12].
Координационное число серебра в устойчивых комплексах, как правило, равно 4. Описаны комплексы, в которых количество связей Ag–Sb изменяется от одной до четырех [13 - 16]. Сурьмасодержащими лигандами при этом являются, как правило, трифенилстибин, реже - три( пара -толил)стибин. Исключением составляют комплексы с гетероароматическими, например 2-C4H3X, где X = S, O, N - Me [17], или замещенными арильными группами 2-MeO-5-BrC 6 H 3 [18 - 20].
Из литературных данных следует, что соединения со связями Ag–Sb синтезируют из солей серебра (AgNO 3 , AgHal) и триарилстибина в разнообразных растворителях при варьировании мольных соотношений реагентов, что обусловливает образование комплексов определенной стехиометрии. Комплексы, в которых нитрогруппа замещена на карбоксильную группу, ограничиваются несколькими примерами [12, 20, 21].
Настоящая работа является продолжением исследований особенностей синтеза и установления строения комплексов со связями Ag–Sb.
Экспериментальная часть
[( p -Tol 3 Sb) 4 Ag]+[NO 3 ] – ( 1 ). Растворяли 0,791 г (2,0 ммоль) три( пара -толил)сурьмы в 7 мл смеси CH 3 OH и CH 3 CN (соотношение 1 : 1 объем.) и 0,085 г (0,5 ммоль) нитрата серебра в 3 мл той же смеси растворителей в отдельных стаканчиках. Затем растворы сливали и перемешивали до исчезновения осадка. Оставляли на сутки в темном месте. Получили 0,771 г (88 %) кристаллов 1 серебристого цвета. Т. пл. 174 °С.
ИК-спектр (ῡ, см–1): 3061, 3037, 3022, 3008, 2949, 2918, 2862, 1905, 1805, 1743, 1651, 1591, 1490, 1442, 1390, 1340, 1309, 1280, 1211, 1186, 1114, 1062, 1037, 1014, 854, 844, 831, 794, 702, 634, 574, 484, 480, 432.
(Ph 3 Sb) 3 AgNO 3 ( 2 ). Растворяли 0,530 г (1,5 ммоль) трифенилсурьмы в 7 мл смеси CH 3 OH и CH 3 CN (соотношение 1 : 1 объем.) и 0,085 г (0,5 ммоль) нитрата серебра в 3 мл той же смеси растворителей в отдельных стаканчиках. Затем растворы сливали и перемешивали до исчезновения осадка. Оставляли на сутки в темном месте. Получили 0,502 г (82 %) кристаллов 2 белого цвета. Т.пл. 216 °С. (212 °С [12]).
ИК-спектр (ῡ, см–1): 3064, 3043, 3020, 2991, 2951, 1961, 1880, 1815, 1593, 1575, 1477, 1431, 1406, 1384, 1332, 1300, 1265, 1180, 1157, 1066, 1035, 1020, 997, 916, 856, 848, 821, 742, 731, 694, 657, 615, 453, 447.
(Ph 3 Sb) 3 AgOC(O)C 6 H 4 OMe-2 ⋅ (Ph 3 Sb) 3 AgNO 3 ⋅ 2СН 3 ОН ( 3 ). Растворяли 0,100 г (0,08 ммоль) нитрато трис (трифенилстибин)серебра(I) в 3 мл смеси CH 3 OH и CH 3 CN (соотношение 1 : 1 объем.) и 0,014 г (0,08 ммоль) 2-метоксибензойной кислоты в 3 мл той же смеси растворителей. Затем растворы сливали и перемешивали до исчезновения осадка. После добавляли 0,5 мл (3,5 ммоль) триэтиламина. Оставляли на сутки в темном месте. Получили 0,089 г (84 %) кристаллов 3 белого цвета. Т. пл. 177 °С.
ИК-спектр (ῡ, см–1): 3062, 3043, 2964, 2885, 2833, 1963, 1884, 1816, 1598, 1575, 1554, 1477, 1431, 1384, 1330, 1302, 1246, 1236, 1180, 1157, 1091, 1066, 1049, 1020, 997, 918, 881, 844, 785, 731, 694, 657, 615, 451.
ИК-спектры соединений 1 - 3 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1-3 проведен на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [22]. Все расчеты по определению и уточнению структур выполнены по программам SHELXL/PC [23] и OLEX2 [24]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника (Uизо(H) = 1,2Uэкв(C)). Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 1991188 (1), № 1974755 (2), № 2082739 (3); ; . Основные кристаллографические данные и результаты уточнения структур 1-3 приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 - 3
|
Параметр |
1 |
2 |
3 |
|
Стехиометрическая формула |
C 84 H 84 AgNO 3 Sb 4 |
C 54 H 45 AgNO 3 Sb 3 |
C118H105Ag2NO8Sb6 |
|
М |
1750,39 |
1229,03 |
2611,26 |
|
Сингония |
Моноклинная |
Моноклинная |
Триклинная |
|
Пространственная группа |
С 2/ с |
Р 2 1 / n |
Р - 1 |
|
a , Å |
13,836(7) |
17,893(15) |
13,530(7) |
|
b , Å |
28,797(15) |
14,493(8) |
14,193(6) |
|
c , Å |
19,597(10) |
19,646911) |
14,830(10) |
|
α , град. |
90,00 |
90,00 |
82,73(2) |
|
β, град. |
95,60(3) |
96,94(3) |
86,74(3) |
|
γ , град. |
90,00 |
90,00 |
76,182(17) |
|
V , Å3 |
7771(7) |
5057(6) |
2742(3) |
|
Z |
4 |
4 |
1 |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
|
ρ выч, г/см |
1,496 |
1,614 |
1,581 |
|
µ , мм–1 |
1,666 |
2,008 |
1,858 |
|
F (000) |
3480,0 |
2400,0 |
1284,0 |
|
Размер кристалла, мм |
0,36 × 0,16 × 0,1 |
0,32 × 0,14 × 0,1 |
0,28 × 0,15 × 0,1 |
|
Диапазон сбора данных по 2 θ , град. |
5,54 - 48,22 |
5,738 - 48,878 |
5,976 - 50,332 |
|
Диапазон индексов |
- 15 ≤ h ≤ 15 - 32 ≤ k ≤ 33 - 22 ≤ l ≤ 22 |
- 20 ≤ h ≤ 20 - 16 ≤ k ≤ 16 - 22 ≤ l ≤ 22 |
- 16 ≤ h ≤ 16 - 16 ≤ k ≤ 16 - 17 ≤ l ≤ 17 |
|
Число измеренных рефлексов |
80923 |
51463 |
54195 |
|
Чисто независимых рефлексов |
6159 |
8303 |
9673 |
|
R int |
0,0366 |
0,0717 |
0,0456 |
|
GOOF |
1,053 |
1,026 |
1,022 |
|
Число параметров |
427 |
570 |
733 |
|
R -факторы по I > 2 σ ( I ) |
R 1 = 0,0215 wR 2 = 0,0491 |
R 1 = 0,0323 wR 2 = 0,0732 |
R 1 = 0,0400, wR 2 = 0,0862 |
|
R -факторы по всем рефлексам |
R 1 = 0,0290, wR 2 = 0,0526 |
R 1 = 0,0547, wR 2 = 0,0857 |
R 1 = 0,0640, wR 2 = 0,0987 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,39/ - 0,41 |
0,90/ - 0,72 |
0,75/ - 1,24 |
Таблица 2
|
Связь \ |
d , Å 1 |
Угол 1 |
ω, град. |
|
1 |
|||
|
Ag(1)–Sb(1) |
2,7521(11) |
Sb(1)Ag(1)Sb(2) |
108,90(3) |
|
Ag(1)–Sb(2) |
2,7412(11) |
Sb(1)1Ag(1)Sb(1) |
102,57(4) |
|
Sb(1)–C(1) |
2,138(3) |
Sb(1)1Ag(1)Sb(2) |
116,07(3) |
|
Sb(1)–C(11) |
2,139(3) |
C(1)Sb(1)Ag(1) |
113,37(7) |
|
Sb(1)–C(21) |
2,128(3) |
C(11)Sb(1)Ag(1) |
123,18(8) |
|
Sb(2)–C(31) |
2,145(3) |
C(21)Sb(1)Ag(1) |
118,57(8) |
|
Sb(2)–C(41) |
2,139(3) |
C(1)Sb(1)C(11) |
98,00(11) |
|
Sb(2)–C(51) |
2,130(3) |
C(1)Sb(1)C(21) |
99,39(11) |
|
O(1)‒N(1) |
1,164(4) |
C(11)Sb(1)C(21) |
100,05(11) |
|
O(2)‒N(1) |
1,148(6) |
O(2)N(1)O(1) |
124,8(4) |
|
11 - X, +Y, 1/2 - Z; 2 - X, +Y, 1/2 - Z |
|||
|
2 |
|||
|
Ag(1)–Sb(1) |
2,7601(15) |
Sb(1)Ag(1)Sb(2) |
110,75(3) |
|
Ag(1)–Sb(2) |
2,7078(15) |
Sb(1)Ag(1)Sb(3) |
114,16(5) |
|
Ag(1)–Sb(3) |
2,7280(14) |
Sb(2)Ag(1)Sb(3) |
113,96(2) |
|
Sb(1)–C(1) |
2,133(5) |
C(1)Sb(1)Ag(1) |
113,84(14) |
|
Sb(1)–C(11) |
2,139(5) |
C(11)Sb(1)Ag(1) |
119,06(16) |
|
Sb(1)–C(21) |
2,147(5) |
C(21)Sb(1)Ag(1) |
123,39(13) |
|
Sb(2)–C(31) |
2,132(6) |
C(1)Sb(1)C(11) |
99,5(2) |
|
Sb(2)–C(41) |
2,138(5) |
C(1)Sb(1)C(21) |
100,5(2) |
|
Sb(2)–C(51) |
2,131(5) |
C(11)Sb(1)C(21) |
96,3(2) |
|
Sb(3)–C(61) |
2,127(5) |
C(31)Sb(2)Ag(1) |
108,39(16) |
|
Sb(3)–C(71) |
2,139(6) |
C(41)Sb(2)Ag(1) |
122,22(13) |
|
Sb(3)–C(81) |
2,135(5) |
C(51)Sb(2)Ag(1) |
119,54(14) |
|
O(1)‒N(1) |
1,227(13) |
О(1)Ag(1)Sb(1) |
116,7(3) |
|
O(2)‒N(1) |
1,136(15) |
О(1)Ag(1)Sb(2) |
106,4(3) |
|
O(3)‒N(1) |
1,192(6) |
О(1)Ag(1)Sb(3) |
93,8(4) |
|
Ag(1)–О(1) |
2,306(13) |
O(1)N(1)O(2) |
116,0(11) |
|
Ag(1)–О(2) |
2,848(15) |
O(1)N(1)O(2) |
123,5(8) |
Окончание табл. 2
|
Связь |
d , Å |
Угол |
ω, град. |
|
3 |
|||
|
Ag(1)–Sb(1) |
2,7459(17) |
Sb(1)Ag(1)Sb(2) |
115,79(4) |
|
Ag(1)–Sb(2) |
2,7234(12) |
Sb(1)Ag(1)Sb(3) |
110,55(3) |
|
Ag(1)–Sb(3) |
2,7087(13) |
Sb(2)Ag(1)Sb(3) |
111,31(4) |
|
Sb(1)–C(1) |
2,133(8) |
C(1)Sb(1)Ag(1) |
119,1(2) |
|
Sb(1)–C(11) |
2,156(6) |
C(11)Sb(1)Ag(1) |
120,05(18) |
|
Sb(1)–C(21) |
2,138(7) |
C(21)Sb(1)Ag(1) |
116,00(17) |
|
Sb(2)–C(31) |
2,146(6) |
C(1)Sb(1)C(11) |
99,7(3) |
|
Sb(2)–C(41) |
2,142(7) |
C(1)Sb(1)C(21) |
99,6(3) |
|
Sb(2)–C(51) |
2,129(6) |
C(11)Sb(1)C(21) |
98,4(3) |
|
Sb(3)–C(61) |
2,124(6) |
C(31)Sb(2)Ag(1) |
115,33(16) |
|
Sb(3)–C(71) |
2,139(6) |
C(41)Sb(2)Ag(1) |
119,48(16) |
|
Sb(3)–C(81) |
2,132(6) |
C(51)Sb(2)Ag(1) |
119,90(19) |
|
Ag(1)–О(1) |
2,352(18) |
О(1)Ag(1)Sb(1) |
92,8,7(6) |
|
Ag(1)–О(4) |
2,263(14) |
О(1)Ag(1)Sb(2) |
104,4(6) |
|
O(1)‒С(97) |
1,06(3) |
О(1)Ag(1)Sb(3) |
121,1(5) |
|
O(2)‒С(97) |
1,09(2) |
О(4)Ag(1)Sb(1) |
111,7(5) |
|
O(4)‒N(1) |
1,175(16) |
О(4)Ag(1)Sb(2) |
102,3(7) |
|
O(5)‒N(1) |
1,184(14) |
О(4)Ag(1)Sb(3) |
104,3(5) |
|
O(6)‒N(1) |
1,210(16) |
O(4)N(1)O(6) |
104(2) |
|
O(4)N(1)O(5) |
124,0(18) |
||
Обсуждение результатов
Из литературных данных следует, что для получения комплексов присоединения со связями Ag–Sb определенной стехиометрии используют соли серебра и триарилстибины при варьировании мольных соотношений реагентов.
Однако мы установили, что при взаимодействии три( пара -толил)сурьмы с нитратом серебра в мольном соотношении 3:1 в смеси метанол–ацетонитрил (1:1 объемн.) вместо комплекса ожидаемой стехиометрии ( p -Tol 3 Sb) 3 AgNO 3 образуется нитрат тетракис ( пара -толилстибин)серебра [( p -Tol 3 Sb) 4 Ag][NO 3 ] ( 1 ) с температурой плавления 174 ° С [20], который выделен также при проведении реакции в соотношении реагентов 4:1, при этом выход продукта увеличивается с 66 % до 88 %.
4 p -Tol 3 Sb + AgNO 3 ^ [(p -Tol 3 Sb) 4 Ag][NO 3 ]
1
Напротив, трифенилсурьма и нитрат серебра реагируют в той же смеси растворителей в любом из мольных соотношений (2:1, 3:1 или 4:1) с образованием только комплекса (Ph 3 Sb) 3 AgNO 3 ( 2 ) с максимальным выходом (82 %) при соотношении 3:1.
3 Ph 3 Sb + AgNO 3 ^ (Ph 3 Sb) 3 AgNO 3
2
Температура плавления полученного нами соединения 2 составила 216 °С и отличается от значения 212 °С, приведенного в работе [12], незначительно.
Одним из возможных путей синтеза новых комплексов со связями Sb–Ag являются реакции замещения лигандов. Как следует из работы [12], в комплексе (Ph 3 Sb) 3 AgNO 3 возможно замещение лиганда NO 3 ‒ на остатки карбоновых кислот. Нами ранее такие реакции также были успешно осуществлены [20]. Реакции с кислотами проводят в смеси растворителей CH3OH / CH3CN в присутствии избытка триэтиламина (CH3CH2)3N, который связывает свободную азотную кислоту в нитрат триэтиламмония.
Однако в результате реакции нитрато трис (трифенилстибин)серебра с 2-метоксибензойной кислотой (1:1 мольн.) был выделен аддукт (Ph3Sb)3AgOC(O)C6H 4 OMe-2 - (Ph3Sb)3AgNO3 - 2CH3OH ( 3 )
в в и д е н е ок раш е н н ых кр и с та ллов с те мп е р а ту рой п ла в ле н и я 177 ° С, выход которого составил 84 %.
CH 3 CN/CH 3 OH
(Ph 3 Sb) 3 AgNO 3 + HOC(O)C 6 H 4 O Me-2
----------— (Ph з Sb) з AgOC(O)C 6 H 4 OMe-2 • (Ph з Sb) з AgNO з • 2СН з ОН
3
Для и д е н тифи к а ц и и п роду к тов реакций были выбраны методы ИК-спектроскопии и РСА.
В ИК- сп е к тре сое д и н е н ия 1 присутствуют полосы поглощения, характеризующие колебания нитрат-аниона при 1391 и 1341 см -1 (сильные) и в области 860 - 800 см -1 (слабые) [25]. Полоса поглощения связей Sb–С р а с п олож е н а п ри 480 с м–1 и перекрывается с сильной полосой (484 см–1), о т н ес е н н ой к к ол е ба н и я м а ромат и чес кого к о ль ца.
В ИК-спектре комплекса 2 полосы поглощения асимметричных и симметричных колебаний нитратных г руп п н а б л ю даю тс я п ри 1406 и 1385 см–1 соответственно. Полоса валентных колебаний связей Sb–С (447 см–1 ) п е рек рыв ае тс я с с ильной п олос ой ( 453 с м–1), относящейся к поглощению фенильных фрагментов , что с о гла с у е тс я с И К-спектром, приведенном в работе [12] (1406, 1384 и 450 см–1соответс тве н н о) .
ИК-спектр аддукта 3 наря ду с полосами поглощения, характерными для комплекса (Ph 3 Sb) 3 AgNO 3 (1385, 1331 см– 1 ) содержит полосы колебаний при 1555 и 1302 см–1, относящиеся к ас и мм етричн ы м и с и м метри чн ым к ол е ба н и ям гру п п ы С ОО - в карбоксилат-анионе фрагмента (Ph 3 Sb) 3 AgOC(O)C 6 H 4 OMe-2.
Строение комплексов 1 и 2 ранее описано в [20] и [12] соответственно, в настоящей работе р е н тге н ос т ру к турн ый эк с п е ри ме н т в ып о лн е н с лу чш и ми R -факторами. По данным р е н тге н ос т ру к турн ого ан а ли за , атом се р е б р а в симметричном катионе комплекса 1 имеет тетра э д ри че ск у ю к оорд ин а ц и ю с ок ру же н и е м [AgSb4], как и атомы сурьмы с окружением [SbС 3 Ag] (рис. 1). Ва л е нтн ые у глы п ри а томе с ере б ра SbAgSb незначительно отличаются от теоретического значе н и я и с ос та в ляю т 102, 5 7( 4 )–116,07(3)°. Длины связей Ag–Sb(1) и Ag–Sb(2) равны 2,7522(11) и 2,7412(11 ) Å. Валентные углы СSb(1)С и СSb(2)С изменяются в интервалах 98,00(11)–100,05(11)° и 97, 34(12)–101,71(11)°, углы СSb(1)Ag и СSb(2)Ag имеют большие значения (113,37(7)–123,18(8 )° и 115,99(8)–120,46(8)° соответственно). Расстояния Sb(1)–C составляют 2,128(3)-2,139(3) A, S b (2)-C - 2,130(3)-2,145(3) А.
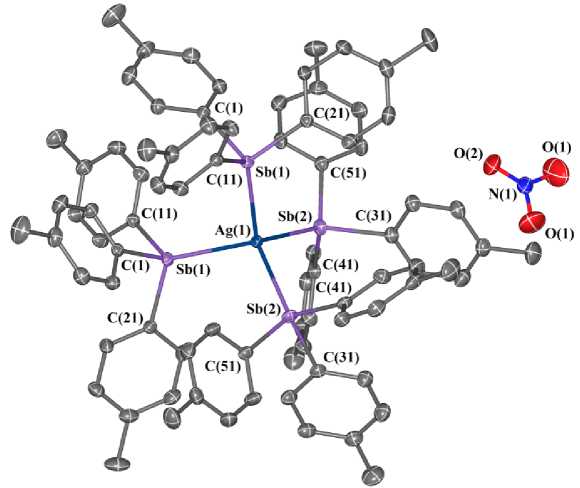
Рис. 1. Строение комплекса [( p -Tol 3 Sb) 4 Ag]+[NO 3 ]– (1) (атомы водорода не приведены)
Нитрат-анион плоский, ось симметрии С 2 совпадает со связью O(2) - N, углы ONO отличаются от теоретического значения 120°: один из углов составляет только 110,4(7)°, при том что два других равны по 124,8(4)°. Одна из связей O(2)–N (1,148(6) Å) короче двух других одинаковых связей O(1)–N (1,164(4) Å).
Анион определяет структурную организацию кристалла через систему водородных связей с катионами (рис. 2). Каждый анион окружен тремя катионами, при этом атомы кислорода образуют по две водородные связи N - O—Н - С с двумя катионами (О(2) --- Н 2,61 и 2,61 А, О(1) --- Н 2,47 и 2,51 Å).
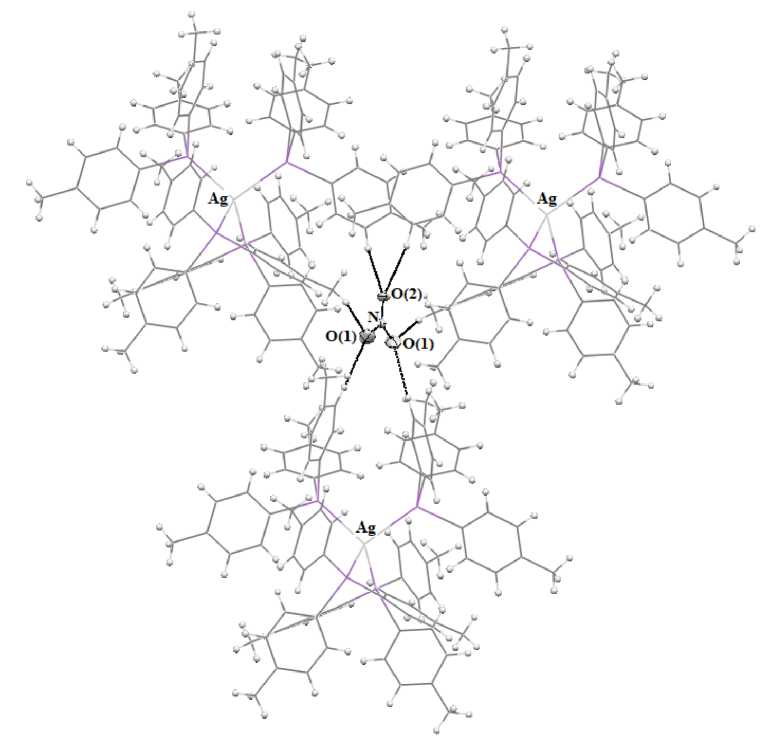
Рис. 2. Система водородных связей в кристалле 1
Согласно данным рентгеноструктурного анализа, в комплексе 2 атом серебра имеет искаженную тетраэдрическую координацию (рис. 3). Валентные углы при атоме серебра варьируются от 93,8(4)° до 116,7(3)°. При этом углы Sb(2)AgSb(1), Sb(3)AgSb(1), Sb(3)AgSb(2) составляют 110,75(3), 114,16(5), 113,96(2)°; углы O(1)AgSb(1), O(1)AgSb(2) и O(1)AgSb(3) равны 116,7(3)°, 106,4(3)° и 93,8(4)° соответственно. Длины связей Ag–Sb имеют значения 2,7078(15), 2,7280(14) и 2,7601(15) Å. Среднее значение связей Ag–Sb (2,732 Å) в 2 немного меньше аналогичного значения в 1 (2,747 Å). Расстояние Ag–O составляет 2,306(13) Å.
Валентные углы CSb(1)C, CSb(2)C и CSb(3)C составляют 96,3(2) - 100,5(2) ° , 99,0(2) - 102,1(1) ° , 99,3(2) °- 102,7(2) ° , углы CSb(1)Ag, CSb(2)Ag и CSb(3)Ag - 113,84(14) °- 123,39(13) ° , 108,39(16) - 122,22(13) ° , 111,31(13) - 124,64(16) ° соответственно. Расстояния Sb(1)-C, Sb(2)-C и Sb(3)–C изменяются в диапазонах 2,133(5)–2,147(5) Å, 2,131(5)–2,138(5) Å, 2,127(5)–2,139(5) Å. Для сравнения, среднее значение длин связей Sb–C в свободной молекуле трифенилстибина равно 2,15 Å, т. е. несколько превышает среднее значение аналогичных связей в комплексе. Длины связей N–O в нитратной группе равны 1,136(15), 1,192(6) и 1,227(13) Å.
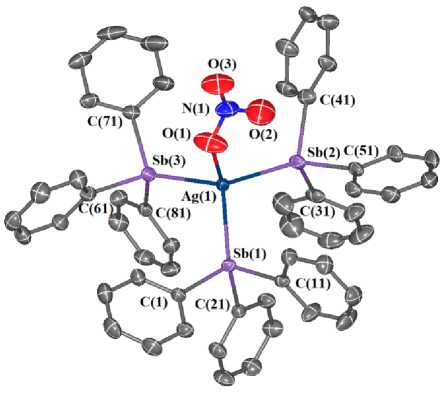
Рис. 3. Строение комплекса (Ph 3 Sb) 3 AgNO 3 (2) (атомы водорода не приведены)
В кристалле 3 присутствуют два одинаковых фрагмента (Ph 3 Sb) 3 Ag, к которым координируют н и тра тн а я и к а рб о к с ила тн а я группы с заселенностью 50% (рис. 3). На к ажд ый фра гм е н т п р их од и тс я п о од н ой р а зу п оря доченной молекуле сольватного метанола. Геоме три че с к и е п ара ме тр ы фрагментов (Ph3Sb)3Ag м ало отличаются от аналогичных в соедин е н и и 2 . Так, углы Sb(2)AgSb(1), Sb(3)AgS b(1) , Sb(3)AgSb(2) равны 115,79(4) ° , 110,55(3) ° , 111,31(4) ° ; углы O(1)AgSb(1), O(1)AgSb(2) и O (1) Ag Sb(3), где О(1) принадлежит карбоксилатной группе, составляют 92,8,7(6) ° , 104,4(6) ° и 1 21, 1( 5) ° , а углы O(4)AgSb(1), O(4)AgSb(2) и O(4)AgSb(3) (О(4) - отн осится к ни трат н ой гру п п е ) - 111,7(5) ° , 102,3(7) ° и 104,3(5) ° . Расстояния Ag-O(1) и Ag-O(4) равны 2,352(18) и 2,263(14) Å. Отметим, что в синтезированных и структурно охарактеризованных ранее комплексах [(Ph 3 S b) 3 AgOC(O)CH 2 Cl] и [(Ph 3 Sb) 3 AgOC(O)C 5 H 4 FeC 5 H 5 ] расстояния Ag– О короче (2,307(4) и 2,308(4) Å соответственно) [20].
Углы CSb(1)C, CSb(2 ) C и CSb(3)C изменяются в диапазонах 99,6(3) - 98,4(3) ° , 98,9(2) - 100,2(3) ° и 99,4(2) - 1 01, 6(2) ° ; CSb(1)Ag, CSb(2)Ag и CSb(3)Ag - 116,00(17) - 120,05(18) ° , 115,33(16) - 119,90(19) ° и 110, 83(15) - 122,76(16) ° соответственно. Длины связей Sb(1)-C, Sb(2)-C и Sb(3)–C варьи ру ю т в и н те рв а лах 2,133(8)–2,156(6) Å, 2,129(6)–2,146(6) Å, 2,124(6)–2,139(6) Å.
В н и тра тн ой гру п п е с в язи N–O равны 1,175(16); 1,184(14) и 1,210(16) Å.
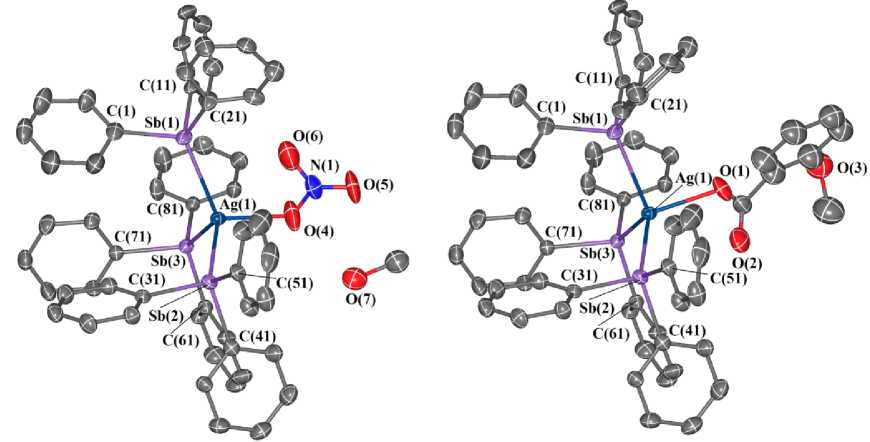
Рис. 4. Строение аддукта (Ph 3 Sb) 3 AgOC(O)C 6 H 4 OMe-2 · (Ph 3 Sb) 3 AgNO 3 · 2СН 3 ОН (3)
Выводы
Установлено, что стехиометрия комплексов присоединения, получаемых из три( пара -толил)- или трифенилсурьмы и нитрата серебра в смеси метанол/ацетонитрил, не определяется соотношением исходных реагентов и как при соотношении 3:1 (мольн.), так и 4:1 (мольн.) приводит к комплексам [( p -Tol 3 Sb) 4 Ag][NO 3 ] или (Ph 3 Sb) 3 AgNO 3 соответственно. Замещение нитратной группы в нитрато трис (трифенилстибин)серебре на карбоксилатную при действии 2-метоксибензойной кислоты в смеси метанол/ацетонитрил при комнатной температуре за сутки не достигает полноты, из раствора кристаллизуется аддукт состава (Ph 3 Sb) 3 AgOC(O)C 6 H 4 OMe-2 ⋅ (Ph 3 Sb) 3 AgNO 3 ⋅ 2СН 3 ОН.


