Биодеградация биологических протезов аортального клапана: клинические предикторы и анализ выживаемости на основе машинного обучения и метода Propensity Score Matching
Автор: Майстренко А.Д., Курашенко В.В., Успенский В.Е., Гурщенков А.В., Крылова Ю.С., Генералов М.В., Гордеев М.Л.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.21, 2026 года.
Бесплатный доступ
Обоснование. Биологические протезы аортального клапана широко применяются в кардиохирургии благодаря снижению риска тромбоэмболий и отсутствию необходимости пожизненной антикоагулянтной терапии. Однако их долговечность ограничена риском структурной деградации, что остаётся нерешённой клинической проблемой. Недостаточно изучены факторы, определяющие сроки и вероятность деградации, особенно при использовании методов многофакторного анализа и машинного обучения. Цель. Определить частоту и сроки биодеградации биопротезов аортального клапана и выявить клинические и ЭхоКГ предикторы её развития с использованием статистического моделирования, машинного обучения и Propensity Score Matching. Методы. Проведено ретроспективное когортное исследование, включившее 259 пациентов, перенесших протезирование аортального клапана биопротезом в 2012–2022 гг. Критериями деградации служили: морфологические изменения створок (фиброз, кальциноз), нарастание трансвальвулярного градиента (максимального > 40 мм рт. ст. или среднего > 30 мм рт. ст.), аортальная регургитация ≥ 2 степени, повторная операция или смерть, связанная с дисфункцией протеза. Первичной конечной точкой было время до развития деградации. Использованы логистическая регрессия, алгоритм случайного леса (Random Forest), анализ Kaplan–Meier и PSM. Результаты. За медианный срок наблюдения 48 месяцев признаки деградации выявлены у 62 (23,9%) пациентов. Логистический анализ выявил значимые ассоциации с индексом массы тела (p < 0,001), сниженной фракцией выброса (p < 0,001), ишемической болезнью сердца (p = 0,010), хронической сердечной недостаточностью III ФК и выше (p = 0,020) и уровнем креатинина (p = 0,048). Модель Random Forest показала AUC = 0,72, наибольшую значимость имели фракция выброса, индекс массы тела, уровень креатинина и возраст. PSM-анализ подтвердил достоверное сокращение срока функционирования протезов в группе с деградацией (38 против 48 месяцев; log-rank p = 0,010). Заключение. Структурная деградация биопротезов аортального клапана развивается у четверти пациентов в течение первых пяти лет после операции. Применение многоуровневого анализа, включающего машинное обучение и PSM, позволяет точнее идентифицировать пациентов группы риска и способствует персонализации клинического наблюдения и выбора тактики хирургического лечения.
Биопротез аортального клапана, структурная деградация, машинное обучение
Короткий адрес: https://sciup.org/140314174
IDR: 140314174 | DOI: 10.25881/20728255_2026_21_1_9
Biodegradation of Bioprosthetic Aortic Valves: Clinical Predictors and Survival Analysis Using Machine Learning and Propensity Score Matching
Background. Bioprosthetic aortic valves (AV) are widely used in cardiac surgery due to the absence of lifelong anticoagulation requirements and a lower risk of thromboembolic complications. However, their durability is limited by structural valve deterioration (SVD), which may lead to prosthetic dysfunction, reoperations, and increased mortality. Despite numerous reports, the predictors of accelerated valve degeneration remain insufficiently understood, particularly in the context of multifactorial analysis and machine learning applications. Aims. To determine the frequency and timing of bioprosthetic AV degeneration and to identify clinical and echocardiographic predictors of structural deterioration using statistical modeling, machine learning, and propensity score matching (PSM). Materials and methods. A retrospective cohort study included 259 patients who underwent surgical aortic valve replacement with a bioprosthesis between 2012 and 2022. Criteria for SVD were morphological leaflet changes (fibrosis, calcification), increased transvalvular gradients (peak > 40 mmHg or mean > 30 mmHg), aortic regurgitation ≥ grade 2, reoperation, or death due to prosthetic dysfunction. The primary endpoint was time to valve degeneration. Statistical methods included logistic regression, random forest modeling, Kaplan–Meier survival analysis, and PSM. Results. Structural valve deterioration was detected in 62 patients (23.9%) during a median follow-up of 48 months. Logistic regression demonstrated significant associations with body mass index (OR 3.39; 95% CI: 2.54–4.53; p < 0.001), reduced left ventricular ejection fraction (p < 0.001), coronary artery disease (p = 0.010), chronic heart failure class III or higher (p = 0.020), and serum creatinine (p = 0.048). The random forest model achieved an AUC of 0.72, with the most relevant predictors being ejection fraction, body mass index, creatinine, and age. PSM analysis confirmed significantly shorter prosthesis durability in the SVD group compared with matched controls (median 38 vs. 48 months; log-rank p = 0.010). Conclusions. Bioprosthetic AV deterioration occurs in nearly one-quarter of patients within 4–5 years after surgery. A multilevel approach using machine learning and PSM improves risk stratification and may support personalized follow-up and surgical decision-making.
Текст научной статьи Биодеградация биологических протезов аортального клапана: клинические предикторы и анализ выживаемости на основе машинного обучения и метода Propensity Score Matching
2021 г. выполнено 7911 вмешательств по причине дегенеративных изменений клапанов сердца. При этом доля изолированных протезирований аортального клапана (АК) составила 48,8% (3911 операций).

У 29,1% пациентов данной категории было выполнено биопротезирование АК [1].
Несмотря на ряд преимуществ биопротезов сердца (в первую очередь – отсутствие необходимости постоянной антигокоагулянтной терапии) основной проблемой их использования является ограниченный срок службы в связи с естественной деградацией. По данным Johnston D.R. и соавт. (2015), при анализе более 12 тыс. случаев операций биопротезирования АК необходимость реопераций у пациентов младше 60 лет составляла 45% через 20 лет после операции [2].
Однако, по другим данным, отсутствие структурных изменений створок биологических протезов АК через 10 лет после операции наблюдалось у 44,2–50% пациентов [3; 4].
Основными причинами склеродегенеративных процессов биопротезов с последующей дисфункцией являются:
-
1. Механический износ створок протеза – ткани ксеноперикарда (бычьего или свиного) более плотные и жесткие чем створки АК. Постоянная гемодинамическая нагрузка на них приводит к их естественному старению и износу.
-
2. Кальциноз створок биологического протеза – основной причиной является хроническое воспаление в зоне операции в связи с аутоиммунным ответом на инородный материал в организме.
-
3. Инфекционный эндокардит – все пациенты после протезирования клапанов сердца включаются в группу высокого риска данного осложнения. В связи с чем всем пациентам рекомендована строгая антибиоти-копрофилактика при инвазивных стоматологических манипуляциях, операциях и тд.
Основным методом оценки функционального состояния биологических протезов сердца является ЭхоКГ. Она позволяет оценить скоростные показатели на клапанах (в случае формирования стеноза вследствие биодеградации увеличивается скорость кровотока на клапане), косвенно определить структурную детериорацию (утолщение створок, уплотнение их), грубые морфологические изменения (отрыв биопротеза, отрыв створки). При УЗИ клапана сердца невозможно определить активность дегенеративных процессов у конкретного пациента. Описанные изменения характерны уже для поздней стадии структурных изменений биопротеза сердца, когда зачастую формируется дисфункция биологического клапана [5].
Структурную деградацию биологического протеза можно заподозрить при следующих показателях ЭхоКГ:
-
1) Снижение или повышение подвижности створок;
-
2) Истончение створок;
-
3) Систолическое ускорение кровотока по данным допплерографии;
-
4) Средний градиент на биопротезе АК более 20 мм рт. ст.;
-
5) Увеличение среднего градиента на 10 мм рт. ст. и более в течение срока наблюдения;
-
6) EOA < 1,1 см2;
-
7) DVI <0,35;
-
8) AT/LVET >0,32;
-
9) Внезапное появление симптомов сердечной недостаточности;
-
10) Появление аортальной недостаточности 1-й и более степени.
При сопоставлении клинических проявлений и данных ЭхоКГ можно определить степень биодеградации биологического протеза:
-
1 стадия – морфологические признаки структурной детериорации протеза без глобального нарушения функции биопротеза.
-
2 стадия – появление гемодинамических нарушений на биопротезе (увеличение среднего градиента более 20 мм рт. ст., уменьшение площади открытия более чем на 0,3 см 2 , уменьшение DVI более чем на 0,1 или появление аортальной недостаточности 1-й и более степени).
-
3 стадия – выраженные гемодинамические нарушения на биопротезе (увеличение среднего градиента более 30 мм рт. ст., уменьшение площади открытия более чем на 0,6 см2, уменьшение DVI более чем на 0,2 или появление аортальной недостаточности 2-й и более степени).
-
4 стадия – дисфункция биологического протеза (морфологические и гемодинамические нарушения на биопротезе в совокупности с клиникой хронической сердечной недостаточности, дилатацией или гипертрофией левого желудочка, легочной гипертензией).
Рутинные методы диагностики, такие как ЭхоКГ и компьютерная ангиография, позволяют регистрировать изменения в биопротезах клапанов сердца только на 2–3 стадии, когда формирующиеся изменения становятся практически необратимыми. Это ограничивает возможность своевременной диагностики и вмешательства, что обуславливает необходимость разработки методов раннего выявления структурных изменений в биопротезах.
При этом остаются не до конца изученными факторы, способствующие ускоренной биодеградации, особенно в отдалённом периоде.
В последние годы методы машинного обучения и балансировка групп методом Propensity Score Matching (PSM) применяются в клинической аналитике, позволяя выявлять скрытые закономерности и минимизировать влияние систематической ошибки при анализе ретроспективных данных.
Целью настоящего исследования является определение частоты и сроков биодеградации биологических протезов АК, а также выявление клинических и инструментальных факторов, ассоциированных с риском её развития, с использованием современных статистических и вычислительных методов.
Цель
Определить частоту и сроки развития биодеградации биологических протезов АК, а также выявить клинические и ЭхоКГ предикторы её возникновения с примене-

Майстренко А.Д., Курашенко В.В., Успенский В.Е. и др.
БИОДЕГРАДАЦИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ АОРТАЛЬНОГО КЛАПАНА: КЛИНИЧЕСКИЕ ПРЕДИКТОРЫ И АНАЛИЗ ВЫЖИВАЕМОСТИ НА ОСНОВЕ МАШИННОГО ОБУЧЕНИЯ И МЕТОДА PROPENSITY SCORE MATCHING нием современных статистических методов, машинного обучения и Propensity Score Matching.
Методы
Дизайн исследования
Проведено ретроспективное исследование. Анализу подверглись медицинские карты пациентов, перенёсших хирургическое протезирование АК биологическим протезом с 2012 по 2022 гг. в условиях кардиохирургического стационара. Все пациенты дали информированное согласие на обработку данных.
Критерии включения:
-
• Возраст старше 18 лет;
-
• Изолированное или комбинированное хирургическое протезирование аортального клапана (сочетание с АКШ, пластикой митрального, трикуспидального клапанов, РЧА) с использованием биологического протеза;
-
• Наличие данных об эхокардиографии в отдалённом периоде (не менее 6 месяцев после операции).
Критерии исключения:
-
• Инфекционный эндокардит в активной фазе на момент осмотра;
-
• Нарушения свертывающей системы, требующие постоянного приёма варфарина;
-
• Наличие механического протеза.
-
• Наличие биологического протеза митрального или трикуспидального клапана.
-
• Исключение пациентов с пациент-протезным несоответствием.
Для последующего анализа все пациенты, включённые в исследование, были разделены на две группы в зависимости от наличия признаков биодеградации аортального биологического протеза в отдалённом послеоперационном периоде.
Критерии отнесения к группе с биодеградацией
Пациенты были классифицированы как имеющие признаки биодеградации биологического протеза при наличии хотя бы одного из следующих критериев:
-
1. Морфологические изменения , зафиксированные при ЭхоКГ контроле в отдаленном периоде: фиброз створок биопротеза; кальциноз биологического материала клапана.
-
2. Гемодинамическая дисфункция протеза, определяемая по данным ЭхоКГ:
-
3. Клинические исходы , связанные с нарушением функции протеза: выполненная повторная операция по поводу дисфункции биопротеза; смерть пациента вследствие сердечной недостаточности обусловленной дисфункцией биопротеза.
Нарастание максимальный градиент давления на АК более 40 мм рт. ст. или среднего градиента давления более 30 мм рт. ст. в сравнении с параметрами послеоперационной ЭхоКГ при выписке. При этом исключен вариант пациент-протезного несоответствия.
Наличие любого из указанных признаков рассматривалось как достоверное свидетельство биодеградации протеза, и пациент включался в соответствующую группу.
Контрольная группа
Контрольная группа включала пациентов, у которых ни один из вышеописанных критериев не был выявлен в период наблюдения. Эти пациенты рассматривались как перенесшие имплантацию биопротеза без признаков деградации на момент последнего осмотра.
Общее распределение по группам
Из общего числа включённых пациентов (n = 259) были выделены:
-
• Группа с биодеградацией биопротеза – n = 62 человек,
-
• Группа без признаков биодеградации – n = 197 человек.
Такое распределение позволило провести сравнительный статистический анализ между двумя когортами пациентов для выявления факторов риска деградации биопротеза и оценки выживаемости.
Статистический анализ
Описательные характеристики количественных переменных представлены в виде медианы с межквартильным размахом [Q1; Q3] либо как среднее значение ± стандартное отклонение, в зависимости от типа распределения. Для категориальных переменных использовались абсолютные и относительные (%) частоты.
Сравнение групп пациентов с биодеградацией биопротеза и без неё осуществлялось с использованием t-критерия Стьюдента (при нормальном распределении) либо критерия Манна–Уитни для количественных переменных. Для категориальных переменных применялись χ 2-критерий Пирсона или точный тест Фишера, в зависимости от ожидаемой частоты.
Для выявления факторов, ассоциированных с биодеградацией, проводился логистический регрессионный анализ. На первом этапе выполнен унивариантный анализ: для каждого предиктора рассчитывались отношения шансов (odds ratio, OR) с 95% доверительными интервалами (confidence interval, CI). Переменные с уровнем значимости p<0,10 включались в мультивариантную логистическую модель. Для исключения мультиколлинеарности рассчитывался коэффициент инфляции дисперсии (VIF), при превышении которого переменные исключались. Построение итоговой модели осуществлялось с использованием пошагового метода (stepwise selection).
Уровень статистической значимости во всех анализах принимался равным p<0,05. Статистическая обработка данных выполнялась с использованием пакетов R версии 4.3 и Python версии 3.10 (библиотеки: pandas, statsmodels, scipy ).
Результаты
Базовые характеристики исследуемой популяции
В результате стратификации все пациенты были разделены на две группы: с наличием и отсутствием признаков

биодеградации аортального биологического протеза. Далее был проведён сравнительный анализ демографических, клинических и ЭхоКГ характеристик между этими группами.
В таблице 1 представлены основные клинические и лабораторные параметры пациентов до операции, сравнение проводилось между группами с биодеградацией и без неё. Количественные переменные представлены в виде медианы [25-й; 75-й перцентиль], сравнение проводилось с использованием критерия Манна–Уитни. Для категориальных переменных указаны абсолютные значения и доли в процентах, статистическая проверка проводилась с использованием χ 2-критерия Пирсона или точного теста Фишера, в зависимости от условий.
Гиперлипидемия достоверно чаще встречалась в группе без деградации (50% против 33%; p = 0,032), что может свидетельствовать о потенциальной защитной роли медикаментозной коррекции липидного обмена.
По остальным показателям различий между группами не обнаружено. Доля пациентов с почечной дисфункцией (ХБП ≥3А стадии) и распространённым атеросклерозом была выше в группе без деградации, но различия не достигли статистической значимости.
После проведения описательного и сравнительного анализа исходных характеристик пациентов, следующим этапом стало определение факторов, ассоциированных с риском деградации биопротеза. Для этого был выполнен унитариантный логистический регрессионный анализ, направленный на оценку степени влияния каждого из клинических предикторов на вероятность структурной дисфункции клапана.
В рамках анализа рассчитывались отношения шансов (odds ratio, OR), 95% доверительные интервалы (CI) и p-значения. Результаты представлены в таблице 2.
Анализ продемонстрировал, что ряд факторов достоверно ассоциирован с повышенным риском биодеградации аортального клапанного биопротеза.
Наиболее значимыми предикторами оказались: индекс массы тела (OR = 3,39; 95% CI: 2,54–4,53; p<0,001), фракция выброса по Симпсону, ХСН III ФК и выше, фибрилляция предсердий, ИБС, онкология в анамнезе и двустворчатый АК – все имели аналогичные коэффициенты OR и статистически значимую ассоциацию с деградацией.
Пол, возраст, уровень гемоглобина и пол не показали статистически значимой связи с развитием деградации (p>0,05). В унитарном логистическом анализе не было выявлено достоверной связи между наличием двустворчатого АК (OR = 0,79; 95% ДИ: [0,37–1,70]; p = 0,547) и онкологическими заболеваниями в анамнезе (OR = 1,45; 95% ДИ: [0,57–3,68]; p = 0,436) с риском биодеградации биопротеза.
Учитывая ограниченные возможности классического логистического регрессионного анализа в условиях большого количества потенциально значимых, но взаимосвязанных признаков, на следующем этапе исследования было принято решение использовать подходы машинного обучения. Для построения прогностической модели риска
Табл. 1. Сравнение клинико-лабораторных характеристик групп пациентов до операции
|
Параметр |
Без деградации |
С деградацией |
p |
|
Возраст, лет |
73.0 [70.8; 78.0] |
73.0 [72.0; 77.5] |
0,811 |
|
Пол (мужчины), n (%) |
121 (60%) |
39 (66%) |
0,532 |
|
Гемоглобин, г/л |
129.0 [119.5; 137.0] |
131.0 [121.7; 137.5] |
0,462 |
|
Креатинин, мкмоль/л |
87.0 [72.6; 100.2] |
83.0 [72.5; 94.2] |
0,192 |
|
ХБП ≥ 3А стадии, n (%) |
14 (7%) |
2 (3%) |
0,481 |
|
Гиперлипидемия, n (%) |
96 (50%) |
18 (33%) |
0,032 |
|
Сахарный диабет, n (%) |
1 (0%) |
1 (2%) |
— |
|
Распространённый атеросклероз*, n (%) |
30 (15%) |
5 (8%) |
0,284 |
Примечание : ХБП – хроническая болезнь почек; p – уровень статистической значимости.
Табл. 2. Результаты унитарного логистического анализа факторов, ассоциированных с биодеградацией биопротеза аортального клапана
|
Параметр |
OR |
95% CI |
p |
|
Возраст, лет |
1,01 |
[0.97; 1.06] |
0,578 |
|
Мужской пол |
0,79 |
[0.43; 1.44] |
0,437 |
|
Индекс массы тела |
3,39 |
[2.54; 4.53] |
0 |
|
Фракция выброса (Симпсон), % |
3,39 |
[2.54; 4.53] |
0 |
|
Гемоглобин, г/л |
1,01 |
[0.99; 1.03] |
0,435 |
|
Креатинин, мкмоль/л |
0,99 |
[0.97; 1.00] |
0,117 |
|
ИБС |
3,39 |
[2.54; 4.53] |
0 |
|
ХСН ≥ III ФК |
3,39 |
[2.54; 4.53] |
0 |
|
ХБП ≥ 3А стадии |
2,15 |
[0.47; 9.72] |
0,322 |
|
Фибрилляция предсердий |
3,39 |
[2.54; 4.53] |
0 |
|
Гиперлипидемия |
1,47 |
[0.88; 2.47] |
0,141 |
|
Сахарный диабет |
0,94 |
[0.81; 1.09] |
0,413 |
|
Распространённый атеросклероз |
1,91 |
[0.70; 5.16] |
0,204 |
|
Онкология в анамнезе |
3,39 |
[2.54; 4.53] |
0 |
|
Двустворчатый аортальный клапан |
3,39 |
[2.54; 4.53] |
0 |
Примечание : OR – отношение шансов, 95% CI – 95% доверительный интервал, p – уровень статистической значимости, ИБС – ишемическая болезнь сердца, ХСН ≥ III ФК – хроническая сердечная недостаточность III функционального класса и выше, ХБП ≥ 3А стадии – хроническая болезнь почек стадии 3А и выше.
деградации биопротеза был выбран метод случайного леса (Random Forest) – как один из наиболее устойчивых и интерпретируемых ансамблевых алгоритмов.
Основными причинами выбора данного метода стали:
-
• высокая устойчивость к мультиколлинеарности предикторов;
-
• способность учитывать нелинейные зависимости и взаимодействия между признаками без явного их задания;
-
• наличие встроенного механизма оценки важности признаков (feature importance) ;
-
• возможность эффективно работать с данными, содержащими пропущенные значения (при условии предварительной иммутации).
Использование деревьев решений и ансамблевых моделей позволило дополнительно верифицировать результаты
Майстренко А.Д., Курашенко В.В., Успенский В.Е. и др.
БИОДЕГРАДАЦИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ АОРТАЛЬНОГО КЛАПАНА: КЛИНИЧЕСКИЕ ПРЕДИКТОРЫ И АНАЛИЗ ВЫЖИВАЕМОСТИ НА ОСНОВЕ МАШИННОГО ОБУЧЕНИЯ И МЕТОДА PROPENSITY SCORE MATCHING регрессионного анализа, а также выявить новые потенциальные взаимосвязи между переменными, не очевидные при применении традиционных статистических подходов.
С целью повышения прогностической точности предсказания биодеградации биологического протеза была обучена модель случайного леса (Random Forest) на расширенном наборе клинико-лабораторных параметров. В анализ были включены дооперационные переменные, в том числе: индекс массы тела, фракция выброса, уровни креатинина и гемоглобина, возраст, пол, а также наличие ИБС, хронической сердечной недостаточности (ХСН), сахарного диабета, гиперлипидемии и хронической болезни почек (ХБП). Все количественные показатели были нормализованы и предварительно обработаны методом медианной иммутации.
Модель обучалась с использованием балансировки классов и тестировалась на отложенной выборке (30% исходных данных). Общая точность модели составила 70,5%. При выявлении случаев биодеградации (класс 1) чувствительность составила 42%, специфичность – 80%, F1-метрика – 0,41.
На рисунке 1 представлена относительная важность признаков на основе критерия Джини (Gini Importance), отражающая вклад каждой переменной в уменьшение неопределённости в деревьях модели. Наибольшую значимость продемонстрировали уровни креатинина и гемоглобина, за ними следовали возраст и наличие сахарного диабета. Индекс массы тела, фракция выброса и наличие ХСН в данной модели оказались менее информативными, что может быть связано с ограниченным размером обучающей выборки или перекрытием информативности между признаками. Такая оценка важности позволяет использовать выявленные параметры при дальнейшей стратификации риска и построении прогностических моделей.
С учётом ретроспективного характера исследования и отсутствия рандомизации, сравнение исходов между группами пациентов с биодеградацией и без неё сопряжено с риском систематического смещения. Для минимизации влияния исходных различий применялась методика сопоставления по склонности (Propensity Score Matching, PSM), которая позволяет балансировать когорты по известным клиническим факторам.
Для расчёта propensity scores была использована логистическая регрессия, в которую включались следующие переменные: возраст, пол, индекс массы тела, функциональный класс ХСН, уровни креатинина и гемоглобина, наличие ИБС, распространённого атеросклероза, сахарного диабета, гиперлипидемии и ХБП. Категориальные переменные были закодированы, пропущенные значения удалены. Сопоставление осуществлялось в формате 1:1 по алгоритму ближайшего соседа (Nearest Neighbor Matching) без возврата. В результате были сформированы matched-группы по 14 пациентов в каждой.
Сравнение выживаемости биопротезов между сопоставленными группами проводилось методом Каплана-Мейера с учётом цензурирования. Медианный срок до деградации в основной группе составил 38 месяцев, в то время creatinine hb age_ dm lipids sex_ ckd_ ids_ chf ef bmi__________________________________________________
0.00 0.05 0.10 0.15 0.20 0.25 0.30 0.35
Важность признака (Gini Importance)
Рис. 1. Вклад признаков в модель случайного леса (Random Forest).
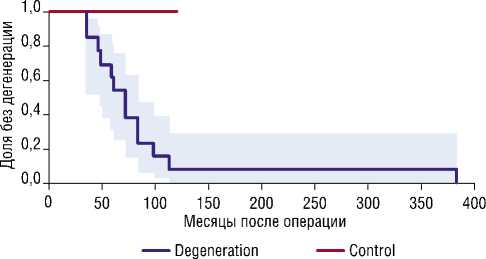
Рис. 2. Кривые выживаемости биопротеза в matched-группах (метод Каплана-Мейера). Примечание. Кривые выживаемости биологических протезов АК после проведения сопоставления методом Propensity Score Matching (Kaplan–Meier). В группе с деградацией отмечено достоверное снижение «выживаемости» протезов по сравнению с matched-контролем (log-rank test, p = 0.01).
как в matched-контрольной группе медиана наблюдения составила 48 месяцев. Лог-ранговый тест выявил статистически значимое различие между кривыми (p = 0,01).
На рисунке 2 представлены кривые выживаемости биологических протезов в matched-группах. Синяя линия отображает группу пациентов с деградацией: наблюдается выраженное снижение доли функционирующих протезов в течение первых 100 месяцев. Оранжевая линия соответствует matched-группе контроля, где случаи деградации не зарегистрированы на протяжении всего срока наблюдения. Это подчёркивает устойчивость результата, даже после балансировки по основным клиническим характеристикам.
Обсуждение
В настоящем исследовании проведён многоуровневый анализ факторов, ассоциированных с биодеградацией биологических протезов АК. Полученные результаты подтверждают, что деградация биопротезов является сложным и многофакторным процессом, зависящим как от клиниколабораторных характеристик пациента, так и от конструктивных особенностей имплантированного протеза.
На этапе унитарного логистического анализа были выявлены достоверные ассоциации между риском био-
деградации и следующими факторами: индекс массы тела, сниженная фракция выброса, наличие ИБС, ХСН III ФК и выше. Эти результаты согласуются с ранее опубликованными данными, согласно которым метаболическая и гемодинамическая перегрузка являются ключевыми триггерами структурной дисфункции биопротезов [4; 6].
Попытка построения мультивариантной логистической модели была ограничена из-за сингулярности матрицы предикторов, что, вероятно, связано с высокой коррелированностью факторов и недостаточным числом событий. Это обусловило необходимость применения методов машинного обучения, в частности – алгоритма случайного леса. Полученная модель продемонстрировала удовлетворительное качество классификации (accuracy 70,5%, recall 42%), а наибольший вклад в прогноз дали фракция выброса, индекс массы тела и уровень креатинина.
Для устранения систематического смещения, обусловленного нерандомизированным распределением пациентов, был применён метод сопоставления по склонности (Propensity Score Matching). Результаты анализа выживаемости методом Каплана-Мейера в matched-группах показали достоверно более короткий срок функционирования протезов в группе с деградацией (p = 0,01), что подчёркивает независимый характер этих различий.
Ограничениями настоящего исследования являются ретроспективный дизайн, относительно небольшая выборка, гетерогенность данных ЭхоКГ и потенциальные потери информации при заполнении документации.
Согласно литературным данным, ключевыми факторами, способствующими структурной деградации биопротезов, являются хроническая болезнь почек, метаболический синдром и сахарный диабет, курение, женский пол и дефицит витамина К. Деструктивные процессы обусловлены не только кальцинозом створок, но и фиброзом, дезорганизацией коллагена и аутоиммунной реакцией организма на биоматериал [7].
Иммунологическая реакция на биопротез развивается в ответ на повреждение тканей при имплантации и активацию каскадов комплемента и фибринолиза. Образующиеся фиброзные разрастания (паннус) могут нарушать движение створок, приводя к стенозу. Современные исследования также указывают, что глутаровый альдегид не полностью предотвращает иммунный ответ [7].
Таким образом, биодеградация биологических протезов АК представляет собой результат взаимодействия множества факторов: механических, метаболических, иммунных и конструктивных. Многоуровневый подход к анализу, включающий машинное обучение и методы балансировки когорты, позволяет глубже понять причины преждевременного выхода клапанов из строя и формировать более точные стратегии клинического наблюдения и выбора протеза.
Резюме основного результата исследования
В ходе исследования установлено, что структурная деградация биологических протезов АК развивается у примерно четверти пациентов в течение первых пяти лет после операции. Наиболее значимыми предикторами оказались индекс массы тела, сниженная фракция выброса, наличие ИБС, ХСН III ФК и выше, а также уровень креатинина. Применение машинного обучения и Propensity Score Matching позволило подтвердить независимый характер выявленных ассоциаций и повысить точность стратификации риска.
Обсуждение основного результата исследования
Полученные данные показали, что структурная деградация биологических протезов АК развивается у примерно четверти пациентов в течение первых 4–5 лет после операции. Этот результат подтверждает и дополняет сведения литературы, где сообщается о значительном снижении долговечности биопротезов у пациентов трудоспособного возраста (Johnston et al., 2015; Bourguignon et al., 2015). В то время как ряд исследований указывает на более поздние сроки начала биодеградации (10–15 лет), выявленный медианный срок в 38 месяцев подчёркивает важность раннего мониторинга у определённых категорий пациентов.
Наш анализ выявил, что ключевыми предикторами ускоренной деградации являются индекс массы тела, сниженная фракция выброса, ИБС, ХСН III ФК и выше, а также уровень креатинина. Эти факторы во многом согласуются с ранее опубликованными данными, согласно которым метаболическая перегрузка, снижение насосной функции миокарда и сопутствующие заболевания почек повышают риск дисфункции биопротезов (Flameng et al., 2010; Zorn et al., 2010). В то же время выявленная ассоциация с индексом массы тела и функцией почек позволяет рассматривать механизмы хронического воспаления, ок-сидативного стресса и кальциноза как возможные звенья патогенеза ускоренной биодеградации.
Применение машинного обучения и метода Propensity Score Matching усилило достоверность наших выводов, минимизировав эффект систематического смещения и выявив нелинейные взаимосвязи между переменными. Интересно, что в модели случайного леса наибольший вклад внесли показатели фракции выброса, креатинина и возраста, что может отражать сложное взаимодействие между функциональным состоянием миокарда, метаболическими процессами и старением тканей биопротеза. Эти данные подтверждают, что классические предикторы риска могут изменять своё значение в зависимости от популяции и применённых методов анализа.
Таким образом, наше исследование подтверждает гипотезу о многофакторной природе деградации биопротезов и подчёркивает необходимость персонализированного подхода к наблюдению за пациентами. Ранняя идентификация групп риска с помощью расширенного анализа данных может позволить своевременно корректировать тактику ведения и, возможно, выбирать более оптимальные варианты клапанных протезов для конкретных пациентов.

Майстренко А.Д., Курашенко В.В., Успенский В.Е. и др.
БИОДЕГРАДАЦИЯ БИОЛОГИЧЕСКИХ ПРОТЕЗОВ АОРТАЛЬНОГО КЛАПАНА: КЛИНИЧЕСКИЕ ПРЕДИКТОРЫ И АНАЛИЗ ВЫЖИВАЕМОСТИ НА ОСНОВЕ МАШИННОГО ОБУЧЕНИЯ И МЕТОДА PROPENSITY SCORE MATCHING
Ограничения исследования
Настоящее исследование имеет ряд ограничений, которые необходимо учитывать при интерпретации полученных результатов.
Во-первых, ретроспективный дизайн накладывает ограничения на полноту и точность собранных данных, а также повышает риск систематических ошибок, связанных с неполнотой медицинской документации. Отсутствие рандомизации не позволяет полностью исключить влияние неучтённых факторов на исходы.
Во-вторых, выборка исследования, несмотря на включение 259 пациентов, остаётся относительно небольшой для многофакторного анализа. Особенно это касается подгруппового анализа, где количество наблюдений было ограниченным, что снижает статистическую мощность и может приводить к завышению или занижению значимости отдельных факторов.
В-третьих, основным методом оценки функции биопротеза использовалась ЭхоКГ. Несмотря на её доступность и клиническую ценность, она имеет субъективный характер и ограниченную воспроизводимость. Отсутствие данных морфологического анализа и современных методов визуализации (например, мультиспиральной КТ или МРТ) ограничивает точность оценки структурных изменений клапанов.
В-четвёртых, применение алгоритмов машинного обучения и Propensity Score Matching улучшило качество анализа, однако полученные модели требуют внешней валидации на независимых когортах пациентов. Перекрёстная проверка (cross-validation) внутри одной выборки не исключает риска переобучения и ограничивает переносимость результатов на другие популяции.
Наконец, интерпретация клинической значимости выявленных факторов осложняется тем, что часть из них (например, индекс массы тела или уровень креатинина) может изменяться со временем и подвергаться влиянию терапии, что требует динамического учёта при долгосрочном прогнозировании.
Таким образом, выводы данного исследования следует рассматривать как предварительные и требующие подтверждения в более масштабных проспективных исследованиях с использованием комплексной оценки функции биопротезов.
Заключение
Биопротезы АК обладают ограниченной долговечностью: частота структурной деградации существенно возрастает в сроки от 5 до 15 лет после имплантации, что подтверждается как крупными регистрами, так и отдельными когортными исследованиями. Несмотря на накопленный опыт, остаются нерешёнными вопросы ранней идентификации пациентов группы риска и точного прогнозирования сроков биодеградации, что ограничивает возможность своевременного вмешательства и персонализации тактики лечения.
В рамках проведённого анализа показано, что у примерно четверти пациентов структурная деградация биопротеза развивается уже в течение первых 4–5 лет после операции. Установлены значимые клинические предикторы данного осложнения: индекс массы тела, сниженная фракция выброса, ИБС, хроническая сердечная недостаточность III ФК и выше, а также уровень креатинина. Использование алгоритмов машинного обучения и метода Propensity Score Matching позволило подтвердить независимый характер выявленных ассоциаций, минимизировать влияние систематического смещения и выявить нелинейные взаимосвязи между предикторами. Наши результаты дополняют имеющиеся данные, уточняя роль метаболических и функциональных факторов в ускорении деградации, и показывают возможность применения многоуровневого аналитического подхода для повышения прогностической точности.
С научной точки зрения, исследование демонстрирует перспективность интеграции классических статистических методов с современными алгоритмами машинного обучения в кардиохирургических регистрах. С клинической позиции полученные результаты могут быть использованы для стратификации риска, персонализированного наблюдения пациентов и выбора наиболее подходящей тактики протезирования АК. Однако окончательная валидация предложенных моделей требует более масштабных проспективных исследований.


