Биологическая гетерогенность первичной и церебральной метастатической опухолей при раке молочной железы
Автор: Субботина Д.Р., Гуляев Д.А., Митрофанова Л.Б.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Нейрохирургия
Статья в выпуске: 4 т.17, 2021 года.
Бесплатный доступ
Цель; оценка частоты дискордантности рецепторного статуса и статуса HER2 в первичной и церебральной метастатической опухолях у больных раком молочной железы (РМЖ). Материал и методы. В исследование включены 18 пациентов, оперированных по поводу метастазов РМЖ в головной мозг. Выполнено иммуногистохимическое исследование опухолевого материала с целью оценки экспрессии ER, PR, HER2. Полученные результаты сравнивали в парах с материалами от первичных опухолей. Результаты. У 50% больных рецепторный статус первичной опухоли и метастаза в головной мозг был постоянным, в то время как дискордантность по HR-статусу выявлена в 44% случаев. Наиболее редкими рецепторными преобразованиями были приобретение HER 2+-статуса - 6% (л=1) и утрата HER 2+-статуса - 11 % (п=2). 67% пациенток с HR+-oпyxoлями молочной железы, получавших адъювантную антиэстрогенную терапию, потеряли экспрессию целевого рецептора в метастазах. Заключение. В половине исследуемых пар опухолей выявлена дискордантность хотя бы по одному из показателей (ER, PR, HER2) биологической гетерогенности опухолей. Чаще других морфологических преобразований в метастатической опухоли отмечается утрата HR+-craTyca.
Биологическая гетерогенность, рак молочной железы, церебральные метастазы
Короткий адрес: https://sciup.org/149139774
IDR: 149139774 | УДК: 616.8-089
Biological heterogeneity of primary and metastatic brain tumor in breast cancer patients
Purpose: to evaluate the frequency of discordance of receptor status and HER2 status in primary and metastatic brain tumor in patients with breast cancer. Material and methods. The study included 18 patients whose brain metastases from breast cancer were treated surgically. An immunohistochemical assay of tumoral samples was performed to assess the expression of ER, PR, HER2. The results obtained were compared in pairs with samples from primary tumors. Results. The receptor status of the primary tumor and brain metastasis was constant in 50% of patients, while discordance in HR status was detected in 44% of cases. The rarest receptor conversions were the acquisition of HER 2+ status at 6% (n=1) and the loss of HER 2+ status at 11 % (n=2). 67% of patients with HR+ primary breast tumors, receiving adjuvant anti-estrogen therapy lost expression of the target receptor in brain metastases. Conclusion. In half of the tumor pairs under study we detected discordance in at least one of the indicators (ER, PR, HER2) of tumor biological heterogeneity. Loss of HR+ status in metastatic tumor was observed more often than other morphological transformations.
Текст научной статьи Биологическая гетерогенность первичной и церебральной метастатической опухолей при раке молочной железы
клинической проблемой. Такая прогрессия основного заболевания значительно усложняет лечение, ограничивая возможности системной терапии. Выбор химиопрепаратов основывается на исследовании молекулярно-биологических особенностей первичной опухоли. Однако зачастую метастазы де- монстрируют различный уровень экспрессии рецепторов, что обусловливает необходимость изменения терапевтического агента. В 2017 г. M. Timmer и соавт. показали важность ретестирования биологического подтипа при прогрессировании РМЖ в головной мозг. В результате морфологического исследования 24 пар опухолей выявлено, что если первичная опухоль имела статус ER+ и PR+ в 41,6% случаев, то церебральные метастазы имели гормонопозитивный статус всего в 12,5 и 16,6% случаев соответственно, у 23,6% пациенток с HER2-негативным РМЖ выявлены HER2-позитивные метастазы в головном мозге, последнее позволило применить современную анти-HER2-терапию у данных больных [1]. Изучение биологической гетерогенности первичной и метастатической опухолей может изменить системные подходы к лечению у конкретного пациента. В настоящее время знания о дискордантности рецепторного статуса (ER/PR/HER2) в церебральных метастатических опухолях малочисленны, а клинические особенности отдельных биологических подтипов РМЖ остаются малоизученными.
Цель — оценить частоту дискордантности рецепторного статуса и статуса HER2 в первичной и церебральной метастатической опухолях у больных РМЖ.
Материал и методы. Проведен анализ комплексного обследования и хирургического лечения 18 паци- ентов с метастазами РМЖ в головной мозг, находившихся на лечении в нейрохирургическом отделении ФГБУ «НМИЦ им. В. А. Алмазова» в возрасте от 33 до 78 лет (медианный возраст 50,5 (39,75; 60,25) года). Медиана времени без прогрессирования в головной мозг составила 21,5 (14,5; 37,75) мес. Средний период наблюдения составил 12,5 мес. Катамнестические данные собраны у 16 (89%) пациентов. В качестве основного метода нейровизуализации проводилась магнитно-резонансная (МР) томография головного мозга с магнитной индукцией 1,5 и 3 Тс в режимах Т1 и Т2, FLAIR, DWI и внутривенным контрастированием парамагнетиками. Оценивали локализацию очагов и характер поражения головного мозга, мозговых оболочек и костей черепа. Проведено стандартное гистологическое исследование материала полученной метастатической опухоли методом световой микроскопии и окрашивания гематоксилин — эозином, а также иммуногистохимическое исследование с антителами к HER2, ER, PR, Ki67. Определяли уровень экспрессии HR (процентное содержание ER+- и PR+-клеток и интенсивность их окрашивания), уровни экспрессии HER2 и Ki67 (рис. 1).
В случае неопределенного статуса HER2 (2+) применялось определение амплификации гена HER2 методом in situ гибридизации (FISH). На основании медицинской документации проанализированы данные
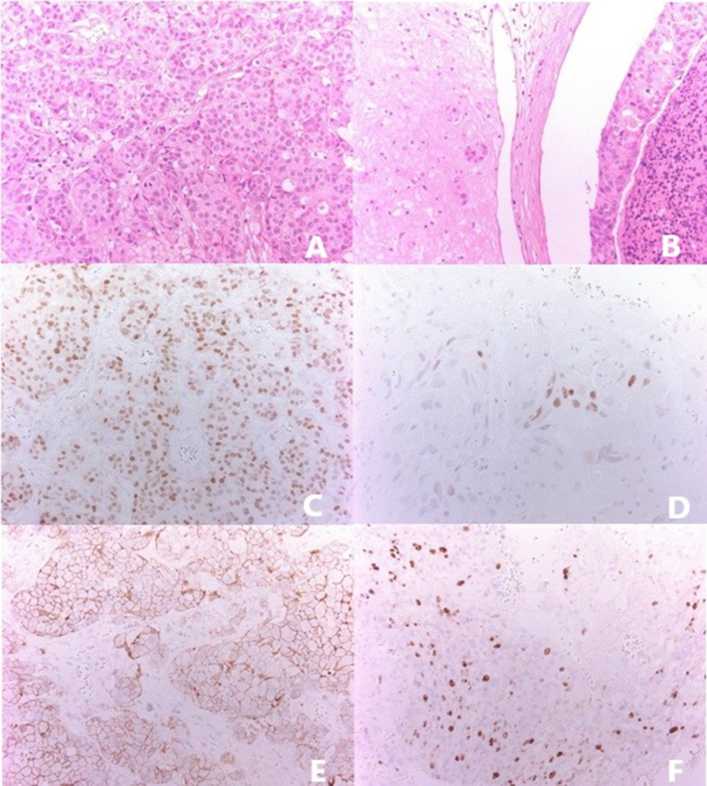
Рис. 1. Морфологическая картина метастаза рака молочной железы в головной мозг:
А — эпителиальная злокачественная опухоль, формирующая протоковые структуры; окрашивание Гематоксилином и эозином; ×200;
В — опухолевые структуры в просвете сосуда; окрашивание Гематоксилином и эозином; ×200; С — ядерное окрашивание рецепторов к эстрогену в клетках опухоли (коричневое окрашивание); ×200; D — ядерное окрашивание рецепторов к прогестерону в клетках опухоли (коричневое окрашивание); ×200; E — мембранное окрашивание рецепторов к HER2 в клетках опухоли (коричневое окрашивание); ×200;
F — высокая пролиферативная активность в опухоли, ядерное окрашивание, Ki67 (коричневое окрашивание); ×200
о молекулярно-биологических особенностях первичной опухоли (гистологический вариант, уровень экспрессии ER, PR, HER2 и Ki67), состоянии экстракраниального процесса, характере и объеме ранее проводимой системной терапии. Проведен сравнительный анализ молекулярно-биологических показателей первичной и метастатической опухолей с учетом базовых характеристик пациентов (табл. 1). Средний период наблюдения составил 12,6 мес. Катамнестические данные собраны у 16 (89%) пациентов.
Накопление и фиксация полученных результатов осуществлялись в электронных таблицах Microsoft Office Excel 2016. Статистический анализ параметров проведен с помощью программы Statistica 10.0. Совокупности количественных показателей приве- дены в виде значений медианы, нижнего и верхнего квартилей. Номинальные данные описывались с указанием абсолютных значений и процентных долей.
Результаты. Единичные метастазы диагностированы в 45% случаев ( n =8), олигометастазы в 33% ( n =6), множественные церебральные метастазы в 22% случаев ( n =4). Интраоссальное поражение выявлено у 1 пациента (6%), метастатическое поражение мозговых оболочек — у 1 больного. До хирургического лечения и гистологической верификации опухоли стереотаксическую лучевую терапию на интракраниальные очаги получили 3 пациента (17%). В послеоперационный период облучение ложа удаленной опухоли выполнено в 17% случаев ( n =3), облучение всего головного мозга — в 6% ( n =1) случаев.
Таблица 1
Сравнительные клинико-морфологические характеристики пациентов
|
Клинико-морфологические характеристики |
Число |
|
N |
18 |
|
Средний возраст |
51 |
|
ER-статус первичной опухоли, % |
|
|
«+» |
50% ( n =9) |
|
« — » |
50% ( n =9) |
|
PR-статус первичной опухоли, % |
|
|
«+» |
44% ( n =8) |
|
«–» |
56% ( n =10) |
|
HER-2-статус первичной опухоли, % |
|
|
«+» |
39% ( n =7) |
|
«–» |
61% ( n =11) |
|
Гормональная терапия до появления церебральных метастазов РМЖ, % |
33% ( n =6) |
|
Анти-HER-2-терапия до появления церебральных метастазов РМЖ, % |
39% ( n =7) |
|
Экстракраниальные метастазы до появления церебральных метастазов РМЖ, % |
56% ( n =10) |
|
Медиана времени без прогрессирования в головной мозг (мес.) |
32 |
|
ER статус метастатической опухоли, % |
|
|
«+» |
22% (n=4) |
|
«–» |
78% (n=14) |
|
PR-статус метастатической опухоли, % |
|
|
«+» |
22% ( n =4) |
|
«–» |
78% ( n =14) |
|
HER-2-статус метастатической опухоли, % |
|
|
«+» |
39% ( n =7) |
|
«–» |
61% ( n =11) |
|
Лечение церебральных метастазов РМЖ, % |
|
|
Нейрохирургическое удаление |
100% ( n =17) |
|
Радиохирургическое облучение |
17% ( n =3) |
|
Облучение всего головного мозга |
6% ( n =1) |
|
Характер поражения головного мозга, % |
|
|
Единичные |
45% ( n =8) |
|
Олигометастазы |
33% ( n =6) |
|
Множественные |
22% ( n =4) |
|
Интраоссальный рост |
6% ( n =1) |
|
Поражение мозговых оболочек |
|
Таблица 2
Гетерогенность первичной и метастатической церебральной опухолей при раке молочной железы
|
Статус HER2 опухоли |
ER-статус опухоли |
PR-статус опухоли |
|||
|
первичной |
метастатической |
первичной |
метастатической |
первичной |
метастатической |
|
– |
– |
+ |
+ |
+ |
+ |
|
– |
– |
+ |
– |
+ |
– |
|
+ |
+ |
– |
– |
– |
– |
|
+ |
– |
– |
– |
– |
– |
|
– |
– |
– |
– |
– |
– |
|
+ |
+ |
– |
– |
– |
– |
|
– |
– |
+ |
+ |
+ |
– |
|
+ |
+ |
– |
– |
– |
– |
|
– |
– |
+ |
+ |
+ |
– |
|
– |
+ |
+ |
– |
+ |
– |
|
+ |
+ |
+ |
– |
+ |
– |
|
+ |
– |
+ |
– |
+ |
+ |
|
– |
+ |
+ |
– |
– |
– |
|
– |
– |
– |
– |
– |
+ |
|
– |
– |
– |
– |
– |
– |
|
+ |
+ |
+ |
+ |
+ |
+ |
|
– |
– |
– |
– |
– |
– |
|
– |
– |
– |
– |
– |
– |
П р и м еч а н и е : Заливкой обозначены случаи выявленной дискордантности рецепторного статуса по показателям HER2, ER, PR.
Неоадъювантную химиотерапию получали 12 (67%), адъювантную химиотерапию — 14 человек (78%). Таргетную терапию, при наличии гиперэкспрессии HER2/neu в первичной опухоли, получали 7 пациенток (39%), эндокринотерапия HR + РМЖ проводилась в 33% случаев ( n =6) (табл. 1).
Пациенты с HER2-положительным РМЖ имели более короткий период без прогрессирования в головной мозг, в сравнении с HER2-отрицательным статусом (32,1/39 месяцев). Анализ результатов морфологического исследования 18 пар опухолей показал высокий уровень конверсии рецепторного статуса (44%, n =8). Потеря положительного статуса ER отмечена в 28% ( n =5), статуса PR — в 28% ( n =5). В одном случае (6%) наблюдалось приобретение PR+ статуса. Расхождение по статусу HER2 выявлено в 17% ( n =3) случаев. У 11% ( n =2) пациенток с HER2-позитивной первичной опухолью выявлены HER2-негативные метастазы в головном мозге. В одном случае (6%) HER2-негативого РМЖ определялась гиперэкспрессия HER2-фактора в церебральном метастазе. Таким образом, в половине случаев (n=9) выявлена дискордантность хотя бы по одному из показателей (ER, PR, HER2) биологической гетерогенности опухолей (табл. 2).
Клиническое наблюдение. Больная Н., 34 года, социально адаптирована, нормостенического телосложения, сниженного питания поступила в плановом порядке в отделение нейрохирургии ФГБУ «НМИЦ им. В. А. Алмазова». За три недели до госпитализации появились жалобы на интенсивную головную боль в лобной области давящего, затем пульсирующего характера, плохо купирующуюся анальгетиками, нарушение речи в виде сложности произнесения слов и составления фраз, сложность написания слов, легкую шаткость при ходьбе. В 2015 г. диагностирован РМЖ, вы- полнена расширенная секторальная резекция левой молочной железы (ER — 90% — 8 б., PR — 80% — 8 б., HER 2 — негативная, Ki67 — 90%). Проведены 6 курсов полихимиотерапии. Через 2 года — прогрессирование заболевания в виде метастазирования в ткань легкого. Выполнена миниторакотимия, энуклеация образования легкого с последующими многократными курсами химиотерапии. За месяц до появления неврологической симптоматики зафиксирована стабилизация экстракраниального процесса.
При поступлении функциональный статус по шкале Карновского 70%, индекс GPA 1,5 балла, клиническая картина была представлена общемозговой гипертензионной симптоматикой, легкими интел-лектуально-мнестическими нарушениями (24 балла по шкале краткого исследования психического состояния Mini Mental State Examination — MMSE), элементами эфферентной моторной афазии, дисгра-фией, правосторонней рефлекторной пирамидной и псевдомозжечковой симптоматикой. По данным МР-томограмм головного мозга с внутривенным контрастным усилением на серии МР-томограмм, взвешенных по Т1 и Т2 в трех проекциях, в левой лобной доле визуализированы два кистозно-солидных образования, размерами 36×37×37 мм и 43×27×23 мм, с четкими неровными контурами и выраженным перифокальным отеком; на постконтрастных изображениях определяется усиление МР-сигнала от пристеночных солидных компонентов опухолей (рис. 2).
Проведено плановое нейрохирургическое вмешательство. В ходе операции после вскрытия твердой мозговой оболочки визуализирован небольшой участок опухоли, выходящий на кору головного мозга. Опухоли желтовато-серого цвета, мягко-эластической консистенции, с четкими границами, умеренно
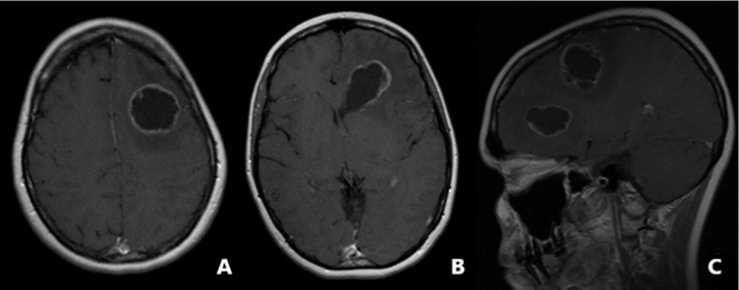
Рис. 2. Постконтрастные МР-изображения больной Н. в режиме Т1 в аксиальной (А, B) и сагиттальной (C) проекциях
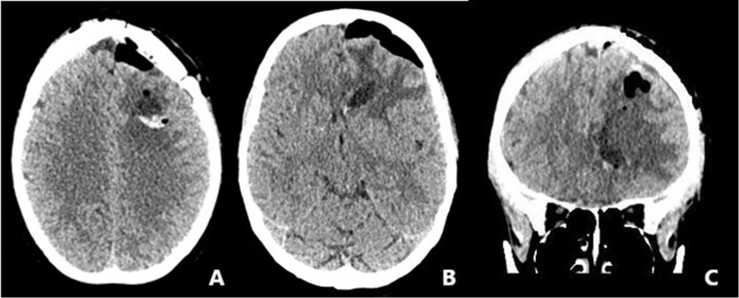
Рис. 3. Послеоперационные компьютерные томограммы больной Н. в аксиальной (А, B) и коронарной (C) проекциях
васкуляризированы, с преобладающим кистозным компонентом в центре. Обе опухоли последовательно удалены двумя блоками с включением предполагаемой зоны инвазии. По данным контрольной муль-тиспиральной компьютерной томографии головного мозга подтверждены радикальность удаления опухолей и отсутствие возможных осложнений (рис. 3).
По данным гистологического исследования: метастаз карциномы. Иммуногистохимическое исследование: экспрессия маммаглобина и GATA3 фокальная, CK7 — тотальная, HER2–3+, ER — «–», PR — «-», Ki67 — 35%. Заключение: метастаз карциномы молочной железы.
Ранний послеоперационный период с отчетливой положительной динамикой в виде регресса гипер-тензионного синдрома, частичного регресса афатических нарушений. Пациентка выписана на 8-е сутки после операции для проведения стереотаксической лучевой терапии на постоперационную зону, продолжения химиотерапии.
Данное клиническое наблюдение демонстрирует редкий случай конверсии HER2-/HR+ РМЖ на HER2+/HR- метастазы в головном мозге. Приоб- ретение мишени для таргетного лечения у данной больной дает возможность на улучшение прогноза заболевания.
Обсуждение. Биологическая гетерогенность первичной и церебральной метастатической опухолей изучается более 10 лет. Интерес клиницистов к данному вопросу очевиден: детальное исследование метастатической опухоли и преобразование в ней HR/HER2-статуса могут влиять на тактику целевого лечения. В нашем исследовании чаще встречалась утрата HR+-статуса, что ассоциировалось с приемом антиэстрогенной терапии. Изменения статуса HER2 носили эпизодический характер и не были связаны с проводимой анти-HER2-терапией. Причинами таких биологических изменений могут быть генетическая нестабильность опухоли, приводящая к гетерогенности опухолевого пула, а также опухолевая селекция под действием противоопухолевого лечения и как исход — выживание наиболее агрессивных биологических клонов РМЖ [2]. Полученные нами результаты согласуются с данными мировой литературы (табл. 3).
Таким образом, гетерогенность опухолей не только возможна, но и реализуется у значимого числа
Таблица 3
Оценка биологической гетерогенности первичной и церебральной метастатической опухолях при раке молочной железы
|
Автор, ссылка |
Год |
Число больных |
Уровень дискордантности между первичной и церебральной метастатической опухолями, % |
||
|
ER |
PR |
HER2 |
|||
|
C. Bachmann и соавт. [3] |
2013 |
107 |
18,4 |
28,6 |
18,0 |
|
Qi. Shen и соавт. [4] |
2015 |
140 |
28,0 |
20,0 |
3,0 |
Окончание табл. 3
Кроме того, следует отметить, что стереотаксическая лучевая терапия в отношении метастатического поражения головного мозга позволяет добиться удовлетворительных результатов в отношении локального контроля, однако нивелирует шансы на возможное проведение таргетной терапии у значительной доли пациенток ввиду отсутствия материала для морфологического исследования.
Заключение. Метастатический РМЖ является высоко гетерогенным заболеванием, его лечение является сложной мультидисциплинарной проблемой, включающей не только обеспечение локального контроля за счет современных методов местного воздействия, но и адекватную терапевтическую поддержку, основанную на скрупулезном изучении молекулярно-биологических особенностей метастатической и первичной опухолей. По результатам исследования выявлено, что в половине случаев определяется дискордантность хотя бы по одному из показателей (ER, PR, HER2) биологической гетерогенности опухолей. Основным клинически значимым морфологическим преобразованием в метастатической опухоли является приобретение положительного статуса HER2 как мишени для проведения таргетной противоопухолевой терапии.
Список литературы Биологическая гетерогенность первичной и церебральной метастатической опухолей при раке молочной железы
- Timmer M, Werner JM, Rbhn G, et al. Discordance and conversion rates of progesterone-, estrogen-, and HER2/neu-receptor status in primary breast cancer and brain metastasis mainly triggered by hormone therapy. Anticancer Res 2017; 37 (9): 4859-65.
- Колядина И.В., Андреева Ю.Ю., Франк Г.А. и др. Роль биологической гетерогенности при рецидивирующем и метастатическом раке молочной железы. Архив патологии 2018; 80 (6): 62-7.
- Bachmann С, Grischke Е М, Fehm Т, et al. CNS metastases of breast cancer show discordant immunohistochemical phenotype compared to primary. Clin Oncol 2013; (139): 551-6.
- Shen Qi, Sahin AA, Hess KR, et al. Breast cancer with brain metastases: clinicopathologic features, survival, and paired biomarker analysis. Oncologist 2015; 20 (5): 466-73.
- Joubert C, Boissonneau S, Fina F, et al. Immunohistochemical hormonal mismatch and human epidermal growth factor type 2 [HER2] phenotype ofbrain metastases in breast cancer carcinoma compared to primary. Neurochirurgie 2016; (62): 151-6.
- Jung J, Lee SH, Park M, et al. Discordances in ER, PR, and HER2 between primary breast cancer and brain metastasis. Journal of Neuro-Oncology 2018; 137 (2): 295-302.
- Hulsbergen AFC, Claes A, Kavouridis VK, et al. Subtype switching in breast cancer brain metastases: a multicenter analysis. Neuro Oncol 2020; 22 (8): 1173-81.
- Kao J-Y, Tsai J, Wu T, et al. Receptor discordance and phenotype change in metastatic breast cancer. Asian Journal of Surgery 2020; 44(1): 192-8.
- Kotecha R, Tonse R, Rubens M, et al. Systematic review and meta-analysis of breast cancer brain metastasis and primary tumor receptor expression discordance. Neurooncol Adv 2021; 3(1): vdab010.


