Биологическая эффективность почвенных актинобактерий при выращивании растений огурца (Cucumis sativus L.) в защищенном грунте
Автор: Батаева Ю.В., Григорян Л.Н., Батаева А.Д.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Иммунитет и защита растений
Статья в выпуске: 3 т.60, 2025 года.
Бесплатный доступ
Для борьбы с вирусными, грибными болезнями растений и насекомыми-вредителями используют химические пестициды, однако в связи с многократными обработками резистентность патогенов к ним повышается. Альтернативой химическим пестицидам служат биопестициды. Использование штаммов актинобактерий перспективно для разработки новых биопрепаратов с противовирусным, фунгицидным и инсектоакарицидным эффектом. В настоящей работе впервые установлена эффективность штаммов актинобактерий Nocardiopsis umidischolae RCAM04882, N. Umid-ischolae RCAM04883, Streptomyces carpaticus RCAM04697 при выращивании растений огурца в закрытом грунте в условиях аридного климата юга Российской Федерации. Цель исследования состояла в изучении влияния штаммов почвенных актинобактерий Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 на урожай и поражаемость грибными, вирусными заболеваниями и насекомыми-вредителями культуры огурца ( Cucumis sativus L.) в закрытом грунте. Эксперименты были выполнены в ФГБУ Российский сельскохозяйственный центр по Астраханской области в 2019 году в условиях защищенного грунта. Исследования проводили на культуре огурца сорта Форвард. Растения обрабатывали суспензией 3-суточных культур и суспензией из сухой биомассы (разведенной в стерильной дистиллированной воде в соотношении 1 мг/1 мл) штаммов Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697, выделенных из засоленных почв в Астраханской области в 2013 году, в концентрации 109 КОЕ/мл. Опыт проводили на естественном инфекционном фоне по следующей схеме: полив под корень через 1 сут после высадки рассады в тепличный грунт в фазу 2-3 настоящих листьев; полив под корень в стадии активного роста растений через 8 сут после первой обработки; полив под корень в фазу цветения и бутонизации через 8 сут после второй обработки; опрыскивание в фазу образования завязи и молочной спелости через 14 сут после третьей обработки; опрыскивание в фазу активного плодоношения через 14 сут после четвертой обработки; опрыскивание в фазу сбора урожая через 14 сут после пятой обработки. Схема опыта включала 8 вариантов: 1 - обработка эталонным биопрепаратом Фитоспорин-М (ПС, паста) (ООО «НВП «БашИнком», Россия) (положительный контроль); 2 - обработка водопроводной водой (отрицательный контроль); 3 - обработка суспензией N. umidischolae RCAM04882; 4 - обработка суспензией N. umidischolae RCAM04883; 5 - обработка суспензией S. carpaticus RCAM04697; 6 - обработка суспензией из сухой биомассы штамма N. umidischolae RCAM04882; 7 - обработка суспензией из сухой биомассы штамма N. umidischolae RCAM04883; 8 - обработка суспензией из сухой биомассы штамма S. carpaticus RCAM04697. Предшественниками растений огурца были томаты ( Solanum lycopersicum L.) сорта Гранд. Почву перед высадкой рассады дезинфицировали раствором медного купороса. Пролив проводили капельным способом с нормой 4,5-5 л на 1 растение водопроводной водой, прогретой до 26 °С. Сбор урожая на испытательном участке начался 1 июня, дата последнего сбора - 31 августа. Учет инсектоакарицидной активности штаммов актинобактерий в отношении бахчевой тли Aphis gossypii и паутинного клеща Tetranychus urticae проводили на 3-и сут после третьей и четвертой обработок. Пораженность растений вирусными инфекциями выявляли серологическим методом на стадии образования завязей (через 3 сут после третьей обработки) и созревания плодов (через 3 сут после четвертой обработки). Для диагностики вирусов методом иммунохимического анализа (ИХА) использовали иммунострипы марки Flashkits («ImmunoStrip Test Kit», США). Противовирусную активность рассчитывали в процентном соотношении от числа растений без симптомов. Идентификацию фитопатогенных грибов проводили на базе филиала ФГБУ «Россельхозцентр» по Астраханской области методом полимеразной цепной реакции с гибридизационно-флуоресцентной детекцией продуктов ПЦР в режиме реального времени с использованием микрочипового амплификатора нуклеиновых кислот АриаДНА (ООО «ЛЮМЭКС», Россия). Урожай определяли, суммируя массу созревших плодов в каждом варианте. Максимальная инсектицидная (85,3 %) и акарицидная (69,2 %) активность были зафиксированы при обработке суспензией 3-суточной культуры S. carpaticus RCAM04697. Наибольшая противовирусная активность (100 %) обнаружена также при обработке суспензией S. carpaticus RCAM04697 - все растения были без симптомов заражения ВОМ (вирус огуречной мозаики) и ВМТо (вирус мозаики томата). В вариантах с бактеризацией всеми штаммами актинобактерий симптомы болезней, вызываемых Fusarium oxysporum и Alternaria infecta , полностью отсутствовали. В варианте с обработкой растений огурца суспензией 3-суточной культуры S. carpaticus RCAM04697 показана наибольшая биологическая эффективность с высоким показателем урожая (62,9 кг), что оказалось в 3,8 раза больше значения в отрицательном контроле.
Актинобактерии, растения огурца, противовирусная активность, фунгицидная активность, инсектоакарицидная активность
Короткий адрес: https://sciup.org/142246212
IDR: 142246212 | УДК: 635.63:632:579.64 | DOI: 10.15389/agrobiology.2025.3.516rus
Biological effectiveness of soil actinobacteria for growing Cucumis sativus L. in greenhouses
Chemical pesticides are used to control viral and fungal plant diseases and insect pests, but due to multiple treatments, the resistance of pathogens to them increases. Biopesticides serve as an alternative to chemical pesticides. The use of actinobacteria strains is promising for the development of new biologicals with antiviral, fungicidal and insecticidal effects. In this work, the effectiveness of actinobacterium Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 in growing cucumber plants in greenhouses under the arid climate of the south of the Russian Federation were shown for the first time. Our goals was to investigate the effect of three strains of soil actinobacteria on cucumber ( Cucumis sativus L.) cv. Forvard yield and the incidence of fungal and viral diseases and attacks of insect pests in a greenhouse (Astrakhan Province, 2019).. The plants were inoculated with 3-day cultures of the actinobacteria and suspensions of their dry biomass diluted in sterile distilled water to 1 mg/1 ml. N. umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 strains (109 CFU/ml) were isolated from saline soils in the Astrakhan region in 2013. Tests were carried out under natural infectious loads. Root watering was applied 1 day after planting 2-3 true leaves’ seedling, 8 days after the first treatment during plant active growth, 8 days after the second treatment at budding and flowering. Then the plants were sprayed 14 days after the third treatment at ovary formation and milk ripeness, 14 days after the fourth treatment during active fruiting, and 14 days after the fifth treatment at harvesting. The treatments were as follows: 1 - positive control (treatment with the reference biological preparation Phytosporin-M (PS), paste) (NVP BashInkom LLC, Russia); 2 - negative control (treatment with tap water); 3 - treatment with suspension of N. umidischolae RCAM04882; 4 - treatment with suspension of N. umidischolae RCAM04883; 5 - treatment with suspension of S. carpaticus RCAM04697; 6 - treatment with suspension from dry biomass of strain N. umidischolae RCAM04882; 7 - treatment with suspension from dry biomass of strain N. umidischolae RCAM04883; 8 - treatment with suspension of dry S. carpaticus RCAM04697 biomass. The precursors of cucumber plants were tomatoes ( Solanum lycopersicum ) of the Grand variety. The soil was disinfected with copper sulfate before planting seedlings. The watering was carried out by drip method with a rate of 4.5-5 l per plant with tap water heated to 26 °С. Harvesting began on June 1, with the last harvest date being August 31. The insecticidal activity of actinobacteria strains against the melon aphid Aphis gossypii and the spider mite Tetranychus urticae was recorded on days 3 after the third and fourth treatments. The viral infections was detected by serological method at the stage of ovary formation (3 days after the third treatment) and fruit ripening (3 days after the fourth treatment). For immunochemical detection of viruses, Flashkits immunostrips (ImmunoStrip Test Kit, USA) were used. Antiviral activity was calculated as a percentage of the number of plants without symptoms. The identification of phytopathogenic fungi was carried out by hybridization-fluorescence detection of PCR products in real time using the AriaDNA microchip nucleic acid amplifier (LUMEX LLC, Russia). The yield was determined by summing the mass of ripe fruits in each variant. The maximum insecticidal (85.3 %) and acaricidal (69.2 %) activity was recorded during suspension treatment of a 3-day culture of S. carpaticus RCAM04697. The highest antiviral activity (100 %) was also found when treated with S. carpaticus RCAM04697 suspension - all plants were without symptoms of cucumber mosaic virus and tomato mosaic virus. For bacterization with all strains of actinobacteria, the symptoms of diseases caused by Fusarium oxysporum and Alternari a infecta were completely absent. In the variant with the treatment of cucumber plants with a suspension of 3-day culture S. carpaticus RCAM04697 showed the highest biological efficiency at a high yield (62.9 kg), which was 3.8 times higher compared to the negative control. The studied strains can be recommended for further testing in industrial field experiments when growing vegetables in an integrated plant protection system.
Текст научной статьи Биологическая эффективность почвенных актинобактерий при выращивании растений огурца (Cucumis sativus L.) в защищенном грунте
В связи с ухудшением фитосанитарной обстановки на территории юга России и повышением резистентности фитопатогенов к пестицидам химического происхождения микробиологические средства защиты растений вызывают все больший практический интерес (1-3). Химическая защита растений, направленная на полное удаление нежелательных компонентов агроценоза, часто приводит к нарушениям экологического равновесия как в самом агроценозе, так и в связанных с ним природных системах. Биологические средства защиты оказывают избирательный ингибирующий эффект на фитопатогены, повышают иммунный статус растений, участвуют в увеличении почвенного плодородия и биоразнообразия экосистем (4).
Перспективными для разработчиков считаются актинобактерии, которые служат постоянным компонентом почвенных и ризосферных микробных сообществ (5-7). Чрезвычайно широкое распространение актинобактерий в природе дает основание полагать, что этим организмам принадлежит значительная роль в круговороте органических и минеральных веществ (8). Например, при попадании в почву доступных многим микроорганизмам субстратов (хитина, кератина, крахмала) наблюдается значительное количественное увеличение числа актинобактерий помимо других гетеротрофов (9).
Актинобактерии, наряду с другими ризосферными микроорганизмами, играют важную роль в развитии растений, участвуя в снабжении последних элементами питания, фитогормонами, витаминами и другими факторами роста (10-13). Известные как продуценты антибиотических веществ, актинобактерии служат сильными антагонистами по отношению к фитопатогенам. Штаммы рода Nocardiopsis продуцируют противомикробные и биоактивные агенты — цитотоксический фунгицидный антибиотик калафун-гин, антибактериальный 3-трегалозамин, ингибитор протеинкиназы C, ме-тилпендолмицин, стауроспорин-подобный ингибитор фермента циклической АМФ-зависимой протеинкиназы (14). Бактерии вида N. umidischolae вырабатывают соединение валиномицин — пептидный антибиотик, повышающий проницаемость мембраны для ионов калия (15). Актинобактерии выделяются среди бактерий наиболее сложной организацией генома и фенотипа и превосходят все прочие группы микроорганизмов по способности синтезировать антибиотики и другие физиологически активные соединения (16, 17). Благодаря наличию таких ферментов, как протеазы и хитиназы, актинобактерии используются в качестве естественных регуляторов насекомых и фитопатогенных грибов (18). Хитиназы стрептомицетов ингибируют рост грибов, разрушая их клеточную стенку (19, 20), а у насекомых — наружный покров, состоящий из хитина (21). Механизмы образования хитиназ у актинобактерий изучены на генетическом уровне экспрессии функциональных генов (22).
Биопрепараты на основе актинобактерий зарекомендовали себя как биологические инсектициды, эффективные для борьбы с вредными членистоногими (23, 24). Им присуща специфичность, низкая токсичность, а также способность к деградации в естественных круговоротах веществ, что позволяет не нарушать природное равновесие при их использовании (25, 26). Разнообразие метаболитов этих бактерий обусловливает низкую сте- пень адаптации к ним вредных насекомых (16). Большинство биопрепаратов, разработанных на основе вторичных метаболитов, синтезируемых актинобактериями, имеет антибиотические свойства, однако описан ряд веществ с другим характером биологического действия: ингибиторы ферментов, гербициды, инсектициды, находящие применение в растениеводстве (10, 13).
Одними из первых инсектоакарицидных и антигельминтных веществ, полученных из бактерий Streptomyces avermitilis в России и за рубежом, были авермектины, действующие за счет блокирования передачи нервного импульса (27, 28). Штамм Streptomyces cremeus biovar. octemberanum var. nov. — продуцент ингибитора протеаз (трипсина, химотрипсина, фибринолизина, калликреина, папаина) проявлял высокую инсектицидную активность в отношении Myzodes persicae , а также антагонистическую активность в отношении фитопатогенных грибов и бактерий (29). На основе штамма S. aurantiacus разработан препарат Алейцид, основным действующим веществом которого является 9-деметилпиерицидин, обладающий высокой инсектицидной активностью (29). С использованием штаммов S. loidensis и S. herbaricolor разработаны препараты, включающие полипептиды, эффективные в отношении большой группы сосущих членистоногих (тлей, паутинного клеща, оранжерейной белокрылки), хлопковой совки, галловой нематоды (29).
Известен противовирусный эффект актинобактерий в отношении таких опасных вирусов растений, как вирус мозаики томата (ВМТо) и вирус огуречной мозаики (ВОМ), которые переносятся насекомыми и клещами (30, 31). Влияние актинобактерий на вирусы растений мало изучено, но в литературе имеются сведения об их воздействии на другие вирусы. Например, метаболит S. kaviengensis антимицин А обладает широким спектром действия против РНК-вирусов в отношении представителей семейств Togavir-idae , Flaviviridae , Bunyaviridae , Picornaviridae и Paramyxoviridae (32).
Актуальна проблема поиска новых актинобактерий, продуцирующих биологически активные вещества с инсектицидными, акарицидными, противомикробными и фитостимулирующими свойствами, применение которых способно сдерживать распространение вирусных и грибных фитопатогенов.
В представленной работе впервые установлена эффективность штаммов актинобактерий Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 при выращивании растений огурца в закрытом грунте в условиях аридного климата юга Российской Федерации.
Цель исследования состояла в изучении влияния штаммов почвенных актинобактерий Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 на урожай и поражаемость грибными, вирусными заболеваниями и насекомыми-вредителями растений огурца ( Cucumis sativus L.) при выращивании в закрытом грунте.
Ìåòîäèêà. Эксперименты выполняли в филиале ФГБУ Российский сельскохозяйственный центр по Астраханской области в 2019 году в условиях защищенного грунта. Теплица была оснащена светоустановками и капельной лентой для полива.
Исследования проводили на растениях огурца сорта Форвард, предназначенного для выращивания в теплицах. Это болезнестойкий партено-карпический гибрид с поздним сроком созревания — 60-65 сут. Культуру выращивали с марта по август. До начала плодоношения температура воздуха была не ниже 20 °C днем и 17-18 °C ночью, влажность составляла 80 %. В период плодоношения температура воздуха в теплице колебалась от 24-28 °C днем до 18-20 °C ночью, влажность составила 90 %. Контроль температуры и влажности проводили на гигрометре психрометрическом ВИТ-2 (ОАО «Термоприбор», Россия).
В работе использовали штаммы Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697, выделенные из засоленных почв в Астраханской области в 2013 году, в концентрации 109 КОЕ/мл. Растения огурца обрабатывали суспензией 3-суточных культур и суспензией из сухой биомассы, разведенной в стерильной дистиллированной воде в соотношении 1 мг/1 мл
Штаммы хранили при 4±2 ° С на скошенном крахмально-казеино-вом агаре следующего состава: растворимый крахмал — 10,0 г/л, казеин (без витаминов) — 0,30 г/л, KNO 3 — 2,0 г/л, MgSO 4 7H 2 O — 0,05 г/л, К 2 HPO 4 — 2,0 г/л, NaCl — 2,0 г/л, CaCO 3 — 0,02 г/л, FeSO 4 7H 2 O — 0,01 г/л, агар — 18,0 г/л (pH 7,0). Для получения суспензий штаммы выращивали в картофельной среде (отвар картофеля из расчета 200 г/л; рН 7,0) при 28 ° С на шейкере ПЭ-6500 («Экрос», Россия) при 120 об/мин в течение 3 сут. Сухую биомассу получали при высушивании суспензии 3-суточной культуры штаммов в ротационном испарителе IKA RV 10 digital (ООО «ЛабСПЕЙС», Россия) с досушиванием в термостате ТСО-1/80 СПУ (ООО «Стеримед», Россия) при 37 ° С в течение 1 сут.
Опыт проводили на естественном инфекционном фоне в двух повторностях с 6-кратными обработками по следующей схеме (33): полив под корень через 1 сут после высадки рассады в тепличный грунт в фазу 2-3 настоящих листьев; полив под корень в стадии активного роста растений через 8 сут после первой обработки; полив под корень в фазу цветения и бутонизации через 8 сут после второй обработки; опрыскивание в фазу образования завязи и молочной спелости через 14 сут после третьей обработки; опрыскивание в фазу активного плодоношения через 14 сут после четвертой обработки; опрыскивание в фазу сбора урожая через 14 сут после пятой обработки. Полив и опрыскивания проводили из расчета 10 мл на 1 растение. В каждом варианте учитывали по 16 растений.
Схема опыта включала 8 вариантов: 1 — положительный контроль (обработка эталонным биопрепаратом Фитоспорин-М (ПС), паста) (ООО «НВП «БашИнком», Россия); 2 — отрицательный контроль (обработка водопроводной водой); 3 — обработка суспензией штамма N. umidischolae RCAM04882; 4 — обработка суспензией штамма N. umidischolae RCAM04883; 5 — обработка суспензией штамма S. carpaticus RCAM04697; 6 — обработка суспензией из сухой биомассы штамма N. umidischolae RCAM04882; 7 — обработка суспензией из сухой биомассы штамма N. umidischolae RCAM04883; 8 — обработка суспензией из сухой биомассы штамма S. carpaticus RCAM04697. Фитоспорин-М (ПС) разводили с водопроводной водой согласно инструкции производителя.
Предшественниками растений огурца были томаты (Solanum lyco-persicum L.) сорта Гранд. Почву перед высадкой рассады дезинфицировали раствором медного купороса: 2 л готового раствора (50 г CuSO4/10 л воды) использовали для обрабатки почвы на площади 1 м2. Рассаду огурца получали в пластмассовых кассетах (по одному семени в каждой ячейке) при 25 °С (светоустановка Фитотрон ЛиА-2, «Аэромед», Россия). Рассаду на стадии развития 2-3 настоящих листьев высаживали на постоянное место произрастания с плотностью 2-3 растения на 1 м2 и интервалом между рядами 65-70 см. Температура почвы составляла 16-17 °С. Во время роста культуры стебель привязывали к вертикальной сетке, боковые плети обрезали на высоте 12-15 см. Полив проводили капельным способом с нормой 4,5-5 л на 1 растение водопроводной водой, прогретой до 26 °С. Сбор урожая начался 1 июня, дата последнего сбора — 31 августа. За весь период вегетации растений огурца проведено 13 сборов: 1 июня, 8 июня, 15 июня, 22 июня, 6 июля, 13 июля, 20 июля, 27 июля, 3 августа, 10 августа, 17 августа, 24 августа, 31 августа.
Инсектоакарицидную активность штаммов актинобактерий в отношении бахчевой тли Aphis gossypii Glov. и паутинного клеща Tetranychus urticae C.L. Koch , на растениях огурца учитывали на 3-и сут после третьей и четвертой обработок. Активность выражали в процентах с учетом гибели тест-объектов в контроле.
Пораженность растений вирусными инфекциями выявляли серологическим методом на стадии образования завязей (через 3 сут после третьей обработки) и созревания плодов (через 3 сут после четвертой обработки). Для диагностики вирусов методом иммунохимического анализа (ИХА) использовали иммунострипы марки Flashkits (« ImmunoStrip Test Kit», США) (34). Навески листа (0,15 г) исследуемого растения помещали в пакет с буфером и разминали. Используя тест-полоски, определяли наличие или отсутствие вируса. Противовирусную активность рассчитывали как процент от числа растений без симптомов.
Фитопатологическую оценку проводили согласно методическим рекомендациям (35, 36). Идентификацию фитопатогенных грибов проводили на базе филиала ФГБУ «Россельхозцентр» по Астраханской области методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией продуктов ПЦР в режиме реального времени с использованием микрочипового амплификатора нуклеиновых кислот АриаДНА (ООО «ЛЮМЭКС», Россия). ДНК из подготовленного растительного материала выделяли в соответствии с инструкцией к набору ДНК-сорб-B (ФГУН ЦНИИЭ Роспотребнадзора, Россия). Для идентификации фитопа-тогенных грибов использовали микрочипы с нанесенной лиофилизированной ПЦР-смесью. Время проведения ПЦР — 45 циклов (20 мин), 45 циклов (40 мин) при высокой скорости нагрева/охлаждения образцов (10-12 ° С/с). Результаты анализировали с помощью программного обеспечения микро-чипового амплификатора в режиме реального времени.
Урожай определяли, суммируя массу созревших плодов в каждом варианте.
Статистическую обработку данных выполняли с использованием пакетов программ Microsoft Excel 8, BioStat 2008, определяя средние значения показателей ( M ), стандартную ошибку средней (±SEM), доверительную вероятность, выполняли дисперсионный анализ.
Ðåçóëüòàòû . Влияние длительности культивирования на активность изученных штаммов актинобактерий и их биологические свойства были описаны ранее (37, 38). Штаммы проявляли фитостимулирующую, инсектицидную, антиоксидантную активность в лабораторных и полевых опытах (30, 39). На штамм S. carpaticus RCAM04697 в 2019 году получен патент, описывающий его ингибирующее влияние на насекомых-вредителей, грибные, вирусные болезни и стимуляцию роста томатов (30).
Средняя исходная (до третьей обработки) численность бахчевой тли на одном растении огурца в теплице составила от 30 до 35 особей, паутинного клеща — от 18 до 27 особей. Исследование инсектицидной активности штаммов актинобактерий показало, что максимальная (85,3 %) смертность бахчевой тли A. gossypii после четвертой обработки была зафиксирована при использовании суспензии 3-суточной культуры S. carpaticus RCAM04697, 520
минимальная (51,1 %) — при обработке суспензией из сухой биомассы штамма N. umidischolae RCAM04883 (рис. 1, А).
Оценка акарицидной активности штаммов актинобактерий показала аналогичные результаты. Наибольшее влияние на смертность паутинного клеща после четвертой обработки оказала суспензия 3-суточной культуры S. carpaticus RCAM04697 (69,2 %), наименьшее — суспензия из сухой биомассы штамма N. umidischolae RCAM04883 (40,7 %). Процент смертности T. urticae при остальных обработках колебался от 46,9 до 61,5 % (см. рис. 1, Б).
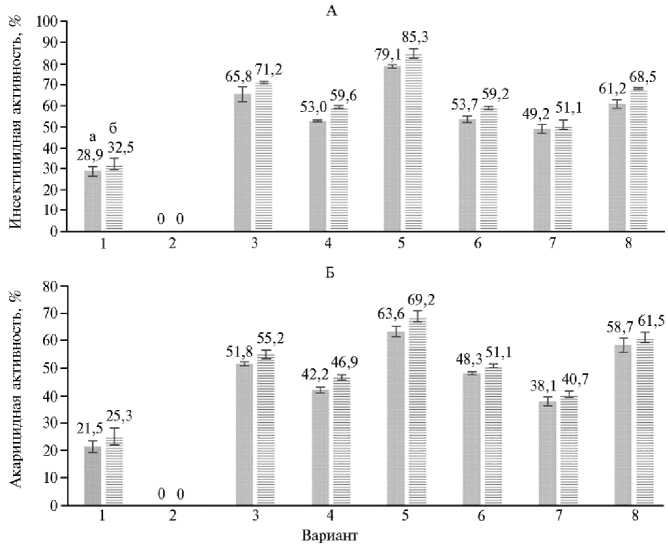
Рис. 1. Инсектицидная активность штаммов почвенных актинобактерий в отношении бахчевой тли Aphis gossypii (А) и акарицидная активность в отношении паутинного Tetranychus urticae (Б) после третьей (а) и четвертой (б) обработок огурца ( Cucumis sativus L.) сорта Форвард: 1 — положительный контроль, Фитоспорин-М (ПС), 2 — отрицательный контроль, водопроводная вода, 3 — суспензия 3-суточной культуры Nocardiopsis umidischolae RCAM04882, 4 — суспензия 3-суточной культуры N. umidischolae RCAM04883, 5 — суспензия 3-суточной культуры Streptomyces carpaticus RCAM04697, 6 — суспензия из сухой биомассы N. umidischolae RCAM04882, 7 — суспензия из сухой биомассы N. umidischolae RCAM04883, 8 — суспензия из сухой биомассы S. carpaticus RCAM04697 ( M ±SEM, N = 2, n = 16, опыт в закрытом грунте, филиал ФГБУ Российский сельскохозяйственный центр по Астраханской области, 2019 год).
Высокий показатель инсектоакарицидной активности можно обосновать присутствием вторичных метаболитов актинобактерий, которые обладают токсичным действием в отношении насекомых-вредителей (40, 41). Актинобактерии служат продуцентами различных алкалоидов с противо-микробным и инсектицидным действием (42). В литературе описано ингибирующее влияние алкалоидов растительного и микробного происхождения на насекомых-вредителей (43, 44).
Обработка суспензией из сухой биомассы слабее влияла на смертность тли и паутинного клеща, чем обработка суспензией 3-суточных культур, во всех вариантах опыта после третьей и четвертой бактеризации. Возможно, при высыхании и повторном увлажнении активность вторичных метаболитов, антагонистически воздействующих на вредителей, снижалась.

Рис. 2. Листья растений огурца ( Cucumis sativus L.) сорта Форвард при заражении вирусом огуреченой мозаики: А — отрицательный контроль (водопроводная вода), Б — обработка суспензией штамма Streptomyces carpaticus RCAM04697 (опыт в закрытом грунте, филиал ФГБУ Российский сельскохозяйственный центр по Астраханской области, 2021 год).
Условия теплицы благоприятны для многих инфекций в ризосфере, вызывающих болезни растений разной этиологии. При заражении ВОМ (CMV, Cucumber mosaic virus, Cucumovirus , Bromoviridae ) и ВМТо (ToMV, Tomato mosaic virus , Tobamovirus , Virgaviridae ) у растений огурца наблюдали деформацию листьев и значительную задержку роста (рис. 2). Исследуемые штаммы актинобактерий проявляли противовирусную активность в отношении ВОМ и ВМТо. Наибольшая противовирусная активность (100 %) была отмечена при обработке суспензией штамма S. carpaticus RCAM04697 (табл. 1). Однако следует отметить, что суспензия из сухой биомассы штамма RCAM04697 показала меньшую активность в отношении ВОМ (93,8 %) и ВМТо (81,3 %).
-
1. Противовирусная активность штаммов Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 на растениях огурца ( Cucumis sativus L.) сорта Форвард (опыт в закрытом грунте, филиал ФГБУ Российский сельскохозяйственный центр по Астраханской области, 2019 год)
|
Вариант |
Растений без симптомов |
|
|
всего |
% |
|
Вирус огуречной мозаики ВОМ
|
1 |
5 |
31,3 |
|
2 |
1 |
6,3 |
|
3 |
11 |
68,8 |
|
4 |
12 |
75,0 |
|
5 |
16 |
100,0 |
|
6 |
8 |
50,0 |
|
7 |
9 |
56,3 |
|
8 |
15 |
93,8 |
|
Вирус мозаики томата ВМТо |
||
|
1 |
7 |
43,8 |
|
2 |
2 |
12,5 |
|
3 |
10 |
62,5 |
|
4 |
9 |
56,3 |
|
5 |
16 |
100,0 |
|
6 |
6 |
37,3 |
|
7 |
7 |
43,8 |
|
8 |
13 |
81,3 |
Примечание. 1 — положительный контроль, Фитоспорин-М (ПС), 2 — отрицательный контроль, водопроводная вода, 3 — суспензия 3-суточной культуры Nocardiopsis umidischolae RCAM04882, 4 — суспензия 3-суточной культуры N. umidischolae RCAM04883; 5 — суспензия 3-суточной культуры Streptomyces carpaticus RCAM04697, 6 — суспензия из сухой биомассы N. umidischolae RCAM04882, 7 — суспензия из сухой биомассы N. umidischolae RCAM04883, 8 — суспензия из сухой биомассы S. carpaticus RCAM04697.
Следует отметить, что противовирусная активность суспензий 3-суточных культур RCAM04882 и RCAM04883 также оказалась выше, чем ак- тивность суспензией из их сухой биомассы. При заражении ВОМ в варианте с обработкой штаммом N. umidischolae RCAM04882 активность суспензии составила 68,8 %, а суспензии из сухой биомассы — 50,0 %, при заражении ВМТо — соответственно 62,5 и 37,3 %. В варианте с обработкой суспензией N. umidischolae RCAM04883 активность 3-суточной культуры на растениях огурца, зараженных ВОМ, составила 75,0 %, а суспензии из сухой биомассы — 56,3 %, однако при заражении ВМТо противовирусная активность этих суспензий была соответственно 56,3 и 43,8 %. Ранее противовирусную активность обнаружили у 3-суточных культур исследованных штаммов в лабораторных испытаниях на томатах, зараженных ВОМ (45). Л.Н. Григорян с соавт. (46) в полевых экспериментах на территории Астраханской области получили высокий урожай картофеля, зараженного Y- и X-вирусами картофеля и обработанного 3-суточной суспензией штамма S. carpaticus RCAM04697. Кроме того, штамм S. carpaticus RCAM04697 оказывал противовирусное действие на ВОМ и вирус мозаики томата, а также инсектицидное влияние на насекомых — переносчиков фитовирусов (30, 47).
Основные симптомы фузариоза проявились в нашем опыте в период цветения на нижних ярусах кустов в виде пожелтения листьев и покрытия их коричневыми пятнами. При развитии грибной инфекции стебли растений темнели, истончались и трескались, а завязи желтели и отмирали. Симптомы альтернариоза у исследуемых растений были изначально зафиксированы на нижних листьях (многочисленные сухие мелкие, до 2 см, пятна округлой формы желтовато-коричневой окраски со светлым участком посередине). Края пораженных участков листьев имели коричневую окраску. Из грибных фитопатогенов на растениях обнаружили Fusarium oxysporum L. и Alternaria infecta E.G. Simmons. Исследуемые штаммы проявляли фунгицидную активность по отношению к этим грибам. В положительном контроле при обработке фунгицидом Фитоспоринои-М (ПС) было выявлено 10 % растений с фузариозом и 5 % — с альтернариозом. В отрицательном контроле обнаружили 15 % растений с симптомами фузариоза, и 10 % — с симптомами альтернариоза. В вариантах с бактеризацией штаммами актинобактерий симптомы этих болезней полностью отсутствовали. Следовательно, изученные штаммы, независимо от способа их применения, проявляли фунгицидную активность.
И.И. Новикова с соавт. (48) описали штамм S. chrysomallus Р-21, выделенный из почвы Прибалтийского региона (Литва), который проявлял фунгицидные свойства в отношении фитопатогенного гриба Rhizoctonia solani и активность против вируса мозаики костра (49). В литературе отмечено, что актиномицеты могут активировать защиту растений в зависимости от инфицирующего агента (50). Изолированные из вермикомпоста актинобактерии усиливали активность ферментов пероксидазы, полифе-нолоксидазы и фенилаланинаммиачной лиазы в растениях томата, зараженных R . solani (51).
Фитостимулирующее влияние обработок штаммами актинобактерий оценивали по увеличению урожая растений огурца (рис. 3). Обработка штаммами стимулировала процесс роста и развития растений. Плоды у растений, обработанных штаммами N. umidischolae RCAM04882, N. umidischolae RCAM04883, S. carpaticus RCAM04697, оказались заметно большего размера, чем у растений в положительном и отрицательном контроле.
Разница в урожае в опытных и контрольных вариантах оказалась существенной. Наибольший урожай у растений огурца отмечали в варианте с обработкой суспензией 3-суточной культуры S. carpaticus RCAM04697, он составил 62,9 кг при урожае в остальных опытных вариантах 39,8-59,9 кг. В вариантах с обработкой растений суспензией штамма RCAM04882 урожай оказался на 12,0 %, RCAM04883 — на 5,5 %, RCAM04697 — на 4,8 % выше, чем при обработке суспензией из сухой биомассы.
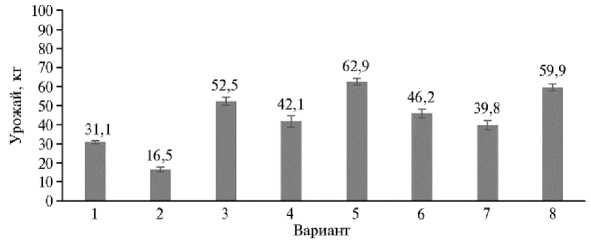
Рис. 3. Урожай растений огурца ( Cucumis sativus L.) сорта Форвард в зависимости от обработки штаммами почвенных актинобактерий: 1 — положительный контроль, Фитоспорин-М (ПС), 2 — отрицательный контроль, водопроводная вода, 3 — суспензия 3-суточной культуры Nocardiopsis umidischolae RCAM04882, 4 — суспензия 3-суточной культуры N. umidischolae RCAM04883; 5 — суспензия 3-суточной культуры Streptomyces carpaticus RCAM04697, 6 — суспензия из сухой биомассы N. umidischolae RCAM04882, 7 — суспензия из сухой биомассы N. umidischolae RCAM04883, 8 — суспензия из сухой биомассы S. carpaticus RCAM04697 ( M ±SEM, N = 2, n = 16, опыт в закрытом грунте, филиал ФГБУ Российский сельскохозяйственный центр по Астраханской области, 2019 год).
Результаты двухфакторного дисперсионного анализа данных показали, что вклад фактора «суспензия штамма» ( F = 92,62; Р ≥ 0,95) более чем в 9 раз превосходил вклад фактора «суспензия из сухой биомассы штамма» ( F = 9,83; Р ≥ 0,95) (табл. 2).
2. Дисперсионный анализ влияния штаммов актинобактерий Nocardiopsis umidis-cholae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 на урожай растений огурца ( Cucumis sativus L.) сорта Форвард (опыт в закрытом грунте, филиал ФГБУ Российский сельскохозяйственный центр по Астраханской области, 2019 год)
|
Источник варьирования |
SS 1 |
df 1 |
MS |
F |
p |
|
Суспензия 3-суточной культуры штамма (фактор А) |
422,64 |
2 |
211,32 |
92,62 |
0,0107* |
|
Суспензия из сухой биомассы штамма (фактор В) |
22,42 |
1 |
22,43 |
9,83 |
0,0884* |
Примечание. SS — сумма квадратов, df — число степеней свободы, MS — средние квадраты, F — критерий Фишера, p — уровень значимости.
* Влияние на варьирование признака достоверно при Р ≥ 0,95.
Вклад в варьирование урожая взаимодействия факторов «суспензия штамма» и «суспензия из сухой биомассы штамма» оценивался как существенный (Р ≥ 0,95), тогда как сам по себе фактор «суспензия из сухой биомассы штамма» не оказал значимого влияния на урожай растений огурца.
В целом, учет урожая показал высокий фитостимулирующий эффект обработок штаммами актинобактерий N. umidischolae RCAM04882 и S. carpaticus RCAM04697. Наибольшей биологической эффективностью обладал штамм бактерий S. carpaticus RCAM04697. Одной из причин увеличения урожая было подавление жизнедеятельности насекомых-вредителей и возбудителей инфекций исследуемыми штаммами. Применение суспензии 3-суточной культуры во всех вариантах обеспечивало повышенную защиту растений и урожай по сравнению с суспензией из сухой биомассы. Кроме того, в литературе описано усиление эффекта получения высокой урожайности при многократной, а не однократной обработке растений стрепто-мицетами, которую мы и применили в проведенном эксперименте (52).
Культуры закрытого грунта подвержены воздействию насекомых-вредителей и клещей, в связи с чем фактор защиты растений имеет важное значение в реализации потенциала урожайности современных гибридов огурцов. Исследование биологической активности штаммов актинобактерий N. umidischolae RCAM04882, N. umidischolae RCAM04883, S. carpaticus RCAM04697 в тепличных условиях свидетельствуют о высоком ингибирующем действии в отношении распространенных на территории Астраханской области насекомых-вредителей, фитовирусов и фитопатогенных микро-мицетов, что доказывает их полифункциональность и перспективность для разработки биопрепаратов на их основе.
Очевидно, что с помощью подбора биотехнологических параметров и генетических манипуляций можно усилить ценные свойства исследуемых штаммов и использовать их в качестве продуцентов метаболитов с поли-функциональными свойствами. Представители актинобактерий высокотехнологичны и соответствуют требованиям, предъявляемым к микроорганизмам при получении биопрепаратов для интродукции в агробиоценоз (53-55).
Таким образом, при обработке растений огурца сорта Форвард суспензией штаммов почвенных актинобактерий Nocardiopsis umidischolae RCAM04882, N. umidischolae RCAM04883, Streptomyces carpaticus RCAM04697 наибольшую противовирусную активность (100 %) наблюдали при обработке суспензией 3-суточной культуры S. carpaticus RCAM04697. Однако суспензия из сухой биомассы штамма RCAM04697 показала более низкую эффективность в отношении вируса огуречной мозаики (93,8 %) и вируса мозаики томата (81,3 %). Максимальная (85,3 %) смертность бахчевой тли Aphis gossypii после четвертой обработки была зафиксирована при использовании суспензии 3-суточной культуры S. carpaticus RCAM04697. Наибольшее влияние на смертность паутинного клеща после четвертой обработки также оказала суспензия 3-суточной культуры S. carpaticus RCAM04697 (69,2 %). В вариантах с бактеризацией штаммами актинобактерий симптомы альтернариоза и фузариоза болезней полностью отсутствовали. Следовательно, исследуемые штаммы, независимо от способа их применения, проявляли фунгицидную активность. Наибольший урожай растений огурца был отмечен в варианте с обработкой суспензией 3-суточной культуры S. carpaticus RCAM04697 и составил 62,9 кг. Проведенные исследования подтвердили высокую значимость поиска новых актинобактерий, продуцирующих биологически активные вещества с широким спектром биологической эффективности, обладающих инсектоакарицидными и фитостимулирующими свойствами, применение которых способно сдерживать распространение вирусных и грибных фитопатогенов.


