Биологическая эффективность синтетических антиоксидантов
Автор: Клепикова С.Ю., Карабинцева Н.О., Лебедева Т.А., Просенко А.Е., Колесникова О.П.
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Коррекция экологического неблагополучия. Продукты питания
Статья в выпуске: 1-8 т.12, 2010 года.
Бесплатный доступ
В данной статье рассмотрена взаимосвязь антиоксидантных и иммунотропных свойств новых водорастворимых серосодержащих антиоксидантов.
Антиоксидантная активность, иммунодепрессанты, фенольные соединения
Короткий адрес: https://sciup.org/148199217
IDR: 148199217 | УДК: 615.27/.28:547.56
Biological efficiency of synthetic antioxidants
In given article the interrelation between antioxidatiand immunotropic properties of new water-soluble sulphur-containing antioxidants is surveyed.
Текст научной статьи Биологическая эффективность синтетических антиоксидантов
Универсальное значение иммунной и антиоксидантной систем обуславливают необходимость изучения конкретных механизмов их взаимосвязи. Исходя из анализа работ отечественных и зарубежных ученых по изучению антиоксидантной активности и имму-нотропности синтетических антиоксидантов, биологическая значимость поиска новых форм водорастворимых фенольных антиоксидантов очевидна и актуальна.
В настоящей работе приведены результаты исследования антиоксидантной и имму-нотропной активности новых водорастворимых серосодержащих фенольных соединений, синтезированных на основе производных бромзамещенных алкилфенолов [4].
Учитывая, что фенольные соединения проявляют свойства антиоксидантов и способны тормозить цепное окисление органических соединений [1], антиоксидантную активность определяли манометрическим методом, в основу которого положена модельная реакция инициирования окисления субстрата [5]. В качестве эталона сравнения использовали известный водорастворимый монофункциональный антиоксидант фенозан калия (ФК) [6]. Нами установлено, что активность феноксиль-ных радикалов в реакциях свободнорадикального окисления липидного субстрата в водноэмульсионной среде увеличивается с уменьшением количества и объема алкильных заместителей фенольного кольца (рис. 1), чем и объясняется снижение антиоксидантной активности в ряду полученных соединений. Соединения, в орто-положениях которых не содержатся алкильные заместители, в условиях инициированного окисления метилолеата имеют близкие значения периодов индукции с соединениями, в структуре которых присутствует одна трет-бутильная группа и существенно уступают по антиоксидантной активности соединениям содержащим две трет-бутильные группы в орто-положении. Присутствие в ионогенном фрагменте бивалентного атома серы, способствует усилению антиоксидантных свойств полученных соединений, так называемый эффект синергизма, обусловленный анти- радикальной активностью фенольной ОН-группы и противопероксидной активностью ионогенного тиосульфонатного фрагмента. Тиосульфонатные производные, имеющее в своей структуре две мети- или трет-бутильные группы, существенно превосходят по своей способности тормозить окисление метилолеата монофункциональный антиоксидант (ФК).
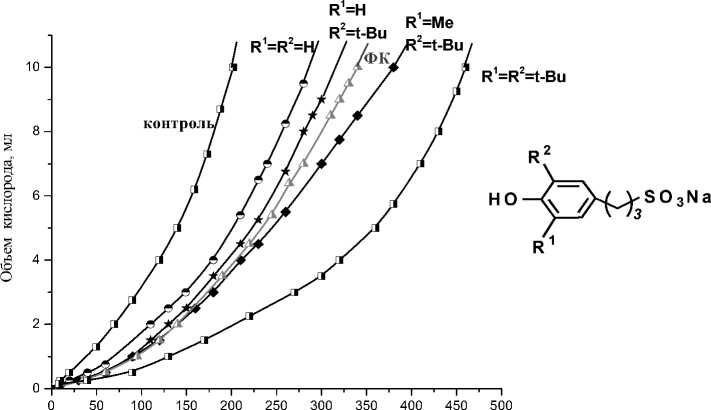
Время, мин
Рис. 1. Кинетические кривые окисления метилолеата в вводно-эмульсионной среде в присутствии ряда соединений с разной степенью пространственной затрудненности PhOH
(60 ° С, [ArOH] = 2мМ, [Cu2+] = 5мМ)
Тестирование антиоксидантной активности полученных соединений также проводили на модели медь-индуцированного окисления липопротеинов низкой плотности [6]. Об эффективности антиоксидантного действия соединений судили по их концентрации, обуславливающей 50% ингибирование накопления малонового диальдегида (LD50) после 30 мин инкубации с ионами металла. В качестве эталона сравнения использовали структурные аналоги тиосульфонатных производных фенолов, ионол и ФК. Было показано (рис. 2), что антиоксидантная активность в ряду полученных соединений также возрастает по мере увеличения степени экранирования фенольной ОН-группы, при этом наличие ионогенном фрагменте бивалентного атома серы способствует усилению антиоксидантных свойств полученных соединений. Как видно из рис. 2, в концентрации 50% ингибирования накопления малонового диальдегида у неэкранированных фенолов выше 160 мкМ, а для пространственно-затрудненных фенолов LD50 составляет всего несколько мкМ. Соединения с двумя трет-бутильными группами по антиоксидантной активности близки к ионолу и превосходят соответствующий по строению ФК.
Таким образом, более эффективными ингибиторами инициированного окисления субстрата оказались орто- ди-замещенные тио-сульфонатные производные фенольных соединений. Учитывая данный факт, была проведена оценка иммунотропных свойств по способности соединений подавлять развитие аутоиммунного заболевания – иммунокомплексный гломерулонефрит. С этой целью хроническое воспаление у мышей самок вызывали двукратным введением лимфоидных клеток от самок родительской линии DBA/2 [9]. За появлением протеинурии начинали следить с 6 недели от начала индукции воспаления.
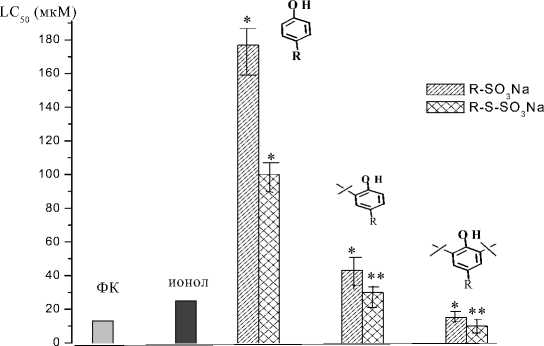
Примечание : достоверно по отношению к контролю *- р < 0,05; ** - р < 0,01; *** - р < 0,001
Рис. 2. Диаграмма значений ингибирования окисления ЛНП в присутствии водорастворимых фенольных антиоксидантов при 60 ° С, [Си2+] = 5 мМ
Содержание белка в моче определяли колориметрически с красителем Kumasi brillant blu (Loba Feinchemie) с помощью Titetrik Multiskan, длина волны λ 570 нм. В опытах использовали мышей со стойкой протеинурией (уровень белка в моче 3 мг/мл и более) на 2-3, 6-7 и 9 месяце заболевания. Введение тестируемых соединений на фоне заболевания осуществляли в два этапа. Первый курс составил 5 инъекций внутрибрюшинно через день. Дозы подобраны экспериментально и соответствуют максимально переносимым дозам у мышей на массу тела и клеточность органов. Перерыв между курсами составил 3 дня. После первого и второго курса на следующий день измеряли протеинурию. Как видно из данных, представленных в табл. 1, оба соединения после 1-го курса лечения не оказывали эффекта, а после 2-го курса наблюдается достоверный эффект действия обоих соединений: снижение протеинурии наблюдалось соответственно на 32% и 43%.
Таблица 1. Влияние курсового введения соединений протеинурию у мышей B6D2F1 с иммунокомплексным гломерулонефритом
|
Водорастворимые фенольные антиоксиданты |
Белок в моче (мг/мл) |
|||||
|
до лечения |
% |
после 5-кратного введения |
% |
после 10-кратного введения |
% |
|
|
HO SO 3 Na 3 (35 мг/кг) |
6,32±0,30 |
100 |
6,47±0,44 |
102 |
4,31±0,35** |
68 |
|
HO 3 SO 3 Na (200 мг/кг) |
6,65±0,75 |
100 |
5,53±0,27* |
83 |
3,82±0,82** |
57 |
Примечание : достоверно по отношению к контролю *- р < 0,05; ** - р < 0,01; *** - р < 0,001.
Выводы: тиосульфонатные производные, представляющие собой новые формы класса пространственно-затрудненных фенолов, обладающие гидрофильными свойствами и выраженной антиоксидантной активностью, по сравнению со своими структурными аналогами и известным антиоксидантом – фенозаном калия в отношении окисления эфиров олеиновой кислоты в водно-эмульсионной среде, а также Си2+-индуцированном окислении ЛНП, проявившие противовоспалительное действие на модели иммунокомплексного гломерулонефрита, являются перспективными веществами для дальнейшего изучения имму-нотропных свойств.
Список литературы Биологическая эффективность синтетических антиоксидантов
- Зенков, Н.К. Окислительный стресс/Н.К. Зенков, В. Ланкин, Е.Б. Меньщикова. -М.: Наука, 2001. С. 15-93.
- Утешев, Б.С. Иммуномодулирующее и антиоксидантное действие витаминов А и Е при воздушном и иммерсионном охлаждении/Б.С. Утешев, Н.А. Быстрова, И.Л. Бровкина и др.//Эксперим. и клинич. фармакол. 2001. Т.64, № 1. С. 60-63.
- Ланкин, В.З. Свободнорадикальные процессы в норме и при заболеваниях сердечно-сосудистой системы/В.З. Ланкин, А.К. Тихазе, Ю.Н. Белен ков//Антиоксиданты в комплексной терапии атеросклероза: pro et contra. -М.: Наука, 2003. С. 25-53.
- Кандалинцева, Н.В. Направленный синтез водорастворимых антиоксидантов с бифункциональным механизмом противоокислительного дейст вия: Матер. VI Междунар. конф. «Биоантиоксидант»/Н.В. Кандалинцева, О.И. Дюбченко, С.Ю. Клепикова и др. -М., 2002. С. 232-234.
- Цепалов, В.Ф. Определение констант скорости и коэффициентов ингибирования фенолов антиоксидантов с помощью модельной цепной реакции/В.Ф. Цепалов, А.А. Харитонов, Г.П. Гладышев и др.//Кинетика и катализ. 1977. Т. 18. С. 1261-1267.
- Орехович, В.Н. Современные методы в биохимии/В.Н. Орехович. -М.: Мир, 1997. С. 533-537.
- Пенков, М.П. Иммунотропная активность бетакаротина и аскорбиновой кислоты/М.П. Пенков -Автореф. дис.. канд. мед. наук. -М., 2001. 22 с.
- Delta Fuente, M. Antioxidants of immunomodulatory activity/М. Delta Fuente, V. M. Victor//Immunol. and Cell-Biol. 2000. Vol. 78, № 1. P. 49-54.
- Gao, X. Immunomodulatory activity of resveratrol: discrepant in vitro and in vivo immunological effects/Х. Gao еt al.//Biochem Pharmacol. 2003. Vol. 15, № 12. Р. 2427-2435.


