Биологические особенности и методы выявления и идентификации возбудителя бактериального увядания (вилта) кукурузы Pantoea stewartii subsp. stewartii (Smith) Mergaert et al. (обзор)
Автор: Клименко Н.С., Верещагина А.Б., Гандрабур Е.С.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Обзоры, проблемы
Статья в выпуске: 1 т.61, 2026 года.
Бесплатный доступ
Черемухово-злаковая тля Rhopalosiphum padi L. — важный вредитель злаковых культур. Этот вид может вызывать значительные экономические потери в сельском хозяйстве, из-за чего представляет интерес для активного изучения. Высокая экологическая адаптивность R. padi обусловлена особенностями ее жизненного цикла и усложняет борьбу с этим вредителем (A.F.G. Dixon, 1976; A.B.M. Austin с соавт., 1996; A.A. Hoffmann с соавт., 2008; C.-A. Dedryver с соавт., 2010; S. Macfadyen с соавт., 2012; M. Savaris с соавт., 2013). Изучение генетического разнообразия R. padi имеет ключевое значение для успешного менеджмента популяций вредителя. Для контроля состояния популяций тлей сначала использовали только фенотипические методы, но разработка и дополнение их молекулярно-генетическими методами открыли новые возможности и позволили значительно ускорить анализ разнообразия R. padi. Цель настоящей публикации состояла в обзоре молекулярно-генетических подходов, применяемых для изучения популяционной структуры Rhopalosiphum padi за рубежом, поскольку аналогичные работы в России пока единичны. Научная новизна работы состоит в комплексном рассмотрении различных подходов — от классических методов аллозимного полиморфизма до современных геномных технологий — и оценке их информативности для изучения генетического разнообразия вредителя. В последние десятилетия для молекулярных исследований R. padi стали применять молекулярные методы, такие как аллозимный и рестрикционный анализы, RAPD-маркеры, SSR-генотипирование и секвенирование (F. Delmotte с соавт., 2001; I. Valenzuela с соавт., 2010; R. Rakauskas с соавт., 2014; A. Gilabert с соавт., 2015; X. Duan с соавт., 2016; W. Sun с соавт., 2022; J. Guo с соавт., 2023). Аллозимный анализ показал низкое аллельное разнообразие соответствующих локусов R. padi, что снижает его пригодность для определения генетической структуры популяций тли (H.D. Loxdale, C.P. Brookes, 1990; P.D.N. Hebert с соавт., 1991; Simon J.-C. с соавт., 1995). По результатам рестрикционного анализа митохондриальной ДНК была обнаружена связь между вариантами жизненного цикла R. padi и гаплотипами мтДНК, однако этот метод также оказался недостаточным для изучения генетического разнообразия тли по причине низкого уровня установленного с его помощью полиморфизма (D.A. Martinez-Torres с соавт., 1996, 1997; J.-C. Simon с соавт., 1996; F. Delmotte с соавт., 2001). RAPD-анализ, хотя и обладает преимуществом универсальности, поскольку не требует точного знания последовательности ДНК объекта, но показал невысокий уровень полиморфизма этого типа маркеров (S.R. Bulman с соавт., 2005; J.-C. Simon с соавт., 1996; D. Martinez-Torres с соавт., 1997; R.M. Tabikha с соавт., 2016). Популярным методом для изучения популяций R. padi стало SSR-генотипирование вследствие сравнительно лучшей дифференцирующей способности маркеров и более высокого полиморфизма выбранных локусов (F. Delmotte с соавт., 2001, 2002; A. Gilabert с соавт., 2009, 2015; I. Valenzuela с соавт., 2010; X. Duan с соавт., 2016; M.E. Rubio-Meléndez с соавт., 2019). В настоящей публикации особое внимание уделено современным подходам, основанным на секвенировании отдельных генов (COI, COII, ND4, Cytb, EF-1α) и полногеномных данных. Секвенирование участков отдельных генов открыло новые возможности для исследований, позволяя выявлять различия на уровне отдельных нуклеотидов (C. Simon с соавт., 1994; M. Harry с соавт., 1998; J. Turčinavičienė с соавт., 2006; I. Valenzuela с соавт., 2010; R. Rakauskas с соавт., 2014; K. Wang с соавт., 2018; Н.В. Алпатьева с соавт., 2022; W. Sun с соавт., 2022; J. Guo с соавт., 2023; Е.Е. Радченко, с соавт., 2024). Полное секвенирование генома R. padi дает исчерпывающую информацию о генетическом разнообразии тли, но остается трудоемким и мало распространенным (R. Morales-Hojas с соавт., 2020; P. Thorpe с соавт., 2018). В то же время обнародование первой аннотированной полногеномной последовательности ядерной ДНК R. padi, опубликованной в базе NCBI (ASM2088224v1) китайскими учеными, открывает новые перспективы для сравнительных популяционных исследований данного организма (China Agricultural University, г. Пекин, Китай). Ряд авторов успешно комбинировали различные молекулярные методики, например SSR-анализ и секвенирование гена COI или рестрикцию митохондриальной ДНК с RAPD-маркерами, что повысило точность и информативность результатов (I. Valenzuela с соавт., 2010; J.-C. Simon с соавт., 1996). В целом, анализ современных молекулярно-генетических методов и результатов их использования для изучения популяционной структуры R. padi за рубежом служит основанием для проведения подобных работ в России с целью генетического контроля адаптивной изменчивости вредителя.
Rhopalosiphum padi, генетическая структура популяций, молекулярно-генетические методы, аллельный полиморфизм
Короткий адрес: https://sciup.org/142247327
IDR: 142247327 | УДК: 632.2:595.752.2:632.911.2:575.2 | DOI: 10.15389/agrobiology.2026.1.3rus
Molecular approaches to studying genetic diversity of the bird cherry-cereal aphids Rhopalosiphum padi L. (review)
The bird cherry-oat aphid Rhopalosiphum padi L. is an important pest of cereal crops. This species can cause substantial economic losses in agriculture and therefore represents a subject of intensive research. The high ecological adaptability of R. padi, determined by specific features of its life cycle, significantly complicates pest control strategies (A.F.G. Dixon, 1976; A.B.M. Austin et al., 1996; A.A. Hoffmann et al., 2008; C.-A. Dedryver et al., 2010; S. Macfadyen et al., 2012; M. Savaris et al., 2013). The study of genetic diversity in R. padi is of key importance for effective pest population management. Initially, aphid population monitoring relied exclusively on phenotypic methods; however, the development and subsequent integration of molecular genetic approaches have opened new opportunities and substantially accelerated the analysis of R. padi diversity. The aim of the present study was to review molecular genetic approaches used abroad to investigate the population structure of Rhopalosiphum padi, as similar studies in Russia remain scarce. The scientific novelty of this work lies in a comprehensive assessment of a wide range of methods—from classical allozyme polymorphism analyses to modern genomic technologies—and in evaluating their informativeness for studying the genetic diversity of this pest. Over recent decades, molecular methods such as allozyme and restriction analyses, RAPD markers, SSR genotyping, and sequencing have been increasingly applied in studies of R. padi (F. Delmotte et al., 2001; I. Valenzuela et al., 2010; R. Rakauskas et al., 2014; A. Gilabert et al., 2015; X. Duan et al., 2016; W. Sun et al., 2022; J. Guo et al., 2023). Allozyme analysis revealed low allelic diversity at the corresponding loci in R. padi, which limits its suitability for resolving the genetic structure of aphid populations (H.D. Loxdale & C.P. Brookes, 1990; P.D.N. Hebert et al., 1991; J.-C. Simon et al., 1995). Restriction analysis of mitochondrial DNA demonstrated an association between life-cycle variants of R. padi and mtDNA haplotypes; however, this method also proved insufficient for comprehensive assessment of aphid genetic diversity due to the low level of polymorphism detected (D.A. Martinez-Torres et al., 1996, 1997; J.-C. Simon et al., 1996; F. Delmotte et al., 2001). RAPD analysis, despite its advantage of universality and the absence of a requirement for prior knowledge of DNA sequences, likewise showed a low level of polymorphism in these markers (S.R. Bulman et al., 2005; J.-C. Simon et al., 1996; D. Martinez-Torres et al., 1997; R.M. Tabikha et al., 2016). SSR genotyping has become a widely used method for studying R. padi populations due to its comparatively higher discriminatory power and increased polymorphism of selected loci (F. Delmotte et al., 2001, 2002; A. Gilabert et al., 2009, 2015; I. Valenzuela et al., 2010; X. Duan et al., 2016; M.E. Rubio-Meléndez et al., 2019). In the present study, particular attention is given to modern approaches based on sequencing of individual genes (COI, COII, ND4, Cytb, EF-1α) and whole-genome data. Sequencing of specific gene fragments has provided new research opportunities by enabling the detection of differences at the level of individual nucleotides (C. Simon et al., 1994; M. Harry et al., 1998; J. Turčinavičienė et al., 2006; I. Valenzuela et al., 2010; R. Rakauskas et al., 2014; K. Wang et al., 2018; N.V. Alpatyeva et al., 2022; W. Sun et al., 2022; J. Guo et al., 2023; E.E. Radchenko et al., 2024). Whole-genome sequencing of R. padi provides comprehensive information on aphid genetic diversity but remains labor-intensive and is still not widely applied (R. Morales-Hojas et al., 2020; P. Thorpe et al., 2018). At the same time, the publication of the first annotated nuclear genome sequence of R. padi in the NCBI database (ASM2088224v1) by Chinese researchers (China Agricultural University, Beijing, China) opens new perspectives for comparative population studies of this species. Several authors have successfully combined different molecular techniques, such as SSR analysis with COI gene sequencing or mitochondrial DNA restriction analysis with RAPD markers, thereby increasing the accuracy and informativeness of the results (I. Valenzuela et al., 2010; J.-C. Simon et al., 1996). Overall, analysis of modern molecular genetic methods and their application in studies of the population structure of R. padi abroad provides a solid foundation for conducting similar research in Russia aimed at genetic monitoring of the pest’s adaptive variability.
Текст научной статьи Биологические особенности и методы выявления и идентификации возбудителя бактериального увядания (вилта) кукурузы Pantoea stewartii subsp. stewartii (Smith) Mergaert et al. (обзор)
Черемухово-злаковая тля Rhopalosiphum padi L. (Hemiptera: Sternor-rhyncha: Aphididae) относится к важным вредителям злаковых культур (1-4). Ущерб посевам, наносимый этими насекомыми, связан с повреждением тканей растений из-за сосущего типа питания R. padi , высокой скоростью размножения и расселения тли (5, 6), а также переносом вирусов — возбудителей многих заболеваний, в том числе желтой карликовости ячменя (79). Высокой экологической адаптивности этого вредителя способствует сложный тип жизненного цикла, включающего партеногенетическое и обоеполое размножение (голоциклия) (10-13).
Партеногенез (существование популяций в виде клонов) тли обеспечивает быстрое нарастание численности и имеет место с весны до осени на злаковых растениях, тогда как осенью на первичном хозяине, черемухе Prunus padus L., появляется половое поколение R. padi , происходит спаривание и откладка яиц (14-17). Также существуют регионы, где черемуховозлаковая тля утратила обоеполое размножение (анголоциклия) и круглый год размножается партеногенетически на злаках (18-21). Иногда голоциклические и анголоциклические популяции R. padi могут даже сосуществовать в одной местности (22-24).
В условиях современных трансформаций в климате, флористическом разнообразии природных и антропогенных ландшафтов важны исследования генетического разнообразия насекомых-вредителей для снижения вызванных ими потерь урожая (25-28). Для контроля состояния популяций фитофагов, в том числе тлей, сначала использовали только фенотипирова-ние, включающее определение демографических показателей (29-32), однако не все популяционные изменения можно проследить таким образом. Добавление молекулярно-генетических методов к фенотипическим значительно повысило информативность исследований о процессах, происходящих в популяциях сосущих насекомых (33-36). Кроме того, благодаря повсеместному распространению, высокой скорости воспроизведения и небольшому числу хромосом R. padi служит удобным объектом для изучения генетического полиморфизма тлей (37). В настоящее время не вызывает сомнений необходимость получения информации об особенностях пищевых связей и эколого-географической структуре различных популяций этого вида.
В представленной публикации мы сравниваем молекулярно-генетические методы, используемые исследователями из разных стран для изучения генетического разнообразия Rhopalosiphum padi.
Научная новизна работы состоит в комплексном рассмотрении различных подходов (от классических методов аллозимного полиморфизма до современных геномных технологий) и оценке их информативности для изучения генетического разнообразия вредителя.
Аллозимный анализ. Работам по изучению генетического разнообразия тлей с использованием молекулярно-генетических методов предшествовали попытки аллозимного анализа (38-41). Этот метод основан на свойствах аллозимов — молекулярных форм определенного фермента, синтез которых контролируется разными аллелями одного гена. К преимуществам аллозимов относится то, что они являются кодоминантными, следо- вательно, с помощью белкового электрофореза можно обнаружить все продукты экспрессии соответствующих аллелей (42, 43).
Однако при работе с аллозимами у тлей, включая R. padi , исследователи столкнулись с проблемой низкого аллельного разнообразия соответствующих локусов (44-47), что затрудняет определение структуры популяций и указывает на необходимость использования других, например молекулярных, маркеров, которые могут выявить скрытую изменчивость на уровне последовательности ДНК (48, 49).
Рестрикционный анализ митохондриальной ДНК. Следующим способом, который был использован для изучения популяционной структуры R. padi , стал рестрикционный анализ ДНК (50-53). В отличие от аллозимного метода, исследование полиморфизма длин фрагментов, получающихся с помощью ферментов-рестриктаз (эндонуклеаз), позволяет анализировать последовательность ДНК тли (54-57). Особенно показателен для отслеживания недавней эволюционной истории вида R. padi , включая моменты интродукции в новые места обитания, полиморфизм митохондриальной ДНК (мтДНК), наследуемой по материнской линии (51-53, 58).
Рестриктазами обрабатывали как целую фракцию мтДНК (50, 51), так и сегмент митохондриального генома длиной 2200 п.н., включающий ген субъединицы 1 гена НАД-дегидрогеназы (ND1) и части генов 16S и цитохрома b (52, 53, 58). Показано, что за немногочисленными исключениями неполному жизненному циклу соответствовал один гаплотип мтДНК (авторы обозначали его как hI), а полному жизненному циклу — другой (hII) (51-53, 58). Стоит отметить, что в литературе сообщалось также об идентификации этим методом у голоциклических популяций минимально отличимых от hII гаплотипов — hIII и hIV, суммарная доля которых не превышала 7 % от объема изученной выборки и которые учитывали вместе со вторым гаплотипом (51-53).
Таким образом, с помощью рестрикционного анализа была показана связь между типом жизненного цикла и типом мтДНК у R. padi (51-53, 58). Интересно, что из 16 протестированных эндонуклеаз J.-C. Simon с соавт. (52) отметили два фермента рестрикции (EcoRI, SspI) как достаточные для различения гаплотипов у R. padi в амплифицированном участке мтДНК длиной 2200 п.н. Это заключение позволило сократить перечень рестриктаз, задействованных для определения гаплотипа мтДНК (53, 58).
Из сложившейся закономерности выбивались клоны с неполным жизненным циклом, неожиданно отнесенные к гаплотипу hII. Согласно данным литературы, причины могли быть следующими: вторичная потеря полового процесса среди голоциклических линий из-за мутации в локусе, контролирующем производство половых самок; возможность периодического потока ядерных генов между голоциклическими и неполноциклыми популяциями (последние в таком случае называют андроциклическими из-за иногда появляющихся в их составе самцов) (51-53).
Несмотря на пользу от обнаружения связи между вариантами жизненного цикла R. padi и гаплотипами мтДНК, для изучения генетического разнообразия тли рестрикционный анализ оказался явно недостаточным вследствие низкого установленного с его помощью полиморфизма —максимум четыре гаплотипа (51-53, 58). В более поздних исследованиях рестрикционный анализ мтДНК использовался как дополнение к методикам, основанным на принципах полимеразной цепной реакции (ПЦР) (58).
SSR- генотипирование. С распространением метода ПЦР SSR-генотипирование (simple sequence repeats) стало мощным инструментом, широко применяемым для изучения генетической структуры популяций различных видов тлей-вредителей, например Sitobion miscanthi Takahashi (59), Sitobion avenae Fabricius (60, 61), Aphis gossypii Glover (61, 62), Myzus persicae Sulzer (63), Diuraphis noxia Kurdjumov (64) и т.д. Для изучения генетического разнообразия R. padi J.-C. Simon с соавт. (65) — исследователи из Франции разработали маркеры 11 микросателлитных локусов ядерной ДНК, из которых после апробации на 55 партеногенетических линиях были отобраны восемь наиболее полиморфных: R5.29.b, R6.3 (1-я хромосома), R1.35, R5.10, R5.138 (2-я хромосома), R3.171, R5.50 (3-я хромосома), R2.73 (4-я хромосома).
Разработчики особо подчеркнули высокую чувствительность отобранных SSR-маркеров, которые позволили обнаружить несколько копий одних и тех же генотипов R. padi в анализируемой выборке, что подтверждает значимость микросателлитов в популяционно-генетических исследованиях партеногенетических организмов (65). Примечательно, что маркеры из этого набора в настоящее время наиболее часто используются для мик-росателлитного генотипирования популяций R. padi из разных стран — Франции (49, 58, 66, 67), Китая (68), Австралии (19), Чили (21) (табл. 1).
В то же время в литературе имеются сведения об изучении популяционного разнообразия R. padi с использованием указанного выше набора из восьми SSR-маркеров не в полном составе (19, 68) или в сочетании с маркерами, разработанными другими авторами (49, 58, 66, 67). Следует отметить, что существуют данные о возможных методических проблемах при работе с некоторыми маркерами из набора J.-C. Simon с соавт. (65), например R1.35, R6.3 и R5.138 (21, 69) (см. табл. 1).
Кроме того, в дополнение к упомянутым восьми маркерам для генотипирования популяций R. padi могут быть применены SSR-маркеры S17b и S16b (59), разработанные с использованием генетического материала тли S. miscanthi (49, 61) (см. табл. 1).
На примере популяции R. padi , собранной во Франции, F. Delmotte с соавт. (49) наглядно продемонстрировали преимущество использования рассмотренных SSR-маркеров (61, 65) по сравнению с аллозимными: число детектированных аллелей микросателлитных маркеров варьировало от 4 до 25 на локус (см. табл. 1), тогда как аллозимные маркеры были менее полиморфными (2-4 аллеля на локус). В общей сложности во всех семи изученных SSR-локусах был идентифицирован 81 аллель, а в четырех аллозимных локусах — 13 аллелей.
По результатам секвенирования транскриптома R. padi исследователи из Китая (70) разработали еще ряд SSR-маркеров. В итоге авторы отобрали 14 наиболее полиморфных микросателлитных локусов, которые были задействованы для генотипирования популяций R. padi (по 12 партеногенетических клонов) из четырех провинций Китая (70) (табл. 2). Однако широкого распространения эти маркеры пока не приобрели.
В целом, в настоящее время для изучения генетического разнообразия R. padi доступны маркеры 24 микросателлитных локусов, большая часть из которых (10 локусов) находится на 2-й хромосоме (59, 65, 70) (см. табл. 1, 2). К сожалению, не во всех работах, где они были задействованы, исчерпывающе описаны результаты применения этих SSR-маркеров (см. табл. 1). Такая ситуация затрудняет оценку информативности маркеров микроса-теллитных локусов для генетических исследований.
-
1. ДНК-маркеры SSR локусов, разработанные J.-C. Simon с соавт. (65) и A. Wilson с соавт. (59) , и использованные в работах по изучению генетического разнообразия Rhopalosiphum padi L.
-
2. ДНК-маркеры SSR локусов, разработанные X. Duan с соавт. (70) и использованные для изучения четырех китайских популяций Rhopalosiphum padi L.
Место сбора
Показатель
Локус, номер хромосомы, диапазон размеров детектированных фрагментов, п.н.
RP06
RP24
RP30
RP43
RP08
RP13
RP14
RP23
RP31
RP48
RP42
RP45
RP22
RP60
1-я
1-я
1-я
1-я
2-я
2-я
2-я
2-я
2-я
2-я
3-я
3-я
4-я
4-я
148-168
146-166
144-168
120-140
133-153
146-166
146-166
150-170
143-167
141-165
129-149
125-145
147-171
145-172
п. Ганьсу N a 7 2 3 3 3 4 4 5 5 3 7 5 4 2
PIC 0,67 0,36 0,47 0,34 0,43 0,56 0,48 0,64 0,63 0,42 0,76 0,66 0,54 0,38
п. Шэньси N a 6 3 2 4 2 5 3 6 4 3 9 6 5 4
PIC 0,73 0,41 0,35 0,43 0,37 0,57 0,31 0,64 0,63 0,40 0,77 0,61 0,75 0,43
п. Хубэй N a 5 2 3 3 2 3 3 4 4 3 6 3 4 4
PIC 0,49 0,38 0,34 0,34 0,37 0,48 0,48 0,64 0,60 0,41 0,64 0,47 0,59 0,52
п. Гирин N a 5 2 3 4 3 4 2 5 5 4 4 6 5 3
PIC 0,58 0,28 0,45 0,22 0,43 0,58 0,33 0,51 0,55 0,47 0,56 0,49 0,62 0,41
Примечание. N a — число выявленных аллелей в указанном локусе, PIC — информативность полиморфизма (polymorphism information content); п. — провинция.
-
3. ПЦР праймеры, применяемые для секвенирования отдельных участков генов с целью изучения генетического разнообразия Rhopalosiphum padi L. и других видов тлей
Ген
Разработчики праймеров
Названия прямого и обратного праймеров
Размер фрагмента, п.н.
Цель использования
ДНК-штрихкодирование для различения нескольких видов тлей
изучение генетического разнообразия популяций R. padi
страна сбора N N h Hd
ссылка
страна сбора
N
N h
Hd
ссылка
COI
O. Folmer с соавт. (85)
LCO1490; HC02198
710
Австралия 15 2 nd
Южная Корея 8 1 nd
Кения –
(79)
(80)
(81)
Австралия
Литва (13), Латвия (4), Эстония (1), публично доступные сиквенсы (26)
510
44
4
10
nd nd
(19)
(82)
C. Simon с соавт. (86)
C1-J-1751; C1-N-2191
440
США, Канада, Гер- –
мания, Япония
Ирак –
(77)
(90)
Китай
287
3
0,53249
83)
R.G. Foottit с соавт. (87)
LepF; LepR
700
Китай –
Китай –
(91)
(90)
Китай
275
7
0,491
(92)
COI
COII
J. Guo с соавт. (84)
F; R
F; R
597
615
Нет сведений об использовании этой пары праймеров для изучения других видов тлей
Китай (467), Бельгия (14), Люксембург (4), Франция (27), Германия (23)
535
29
0,663
(84)
Cytb
M. Harry с соавт. (88)
CP1; CP2
800
Китай –
(90)
Китай
275
15
0,607
(92)
EF-1 α
J. Tur c inavi c ien e с соавт. (78)
J. Guo с соавт. (84)
EloaphisF; EloaphisR
F; R
500
765
Литва –
Нет сведений об использовании этой пары праймеров для изучения других видов тлей
(78)
Литва (13), Латвия (4), Эстония (1), публично доступные сиквенсы (2)
Китай (467), Бельгия (14), Люксембург (4), Франция (27), Германия (23)
20
535
4
32
nd
0,507
(82)
(84)
ND4
Н.В. Алпатьева с соавт. (89)
RpND4-F; RpND4-R
438
Россия Более 4 nd
1000
(89)
Россия
Более 1000
30
nd
(93)
|
Страна сбора |
Объем выборки |
Показатель |
Локус и номер хромосомы, содержащей локус |
||||||||||
|
R5.29.b |
R6.3 |
R1.35 |
R5.10 |
R5.138 |
R5.50 |
R3.171 |
R2.73 |
S16b |
S17b |
Ссылка |
|||
|
1-я |
1-я |
2-я |
2-я |
2-я |
3-я |
3-я |
4-я |
2-я |
3-я |
||||
|
Франция |
55 клонов |
N a |
17 |
5 |
10 |
8 |
20 |
25 |
15 |
6 |
– |
– |
(65) |
|
ДР |
161-216 |
161-183 |
345-360 |
256-274 |
211-287 |
297-403 |
214-252 |
262-285 |
– |
– |
|||
|
PIC |
nd |
nd |
nd |
nd |
nd |
nd |
nd |
nd |
– |
– |
|||
|
Франция |
384 клона |
N a |
25 |
5 |
16 |
14 |
– |
– |
– |
9 |
4 |
8 |
(49) |
|
ДР |
159-209 |
161-183 |
341-360 |
248-276 |
– |
– |
– |
262-285 |
149-155 |
158-172 |
|||
|
PIC |
nd |
nd |
nd |
nd |
– |
– |
– |
nd |
nd |
nd |
|||
|
nd |
384 клона |
N a |
– |
– |
– |
– |
– |
– |
– |
– |
4 |
8 |
(61) |
|
ДР |
– |
– |
– |
– |
– |
– |
– |
– |
149-155 |
158-172 |
|||
|
PIC |
– |
– |
– |
– |
– |
– |
– |
– |
nd |
nd |
|||
|
Австралия |
510 клонов |
N a |
8 |
– |
– |
8 |
13 |
15 |
6 |
8 |
– |
– |
(19) |
|
ДР |
161-201 |
– |
– |
255-272 |
211-263 |
299-343 |
227-294 |
246-286 |
– |
– |
|||
|
PIC |
nd |
– |
– |
nd |
nd |
nd |
nd |
nd |
– |
– |
|||
|
Иран |
35 клонов |
N a |
3 |
2 |
Методические |
1 |
Методические |
2 |
5 |
4 |
– |
– |
(69) |
|
ДР |
nd |
nd |
проблемы |
nd |
проблемы |
nd |
nd |
nd |
– |
– |
|||
|
PIC |
0,1028 |
nd |
nd |
nd |
0,338 |
nd |
– |
– |
|||||
|
Китай |
369 клонов |
N a |
– |
– |
– |
14 |
31 |
12 |
21 |
24 |
– |
– |
(68) |
|
ДР |
– |
– |
– |
253-292 |
221-292 |
292-333 |
229-292 |
243-317 |
– |
– |
|||
|
PIC |
– |
– |
– |
nd |
nd |
nd |
nd |
nd |
– |
– |
|||
|
Чили |
377 клонов |
N a |
12 |
Методические Методические |
14 |
9 |
14 |
10 |
10 |
– |
– |
(21) |
|
|
ДР |
179-249 |
проблемы |
проблемы |
263-319 |
171-253 |
308-344 |
227-259 |
279-309 |
– |
– |
|||
|
PIC |
0,47 |
0,56 |
0,30 |
0,14 |
0,45 |
0,46 |
– |
– |
|||||
Примечание. N a — число выявленных аллелей в указанном локусе, ДР — диапазон размеров детектированных фрагментов (число нуклеотидов), PIC — информативность полиморфизма (polymorphism information content); nd — отсутствие информации, маркер был в анализе, но статистические данные для него не приведены или не могут быть рассчитаны при чтении; прочерки означают, что маркер в работе не использовался.
Примечание. N — число проанализированных особей R. padi , N h — число детектированных гаплотипов R. padi , Hd — индекс разнообразия гаплотипов (haplotype diversity); nd — статистические данные не приведены. Числа, указанные в скобках рядом с названиями отдельных стран, обозначают число клонов, собранных для анализа в этой стране. Прочерки означают, что R. padi в анализе отсутствовала.
Однако некоторые важные характеристики микросателлитных маркеров, например информативность полиморфизма (polymorphism information content, PIC) или число выявленных аллелей в локусе, авторы либо приводили сами (19, 49, 65, 69), либо предоставляли возможность рассчитать читателю (21). На основании этих показателей особенно выделяются разработанные J.-C. Simon с соавт. (65) маркеры локусов R5.50 и R5.29.b с 25 детектированными аллелями (49, 65), что было максимальным значением среди 24 маркеров. В то же время в литературе показатели PIC всех маркеров, разработанных французскими учеными, не превышали 0,56 (21, 69) (см. табл. 1).
Для SSR-маркеров, разработанных X. Duan с соавт. (70), можно наблюдать иную картину: число выявленных аллелей составляет не более 9, но показатель PIC превышает значение 0,7 для маркеров RP06, RP42, RP22 (см. табл. 2).
Таким образом, нельзя однозначно сделать вывод о том, какие маркеры микросателлитных локусов наиболее эффективны при изучении генетического разнообразия R. padi , но большое число доступных вариантов дает широкие возможности для исследований.
RAPD- маркеры. В отличие от SSR-маркеров, RAPD-анализ не требует точного знания последовательности ДНК объекта исследований, благодаря чему этот метод был выбран многими группами исследователей, установившими с его помощью соответствие популяций различных видов тлей и их географического положения, например A. gossypii (71, 72), D. noxia (40, 73), Schizaphis graminum Rondani (73), S. avenae (74) и других.
RAPD-маркеры были использованы также для изучения генетического полиморфизма популяций R. padi из стран Европы (52, 71), Африки (52, 75), Северной Америки (71) и Новой Зеландии (18, 76). Чаще всего для этой цели использовали RAPD-праймеры длиной 10 нуклеотидов (OPA1-OPA20) из набора, разработанного компанией «Operon Technologies» (г. Аламида, штат Калифорния, США) (52, 71, 75). Так, с помощью RAPD-праймеров исследователи из Египта смогли разделить местные популяции R. padi на два кластера (75). J.-C. Simon с соавт. (65) отметили эффективность использования RAPD-праймера OPA-18, поскольку два полученных с его помощью профиля однозначно соответствовали голоциклическому или андроциклическому типу жизненного цикла особей R. padi , собранных во Франции, Испании, Марокко и Великобритании.
В то же время при использовании RAPD-праймеры отмечен невысокий полиморфизм этого типа маркеров, из-за чего проанализированные популяции R. padi характеризовались низким генетическим разнообразием, несмотря на разное географическое происхождение собранных особей (18, 52, 71, 75).
Секвенирование участков генома. Помимо рестрикционного анализа, RAPD и SSR-маркеров, для изучения полиморфизма ДНК тлей используют секвенирование участков генома с последующим анализом однонуклеотидных различий. Причем одни и те же пары праймеров могут быть вовлечены как в процесс ДНК-штрихкодирования нескольких видов тлей с целью наглядно показать межвидовые различия (77-81), так и для изучения популяционного разнообразия отдельных видов, например, R. padi (19, 82-84) (табл. 3).
Митохондриальный ген субъединицы I цитохром с-оксидазы (COI) был выбран для этих целей как один из наиболее консервативных генов в мтДНК животных (94). В ряде статей (84-87) представлены праймеры для амплификации различных участков гена COI мтДНК R. padi, которые сами разработчики (84) или другие авторы (19, 80, 82, 83, 92) использовали для изучения полиморфизма популяций тли из разных стран (см. табл. 3; рис.). Отметим, что праймеры, созданные O. Folmer с соавт. (85) и R.G. Foottit с соавт. (87), крайне схожи: пара прямых LCO1490/LepF и пара обратных праймеров HC02198/LepR имеют одинаковые места посадки на гене COI, а их последовательности различаются только несколькими нуклеотидами, поскольку указанные праймеры были разработаны с использованием ДНК разных групп организмов.
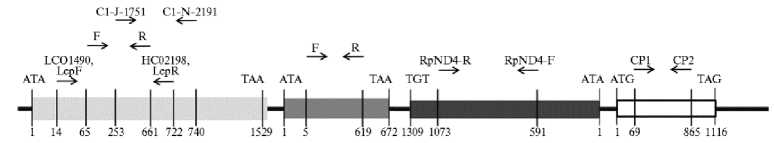
Взаимное расположение трех генов митохондриальной ДНК Rhopalosiphum padi L. и места посадки пяти пар праймеров, используемых для секвенирования участков этих генов. Светло-серым обозначен ген COI, пары праймеров LCO1490—HC02198 (85), C1-J-1751—C1-N-2191 (86), LepF— LepR (87), F—R (84); темно-серым — ген COII, пара праймеров F—R (84); темно-серым — ген ND4, пара праймеров RpND4-F—RpND4-R (89), белым в черной рамке — ген Cytb, пара праймеров CP1—CP2 (88). Стрелками показаны области отжига праймеров; цифры под стрелками соответствуют положению первого нуклеотида на 5´-конце праймера; нумерация нуклеотидов начинается со стартового кодона. Названия праймеров указаны над стрелками. В качестве референсной последовательности была взята последовательность митогенома R. padi KT447631.1 из базы данных NCBI (National Center for Biotechnology, .
В 2023 году J. Guo с соавт. (84) представили публикацию, в которой с использованием праймеров собственной разработки секвенировали участки не только COI , но и еще двух генов в популяциях R. padi, собранных в Китае: митохондриального COII (ген субъединицы II цитохром с-оксидазы) и ядерного EF-1α (ген фактора элонгации 1-alpha). Другая пара праймеров для секвенирования участка гена EF-1a была разработана J. Tur c inavi c iene с соавт. (78) и использована для изучения популяций R. padi из стран Балтии (78, 82). Пару праймеров для секвенирования участка еще одного митохондриального гена R. padi — Cytb (цитохром b) представили ученые из Китая (92). Недавно исследователи из Всероссийского института генетических ресурсов растений им. Н.И. Вавилова подошли к вопросу изучения популяционного разнообразия R. padi с помощью секвенирования фрагмента митохондриального гена ND4 , кодирующего субъединицу 4 NADH-дегидрогеназы (89, 93) (см. табл. 3; рис.).
В общей сложности четыре пары праймеров, используемые для поиска нуклеотидного полиморфизма гена COI — LCO1490—HC02198 (85), C1-J-1751—C1-N-2191 (86), LepF—LepR (87), F—R (84) охватывают чуть меньше половины кодирующей области этого гена у R. padi — 47,5 %. Лучше обстоит дело с праймерами, разработанными для секвенирования фрагментов генов COII (F—R) (84) и Cytb (CP1—CP2) (88), поскольку в этом случае охват секвенируемого участка составляет соответственно 91 и 71 %. Наименьшее покрытие (37 и 21,5 %) доступно при секвенировании участка митохондриального гена ND4 (праймеры RpND4-F—RpND4-R) (89) и участка ядерного гена EF-1α (праймеры EloaphisF—EloaphisR, F —R) (78, 84) (см. табл. 3; рис.).
При секвенировании важным статистическим показателем, позволяющим определить, насколько разнообразны аллели в исследуемой популяции, служит индекс разнообразия гаплотипов (haplotype diversity, Hd). К сожалению, значения этого показателя приведены авторами не во всех работах, где проводили секвенирование участков генов R. padi (см. табл. 3). Однако сравнение доступных нам данных показывает, что наибольшего значения Hd (0,663) удалось добиться J. Guo с соавт. (84) при комбинировании результатов секвенирования участков двух генов, COI и COII. Такой подход — сочетание данных, полученных при секвенировании участков различных генов — может повысить информативность исследований с использованием указанного метода.
Таким образом, анализ однонуклеотидных замен, детектированных по результатам секвенирования различных участков генов COI , COII, ND4 , Cytb и EF-1α , был применен для изучения генетического разнообразия популяций R. padi из Европы, Азии, Австралии (см. табл. 3). Больше всего работ по секвенированию ДНК этого вида выполнено с использованием праймеров, разработанных O. Folmer с соавт. (85), однако созданные другими авторами праймеры также представляют интерес для исследований популяционного разнообразия R. padi (78, 84, 86, 88, 89).
SNP при полном секвенировании генома. Данные, полученные в результате полного секвенирования различных видов тлей, например Rhopalosiphum nymphaeae L. (95), Aphis glycines Matsumura (96), Acyrthosiphon pisum Harris (97), S. avenae (98), R. padi (99, 100), открыли новые возможности в изучении геномов этих видов. Так, R. Morales-Hojas с соавт. (99) для сравнения семи популяций R. padi , собранных на острове Великобритания, использовали данные, полученные при полном секвенировании ядерного генома.
Стоит отметить, что еще два полногеномных сиквенса ядерной ДНК R. padi, полученные двумя группами ученых из Китая, опубликованы в базе данных NCBI (National Center for Biotechnology, в 2021 году — ASM2088224v1 (China Agricultural University, г. Пекин, Китай) и ASM1942551v1 (Institute of Plant Physiology and Ecology, г. Шанхай, Китай). Из них первый сиквенс был аннотирован в 2023 году, благодаря чему стал еще более информативным. Хотя полногеномные последовательности, полученные китайскими учеными, не были использованы авторами для сопоставления с аналогичными данными для других популяций R. padi, сиквенсы ASM2088224v1 и ASM1942551v1 общедоступны и могут быть применены в популяционных исследованиях.
Потенциально однонуклеотидный полиморфизм (single-nucleotide polymorphism, SNP), установленный при полном секвенировании ядерной и митохондриальной ДНК тли, дает самую исчерпывающую информацию о генетическом разнообразии R. padi (99, 100). Однако на данный момент такое секвенирование все еще остается слишком трудоемким и ресурсозатратным, из-за чего широко не используется для изучения черемуховозлаковой тли.
Комбинирование различных методов в одном исследовании. В конце нашего обзора стоит отметить публикации, в которых авторы для работы с одной и той же популяцией тли использовали одновременно различные методы с целью повышения информативности исследований. Обычно в таких публикациях параллельно используют методы, позволяющие проанализировать последовательности ядерной и мтДНК.
Так, I. Valenzuela с соавт. (19) суммировали данные, полученные при изучении австралийских популяций R. padi с помощью методов SSR-генотипирования и секвенирования фрагмента гена COI . Для анализа генетического разнообразия выборки R. padi из трех стран Европы и Марокко J.-C. Simon с соавт. (52) сочетали рестрикционный анализ участка мтДНК длиной 2200 п.н. и RAPD-анализ, связав полученные гаплотипы с типом 12
жизненного цикла тли. Для изучения французской выборки R. padi F. Delmotte с соавт. (58) использовали SSR-маркеры и рестрикцию сегмента митохондриального генома, и полученные результаты показали, что на этой территории было как минимум три независимых случая возникновения бесполых линий у этого вида тлей.
Итак, в настоящее время доступны несколько вариантов молекулярно-генетических методов, которые используются для изучения генетического разнообразия Rhopalosiphum padi в разных странах мира уже более 30 лет: рестрикционный анализ, RAPD-анализ, SSR-генотипирование, секвенирование участков отдельных генов или полного генома. При этом в ряде работ авторы используют не один, а комбинацию нескольких подходов для повышения информативности полученных результатов. Молекулярногенетические методы уже были применены для изучения популяций R. padi , собранных во всех частях света, кроме Антарктиды. При этом исследователи чаще выбирают микросателлитное маркирование и секвенирование как подходы, дающие наиболее полную информацию о последовательности ДНК R. padi . В целом, следует отметить достигнутые результаты при изучении зарубежных популяций R. padi . В России подобные исследования почти не проводились, и их необходимо интенсифицировать, учитывая эффективность молекулярных методов при контроле популяций вредителя.
ФГБНУ Всероссийский НИИ защиты растений,


