Биомеханическое обоснование применения стержневых аппаратов внешней фиксации при лечении раненых с огнестрельными переломами длинных костей конечностей
Автор: Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.20, 2025 года.
Бесплатный доступ
Лечение раненых с огнестрельными переломами длинных костей конечностей – важнейшая задача военной травматологии и ортопедии. В условиях вооруженных конфликтов последних десятилетий происходит постоянное изменение характера ведения боевых действии и увеличение поражающего воздействия современных огнестрельных снарядов и боеприпасов, поэтому лечение данной категории пациентов требует постоянного совершенствования. Традиционно оказание медицинской помощи раненым с переломами длинных костей конечностей заключалось в своевременном выполнении первичной хирургической обработки и проведении лечебно-транспортной иммобилизации, которая предпочтительно должна выполняться путем проведения внеочагового остеосинтеза при помощи стержневых аппаратов внешней фиксации (АВФ). Однако, существующие варианты и модификации АВФ обладают разными биомеханическими и эргономическими характеристиками, которые, на наш взгляд, требуют дальнейшей доработки с целью улучшения качества оказания медицинской помощи раненым на этапах медицинской эвакуации. Цель: на основании анализа биомеханических параметров произвести оценку стабильности внешней фиксации костных отломков в построенных моделях нагружения «кость-АВФ» при использовании различных вариантов стержневых АВФ на примере диафизарного оскольчатого перелома большеберцовой кости (типа С по классификации АО). Материалы и методы: материалом для данного исследования послужила 3D печатная модель большеберцовой кости, построенная на основе КТ в программе Mimics. Модель учитывала губчатую и кортикальную костные ткани. Затем в системе автоматизированного проектирования SolidWorks были построены модели аппаратов внешней фиксации, которые затем совмещались с моделью кости. Далее формировали оскольчатый перелом диафиза кости, типа С по классификации AO. Моделирование нагружения системы кость-АВФ осуществляли в системе конечно-элементного анализа Ansys. Количественный расчет биомеханических характеристик внеочаговой фиксации осуществляли методом конечных элементов (КЭ). Результаты и выводы: на основании проведенного анализа биомеханических характеристик было выявлено, что наибольшими показателями стабильности при фиксации оскольчатого перелома обладает стержневой АВФ, соединительные узлы которого были выполнены из титанового сплава. В то же время аппараты, соединительные узлы которых были выполнены из других материалов, демонстрировали достаточную степень фиксации при длительных циклах нагружения, не испытывая при этом усталостных нарушений как в костной ткани, так и в элементах аппарата, что подтверждает возможность использования различных модификаций стержневых АВФ при лечении оскольчатых, в том числе огнестрельных, переломов диафизов длинных трубчатых костей в клинической практике.
Внеочаговый остеосинтез, аппараты внешней фиксации, биомеханика, огнестрельные переломы, конечные элементы
Короткий адрес: https://sciup.org/140312868
IDR: 140312868 | DOI: 10.25881/20728255_2025_20_4_82
Biomechanical substantiation of the use of rod external fixation devices in the treatment of wounded with gunshot fractures of long bones of the extremities
today, the treatment of wounded with gunshot fractures of long bones of the extremities is the most important task of military traumatology and orthopedics. In the context of armed conflicts of recent decades, the nature of military operations is constantly changing and the damaging effects of modern firearms and ammunition are increasing, which is why the treatment of this category of patients requires constant improvement. Traditionally, medical care for the wounded with fractures of long bones of the extremities consisted of timely primary surgical treatment and therapeutic and transport immobilization, which should preferably be performed by extrafocal osteosynthesis using rod external fixation devices (EFD). However, the existing versions and modifications of EFD have different biomechanical and ergonomic characteristics, which, in our opinion, require further revision in order to improve the quality of medical care for the wounded at the stages of medical evacuation. Objective: based on the analysis of biomechanical parameters, assess the stability of external fixation of bone fragments in the constructed loading models “bone – EFD” using various versions of rod EFD using the example of a diaphyseal comminuted fracture of the tibia (type C according to the AO classification). Materials and methods: the material for this study was a 3D printed model of the tibia, built on the basis of CT in the Mimics program. The model took into account spongy and cortical bone tissue. Then, in the SolidWorks automated design system, models of external fixation devices were built, which were then combined with the bone model. Next, a comminuted fracture of the bone diaphysis was formed, type C according to the AO classification. Modeling of the bone – external fixation device system loading was carried out in the Ansys finite element analysis system. Quantitative calculation of the biomechanical characteristics of external fixation was carried out using the finite element method (FE). Results and conclusions: based on the analysis of the biomechanical characteristics, it was revealed that the highest stability indicators for fixing a comminuted fracture are found in the rod external fixation device, the connecting nodes of which were made of titanium alloy. At the same time, the devices, the connecting units of which were made of other materials, demonstrated a sufficient degree of fixation during long loading cycles, without experiencing fatigue damage either in bone tissue or in the elements of the device, which confirms the possibility of using various modifications of rod EFDs in the treatment of comminuted, including gunshot, fractures of the diaphysis of long tubular bones in clinical practice.
Текст научной статьи Биомеханическое обоснование применения стержневых аппаратов внешней фиксации при лечении раненых с огнестрельными переломами длинных костей конечностей
Ранения, возникающие вследствие воздействия огнестрельных и взрывных боеприпасов, имеют ряд характерных особенностей, напрямую влияющих развитие
BIOMECHANICAL SUBSTANTIATION OF THE USE OF ROD EXTERNAL FIXATION DEVICES IN THE TREATMENT
OF WOUNDED WITH GUNSHOT FRACTURES OF LONG BONES
OF THE EXTREMITIES
-
1 GVKG named after N.N. Burdenko, Moscow
-
2 RUDN University, Moscow
-
3 Pirogov National Medical and Surgical Center, Moscow
Objective: based on the analysis of biomechanical parameters, assess the stability of external fixation of bone fragments in the constructed loading models “bone – EFD” using various versions of rod EFD using the example of a diaphyseal comminuted fracture of the tibia (type C according to the AO classification).
Materials and methods: the material for this study was a 3D printed model of the tibia, built on the basis of CT in the Mimics program. The model took into account spongy and cortical bone tissue. Then, in the SolidWorks automated design system, models of external fixation devices were built, which were then combined with the bone model. Next, a comminuted fracture of the bone diaphysis was formed, type C according to the AO classification. Modeling of the bone – external fixation device system loading was carried out in the Ansys finite element analysis system. Quantitative calculation of the biomechanical characteristics of external fixation was carried out using the finite element method (FE).
Results and conclusions: based on the analysis of the biomechanical characteristics, it was revealed that the highest stability indicators for fixing a comminuted fracture are found in the rod external fixation device, the connecting nodes of which were made of titanium alloy. At the same time, the devices, the connecting units of which were made of other materials, demonstrated a sufficient degree of fixation during long loading cycles, without experiencing fatigue damage either in bone tissue or in the elements of the device, which confirms the possibility of using various modifications of rod EFDs in the treatment of comminuted, including gunshot, fractures of the diaphysis of long tubular bones in clinical practice.
осложнений и тактику лечения. Среди них можно выделить сложную конфигурацию раневого канала, неравномерную протяженность омертвевших и некротизирующихся тканей, первичную микробную контаминацию, а

Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ также частое сочетание данных ранений с переломами костей и травмами нейроваскулярных структур [1]. Особенности раневой баллистики при воздействии огнестрельных снарядов и боеприпасов приводят к возникновению обширных комплексных (мягкотканых и костных) дефектов, которые по своим патоморфологическим свойствам характеризуются значительным повреждением костномозговой полости и собственных питающих артерий, обуславливая тем самым гипоксию окружающих тканей, что замедляет репаративные процессы и зачастую является пусковым механизмом развития огнестрельного остеомиелита [2]. Дополнительные сложности в лечении огнестрельных переломов вносит наличие в раневом канале разнообразной по своему составу и резистентной к воздействию антибиотиков микрофлоры, которая во многом и обуславливает неэффективность классических методов лечения [3].
Исходя из данных фактов, выполнение первичных реконструктивно-восстановительных операций (остеосинтез, эндопротезирование и др.) при огнестрельных переломах возможно только после стабилизации общего состояния пациента и соблюдения строгих рекомендации по переходу на внутреннюю фиксацию [4]. Однако даже в случае соблюдения данных требований при проведении погружного остеосинтеза сохраняется высокий риск возникновения инфекционных осложнений.
Поэтому, при оказании экстренной и неотложной медицинской помощи на этапах медицинской эвакуации раненым с огнестрельными переломами длинных костей конечностей предпочтительно в качестве первого этапа лечения проводить лечебно-транспортную иммобилизацию костных отломков с использованием АВФ, так как данный метод остеосинтеза позволяет эффективно восстановить анатомические взаимоотношения в конечностях и предотвратить развитие таких жизнеугрожающих осложнений как жировая эмболия, травматический шок и др.
Основные требования к оптимальной системе внешней фиксации включают:
-
• простоту использования и универсальность для соответствия различным анатомическим областям;
-
• способность восстанавливать анатомическую длину кости путем выравнивания и положение фрагментов перелома с использованием различных пространственных конфигураций АВФ;
-
• эластичную деформируемость системы для обеспечения микроподвижности в зоне перелома;
-
• устойчивость к внешним воздействиям.
Возникновение механических конструкции для внеочаговой фиксации костных отломком берет свое начало в ХIX веке, когда сначала J. Emsberry (1831), а затем J.F. Malgaigne (1843) опубликовали результаты применения в клинической практике систем для удержания костных фрагментов, элементы которых располагались вне зоны перелома. В то же время Wutzer предложил винтовой аппарат «screw apparatus», который в 1851 г.
был модернизирован и с успехом применен в клинической практике Von Langenbeck [5]. Использование данных моделей АВФ представляло собой единичные попытки использования приспособленных устройств с целью замены неинвазивных средств иммобилизации, которые имели недостаточную управляемость, надежность и эффективность. В последующем R. Hoffmann (1938) предложил и начал широко применять аппарат с оригинальным узлом соединения, который обеспечивал компрессию и дистракцию отломков, а также расширил репозиционные возможности системы внеочаговой фиксации. Разработанный им универсальный фиксационный зажим был настолько удобен в практической работе, что все дальнейшие модернизации были направлены лишь на изменение внешних опор (Haynes, Vidal, Adrey). Именно благодаря работам перечисленных авторов АВФ на стержневой основе получили такое широкое распространение в мире [6].
В нашей же стране развитие чрескостной фиксации при хирургическом лечении переломов неразрывно связано с именем Г.А. Илизарова, который является основателем научной школы внеочагового остеосинтеза, последователи которой продолжают совершенствовать данную методику и по сей день. В ХХ веке были разработаны и внедрены в клиническую практику конструкции АВФ А.А. Коржа, А.Н. Костюка, С.С. Ткаченко и др. [7].
Кроме того, большой толчок в развитии оказания медицинской помощи раненым с огнестрельными переломами костей конечностей путем применения наружной фиксации дали труды военных травматологов в период ведения боевых действий Советской Армии в Афганистане. Участие военных врачей в медицинском обеспечении вооруженных конфликтов, развитие смежных специальностей, улучшение эвакуационных возможностей потребовало усовершенствования методики и аппаратного обеспечения, направленного на оптимизацию техники операции, унификации оснащения, повышения его надёжности [8].
На стабильность фиксации костных отломков при проведении внеочагового остеосинтеза с использованием АВФ влияют биомеханические свойства материалов, из которых изготовлены стержни, узлы и балки аппарата, тип заточки стержня, а также прочность соединения фиксирующего элемента с внешней опорой. Оптимальными на сегодняшний день признаны специальные марки нержавеющей стали, титана и его сплавов. Однако обладая достаточной биологической инертностью и устойчивостью в агрессивной среде, данные материалы не обладают другими важными свойствами, необходимыми для обеспечения стабильной фиксации. В связи с этим, в последние годы активно проводятся исследования, направленные на улучшение остеоинтеграции, придания материалам антибактериального и противовоспалительного эффекта для оптимизации методики внеочаговой фиксации [9].

Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ
Так в исследовании, проведенном на базе ГВКГ им. Н.Н. Бурденко, по изучению эффективности применения методики последовательного остеосинтеза с использованием внеочаговой фиксации АВФ КСВП в качестве первого этапа лечения раненых с огнестрельными переломами длинных костей конечностей было выявлено, что наибольшее число инфекционных осложнений было получено в группе, где использовались стержни с гладким покрытием (41,6%), в то время как в группе с использованием стержней с гидроксиапатитовым покрытием частота данных осложнений составило всего 13,6%. На основании полученных результатов авторы пришли к выводу о том, что стержни с гидроксиапатитовым покрытием, имеющие пористую структуру, могут способствовать интеграции костной ткани в данное покрытие, что в свою очередь приводит к усилению стабильности фиксации стержня в кость, предотвращает остеолиз и расшатывание, что является одним из основных механизмов профилактики остеомиелита [10].
Обобщая всё вышеперечисленное, можно прийти к выводу, что совершенствование систем для внеочаговой фиксации костных отломков требует устранения таких недостатков существующих конструкции как: сложность и длительность установки, необходимость специальной подготовки персонала, трудности при проведении и интерпретации диагностических методов обследования, необходимость наличия в оснащении дополнительного инструментария и др. Особое значение данные проблемы приобретают при массовом поступлении раненых и пострадавших и ограниченных возможностях сил и средств медицинской службы. Поэтому в настоящее время для обеспечения системы этапного лечения раненых необходима разработка материалов и оборудования, способных максимально соответствовать современной концепции, лежащей в основе тактики Damage Control Orthopedics, которая в настоящий момент широко применяется при оказании медицинской помощи раненым с огнестрельными переломами длинных трубчатых костей.
Знание механических характеристик костной ткани, особенно при воздействии нагрузки на конечность, несомненно, имеет основополагающее значение для глубокого понимания различных физиологических и патологических состояний, поиска замещающих материалов и изучения возможностей соединения с другими материалами и устройствами. Что же касается биомеханических аспектов внеочаговой фиксации костных отломков, то при сравнительном анализе стабильности, надежности и механической прочности фиксации различными имплантатами авторами обычно исследуются поля перемещений, деформаций и напряжений как в кости, так и в самих имплантатах [11; 12]. Отечественными биомеханиками предложены и апробированы так называемые критерии успешности лечения. Среди них широко применяются биомеханические критерии успешности, с помощью которых можно количественно сравнить между собой различные варианты хирургического реконструктивного лечения последствий заболеваний и повреждений элементов опорно-двигательного аппарата [13].
Цель исследования – сравнение стабильности и надежности фиксации диафизарного перелома (спиральный, тип С по классификации AO) большеберцовой кости при помощи пяти вариантов АВФ отечественного производства [14–16]:
-
• аппарат «КСВП» с титановыми узлами (далее – аппарат 1);
-
• аппарат «ИДЕАЛ» с быстрозажимными узлами (далее – аппарат 2);
-
• аппарат с карбоновыми узлами MG-FIX (далее – аппарат 3);
-
• аппарат с карбоновыми узлами MG-FIX-universal (далее – аппарат 4);
-
• аппарат с карбоновыми узлами ZX-Остеомед (далее – аппарат 5).
Для достижения поставленной цели нами были решены следующие задачи:
-
• построить по данным КТ здорового добровольца 3D твердотельную модель большеберцовой и малоберцовой костей, учитывающую характеристики кортикальной и губчатой костной ткани;
-
• смоделировать диафизарный перелом (спиральный, тип С по классификации AO) большеберцовой кости;
-
• построить 3D твердотельные геометрические модели пяти АВФ;
-
• создать пять моделей «кость-имплантат», каждая из которых включает модель костей с переломом и модель соответствующего АВФ;
-
• поставить и решить задачу биомеханики о напряженно-деформированном состоянии системы «кость-имплантат» для каждой из пяти построенных моделей;
-
• проанализировать рассчитанные напряженно-деформированные состояния каждой из пяти моделей и оценить их стабильность и надежность с учетом биомеханических критериев успешности лечения, сравнить модели с позиции биомеханики.
Материалы и методы
Построение 3D твердотельной модели большеберцовой кости осуществлялось на основе данных КТ в программе Mimics. Модель учитывала губчатую и кортикальную костные ткани. Затем в системе автоматизированного проектирования SolidWorks строились модели аппаратов внешней фиксации, которые затем совмещались с построенной моделью кости. Спиральный перелом диафиза кости, тип C по классификации AO создавался также в SolidWorks. Результирующие модели систем кость-АВФ представлены на рисунке 1.
Моделирование нагружения систем кость-АВФ осуществлялось в системе конечно-элементного анализа Ansys. Численно методом конечных элементов решалась статическая задачи биомеханики, которая моделирует напряженно-деформированное состояние системы
Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ

Рис. 1. 3D модели системы кость-АВФ аппаратов 1–5.
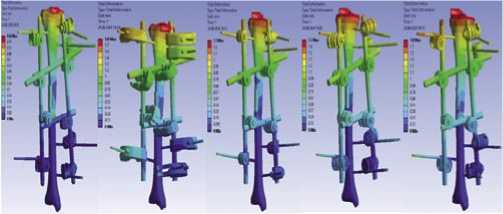
Рис. 3. Поля перемещений для моделей АВФ 1–5 (нагрузка 100 Н).

Рис. 2. Граничные условия: красным (В) показана область нагружения, синим (А) – область закрепления.
Табл. 1. Механические свойства костных тканей и элементов фиксации
|
Материал |
Модуль Юнга, МПа |
Коэффициент Пуассона |
|
Губчатая кость |
800 |
0.3 |
|
Кортикальная кость |
16800 |
0.3 |
|
Титановый сплав |
96000 |
0.36 |
|
Карбон |
181000 |
0.3 |
|
Zedex-324 |
3600 |
0.2 |
«кость-имплантат» под действием внешних нагрузок. Моделировалось и затем анализировалось напряженно-деформированное состояние (НДС) костных отломков и систем фиксации под действием сжимающих усилий, приложенных к верхнему концу кости, нижний конец кости при этом жестко закреплялся, как показано на рисунке 2. Материалы костной ткани и элементов имплантатов предполагались линейно-упругими и изотропными.
Между костными отломками и осколками ставились контактные условия с трением, коэффициент трения принимался равным 0.2.
Механические свойства (модуль Юнга и коэффициент Пуассона) костной ткани и элементов фиксации брались из данных литературы (Табл. 1).
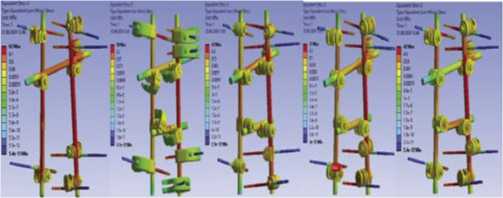
Рис. 4. Поля эквивалентных напряжений по Мизесу в моделях имплантатов аппаратов 1–5 (нагрузка 100 Н).
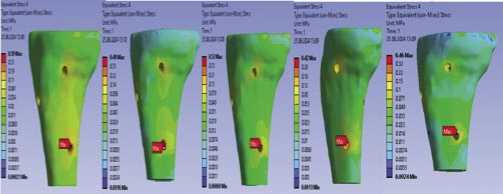
Рис. 5. Типичные поля эквивалентных напряжений по Мизесу в губчатой кости (нагрузка 100Н).
Так как при таких операциях пациенту не разрешено опираться на прооперированную конечность, то в данном исследовании было решено не нагружать модель большими усилиями порядка половины веса тела человека и более, как делается в других работах. При моделировании исследовалось НДС системы кость-имплантат под действием сжимающей нагрузки от 100 до 200 Н с шагом 50 Н.
Результаты и обсуждение
Результаты сравнительного анализа изучения стабильности и надежности фиксации костных отломков при диафизарном переломе большеберцовой кости типа С по АО представлены в таблице 2.
На рисунке 4 представлены типичные поля эквивалентных напряжений по Мизесу в моделях имплантатов (нагрузка 100 Н).
На рисунке 5 представлены типичные поля эквивалентных напряжений по Мизесу в губчатой кости (нагрузка 100 Н).
Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ
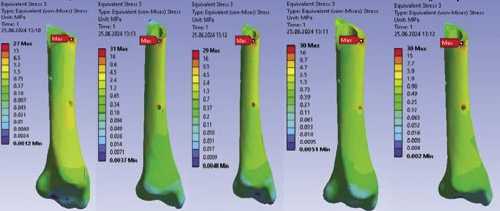
Рис. 6. Поле эквивалентных напряжений по Мизесу в кортикальной кости аппарата 5 (нагрузка 100 Н).
■ ■ Аппарат 1 (КСВП) Аппарат 4 (MG-FIX универсал)
Аппарат 2 (Идеал) Аппарат 5 (ZX Остеомед)
Аппарат 3 (MG-FIX)
На рисунке 6 представлены типичные поля эквивалентных напряжений по Мизесу в кортикальной кости (нагрузка 100 Н).
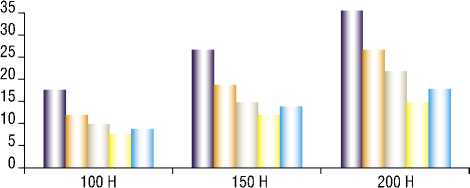
На диаграммах 1–6 графически представлены основные рассчитанные характеристики НДС для всех исследованных АВФ.
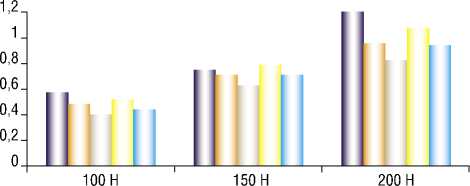
Диаграмма 3. Максимальные напряжения в кортикальной кости.
I ■ Аппарат 1 (КСВП) Аппарат 4 (MG-FIX универсал)
Аппарат 2 (Идеал) Аппарат 5 (ZX Остеомед)
Аппарат 3 (MG-FIX)
■ ■ Аппарат 1 (КСВП) Аппарат 4 (MG-FIX универсал)
Аппарат 2 (Идеал) Аппарат 5 (ZX Остеомед)
Аппарат 3 (MG-FIX)
Диаграмма 4. Максимальные напряжения в губчатой кости.
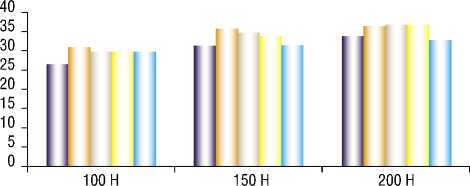
Диаграмма 1. Максимальные перемещения костных отломков при фиксации АВФ.
I Аппарат 1 (КСВП)
Аппарат 2(Идеал)
Аппарат 3 (MG-FIX)
I Аппарат! (КСВП) Аппарат 2 (Идеал) Аппарат 3 (MG-FIX)
Аппарат 4 (MG-FIX универсал)
Аппарат 5 (ZX Остеомед)
Аппарат 4 (MG-FIX универсал)
Аппарат 5 (ZX Остеомед)
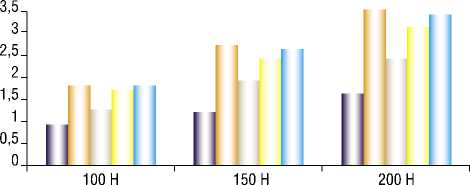
Диаграмма 2. Максимальные напряжения в стержнях Шанца.
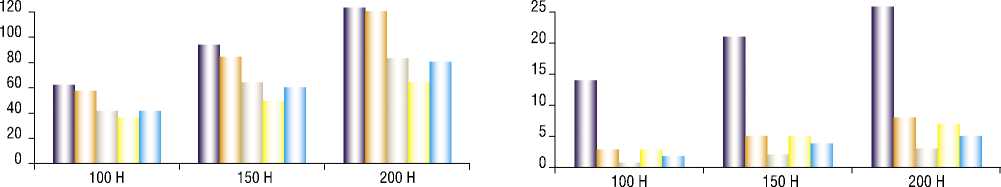
Диаграмма 5. Максимальные напряжения в соединительных узлах.
Табл. 2. Основные рассчитанные характеристики НДС для моделей аппаратов 1–5
|
Модель АВФ |
Аппарат КСВП (аппарат 1) |
ИДЕАЛ (аппарат 2) |
MG-FIX (аппарат 3) |
MG-FIX-universal (аппарат 4) |
ZX-Остеомед (аппарат 5) |
||||||||||
|
Нагрузка, Н |
100 |
150 |
200 |
100 |
150 |
200 |
100 |
150 |
200 |
100 |
150 |
200 |
100 |
150 |
200 |
|
Максимальные перемещения, мм |
0.9 |
1.2 |
1.6 |
1.8 |
2.7 |
3.5 |
1.3 |
1.9 |
2.4 |
1.7 |
2.4 |
3.1 |
1.8 |
2.6 |
3.4 |
|
Максимальные напряжения в стержнях Шанца, МПа |
62 |
95 |
125 |
58 |
86 |
122 |
43 |
65 |
85 |
37 |
51 |
65 |
42 |
61.0 |
81 |
|
Максимальные напряжения в кортикальной кости, МПа |
27 |
32 |
34 |
31 |
36 |
37 |
30 |
35 |
37 |
30 |
34 |
37 |
30 |
32 |
33 |
|
Максимальные напряжения в губчатой кости, МПа |
0.59 |
0.76 |
1.20 |
0.49 |
0.72 |
0.97 |
0.42 |
0.64 |
0.83 |
0.53 |
0.81 |
1.10 |
0.46 |
0.71 |
0.95 |
|
Максимальные напряжения в карбоновых планках, МПа |
18 |
27 |
36 |
12 |
19 |
27 |
10 |
15 |
22 |
8 |
12 |
15 |
9 |
14 |
18 |
|
Максимальные напряжения в соединительных узлах, МПа |
14 |
21 |
26 |
3 |
5 |
8 |
1 |
2 |
3 |
3 |
5 |
7 |
2 |
4 |
5 |

Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ
■ Аппарат 1 (КСВП)
Аппарат 2(Идеал)
Аппарат 3(MG-FIX)
Аппарат 4 (MG-FIX универсал)
Аппарат 5 (ZX Остеомед)
Диаграмма 6. Максимальные напряжения в карбоновых планках.
Поля перемещений костных отломков для всех моделей оказались схожими (Рис. 3). Наибольшую стабильность фиксации обеспечивает аппарат 1 (КСВП), что видно из диаграммы 1. Остальные аппараты демонстрировали более высокую степень перемещения. Однако полные перемещения во всех моделях не превышают 3.5 мм при нагрузке 200 Н, что является допустимым с учетом длины исследуемой кости.
Наибольшие напряжения в имплантатах обнаруживаются на резьбовых стержнях, которые фиксируются в кости (Рис. 4). АВФ КСВП показывает наибольшие напряжения в сравнении с остальными аппаратами, что объясняется его наиболее высокой жесткостью. Наименьшие напряжения в имплантатах демонстрирует аппарат MG-FIX-universal (при нагрузке 200 Н они почти в два раза ниже напряжений в АВФ КСВП).
При этом в кортикальной кости напряжения для всех аппаратов отличаются в пределах 10% при соответствующих нагрузках. Отметим, что их значения не превышают предел прочности кортикальной кости, который может достигать 161 МПа (Табл. 3).
Таким образом, допускаемым напряжением для титановых имплантатов будет являться 287 МПа. Это значение не достигается ни при одной из исследованных нагрузок для всех рассмотренных систем фиксации.
При оценке стойкости имплантатов к циклическим нагрузкам исследователи обычно используют понятие выносливости, а также предел выносливости. Данный параметр характеризует наибольшее значение максимального напряжения цикла, при действии которого не происходит усталостного разрушения образца после произвольно большого или заданного числа циклов нагружения [17]. Если же напряжения в конструкции превышают предел выносливости материала, то рассматривается кривая выносливости Веллера (Рис. 7), в соответствии с которой оценивается количество циклов, при которых конструкция будет работать без образования усталостных трещин и разрушения. К примеру, такой подход был использован Martinez-Mondragon при оценке усталостной прочности зубных имплантатов, выполненных из титанового сплава [18].
Табл. 3. Прочностные характеристики костных тканей и имплантатов
Материал
Медицинская (хирургическая) нержавеющая сталь (316LS/316LVM)
Титановый сплав Ti6Al4V ELI Titanium Alloy
Кортикальная костная ткань
Губчатая костная ткань
Предел прочности, МПа до 1241
(предел текучести до 945)
до 860
до 161 до 15
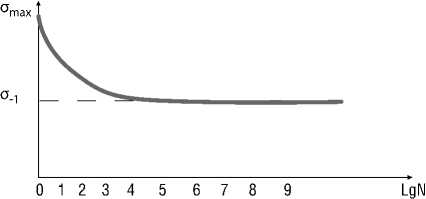
Рис. 7. Типичная кривая Веллера после испытаний на усталость, σ -1– физический предел выносливости, по оси абсцисс – логарифм числа циклов до разрушения.
Известно, что для титановых сплавов предел выносливости составляет от 0.25 до 0.6 предела прочности [17]. Таким образом, в данном исследовании нами был взят предел выносливости титанового сплава, равный четверти его предельной прочности, то есть 215 МПа. Сравнение наибольших напряжений в стержнях Шанца, вызванных осевой нагрузкой, с пределом выносливости показывает, что при таком уровне нагрузок имплантаты будут работать произвольно большое число циклов нагружения.
Также необходимо отметить, что немаловажным биомеханическим свойством систем внеочаговой фиксации является устойчивость резьбовой части стержней АВФ в костной ткани и скорость развития асептического расшатывания чрескостных элементов при нагрузке на конечность. Так при изучении данного параметра Mara Terzini et all при проведении экспериментальной оценки статической и динамической устойчивости одностороннего внешнего фиксатора компоновки бедро-голени установили, что жесткость внешнего фиксатора является решающим фактором в обеспечении поддержания физиологического положения костных отломков в условиях осевой нагрузки и немаловажное влияние на это оказывает температурное повреждение костной ткани во время проведения чрескостных компонентов АВФ, которое в свою очередь приводит к некрозу костной ткани, инфицированию и потере жесткость внешней фиксации [19].
Заключение
Среди исследованных вариантов АВФ наибольшей стабильностью обладает аппарат 1 (КСВП). Это объясняется тем, что фиксирующие элементы данного АВФ состоят из титанового сплава, обладающего высокими
Керимов А.А., Хоминец И.В., Бекшоков К.К., Пиманчев О.В.
БИОМЕХАНИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СТЕРЖНЕВЫХ АППАРАТОВ ВНЕШНЕЙ ФИКСАЦИИ ПРИ ЛЕЧЕНИИ РАНЕНЫХ С ОГНЕСТРЕЛЬНЫМИ ПЕРЕЛОМАМИ ДЛИННЫХ КОСТЕЙ КОНЕЧНОСТЕЙ показателями прочности. В то же время, стабильность внешней фиксации костных отломков при использовании других аппаратов также являлась достаточной. Наибольшие механические напряжения (по Мизесу) при этом отмечены в резьбовых стержнях, вкручивающихся в кость. В ходе проведения сравнительного анализа при рассмотренных нагрузках повреждения костной ткани не возникало ни в одной системе нагружения кость-АВФ.
На основании вышеизложенного можно прийти к выводу, что все исследуемые стержневые АВФ обладают достаточными биомеханическими свойствами для обеспечения стабильной фиксации костных отломков при оскольчатых диафизарных переломах большеберцовой кости, не испытывая при этом усталостных разрушений (в соответствии с рассмотренными осевыми сжимающими нагрузками до 200 Н), что подтверждает возможность успешного применения данных аппаратов в клинической практике при лечении открытых (в том числе и огнестрельных) переломов длинных костей конечностей.
Выводы
-
1. На современном этапе стержневые АВФ являются незаменимым инструментом в лечении раненных с огнестрельными переломами конечностей. При этом данные аппараты должны обладать определенными биомеханическими и эргономическими свойствами (небольшая масса, высокая прочность, стабильность фиксации, производимость);
-
2. Конструкции АВФ, изготовленные из нержавеющей стали и сплавов титана являются наиболее прочными, однако по своим эргономическим свойствам они уступают более современным моделям. В связи с чем нами был разработан ряд АВФ, составные элементы которых состоят из различных материалов (Peek- карбон), обладающими такими важными свойствами как рентгенпрозрачность, лёгкость конструкции, быстрая производимость элементов аппарата и т.д.
-
3. Выполненное экспериментальное исследование демонстрирует, что разработанные конструкции по своим упруго-прочностным и биомеханическим свойствам в должной степени не уступают титановым конструкциям и соответствуют предъявляемым условиям для стабильного остеосинтеза при открытых (в том числе огнестрельных) переломах.


