Биоминералогический анализ мочевых камней человека
Автор: В.И. Силаев, А.А. Слюсарь, А.В. Слюсарь, А.В. Кокин, А.С. Шуйский, А.Ф. Хазов, С.Н. Шанина, Б.А. Макеев, И.В. Смолева, Д.В. Киселева
Журнал: Вестник геонаук @vestnik-geo
Рубрика: Научные статьи
Статья в выпуске: 2 (374), 2026 года.
Бесплатный доступ
С использованием широкого спектра современных экспериментальных методов исследования была изучена эталонная коллекция образцов мочевых камней у мужчин и женщин в возрасте 27—83 лет, а также мочи пациентов с мочекаменной болезнью и хроническим пиелонефритом. Были проанализированы химический и фазовый состав, содержание микроэлементов, аминокислотный состав и содержание в белках, а также изотопный состав углерода и азота. В мочевых камнях были обнаружены биоминералы, охватывающие практически весь современный спектр типов минералов: элементарные вещества (металлы), халькогениды (сульфиды), галогениды (хлориды), оксиды (магнетит, фаза SiO2), силикаты (алюмосиликаты) и кислородные соли. Помимо минералов камни также содержат так называемые минералоиды, представленные водными оксалатами кальция и мочевой кислотой. В исследованных образцах было идентифицировано пятнадцать белковых аминокислот, в том числе семь незаменимых. Три аминокислоты содержат небольшое количество D-энантиомера. Изотопный состав углерода и азота в органическом веществе, содержащемся в камнях и моче человека, уникален и отличается от состава органического вещества, содержащегося в костях человека, атмосфере Земли и в осадочных породах. Однако мочевые камни имеют сходство по изотопному составу углерода с органическими полимерами, образующимися в результате современного вулканизма.
Мочевые камни, минералообразование в организме человека, биоминералы
Короткий адрес: https://sciup.org/149150674
IDR: 149150674 | УДК: 549.3:616.613-003.7 | DOI: 10.19110/geov.2026.2.3
Biomineralogical analysis of human urinary stones
We present a study of a reference collection of urinary stone samples from men and women aged 27—83 years, as well as urine from patients with urolithiasis and chronic pyelonephritis, using a wide range of modern experimental research methods. The chemical and phase composition, trace element content, amino acid composition and content in proteins, and the isotopic composition of carbon and nitrogen are analyzed. Biominerals are found in the urinary stones, covering virtually the entire modern range of mineral types: elementary substances (metals), chalcogenides (sulfides), halides (chlorides), oxides (magnetite, SiO2 phase), silicates (aluminosilicates), and oxygen salts. In addition to minerals, the stones also contain so-called mineraloids, represented by hydrous calcium oxalates and uric acid. Fifteen protein amino acids, including seven essential ones, are identified in the studied samples. Three amino acids contain a small amount of the D-enantiomer. The isotopic composition of carbon and nitrogen in organic matter found in human stones and urine is unique and differs from that found in human bones, the Earth's atmosphere, and sedimentary rocks. However, urinary stones share a carbon isotopic composition similar to organic polymers formed by modern volcanism.
Текст научной статьи Биоминералогический анализ мочевых камней человека
веществ в организме, особенно водно-солевого обмена, и нарушения кислотно-щелочного равновесия в крови и других жидкостях организма человека вследствие инфекционных заболеваний печени и желудочно-кишечного тракта (Севостьянова, Полиенко, 2004). Заболевания желез внутренней секреции, регулирующих водный и солевой обмен (щитовидная железа, паращитовидные железы, гипофиз), также играют значительную роль в возникновении мочекаменной болезни. Развитию заболевания способствует состав пищи, например, растительно-молочная пища приводит к ощелачиванию урины, мясная, наоборот, к повышению её кислотности. Способствует возникновению мочекаменной болезни и недостаточное содержание в пище витаминов A и D. В конечном счете все упомянутые факторы приводят к возникновению у людей биоминерализации (Мак-Коннелл, 1977) вследствие кристаллизации в урине слаборастворимых солей. При нарушении физиологического равновесия, приводящем к снижению растворимости в жидкостях организма человека, из нее выделяются и начинают расти твердые зародыши, формируясь в разноразмерные органоминеральные образования — объекты биоминера-логических исследований (Бородулин, Глыбочко, 2009; Брик, Радчук, 2007; Волков, Волкова, 2004; Каткова, 1996; Каткова, Боровкова, 2007; Козловский, 1973; Кокин, 2020; Колониченко, 2007; Кораго, 1992; Полиенко, Ермолаев, 1996; Полиенко, Севостьянова, 2003, 2010, 2012; Полиенко, Шубин, 1997; Силаев, Кокин, 2017, 2021; Cилаев, Пономарев, 2016; Сребродольский, 1983; Юшкин, 1999, 2002, 2006, 2007).
В настоящее время установлено, что абсолютное большинство уролитов имеет сложный фазовый состав (Боровкова, Филиппов, 2009; Козловский, 1973; Лебедев, Смирнова, 2021; Нигматулина, Сокол, 2004; Ракин, Каткова, 2006; Севостьянова, Полиенко, 2004). К числу наиболее часто встречающихся минералоподобных фаз относятся оксалаты кальция — уэвеллит и уэделлит; урициты (мочевая кислота); фосфаты — брушит, струвит, ньюбериит, бабьеррит, гопеит, биоапатит; сульфаты — гипс и др. Среди смешаннофазных камней наиболее распространены мочекислотно-оксалатные, фосфато-оксалатные, фосфатомочекис-лотные. Очевидно, что уже достигнутый уровень изученности уролитов не является окончательным и может быть существенно повышен благодаря непрерывно развивающимся методам экспериментальных минералогических исследований.
Объекты и методы исследований
В качестве объектов наших исследований (табл. 1) выступили: 1) 12 образцов мочевых камней мужчин и женщин в возрасте 27—83 лет с максимальным размером (5.5 ± 2.3) мм (Vx = 43 %) и массой (160.9 ± 201.4) мг (Vх = 125 %); 2) сопряженные с камнями 10 образцов мочи-1 ; 3) два дополнительных образца мочи-2 пациентов с пиелонефритом. В ходе исследований был использован широкий комплекс методов: оптическая микроскопия (компьютеризированный комплекс OLYMPUS BX51); химический анализ горных пород; определение содержания Сорг методом кулонометрического титрования по величине pH на анализаторе Ан-7529М; термический анализ на автоматическом 18
дериватографе Shimadzu DTG-60A/60AH; рентгеноструктурный анализ с использованием дифрактометра Shimadzu XRD-6000; ИК-спектроскопия с применением прибора «Люмекс ИнфраЛЮМ ФТ-02»; раман-спектроcкопия с использованием прибора Horiba LabRam HR 800; ЭПР на спектроскопе SE/X-2547; рентгенолюминесцентная спектроскопия на основе рентгеновского аппарата УРС-1.0 (трубка БСВ-2, Fe-антикатод, напряжение на катоде 50 кВ, анодный ток 14 мА), монохроматора AAS-1 (Carl Zeiss, Jena) и регистрирующего узла с ФЭУ-106; аналитическая сканирующая электронная микроскопия с применением комплекса Jeol JSM-6400; рентгенофлуоресцентный анализ на ЭД-спектрометре MESA-500W; определение изотопного состава углерода и азота в углеродистом веществе на аналитическом комплексе Flash EA, соединенном с масс-спектрометром Delta V Advantage; газовая пирохроматография с использованием пиролитического устройства и хроматографа «Цвет-800»; масс-спектрометрия с индуктивно связанной плазмой с использованием масс-спектрометра ELAN 9000 (Perkin Elmer). ИСП-МС-анализы на микроэлементы в образцах мочи выполнены в ЦКП «Геоаналитик» Института геологии и геохимии УрО РАН в рамках госбюджетной темы № 123011800012-9.
Для определения содержания аминокислот в белках мочи 1.0 мл пробы помещали в пробирку Eppendorf, добавляли 0.4 мл 40 % раствора трихлоруксусной кислоты (ТХУ) и встряхивали в течение 10 мин. Для отделения белков, выпадающих в осадок, пробирки помещали в микроцентрифугу и подвергали вращению со скоростью 12000 об./мин в течение 5 мин. Супернатант аккуратно сливали. Белковый осадок промывался от ТХУ, для чего к нему добавляли 1 мл смеси метанола и диэтилового эфира в объемной пропорции 1:1. Пробирка подвергалась встряхиванию в течение 1 мин, после чего ее центрифугировали с последующим аккуратным сливанием супернатанта. Операция повторялась трижды. Дальнейшая методика анализа аминокислот была стандартной.
Объекты для исследований были представлены ассистентом кафедры терапии медико-биологического факультета РНИМУ им. Н. И. Пирогова А. А. Слюсарь и врачом-урологом высшей категории Ростовской клинической больницы ЮОМЦ ФМБА России А. В. Слюсарем. В число этих объектов вошли пять образцов мочевых камней и скоррелированные с ними пять образцов мочи мужчин в возрасте 27—71 лет (в среднем 52 года), а также пять образцов мочевых камней и мочи женщин в возрасте 40—83 лет (в среднем 64 года). Масса камней: у мужчин — 236.7 ± 235.9 мг (у более пожилых камни массивнее); у женщин — 104.8 ± 137.2 мг (у более пожилых камни менее массивные). Кроме того, исследовались два образца мочи пациентов с хроническим пиелонефритом. Все образцы мочи варьировались по окраске от бесцветных до бурых.
Морфология, внутреннее строение и химико-фазовый состав
Исследованные мочевые камни характеризовались преимущественно светлой окраской и округлой формой, не обнаруживая корреляции ни с возрастом больных, ни с местом извлечения камней, ни с их раз-
Таблица 1. Реестр пациентов с мочекаменной болезнью (1—10), хроническим пиелонефритом (11, 12) и общая характеристика объектов исследований
Table 1. Registry of patients with urolithiasis (1-10), chronic pyelonephritis (11, 12) and general characteristics of the study subjects
мером (рис. 1). Уролиты широко варьировались по внутреннему строению благодаря сочетанию участков со скрытокристаллической, микрозернистой, пластинчатой, лучистой, лучисто-слоистой структурами (рис. 2—11), что вообще характерно для таких образований (Боровкова, 2004).
По валовому составу исследуемые камни близки к составу карбонатапатита, но по результатам рентгеноспектрального микрозондового анализа (табл. 2) в их составе выявлено до 14 фаз (в последовательности снижения частоты встречаемости, %): 1) органическое вещество, включая эритроциты и урициты (100); 2) водные кальциевые оксалаты (100); 3) силикаты и алюмосиликаты (90); 4) металлоорганические соединения (80); 5) самородные металлические фазы (60); 6) гидроген (Н)-сульфаты и фосфаты (60); 7) биоапатит (40); 8) эритроциты (30); 9) фосфато-сульфаты ба- рия (30); 10) сульфиды (10); 11) гидрокси (ОН)- и ги-дроген-хлориды (20); 12) сульфато-силикатофосфаты (10); 13) магнетит (10); 14) кремниевая (SiO2) фаза (10). По данным рентгеноструктурного анализа, часть микрофаз в составе исследованных камней характеризуется кристалличностью. В число таких фаз входят (d, в скобках индексы hkl):
Вевеллит , CaC2O4 H2O = 5.94—5.95 (10—1); 5.81 (110); 4.78 (200); 4.53 (101); 3.78 (21—1); 3.64—3.65 (020); 3.11 (12—1); 2.97 (10—2); 2.91 (310); 2.84 (121); 2.49 (112); 2.52 (301); 2.49—2.51 (112); 2.45 (31—2); 2.42 (32—1); 2.38 (400); 2.35 (130); 2.30 (11—2); 2.26 (202); 2.24 (031); 2.21 (40— 2); 2.13 (23—1); 2.09 (10—3); 2.08 (321); 1.996 (50—1); 1.976—1.978 (30—3); 1.95 (411); 1.933 (013); 1.890 (42— 2); 1.858 (312); 1.845 (610); 1.837 (510); 1.824 (040); 1.814 (12—3); 1.793 (132); 1.737 (32—3); 1.691 (520); 1.639 (213); 1.589 (600); 1.573 (20—4); 1.573 (20—4); 1.548—1.549 (033).
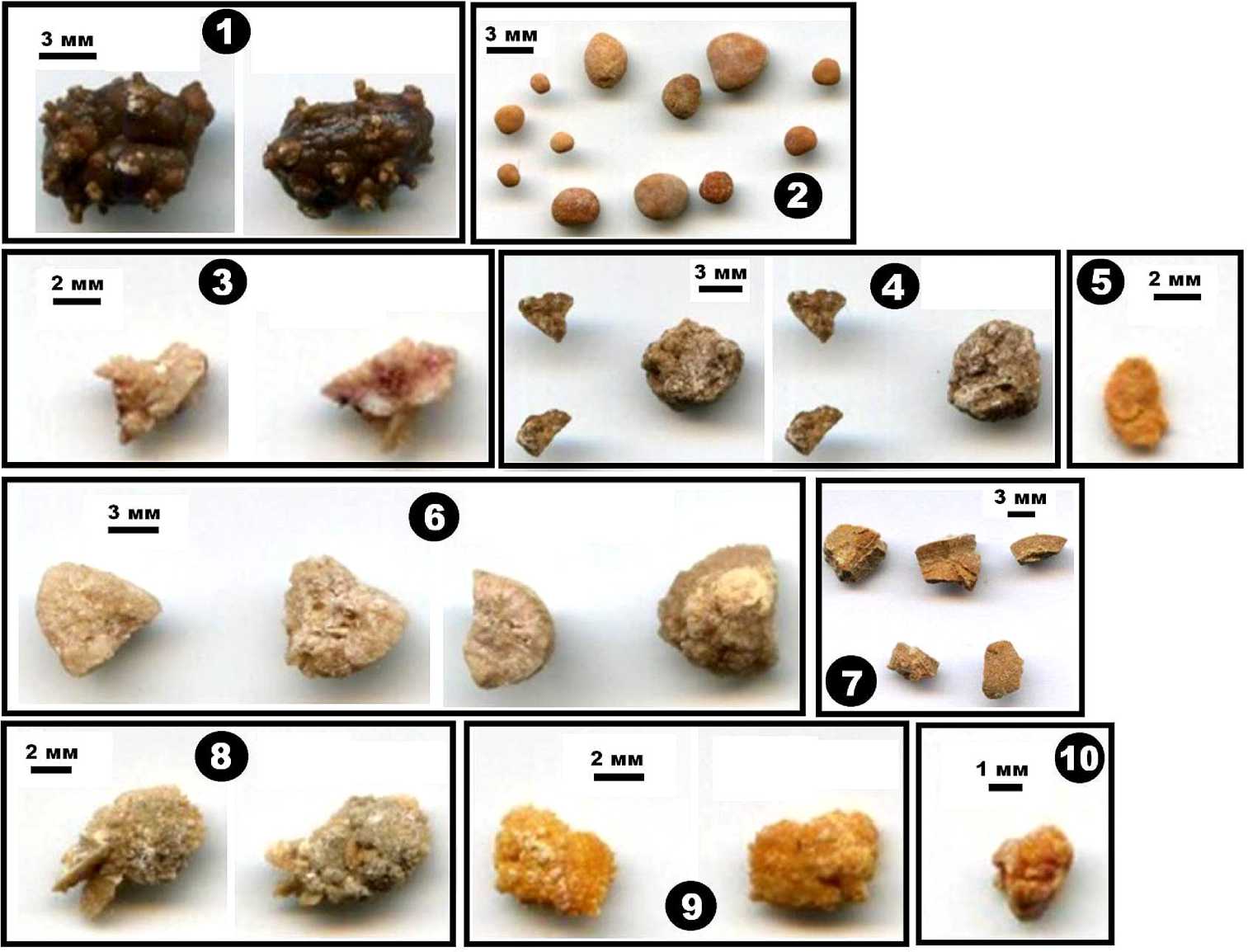
Рис. 1. Фотоизображения исследуемых мочевых камней. Номера изображений совпадают с номерами образцов в табл. 1
Fig. 1. Images of the studied urinary stones. The image numbers correspond to the sample numbers in Table 1
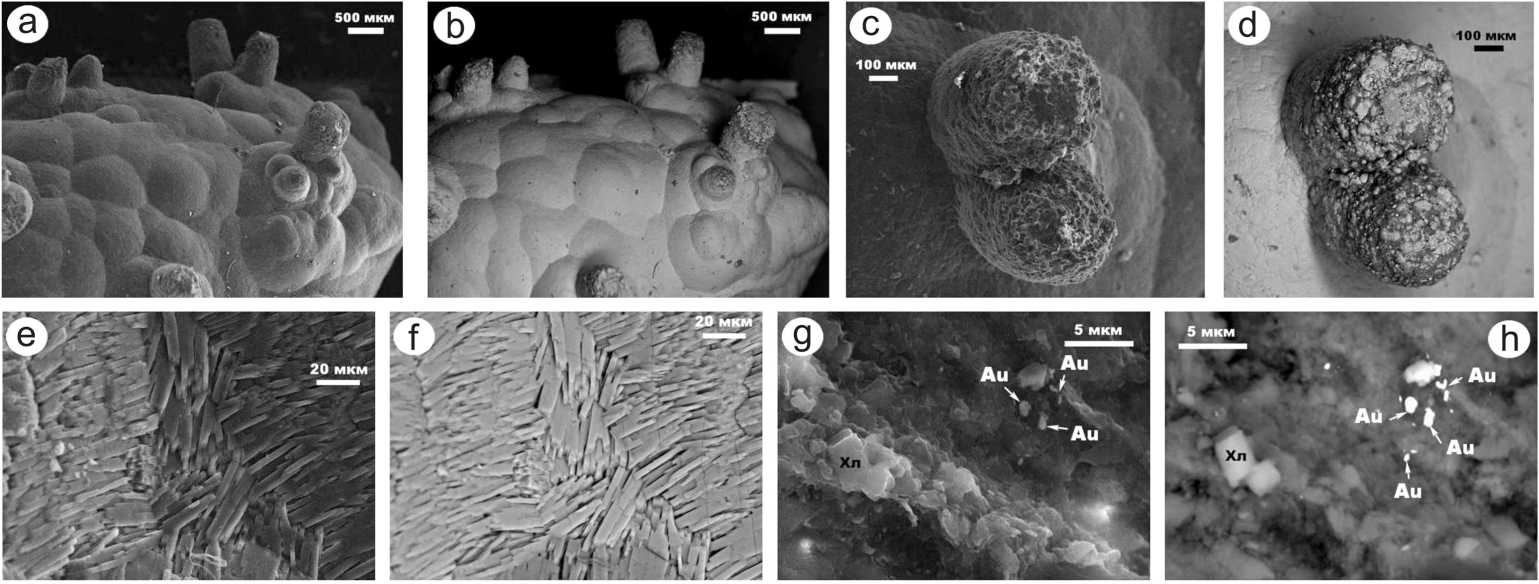
Рис.2 . СЭМ-изображения внутреннего строения обр. № 1 мочевых камней в режимах вторичных (a, c, e, g) и упругоотраженных (b, d, f, h) электронов. Фазы: Au — выделения самородного золота
Fig. 2. SEM images of the internal structure of urinary stones of sample No. 1 in the secondary (a, c, e, g) and elastically reflected (b, d, f, h) electron modes. Phases: Au — native gold precipitates
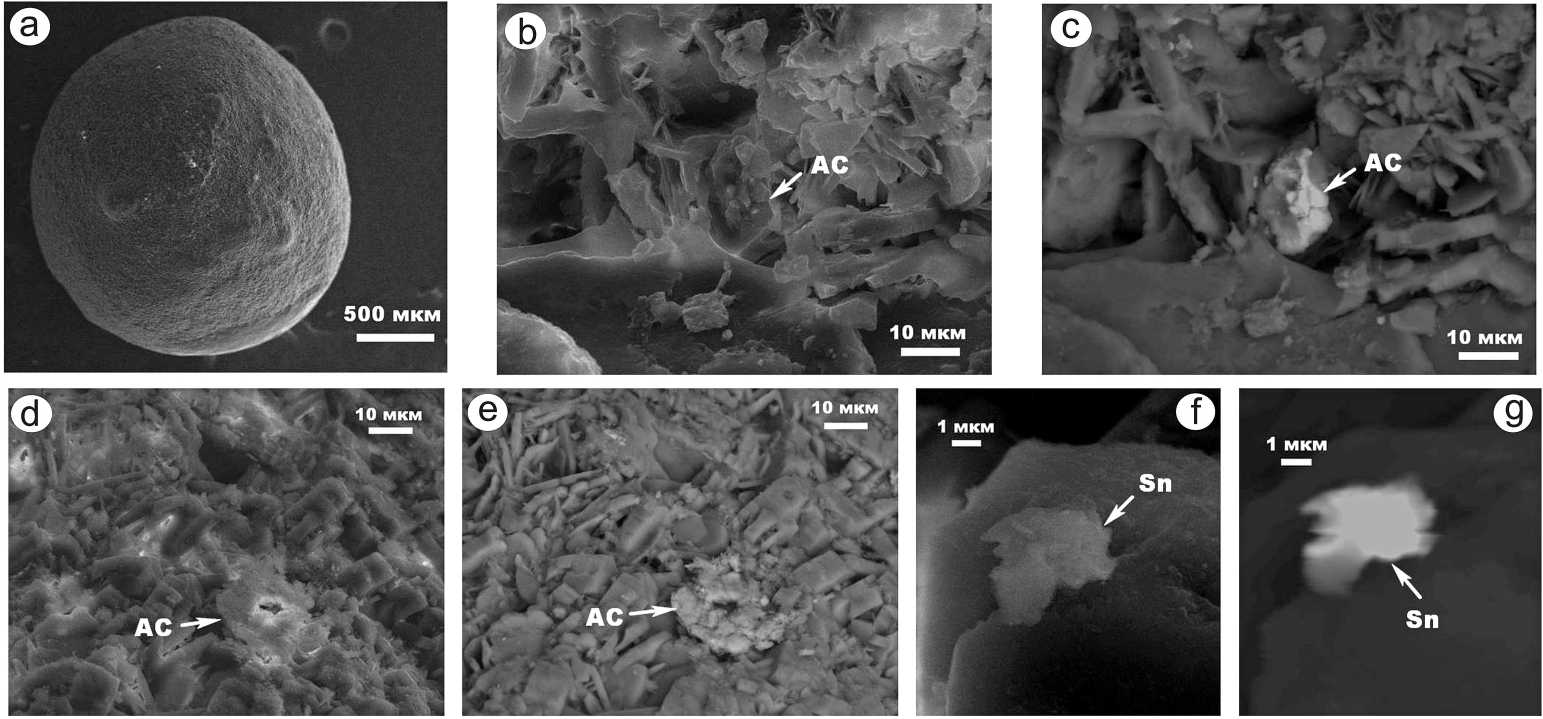
Рис. 3 . СЭМ-изображения внутреннего строения обр. № 2 мочевых камней в режимах вторичных (a, b, d, f) и упругоотраженных (c, e, g) электронов. Фазы: АС — силикаты и алюмосиликаты, Sn — выделения самородных металлов
-
Fig. 3. SEM images of the internal structure of urinary stones of sample No. 2 in the modes of secondary (a, b, d, f) and elastically reflected (c, e, g) electrons. Phases: AC — silicates and aluminosilicates, Sn — precipitates of native metals
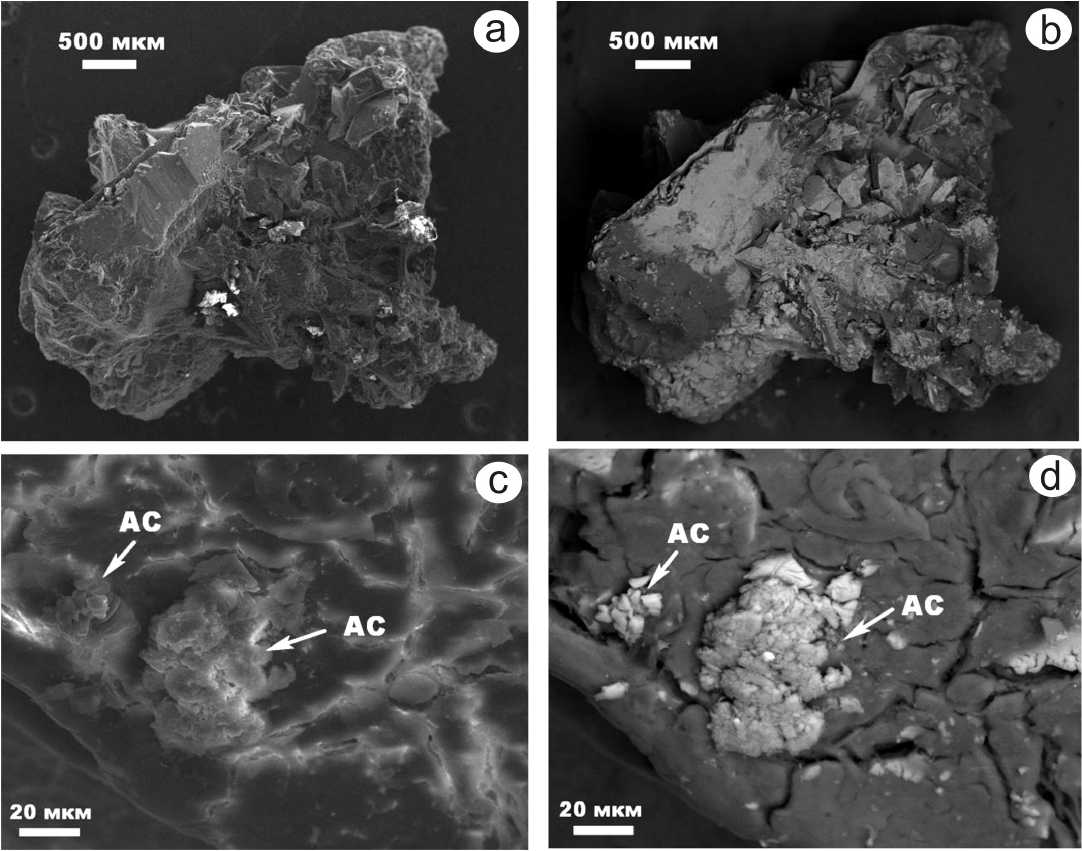
Рис. 4 . СЭМ-изображения внутреннего строения обр. № 3 мочевых камней в режимах вторичных (a, c) и упругоотраженных (b, d) электронов. Фазы: АС — силикаты и алюмосиликаты
-
Fig. 4. SEM images of the internal structure of urinary stones of sample No. 3 in the secondary (a, c) and elastically reflected (b, d) electron modes. Phases: AC — silicates and aluminosilicates

Рис. 5 . СЭМ-изображения внутреннего строения образца № 4 мочевых камней в режимах вторичных (a, c, e, g) и упругоотраженных (b, d, f, h) электронов. Фазы: ЭР — эритроциты
-
Fig. 5. SEM images of the internal structure of urinary stones of sample No. 4 in the secondary (a, c, e, g) and elastically reflected (b, d, f, h) electron modes. Phases: ЭР — erythrocytes

Рис. 6 . СЭМ-изображения внутреннего строения обр. № 5 мочевых камней в режимах вторичных (a, b, d, f) и упругоотраженных (c, e, g) электронов. Фазы: АС — силикаты и алюмосиликаты, Zn — выделение самородных металлов
-
Fig. 6. SEM images of the internal structure of urinary stones of sample No. 5 in the secondary (a, b, d, f) and elastically reflected (c, e, g) electron modes. Phases: AC — silicates and aluminosilicates, Zn — native metal precipitation

Рис. 7 . СЭМ-изображения внутреннего строения обр. № 6 мочевых камней в режимах вторичных (a, c, e, g) и упругоотраженных (b, d, f, h) электронов. Фазы: Sn-Cu и Sn — выделения самородных металлов; Bi-Ca — металлоорганические соединения
-
Fig. 7. SEM images of the internal structure of urinary stones of sample No. 6 in the secondary (a, c, e, g) and elastically reflected (b, d, f, h) electron modes. Phases: Sn-Cu and Sn are precipitates of native metals; Bi-Ca are organometallic compounds

Рис. 8 . СЭМ-изображения внутреннего строения обр. № 7 мочевых камней в режимах вторичных (a, c, e, g, i) и упругоотраженных (b, d, f, h, j) электронов. Фазы: АС — силикаты и алюмосиликаты; Bi-Ca — металлоорганические соединения
-
Fig. 8. SEM images of the internal structure of urinary stones of sample No. 7 in the secondary (a, c, e, g, i) and elastically reflected (b, d, f, h, j) electron modes. Phases: AC — silicates and aluminosilicates; Bi-Ca — organometallic compounds

Рис. 9 . СЭМ-изображения внутреннего строения обр. № 8 мочевых камней в режимах вторичных (a, c, e) и упругоотраженных (b, d, f) электронов
Fig. 9. SEM images of the internal structure of urinary stones of sample No. 8 in the secondary (a, c, e) and elastically reflected (b, d, f) electron modes

Рис. 10 . СЭМ-изображения внутреннего строения обр. № 9 мочевых камней в режимах вторичных (a, c, e, g, i, k) и упругоотраженных (b, d, f, h, j, l) электронов. Фазы: Ca-Ti — сульфато-силикатофосфаты; ФCВа — фосфатосульфаты бария; ГСФ — гидроген-сульфатофосфаты
Fig. 10. SEM images of the internal structure of urinary stones of sample No. 9 in the secondary (a, c, e, g, i, k) and elastically reflected (b, d, f, h, j, l) electron modes. Phases: Ca-Ti — sulfate-silicatephosphates; ФCВа — barium phosphate-sulfates; ГСФ — hydrogen sulfate-phosphates

Рис.11 . СЭМ-изображения внутреннего строения обр. № 10 мочевых камней в режимах вторичных (a, b, d, f, h, j, l, n, p) и упругоотраженных (c, e, g, i, k, m, o, r) электронов. Фазы: АС — силикаты и алюмосиликаты; Fe, Au — выделения самородных металлов; Bi-Ca, Ni-Cu — металлоорганические соединения
Fig. 11. SEM images of the internal structure of urinary stones of sample No. 10 in the secondary (a, b, d, f, h, j, l, n, p) and elastically reflected (c, e, g, i, k, m, o, r) electron modes. Phases: AC — silicates and aluminosilicates; Fe, Au — precipitates of native metals; Bi-Ca, Ni-Cu — organometallic compounds
Ведделлит , CaC2O4 2H2O = 8.76—8.77 (110); 6.19 (200); 4.42—4.43 (211); 4.36 (220); 3.91 (310); 3.68 (002); 3.39 (112); 3.16 (202); 3.09 (400); 2.81-2.82 (222); 2.78 (411); 2.67 (312); 2.42 (510); 2.41 (103); 2.37 (402); 2.34 (501); 2.28 (331); 2.24 (213); 2.21 (422); 2.12 (530); 2.02 (512); 1.994 (323); 1.957 (611); 1.898 (413); 1.836—1.837 (532); 1.797 (602); 1.787 (631); 1.762 (204); 1.741 (503); 1.711 (640); 1.695 (224); 1.624 (730); 1.624 (730); 1.578 (712); 1.564 (613); 1.552 (642).
Урицит (мочевая кислота) , C5H4N4O3 = 6.59—6.63 (200); 5.66—5.68 (001);4.94—4.96 (210); 4.78—4.80 (111); 4.50—4.51 (011); 3.87—3.89 (11—1); 3.72—3.74 (020); 3.6 (20—1); 3.28—3.29 (400): 3.20—3.21 (121); 3.11—3.12 (021); 3.01 (410); 2.88 (12—1); 2.80 (402);2.63—2.64 (012): 2.58(421): 2.46—2.47 (420); 2.42—2.43 (40—1); 2.41 (11— 2); 2.32 (230); 2.28—2.29 (521); 2.25 (022); 2.19—2.24 (600); 2.15 (13—1); 2.10 (12—2); 2.03 (42—12); 1.918— 1.919 (332); 1.879—1.881 (003); 1.801—1.809 (721); 1.796 (731); 1.77 (322); 1.746 (123); 1.667—1.668 (623; 1.641— 1.642 (800); 1.616—1.617 (62—1); 1.594—1.598 (242); 1.553—1.554 (042).
Тиннункулит (урицит дигидрат), С5H4N4O32H2O = 8.84 (200); 5.99 (101); 5.67 (210); 4.23 (211); 3.78 (410; 3.72 (311); 3.42 (220); 3.25 (411); 3.20 (021); 3.15 (121; 3.06 (221); 2.8 (302); 2.72 (610); 2.61 (312); 2.58 (402; 2.50 (611; 2.43 (412); 2.37 (716); 2.19 (800); 2.15 (430).
Брушит , CaH[PO4] 2H2O = 7.6 (020); 4.93 (–111); 4.24 (021; 3.80 (040); 3.64 (–131); 3.05 (041); 3.93 (–221); 2.86 (–112); 2.67 (150); 2.62 (220); 2.60 (–202); 2.52 (–132); 2.42 (–241); 2.41 (022); 2.27 (061; 2.25 (240); 2.17 (151); 2.15 (–242); 2.12 (042); 2.10 (–152); 2.08 (–311); 2.02 (170); 2.0 (171); 1.976 (112); 1.898 (08); 1.876 (260); 1.858 (–223); 1.815 (241); 1.797 (062); 1.787 (081); 1.741 (330).
Именно эти кристаллические фазы считаются в почечных камнях наиболее ранними и наиболее влияющими на регулирование режима пересыщения минералообразующих растворов в организме человека (Изатулина, Гуржий, 2014). Не исключено, что число окристаллизованных фаз не ограничивается оксалатами, урицитами и гидроген-фосфатами, но рентгеновский результат сильно лимитируется содержанием фаз и размером их индивидов.
ИК-поглощение в среднем ИК-диапазоне в основном определяется органическим веществом, на что указывают следующие группы полос в направлении снижения длины волны: 1) 428—540 см–1 — деформационные колебания химических связей –С–Н (ароматические функциональные группы); 2) 710— 770 см–1 — внеплоскостные колебания химических связей С—С (ароматические функциональные группы); 3) 990—1135 см–1 — деформационные колебания химических связей С–Н, –СН2=СН2=СН2– и –СН2–СН3–
Таблица 2. Химико-фазовый состав мочевых камней по данным рентгеноспектрального микрозондового анализа
Table 2. Chemical-phase composition of urinary stones according to X-ray spectral microprobe analysis
|
№ |
Фазы / Phases |
Объекты исследований / Objects of study |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
||
|
1 |
Дисперсное органическое вещество, включая урициты Dispersed organic matter, including uric acid |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
|
2 |
Органическое вещество в форме эритроцитов Organic matter in the form of red blood cells |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
+ |
+ |
+ |
|
3 |
Водные оксалаты кальция (вевеллит и веддделлит) Hydrogenated calcium oxalates (whewellite and weddellite) |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
|
4 |
Металлоорганические соединения Organometallic compounds |
+ |
+ |
н. о. |
+ |
+ |
+ |
+ |
н. о. |
+ |
+ |
|
5 |
Самородные металлические фазы Native metallic phases |
н. о. |
+ |
» |
+ |
+ |
+ |
н. о. |
+ |
+ |
н. о. |
|
6 |
Сульфиды / Sulfides |
» |
н. о. |
» |
н. о. |
+ |
н. о. |
» |
н. о. |
н. о. |
» |
|
7 |
SiO2-фаза / SiO2 phase |
» |
+ |
» |
» |
н. о. |
» |
» |
» |
» |
» |
|
8 |
Магнетит / Magnetite |
» |
+ |
» |
» |
» |
» |
» |
» |
» |
» |
|
9 |
Силикаты и алюмосиликаты Silicates and aluminosilicates |
+ |
+ |
+ |
+ |
+ |
+ |
+ |
» |
+ |
+ |
|
10 |
Сульфато-силикатофосфаты кальция-титана Calcium-titanium sulfate-silicate-phosphates |
н. о. |
н. о. |
н о. |
н. о. |
н. о. |
н. о. |
н. о. |
» |
+ |
н. о. |
|
11 |
Гидроген-гидроксильные фосфатосульфаты бария Barium hydrogen-hydroxyl phosphate-sulfates |
» |
» |
» |
+ |
» |
» |
» |
» |
+ |
+ |
|
12 |
Гидрокси- и гидроген-хлориды Hydroxy- and hydrogen chlorides |
+ |
» |
+ |
н. о. |
» |
» |
» |
» |
н. о. |
н. о. |
|
13 |
Гидроген-сульфаты и гидроген-фосфаты, включая брушит Hydrogen sulfates and hydrogen phosphates, including brushite |
н. о. |
+ |
н. о. |
» |
+ |
+ |
» |
+ |
+ |
+ |
|
14 |
Биоапатит / Bioapatite |
+ |
» |
» |
+ |
н. о. |
+ |
» |
+ |
н. о. |
н. о. |
|
Примечание. + — присутствуют, н. о. — не обнаружены. Note. + — present, н. о. — not detected. |
|||||||||||
|
СН3–СН2– (фенольные гидроксилы, спирты, алифатические эфиры); 4) 1300—1387 см–1 — деформационные колебания групп ОН в химических связях СН2(ОН)–СО–СН2(ОН) (алифатические группы); 5) 1642—1674 см–1 — деформационные колебания химических связей СО–ОН (группы аминов, карбонильные группы) в органическом веществе и биоминералах — биоапатите и сульфатах; 6) 2800—2820 см–1 — валентные колебания химических связей СН и СН2 |
(алифатические функциональные группы); 7) 3006— 3481 см–1 — валентные колебания химических связей NH и групп ОН (группы аминов и гидроксильные группы). Валовый элементный состав органического вещества в исследованных камнях приведен в табл. 3. Полученные для них данные примерно соответствуют данным и для желчных камней (Каткова, Боровкова, 2007), и для человеческого организма в целом (Колониченко, 2007). |
||||||||||
Таблица 3. Элементный состав частиц органического вещества, мас. %
Table 3. Elemental composition of organic matter particles, wt.%
|
Компоненты Components |
2/1 |
2/2 |
2/3 |
7/1 |
7/2 |
7/3 |
7/4 |
9/1 |
9/2 |
9/3 |
9/4 |
Статистика Statistic X ± S x (V x , %) |
|
С |
59.91 |
60.7 |
63.28 |
62.88 |
59.16 |
60.39 |
61.32 |
61.89 |
62.24 |
59.36 |
60.57 |
61.06 ± 1.38 (2.3) |
|
N+ Н |
23.74 |
25.79 |
23.42 |
24.02 |
26.29 |
24.5 |
28.86 |
24.67 |
24.35 |
27.99 |
26.83 |
25.5 ± 1.81 (7.1) |
|
O |
16.35 |
13.51 |
13.3 |
13.1 |
14.55 |
15.11 |
9.82 |
13.44 |
13.41 |
12.65 |
12.6 |
13.44 ± 1.64 (12.2) |
Примечание. Статистические данные: Х — среднее арифметическое, Sх — стандартное отклонение (СКО), Vх — коэффициент вариации. Атомный состав / Atomic composition: 2/1 — С0.66(N+Н)0,21O0.13; 2/2 — С0.66(N+Н)0,23O0.11 ; 2/3 — С0.69(N+Н)0,2O0.11; 7/1 — С0.68(N+Н)0,21O0.11; 7/2 — С0.65(N+Н)0,23O0.12; 7/3 — С0.66(N+Н)0,21O0.13; 7/4 — С0.67(N+Н)0,25O0.08; 9/1 — С 0.67 (N+Н) 0,21 O 0.12 ; 9/2 — С 0.68 (N+Н) 0,21 O 0.11 ; 9/3 — С 0.65 (N+Н) 0,25 O 0.1 ; 9/4 — С 0.66 (N+Н) 0,23 O 0.11 .
Note. Statistical data: X — arithmetic mean, Sx — standard deviation (SD), Vx — coefficient of variation.
Таблица 4. Химический состав неорганической компоненты в обычных урицитсодержащих частицах органического вещества и эритроцитах (*), мас. %
На кривых нагревания присутствуют экзотермические эффекты, отвечающие выгоранию органического вещества: пик В1 = (282—349 °С) отражает «липидный» этап ДТА (выгорание углеводородов); В2 = (365—476 °С) — «аминокислотный» этап ДТА (выгорание белков) (Силаев, Юшкин, 2019). Кроме того, на кривых нагревания наблюдаются и три эндотермических эффекта: 1) экстремум при 55—100 °С (потеря гигроскопической воды); 2) перелом при 660—665 °С (возможно, конституционная вода в алюмосиликатах); 3) экстремум при 800—831 °С (вероятно, диссоциация кислородных солей (Архипенко, Бокий, 1982)).
По характеру распределения выявленных фаз исследуемые мочевые камни подразделяются на два типа. К первому — преобладающему — типу (№ обр. 1, 2, 4—6, 9, 10) относятся многофазные (от 6 до 14 фаз) камни, равномерно распределенные между мужчинами и женщинами с возрасте 27—83 лет. Второму — более редкому — типу (№ обр. 3, 7, 8) соответствуют ограниченно-фазные (3—5 фаз), преимущественно мужские. В целом полученные нами данные значительно расширяют известные представления о фазовом составе данного вида минерализаций (Боровкова, Филиппов, 2009; Изатулина, Гуржий, 2014; Ламанова, 2007; Лебедев, Смирнова, 2021; Мак-Коннелл, 1977; Машина, 2017; Нигматулина, Сокол, 2004; Ракин, Каткова, 2006; Севостьянова, Полиенко, 2004; Huskic, Pecov, 2016).
Органическое вещество составляет до трети вещества мочевых камней, будучи равномерно рассеянным по объему камня в виде микровключений, линзочек и прослоев. По элементному составу — C0.65— 0.68(N+H)0.2—0.25O0.08—0.13(табл. 3) — оно примерно со-
ответствует смеси урицитов и бактериального вещества. Довольно часто наряду с обычными частицами органического вещества встречаются формы, похожие на эритроциты (клетки крови). Как правило, во всех этих органических образованиях присутствует поликомпонентная неорганическая примесь (табл. 4), вполне отражающая сложный минерально-фазовый состав камней. Эритроциты при этом такими примесями беднее раза в 1.5.
В части биоминералов в исследованных камнях преобладают водные оксалаты кальция , часто представленные хорошо окристаллизованными пластинчатыми формами (моноклинно-призматическими). При этом оксалаты характеризуются сильно примесным составом, комплексно отражающим всю сложность фазового состава камней (табл. 5).
Широкое распространение и разнообразие по составу в мочевых камнях имеет металлоорганические соединения , которые современными физиками рассматриваются как вполне закономерные формы конденсации металлов в живых организмах (Миронова, 2006). В нашем случае в камнях выявлены до восьми видов и разновидностей таких форм (табл. 6), которые в последовательности снижения частоты встречаемости металлических компонент могут быть представлены следующим образом: 1) оловянно-медные — Cu0.38— 0.58 Sn 0.05—0.44 Zn 0—0.36 Pb 0—0.04 Ni 0—0.05 Fe 0—0.06 Si 0—0.09 Al 0— 0.07 Ca 0—0.02 P 0—0.22 S 0—0.07 Cl 0—0.12 ; 2) золотые — Au 0.51— 0.77 Cu 0—0.07 Pв 0—0.01 Ni 0—0.06 Si 0—0.18 Al 0—0.31 Ca 0—0.06 K 0— 0.03 Cl 0—0.06 ; 3) железные — Fe 0.88—1 P 0—0.02 S 0—0.03 Cl 0—0.07 ; 4) железистые — Fe 0.42—0.47 Cu 0—0.06 Zn 0.06 Ni 0—0.03 Pb 0—0.01 Au 0.01 Si 0.19—0.25 Al 0.02—0.21 Ca 0.03—0.04
Table 4. Chemical composition of the inorganic component in ordinary uric acid-containing particles of organic matter and erythrocytes (*), wt. %
|
№ |
SiO 2 |
Al2O3 |
Fe 2 O 3 |
MgO |
CaO |
Na2O |
K 2 O |
P 2 O 5 |
SO 3 |
Cl |
Сумма / Sum |
|
1/1 |
1.61 |
н. о. |
н. о. |
н. о. |
4.08 |
н. о. |
0.25 |
н. о. |
3.24 |
2.67 |
11.85 |
|
1/2 |
0.3 |
» |
» |
» |
4.54 |
» |
» |
0.36 |
2.57 |
2.32 |
10.09 |
|
1/3 |
0.35 |
» |
» |
» |
4.03 |
» |
0.25 |
0.6 |
3.03 |
1.33 |
9.59 |
|
1/4 |
Н. о. |
» |
» |
» |
3.18 |
0.91 |
0.32 |
0.34 |
2.88 |
1.34 |
8.97 |
|
1/5 |
0.46 |
» |
» |
» |
0.59 |
н. о. |
0.35 |
0.25 |
2.54 |
2.84 |
7.03 |
|
2/1 |
0.41 |
» |
» |
» |
0.32 |
» |
н. о. |
н. о. |
н. о. |
н. о. |
0.73 |
|
2/2 |
1.11 |
0.54 |
» |
» |
0.16 |
» |
» |
» |
» |
» |
1.81 |
|
2/3 |
0.3 |
н. о. |
» |
» |
0.19 |
» |
0.25 |
» |
0.44 |
» |
1.18 |
|
2/4 |
0.23 |
» |
» |
» |
н. о. |
» |
0.23 |
» |
н. о. |
» |
0.46 |
|
3/1 |
0.25 |
» |
» |
» |
* |
» |
н. о. |
2.18 |
1.45 |
0.01 |
3.89 |
|
3/2 |
0.43 |
» |
» |
» |
0.68 |
» |
1.35 |
2.96 |
1.87 |
0.01 |
7.3 |
|
5/1 |
0.24 |
» |
» |
» |
н. о. |
» |
н. о. |
н. о. |
н. о. |
н. о. |
0.24 |
|
5/2 |
4.16 |
» |
» |
0.85 |
5.41 |
2.16 |
0.75 |
2.72 |
9.36 |
0.1 |
25.51 |
|
5/3 |
1.19 |
» |
» |
н. о. |
0.36 |
н. о. |
0.22 |
0.29 |
0.39 |
0.92 |
3.37 |
|
5/4 |
Н. о. |
» |
» |
» |
7.22 |
» |
0.92 |
4.89 |
5.62 |
0.08 |
18.73 |
|
5/5 |
« |
» |
» |
» |
н. о. |
» |
н. о. |
н. о. |
н. о. |
3.69 |
3.69 |
|
6/1 |
0.6 |
» |
» |
» |
3.16 |
» |
» |
2.03 |
0.4 |
н. о. |
6.19 |
|
7/1 |
0.29 |
» |
» |
» |
н. о. |
» |
» |
н. о. |
н. о. |
» |
0.29 |
|
7/2 |
Н. о. |
» |
» |
» |
0.14 |
» |
0.14 |
» |
» |
» |
0.28 |
|
Х |
0.63 |
0.03 |
0 |
0.04 |
1.79 |
0.16 |
0.26 |
0.87 |
1.78 |
0.81 |
6.38 |
|
S x |
0.96 |
0.12 |
0.19 |
2.3 |
0.53 |
0.37 |
1.4 |
2.43 |
1.21 |
6.79 |
|
|
9/1* |
0.4 |
н. о. |
2.86 |
н. о. |
0.31 |
н. о. |
0.89 |
н. о. |
0.4 |
0.29 |
5.15 |
|
9/2* |
0.93 |
» |
н. о. |
» |
0.54 |
» |
1.63 |
* |
0.39 |
0.47 |
3.96 |
|
10/1* |
0.86 |
» |
» |
» |
0.3 |
0.79 |
1.0 |
0.78 |
1.43 |
1.01 |
6.17 |
|
10/2* |
0.31 |
» |
» |
» |
н. о. |
н. о. |
н. о. |
0.37 |
н. о. |
н. о. |
0.68 |
|
10/3* |
0.28 |
» |
» |
» |
» |
1.11 |
» |
0.95 |
4.04 |
1.41 |
7.79 |
|
X |
0.56 |
0 |
0.57 |
0 |
0.23 |
0.38 |
0.7 |
0.42 |
1.25 |
0.64 |
4.75 |
|
S x |
0.31 |
1.28 |
0.23 |
0.53 |
0.7 |
0.44 |
1.65 |
0.57 |
2.67 |
Таблица 5. Химический состав неорганической компоненты в водных оксалатах кальция, мас. % Table 5. Chemical composition of the inorganic component in aqueous calcium oxalates, wt.%
|
№ |
SiO 2 |
Al2O3 |
CuO |
ZnO |
CaO |
BaO |
K 2 O |
P 2 O 5 |
SO 3 |
Cl |
Сумма / Sum |
|
1/1 |
0.6 |
н. о. |
н. о. |
н. о. |
31.17 |
н. о. |
н. о. |
0.97 |
0.67 |
0.17 |
33.58 |
|
1/2 |
0.71 |
» |
» |
» |
32.55 |
» |
0.2 |
0.83 |
0.69 |
0.15 |
35.13 |
|
2/1 |
0.6 |
» |
» |
» |
31.17 |
» |
н. о. |
0.97 |
0.67 |
0.17 |
33.58 |
|
2/2 |
0.71 |
» |
» |
» |
32.55 |
» |
0.2 |
0.83 |
0.69 |
0.15 |
35.13 |
|
2/3 |
6.2 |
5.53 |
» |
» |
24.86 |
» |
0.32 |
1.45 |
1.24 |
1.08 |
40.68 |
|
2/4 |
18.71 |
16.0 |
» |
» |
21.77 |
» |
0.13 |
0.73 |
1.22 |
0.52 |
59.08 |
|
3/1 |
н. о. |
н. о. |
» |
» |
34.41 |
» |
н. о. |
н. о. |
н. о. |
н. о. |
34.41 |
|
3/2 |
» |
» |
» |
» |
27.26 |
» |
» |
» |
» |
» |
27.26 |
|
3/3 |
» |
» |
» |
» |
35.52 |
» |
» |
» |
0.67 |
» |
36.19 |
|
3.4 |
» |
» |
1.31 |
0.77 |
30.85 |
» |
» |
» |
н. о. |
» |
32.93 |
|
3/5 |
1.19 |
0.97 |
н. о. |
н. о. |
26..44 |
» |
» |
» |
» |
» |
28.6 |
|
4/1 |
н. о. |
н. о. |
» |
» |
31.31 |
» |
» |
0.59 |
0.51 |
» |
31.9 |
|
4/2 |
0.56 |
» |
» |
» |
33.87 |
» |
» |
н. о. |
5.55 |
» |
34.43 |
|
4/3 |
н. о. |
» |
» |
» |
30.91 |
» |
» |
1.15 |
0.32 |
» |
32.57 |
|
4/4 |
0.84 |
» |
» |
» |
32.06 |
9.87 |
» |
н. о. |
0 |
» |
48.32 |
|
4/5 |
н. о. |
» |
» |
» |
31.57 |
н. о. |
» |
« |
0.32 |
» |
31.89 |
|
4/6 |
0.47 |
» |
» |
» |
33.67 |
» |
» |
0.64 |
н. о. |
» |
34.78 |
|
4/7 |
1.49 |
1.03 |
» |
» |
29.45 |
» |
» |
н. о. |
0.6 |
» |
32.57 |
|
6/1 |
н. о. |
н. о. |
» |
» |
32.14 |
» |
» |
0.79 |
0.63 |
0.19 |
33.75 |
|
6/2 |
» |
» |
» |
» |
32.78 |
» |
» |
0.39 |
н. о. |
н. о. |
33.17 |
|
7/1 |
0.7 |
» |
» |
» |
38.18 |
» |
» |
н. о. |
» |
» |
33.88 |
|
7/2 |
0.42 |
» |
» |
» |
33.49 |
» |
» |
0.4 |
» |
» |
34.31 |
|
7/3 |
0.46 |
» |
» |
» |
36.79 |
» |
» |
н. о. |
» |
» |
37.25 |
|
7/4 |
0.63 |
» |
» |
» |
37.76 |
» |
» |
» |
» |
» |
38.39 |
|
8/1 |
н. о. |
» |
» |
» |
35.57 |
» |
» |
0.38 |
» |
» |
35.95 |
|
8/2 |
» |
» |
» |
» |
35.11 |
» |
» |
0.77 |
» |
» |
35.88 |
|
8/3 |
» |
» |
» |
» |
34.42 |
» |
» |
н. о. |
» |
» |
34.42 |
|
9/1 |
» |
» |
» |
» |
32.3 |
» |
» |
0.84 |
0.94 |
0.3 |
34.38 |
|
9/2 |
» |
» |
» |
» |
34.26 |
» |
» |
0.61 |
н. о. |
н. о. |
34.87 |
|
9/3 |
» |
» |
» |
» |
35.35 |
» |
» |
1.19 |
0.95 |
0.41 |
37.9 |
|
9/4 |
» |
» |
» |
» |
32.54 |
» |
» |
0.92 |
0.43 |
н. о. |
33.89 |
|
9/5 |
0.32 |
» |
» |
» |
33.09 |
» |
» |
0.91 |
н. о. |
» |
34.32 |
|
9/6 |
н. о. |
» |
» |
» |
33.59 |
» |
» |
0.39 |
0.46 |
» |
34.44 |
|
9/7 |
» |
» |
» |
» |
34.1 |
» |
» |
0.84 |
0.45 |
» |
35.39 |
|
9/8 |
» |
» |
» |
» |
30.98 |
» |
» |
0.8 |
0.65 |
0.34 |
32.77 |
|
9/9 |
1.46 |
» |
» |
» |
35.29 |
» |
» |
0.78 |
0.75 |
0.29 |
38.57 |
|
9/10 |
н. о. |
» |
» |
» |
29.13 |
» |
» |
0.49 |
0.6 |
0.34 |
30.56 |
|
9/11 |
» |
» |
» |
» |
32.67 |
» |
» |
0.89 |
0.65 |
0.25 |
34.46 |
|
9/12 |
0.68 |
» |
» |
» |
29.45 |
» |
0.16 |
0.68 |
0.83 |
0.54 |
32.34 |
|
9/13 |
н. о. |
» |
» |
» |
33.8 |
» |
н. о. |
0.98 |
0.55 |
н. о. |
35.33 |
|
9/14 |
» |
» |
» |
» |
31.97 |
» |
» |
0.74 |
н. о. |
0.13 |
32.84 |
|
9/15 |
» |
» |
» |
» |
32.13 |
» |
» |
0.85 |
0.41 |
0.13 |
33.52 |
|
X |
0.88 |
0.57 |
0.03 |
0.02 |
31.86 |
0.24 |
0.02 |
0.54 |
0.51 |
0.12 |
35.13 |
|
S x |
2.99 |
2.62 |
0.2 |
1.12 |
4.61 |
1.32 |
0.07 |
0.42 |
0.88 |
0.22 |
4.99 |
Таблица 6. Химический состав (мас. %) металлоорганических соединений
Table 6. Chemical composition (wt.%) of organometallic compounds
|
№ |
Au |
Fe |
Ni |
Cu |
Zn |
Pb |
Sn |
Si |
Al |
Mg |
Ca |
Na |
K |
P |
S |
Cl |
Сумма / Sum |
|
1/1 |
2.41 |
22.7 |
2.07 |
н. о. |
3.29 |
0.9 |
н. о. |
5.95 |
6.41 |
н. о. |
1.23 |
н. о. |
0.54 |
н. о. |
н. о. |
0.93 |
46.43 |
|
1/2 |
1.39 |
26.18 |
2.01 |
» |
4.2 |
н. о. |
» |
5.86 |
6.48 |
» |
1.79 |
» |
0.43 |
» |
0.37 |
1.04 |
49.75 |
|
1/3 |
71.7 |
н. о. |
н. о. |
» |
н. о. |
1.98 |
» |
3.41 |
3.51 |
» |
0.89 |
» |
0.46 |
» |
н. о. |
0.47 |
88.42 |
|
1/4 |
51.72 |
» |
» |
» |
» |
н. о. |
» |
4.23 |
4.39 |
» |
1.27 |
» |
0.68 |
» |
» |
0.98 |
63.27 |
|
2/1 |
н. о. |
» |
» |
2.5 |
» |
» |
3.3 |
н. о. |
н. о. |
» |
н. о. |
» |
н. о. |
» |
» |
0.31 |
6.11 |
|
2/2 |
» |
» |
0.58 |
1.7 |
4.61 |
» |
5.02 |
» |
» |
» |
» |
» |
» |
» |
» |
0.5 |
12.41 |
|
2/3 |
» |
» |
н. о. |
3.66 |
0.82 |
» |
7.86 |
» |
» |
» |
» |
» |
» |
» |
» |
0.26 |
12.6 |
|
2/4 |
» |
» |
0.55 |
4.37 |
4.26 |
» |
2.91 |
» |
» |
» |
» |
» |
» |
» |
» |
0.5 |
12.59 |
|
2/5 |
» |
0.93 |
н. о. |
16.45 |
н. о. |
4.48 |
4.1 |
1.46 |
1.02 |
» |
0.52 |
» |
0.11 |
4.01 |
0.46 |
0.74 |
34.28 |
|
2/6 |
» |
0.57 |
» |
20.0 |
» |
5.39 |
2.18 |
0.88 |
87 |
» |
0.6 |
» |
0.18 |
4.43 |
0.34 |
0.96 |
36.4 |
|
2/7 |
» |
1.56 |
» |
18.92 |
» |
1.46 |
7.69 |
1.16 |
0.52 |
» |
н. о. |
» |
н. о. |
1.78 |
н. о. |
н. о. |
33.09 |
|
2/8 |
» |
1.9 |
» |
19.3 |
» |
2.44 |
11.31 |
1.17 |
0.8 |
» |
» |
» |
» |
2.14 |
0.22 |
39.28 |
|
|
2/9 |
» |
0.8 |
» |
9.35 |
» |
0.58 |
3.83 |
0.5 |
0.5 |
» |
» |
» |
» |
0.66 |
0.44 |
н. о. |
16.66 |
|
4/1 |
» |
0.39 |
» |
15.58 |
5.28 |
н. о. |
н. о. |
н. о. |
н. о. |
» |
» |
» |
» |
н. о. |
н. о. |
» |
21.25 |
|
4/2 |
» |
0.52 |
» |
22.93 |
18.38 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
41..83 |
|
5/1 |
» |
н. о. |
» |
н. о. |
33.28 |
» |
» |
0.34 |
» |
1.18 |
0.93 |
» |
0.46 |
» |
3.36 |
» |
39.55 |
|
5/2 |
» |
» |
» |
» |
58.32 |
» |
» |
0.27 |
» |
н.о. |
0.36 |
» |
0.17 |
0.81 |
н. о. |
» |
59.93 |
|
5/3 |
» |
0.2 |
» |
» |
36.48 |
» |
» |
2.12 |
1.02 |
1.32 |
1.1 |
» |
0.65 |
3.35 |
0.56 |
» |
46.8 |
|
5/4 |
» |
н. о. |
» |
» |
55.43 |
» |
» |
0.24 |
н. о. |
н. о. |
0.36 |
» |
н. о. |
0.89 |
н. о. |
» |
56.92 |
|
10/1 |
» |
11.78 |
» |
» |
н. о. |
» |
» |
н. о. |
» |
» |
н. о. |
» |
» |
0.18 |
0.24 |
0.53 |
12.73 |
|
10/2 |
» |
50.34 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
н. о. |
н. о. |
н. о. |
50.34 |
|
10/3 |
14.89 |
н. о. |
0.33 |
0.41 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
15.63 |
Таблица 7. Химический состав (мас. %) металлических фаз Table 7. Chemical composition (wt.%) of metallic phases
|
№ |
Sn |
Cr |
Zn |
Cu |
Fe |
Ni |
Mn |
Si |
K |
Bi |
Ca |
Cl |
|
2/1 |
н. о. |
0.43 |
н. о. |
н. о. |
95.25 |
н. о. |
4.32 |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
|
2/2 |
» |
н. о. |
1.68 |
» |
98.32 |
» |
н. о. |
» |
» |
» |
» |
» |
|
2/3 |
» |
» |
0.72 |
» |
98.46 |
» |
0.82 |
» |
» |
» |
» |
» |
|
2/4 |
» |
» |
н. о. |
» |
100 |
» |
н. о. |
» |
» |
» |
» |
» |
|
2/5 |
» |
» |
» |
» |
100 |
» |
» |
» |
» |
» |
» |
» |
|
2/6 |
» |
» |
» |
» |
100 |
» |
» |
» |
» |
» |
» |
» |
|
2/7 |
» |
» |
» |
» |
96.08 |
» |
3.92 |
» |
» |
» |
» |
» |
|
2/8 |
96.7 |
» |
» |
3.3 |
н. о. |
» |
н. о. |
» |
» |
» |
» |
» |
|
2/9 |
90.0 |
» |
4.17 |
4.37 |
» |
1.46 |
» |
» |
» |
» |
» |
» |
|
2/10 |
93.1 |
1.12 |
5.03 |
0.75 |
» |
н. о. |
» |
» |
» |
» |
» |
» |
|
2/11 |
85.22 |
н. о. |
6.86 |
7.04 |
» |
0.88 |
» |
» |
» |
» |
» |
» |
|
6/1 |
76.67 |
» |
н. о. |
19.4 |
3.93 |
н. о. |
» |
» |
» |
» |
» |
» |
|
6/2 |
75.45 |
» |
» |
11.15 |
13.4 |
» |
» |
» |
» |
» |
» |
» |
|
6/3 |
н. о. |
» |
» |
н. о. |
н. о. |
» |
» |
» |
» |
100 |
» |
» |
|
6/4 |
» |
» |
» |
» |
» |
» |
» |
0.31 |
» |
98.98 |
0.71 |
» |
|
6/5 |
» |
» |
» |
» |
» |
» |
» |
н. о. |
» |
99.7 |
0.3 |
» |
|
9/1 |
» |
» |
» |
» |
97.09 |
0.03 |
0.5 |
0.37 |
0.18 |
н. о. |
1.62 |
0.21 |
Примечание. Виды и разновидности металлических фаз (в скобках Vx — частота встречаемости, %): 2/4—2/6 — железные (25), 2/1—2/3, 2/7, 9/1 — железистые (16.7), 2/8—2/11 — оловянистые (58.3), 6/3—6/5 — висмутовые (25).
Note. Types and varieties of metallic phases (Vx in brackets is the frequency of occurrence, %): 2/4—2/6 — iron (25), 2/1–2/3, 2/7, 9/1 — ferrous (16.7), 2/8–2/11 — tin (58.3), 6/3–6/5 — bismuth (25).
кремниевой фазы состава (мас. %): SiO2 = 97.63, Al2O3 = 2.37 — с эмпирической формулой (Si0.97Al0.03)O2.
Кислородные соли в составе мочевых камней представлены прежде всего биоапатитом (табл. 10), состав которого характеризуется следующей эмпирической брутто-формулой: (Ca 9.31—9.51 Mg 0.09—0.29 Na 0.2—0.5 K 0— 0.05 Ni 0—0.04 Zn 0—0.07 ) 10 [P 5.38—6 S 0—0.21 C 0—0.41 O 24 ]F 0—1.59 Cl 0— 0.04 (OH) 0—1 85. Судя по приведенной формуле, в камнях мы имеем дело главным образом с фтор-, фторгидро-ксил- и хлоргидроксилапатитом. Изредка встречается фторкарбонатапатит А-типа.
Наряду с биоапатитом в мочевых камнях обнаружена серия так называемых гибридных соединений, в составе которых сочетаются несколько комплексных анионов — силикатных, фосфатных, сульфатных. К таким соединениям отнесены титано-кальциевые суль-
фато-силикатофосфаты с эмпирической брутто-фор-мулой: (Ca 0.47—0.62 Ti 0.19—0.75 ) 0.81—1.22 [PO 4 ] 0.55—0.76 [SiO 4 ] 0.21— 0.42[SO4]0.02—003 (табл. 11) — и гидроген-гидроксильные фосфатосульфаты бария (табл. 12), которым отвечают следующие эмпирические формулы: (Ba0.79—0.99 Ca 0.03—0.25 Sr 0—0.05 K 0—0.05 ) 0.87—1.24 H 0—0.41 [SO 4 ] 0.9—1 [PO 4 ] 0—0.1 (OH) 0—0.48 и (Ba 0.67—0.68 Ca 0.02—0.04 Ni 0.06—0.08 Na 0—0.37 K 0—0.05 Cu 0—0.08 ) 0.79—1.27 H 0—0.53 [SO 4 ] 0.87—0.89 [PO 4 ] 0.11— 0.13 (OH) 0—0.48 .
В качестве галогенидов в мочевых камнях выступают гидрокси- и гидроген-хлориды с незначительной примесью сульфатного и фосфатного анионов (табл. 13). По катионному составу эти минералы можно подразделить на четыре разновидности: натрий-кальций-ка-лиевые гидроксихлориды — (K0.9—0.99Na0—0.09Ca0.05— 0.27 ) 1.03—1.86 [SO 4 ] 0.01—0.02 [PO 4 ] 0—0.02 Cl 0.97—0.99 (OH) 0.07—0.81 ;
Таблица 8. Химический (мас. %), минальный (мол. %) составы и эмпирические формулы магнетита
Table 8. Chemical (wt.%), min. (mol.%) compositions and empirical formulas of magnetite
|
Компоненты / Components |
2/1 |
2/2 |
2/3 |
2/4 |
2/5 |
2/6 |
2/7 |
2/8 |
|
Fe 2 O 3 |
67.07 |
95.62 |
98.53 |
98.63 |
100 |
100 |
100 |
96.43 |
|
TiO 2 |
0.57 |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
|
Al 2 O 3 |
6.89 |
» |
» |
» |
» |
» |
» |
» |
|
Cr 2 O 3 |
13.84 |
0.43 |
» |
» |
» |
» |
» |
» |
|
CuO |
7.73 |
н. о. |
» |
» |
» |
» |
» |
» |
|
NiO |
1.06 |
» |
» |
» |
» |
» |
» |
» |
|
ZnO |
н. о. |
» |
1.47 |
0.58 |
» |
» |
» |
» |
|
MnO |
» |
3.95 |
н. о. |
0.79 |
» |
» |
» |
3.57 |
|
MgO |
2.84 |
н. о. |
» |
н. о. |
» |
» |
» |
н. о. |
|
Миналы / Minals |
||||||||
|
Магнетит FeFe2O4 |
37.5 |
86.5 |
87 |
95 |
100 |
100 |
100 |
88 |
|
Ульвит Fe2TiO4 |
2 |
н. о. |
н. о. |
н.о. |
н. о. |
н. о. |
н. о. |
н. о. |
|
Якобсит MnFe2O4 |
н. о. |
13 |
н. о. |
3 |
» |
» |
» |
12 |
|
Франклинит ZnFe2O4 |
» |
н. о. |
13 |
2 |
» |
» |
» |
н. о. |
|
Треворит NiFe2O4 |
3 |
» |
н. о. |
н о. |
» |
» |
» |
» |
|
Хромит FeCr2O4 |
4.5 |
0.5 |
» |
» |
» |
» |
» |
» |
|
Магнохромит MgCr2O4 |
16 |
н. о. |
» |
» |
» |
» |
» |
» |
|
Герцинит FeAl2O4 |
15 |
» |
» |
» |
» |
» |
» |
» |
|
Купрошпинель CuFe2O4 |
22 |
» |
» |
» |
» |
» |
» |
» |
Примечание/Note. Эмпирические формулы магнетита / Empirical formulas of magnetite: 2/1 — (Fe0.59Cu0.22Mg0.16Ni0.03) (Fe0.55Al0.6Cr0.81Ti0.04)2O4; 2/2 — (Fe0.87Mn0.13)(Fe1.99Cr0.01)2O4; 2/3 — (Fe0.87Zn0.13)Fe2O4; 2/4 — (Fe0.95Mn0.03Zn0.02)Fe2O4; 2/5— 2/7 — FeFe 2 O 4 ; 2/8 — (Fe 0.88 Mn 0.12 )Fe 2 O 4 .
Таблица 9. Химический состав микровключений силикатов и алюмосиликатов в органическом веществе, мас. %
Table 9. Chemical composition of microinclusions of silicates and aluminosilicates in organic matter, wt.%
|
№ |
SiO 2 |
TiO 2 |
Al 2 O 3 |
Fe2O3 |
NiO |
ZnO |
MnO |
MgO |
CaO |
Na2O |
K 2 O |
P 2 O 5 |
SO 3 |
Cl |
Сумма / Sum |
|
1/1* |
24.22 |
0.31 |
18.39 |
0.42 |
н. о. |
н. о. |
н. о. |
н. о. |
3.46 |
1.53 |
0.54 |
н. о. |
0.75 |
1.14 |
50.76 |
|
1/2* |
36.99 |
н. о. |
28.38 |
0.51 |
» |
» |
» |
» |
3.57 |
3.28 |
1.17 |
» |
0.46 |
0.97 |
75.33 |
|
1/3* |
30.09 |
» |
23.29 |
0.32 |
» |
» |
» |
» |
6.7 |
н. о. |
н. о. |
» |
0.39 |
0.48 |
61.27 |
|
1/4* |
39.66 |
0.24 |
31.79 |
0.43 |
» |
» |
» |
» |
0.34 |
» |
» |
» |
Н. о. |
0.33 |
72.79 |
|
1/5* |
23.54 |
0.49 |
18.96 |
н. о. |
» |
» |
» |
» |
7.19 |
» |
1.29 |
» |
0.42 |
1.43 |
53.32 |
|
2/1* |
38.53 |
0.56 |
29.54 |
» |
» |
» |
» |
» |
0.18 |
» |
н. о. |
» |
н. о. |
н. о. |
58.81 |
|
2/2* |
33.76 |
н. о. |
25.87 |
0.44 |
» |
» |
» |
» |
0.67 |
» |
» |
» |
0.46 |
» |
61.1 |
|
2/3* |
47.77 |
» |
37.75 |
0.32 |
» |
» |
» |
» |
0.3 |
» |
» |
» |
н. о. |
» |
86.14 |
|
2/4* |
39.72 |
0.25 |
30.29 |
0.35 |
» |
» |
» |
» |
н. о. |
» |
0.25 |
» |
0.37 |
» |
71.23 |
|
3/1* |
44.98 |
0.57 |
36.63 |
0.58 |
» |
» |
» |
» |
0.59 |
0.49 |
н. о. |
» |
н. о. |
» |
38.86 |
|
3/2* |
52.29 |
0.41 |
41.72 |
0.96 |
» |
» |
» |
» |
н. о. |
0.42 |
» |
» |
95.8 |
||
|
6/1* |
45.64 |
0.73 |
36.63 |
0.55 |
» |
» |
» |
» |
3.66 |
н. о. |
0.3 |
4.56 |
0.69 |
» |
92.76 |
|
6/2* |
49.78 |
н. о. |
39.9 |
0.44 |
» |
» |
» |
» |
3.49 |
» |
0.2 |
3.46 |
н. о. |
» |
07/27 |
|
7/1* |
53.94 |
0.68 |
40.99 |
0.34 |
» |
» |
» |
» |
н. о. |
» |
0.24 |
н. о. |
0.47 |
» |
66.66 |
|
7/2* |
44.08 |
Н. о. |
35.72 |
0.53 |
» |
» |
» |
» |
» |
» |
н. о. |
» |
н. о. |
» |
80.93 |
|
9/1* |
38.16 |
0.51 |
31.23 |
0.35 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
0.13 |
70.38 |
|
9/2* |
42.8 |
0.32 |
34.67 |
0.61 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
н. о. |
78.4 |
|
10/1* |
44.17 |
0.9 |
35.2 |
0.34 |
» |
» |
» |
» |
» |
» |
» |
» |
» |
» |
80.61 |
|
10/2* |
41.14 |
0.85 |
32.84 |
0.41 |
» |
» |
» |
» |
» |
» |
» |
0.48 |
» |
» |
75.72 |
|
10/3* |
48.66 |
0.52 |
38.54 |
0.41 |
0.48 |
» |
» |
» |
» |
» |
» |
н. о. |
» |
» |
88.59 |
|
1/6** |
44.92 |
0.38 |
1.69 |
13.75 |
н. о. |
» |
0.69 |
14.23 |
11.78 |
» |
» |
» |
» |
» |
87.44 |
|
4/1*** |
20.21 |
0.35 |
17.1 |
н. о. |
» |
» |
н. о. |
н. о. |
18.97 |
» |
» |
1.03 |
0.49 |
» |
58.16 |
|
5/1*** |
62.12 |
н. о. |
16.66 |
0.93 |
» |
1.77 |
» |
» |
1.06 |
3.25 |
6.95 |
1.45 |
0.83 |
» |
95.02 |
|
5/3*** |
48.92 |
» |
12.93 |
0.73 |
» |
» |
» |
» |
0.8 |
5.93 |
0.49 |
0.48 |
0.42 |
» |
30.7 |
|
9/3*** |
61.57 |
» |
20.58 |
н. о. |
» |
» |
» |
» |
3.36 |
9.12 |
0.19 |
н. о. |
н. о. |
» |
80.61 |
|
5/4**** |
25.42 |
» |
10.66 |
3.0 |
» |
» |
» |
» |
10.65 |
н. о. |
н. о. |
» |
1.06 |
» |
56.72 |
|
9/4***** |
38.95 |
» |
16.39 |
3.78 |
» |
» |
» |
1.08 |
0.39 |
» |
7.89 |
» |
0.53 |
» |
75.72 |
|
5/5***** |
36.5 |
» |
18.1 |
4.96 |
» |
» |
» |
2.56 |
4.77 |
» |
4.24 |
1.94 |
1.43 |
» |
74.51 |
|
5/6***** |
52.25 |
» |
20.54 |
5.71 |
» |
» |
» |
4.6 |
0.6 |
» |
4.06 |
1.65 |
1.84 |
» |
94.7 |
Примечание. Минералоподобие включений: * каолинит, ** клинопироксены, ***плагиоклазы, анортоклаз, **** гранат, ***** слюды.
Note. Mineral-like inclusions: * kaolinite, ** clinopyroxenes, *** plagioclases, anorthoclase, **** garnet, ***** micas.
Таблица 10. Химический состав (мас. %) и эмпирические формулы микровключений биоапатита Table 10. Chemical composition (wt.%) and empirical formulas of bioapatite microinclusions
|
№ |
CaO |
MgO |
Na 2 O |
K 2 O |
NiO |
ZnO |
P 2 O 5 |
SO 3 |
F |
Cl |
|
1/1 |
52.99 |
0.38 |
1.46 |
0.19 |
0.24 |
н. о. |
41.66 |
0.97 |
3.11 |
н. о. |
|
1/2 |
54.38 |
0.35 |
1.37 |
н. о. |
н. о. |
» |
39.15 |
1.73 |
3.02 |
» |
|
4/1 |
53.68 |
0.76 |
1.6 |
» |
» |
» |
42.82 |
1.14 |
н. о. |
» |
|
6 |
53.62 |
1.18 |
0.62 |
» |
» |
» |
43.74 |
0.72 |
» |
0.12 |
|
8/1 |
51.86 |
0.53 |
1.34 |
0.25 |
» |
0.44 |
41.82 |
3.16 |
» |
н. о. |
|
8/2 |
53.28 |
0.82 |
1.47 |
н. о. |
» |
н. о. |
43.41 |
н. о. |
1.02 |
» |
Примечание / Note. Эмпирические формулы / Empirical formulas: 1/1 — (Ca9.35Mg0.1Na0.47K0.04Ni0.04)10[P5.91S0.09O24]F1.58; 1/2 — (Ca 9.48 Mg 0.09 Na 0.43 ) 10 [P 5.38 S 0.21 C 0.41 O 24 ]F 1.37 ; 4/1 — (Ca 9.31 Mg 0.19 Na 0.5 ) 10 [P 5.86 S 0.14 O 24 ](OH) 1.7 ; 6 — (Ca 9.51 Mg 0.29 Na 0.2 ) 10 [P 5.91 S 0.09 O 24 ]Cl 0.04 (OH) 1.85 ; 8/1 — (Ca 9.32 Mg 0.13 Na 0.43 K 0.05 Zn 0.07 ) 10 [P 5.93 S 0.07 O 24 ]F 1.59 ; 8/2 — (Ca 9.33 Mg 0.2 Na 0.47 ) 10 [P 6 O 24 ]F 0.53 (OH)
калий-натриевые гидроксихлориды — (Na0.62—1.53K0.25— 0.51 Ca 0—0.02 Fe 0.01—0.04 Ti 0.01—0.05 ) 1.17—3.07 Cl(OH) 0.21—2.41 ; натрий-кальциевые гидроксихлориды — (Ca0.54Na0.1)0.64 [SO4]0.02[PO4]0.02Cl0.96(OH)0.12: кальций-натриевые ги-дроген-хлориды — (Na 0.14—0.47 K 0.01—0.02 Ca 0.04—0.28 ) 0.19— 0.57 H 0.15—0.77 [SO 4 ] 0—0.01 [PO 4 ] 0—0.01 Cl 0.98—1 .
Таким образом, в составе изученных нами мочевых камней обнаружены биоминералы, охватывающие практически всю современную номенклатуру минеральных типов: простые вещества (металлы), халькогениды (сульфиды), галогениды (хлориды), оксиды (магнетит, SiO2-фаза), силикаты (алюмосилика-
ты), кислородные соли. В дополнение к минералам в камнях присутствуют так называемые минералоиды, представленные водными оксалатами кальция и урицитами.
Моча, сопряженная с мочевыми камнями и принадлежащая пациентам с пиелонефритом, исследовалась на валовый химический состав. Полученные данные для обеих коллекций мочи оказались схожими (мас. %, в скобках — среднее): H2O = 75—77 (76.3), Cl = = 6—12 (9), SO3 = 1.5—4 (2.8), P2O5 = 2.5—7 (4.4), Na2O = = 3—5 (4), K2O = 2—4 (2.7), CaO = 0.2—0.3 (0.26), MgO = = 0.05—0.25 (0.14), NH4 = 0.6—1.5 (1.5).
Таблица 11. Химический состав (мас. %) микровключений титано-кальциевых сульфато-силикатофосфатов бария
Table 11. Chemical composition (wt.%) of microinclusions of titanium-calcium sulfate-silicate-phosphates of barium
|
№ |
SiO 2 |
TiO 2 |
CaO |
P 2 O 5 |
SO 3 |
Сумма / Sum |
|
9/1 |
12.69 |
16.05 |
22.27 |
32.77 |
1.34 |
85.12 |
|
9/2 |
14.43 |
20.86 |
19.14 |
29.31 |
1.22 |
84.96 |
|
9/3 |
8.33 |
10.03 |
23.18 |
35.81 |
1.67 |
79.02 |
|
9/4 |
10.73 |
15.38 |
22.99 |
35.93 |
1.23 |
86.26 |
|
9/5 |
13.41 |
31.59 |
14.02 |
20.78 |
1.99 |
80.79 |
Таблица 12. Химический состав (мас. %) микровключений гидроген-гидроксильных фосфатосульфатов бария Table 12. Chemical composition (wt.%) of microinclusions of hydrogen-hydroxyl barium phosphate sulfates
|
№ |
BaO |
CaO |
SrO |
NiO |
CuO |
Na2O |
K 2 O |
P 2 O 5 |
SO 3 |
|
9/1 |
62.0 |
0.68 |
2.09 |
н. о. |
н. о. |
н. о. |
н. о. |
н. о. |
35.23 |
|
9/2 |
61.83 |
5.63 |
н. о. |
» |
» |
» |
» |
» |
32.54 |
|
10/1 |
59.35 |
0.75 |
» |
» |
» |
» |
1.16 |
3.41 |
35.33 |
|
10/2 |
49.76 |
0.94 |
» |
2.24 |
2.49 |
5.57 |
1.06 |
4.28 |
33.66 |
|
10/3 |
53.34 |
0.67 |
» |
2.85 |
1.75 |
н. о. |
0.82 |
3.94 |
36.63 |
|
10/4 |
54.11 |
1.15 |
» |
3.03 |
н. о. |
» |
н. о. |
4.23 |
37.48 |
Таблица 13. Химический состав (мас. %) и эмпирические формулы микровключений гидрокси- и гидрогенхлоридов
Table 13. Chemical composition (wt.%) and empirical formulas of microinclusions of hydroxy- and hydrogen chlorides
|
№ |
Ca |
Na |
K |
Fe |
Ti |
Cl |
S |
P |
Сумма |
|
1/1 |
1.54 |
1.49 |
29.06 |
н. о. |
н. о. |
25.75 |
0.22 |
н. о. |
58.06 |
|
1/2 |
14.14 |
0.93 |
17.52 |
» |
» |
15.37 |
0.19 |
0.31 |
48.46 |
|
1/3 |
5.91 |
Н. о. |
19.49 |
» |
» |
18.38 |
0.26 |
0.18 |
44.223 |
|
1/4 |
2.05 |
11.63 |
0.96 |
» |
» |
37.6 |
н. о. |
н. о. |
52.24 |
|
1/5 |
7.11 |
5.14 |
057 |
» |
» |
25.56 |
0.21 |
» |
38.59 |
|
1/6 |
5.79 |
Н. о. |
20.95 |
» |
» |
17.81 |
0.21 |
0.14 |
445.9 |
|
1/7 |
1.93 |
4.13 |
048 |
» |
» |
44.72 |
н. о. |
н. о. |
51.26 |
|
1/8 |
2.14 |
4.47 |
0.63 |
» |
» |
45.29 |
» |
» |
52.53 |
|
1/9 |
10.96 |
1.2 |
н. о. |
» |
» |
16.95 |
0.31 |
0.3 |
29.72 |
|
1/10 |
6.78 |
5.35 |
0.48 |
» |
» |
25.43 |
н. о. |
н. о. |
38.04 |
|
3/1 |
0.35 |
7.69 |
10.72 |
0.24 |
0.27 |
18.8 |
» |
» |
38.07 |
|
3/2 |
0.86 |
3.83 |
5.29 |
0.24 |
0.28 |
3.8 |
» |
» |
14.3 |

Микроэлементы
Определялись в образцах мочевых камней и моче пациентов с мочекаменной болезнью ( моча-1 ) и пиелонефритом ( моча-2 ).
В составе исследованных мочевых камней выявлены 18 микроэлементов, из которых к определяющим сумму относятся Zn > Sr > Ti (табл. 14). Доля (%) групп органофильных элементов (Солонин, 1991) в среднем составляет для эссенциальных (жизненно необходимых) — 46.2, физиогенно-активных — 53.7. Доля эле-ментов-антибионтов крайне незначительна — 0.1 %. Из приведенных данных следует, что в составе мочевых камней абсолютно доминируют именно органофильные микроэлементы. При этом суммарное содержание этих элементов в камнях отрицательно коррелируется с массой камней (r = –0.39) и возрастом человека (r = –0.73). По сравнению с микроорганизмами в человеческих конкрементах (Павлович, Кокин, 2019) общее содержание микроэлементов в исследованных камнях выше в 30—1580 раз. Согласно вычисленным кларкам концентрации, степень обогащения камней эссенциальными и физиогенно-активными микроэлементами несколько уступает таковой в земной коре (КК < 1), но многократно (до КК = 100) превышает степень концентрации тех же элементов в базовых органических субстанциях (Войткевич, Кокин, 1990) в последовательности «наземные растения < бактерии < наземные животные < живое вещество». При этом в сравнении с большинством органических субстанций в мочевых камнях физиогенно-активные микроэлементы значительно преобладают над эссенциальными (рис. 12).
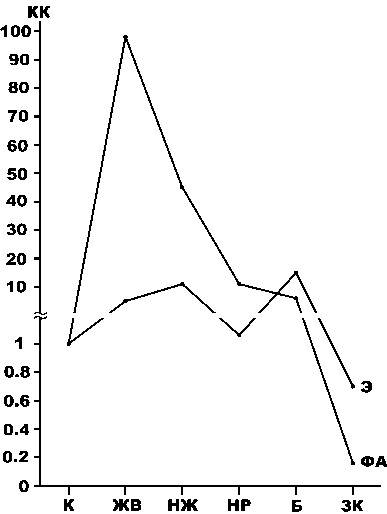
Рис. 12 . Усредненные кларки концентрации микроэлементов в мочевых камнях (К). Объекты сопоставления (по: Войткевич, Кокин, 1990): ЖВ — живое вещество, НЖ — наземные животные, НР — наземные растения, Б — бактерии, ЗК — земная кора
Fig. 12. Averaged clark values of microelement concentrations in urinary stones (K). Objects of comparison (according to: Voitkevich, Kokin, 1990): ЖВ — living matter, НЖ — terrestrial animals, НР — terrestrial plants, Б — bacteria, ЗК — earth's crust
Таблица 14. Содержание микроэлементов в камнях, г/т
Table 14. Content of microelements in stones, g/t
|
Элементы / Elements |
Объекты / Objects |
||||||||
|
5 |
|||||||||
|
1 |
2 |
3 |
4 |
6 |
8 |
9 |
X ± S x (V x , %) |
||
|
Ag |
0.05 |
0.05 |
0.05 |
0.09 |
0.05 |
0.05 |
0.05 |
0.05 |
0.06 ± 0.01 (17) |
|
Cd |
0.05 |
0.05 |
0.05 |
0.05 |
1.4 |
0.05 |
0.05 |
0.05 |
0.22 ± 0.48 (218) |
|
Zn |
13 |
0.7 |
45 |
32 |
2-3 |
1.9 |
194 |
0.05 |
61.21 ± 86.27 (141) |
|
Rb |
0.05 |
0.21 |
0.05 |
0.05 |
0.05 |
0.37 |
0.05 |
0.05 |
0.11 ± 0.12 (109) |
|
Pb |
0.68 |
0.11 |
0.81 |
1.5 |
3.8 |
0.05 |
3.3 |
0.73 |
1.37 ± 1.42 (104) |
|
Bi |
0.05 |
0.05 |
0.05 |
0.05 |
2.1 |
0.05 |
0.05 |
0.05 |
0.31 ± 0.72 (232) |
|
Сумма элементов эссенциальных (Э) |
13.88 |
1.17 |
46.01 |
33.74 |
210.4 |
2.47 |
197.5 |
0.98 |
63.27 ± 88.4 (140) |
|
Sum of essential elements (E) |
|||||||||
|
Cs |
0.34 |
0.09 |
0.35 |
0.1 |
0.43 |
0.04 |
0.13 |
0.38 |
0.23 ± 0.13 (57) |
|
Sr |
50 |
0.49 |
71 |
47 |
156 |
0.72 |
66 |
0.05 |
48.91 ± 31.02 (63) |
|
Ba |
0.05 |
0.05 |
0.05 |
0.05 |
9.1 |
0.05 |
0.88 |
0.05 |
1.29 ± 1.28 (99) |
|
Ti |
4.7 |
2.6 |
11 |
6.6 |
80 |
1.5 |
19 |
0.05 |
15.68 ± 11.51 (73) |
|
Zr |
0.76 |
0.3 |
1.2 |
0.82 |
1.2 |
0.45 |
1.1 |
2.8 |
1.08 ± 0.91 (84) |
|
V |
0.05 |
0.35 |
0.05 |
1.2 |
3.5 |
0.63 |
0.05 |
8.4 |
1.78 ± 3.34 (188) |
|
Cr |
0.05 |
0.05 |
0.05 |
0.05 |
3.6 |
0.05 |
0.05 |
0.05 |
0.49 ± 0.53 (108) |
|
Co |
2.2 |
0.05 |
2.3 |
2 |
2.3 |
0.05 |
2.3 |
0.05 |
1.41 ± 0.96 (68) |
|
Ni |
3.6 |
0.05 |
2.6 |
3.8 |
4.2 |
0.05 |
4.7 |
0.05 |
2.38 ± 1.93 (81) |
|
Cu |
0.45 |
3.1 |
0.05 |
0.37 |
0.05 |
3.1 |
0.05 |
0.05 |
0.9 ± 1.25 (139) |
|
Сумма элементов |
|||||||||
|
физиогенно-активных (ФА) Sum of physiogenically |
62.2 |
7.13 |
88.65 |
61.99 |
260.38 |
6.64 |
94.26 |
11.93 |
74.15 ± 41.52 (56) |
|
active elements (PA) |
|||||||||
|
Ta |
0.06 |
0.04 |
0.05 |
0.07 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 ± 0.01 (20) |
|
Gd |
0.05 |
0.05 |
0.05 |
0.39 |
0.05 |
0.05 |
0.05 |
0.05 |
0.09 ± 0.12 (133) |
|
Сумма элементов-антибионтов (АБ) |
0.11 |
0.09 |
0.1 |
0.46 |
0.1 |
0.1 |
0.1 |
0.1 |
0.15 ± 0.13 (87) |
|
Sum of abiont elements (AB) |
|||||||||
|
Итого / Total |
76.19 |
8.39 |
134.46 |
96.19 |
470.88 |
9.21 |
291.86 |
13.01 |
137.56 ± 164.35 (119) |
Таблица 15. Содержание микроэлементов в образцах мочи-1 , сопряженной с мочевыми камнями, г/л
Table 15. Content of trace elements in urine-1 samples compared to urinary stones, g/l
|
Элементы Elements |
Объекты / Objects |
||||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
Х ± S x (V x , %) |
|
|
Li |
110 |
40 |
50 |
23 |
9 |
23 |
31 |
9 |
26 |
40 |
36.1 ± 29.11 (81) |
|
Rb |
1500 |
380 |
700 |
1000 |
250 |
280 |
900 |
300 |
460 |
1100 |
687 ± 425.21 (62) |
|
Be |
0.05 |
0.05 |
0.23 |
0.05 |
0.8 |
0.05 |
0.05 |
0.05 |
0.4 |
0.22 |
0.2 ± 0.24 (120) |
|
Mo |
60 |
12 |
50 |
70 |
12 |
17 |
44 |
19 |
19 |
50 |
35.3 ± 21.79 (62) |
|
Ag |
0.52 |
0.05 |
0.05 |
0.05 |
0.91 |
0.4 |
0.109 |
0.16 |
0.05 |
0.05 |
0.23 ± 0.29 (126) |
|
Zn |
800 |
0.05 |
400 |
210 |
80 |
40 |
0.05 |
1400 |
300 |
1500 |
473.01 ± 569.08 (120) |
|
Cd |
0.26 |
0.12 |
0.05 |
0.05 |
1.5 |
1.2 |
0.25 |
0.5 |
0.3 |
0.05 |
0.43 ± 0.51 (119) |
|
Pb |
1.9 |
0.05 |
2.4 |
0.14 |
9 |
8 |
0.05 |
0.05 |
0.05 |
0.9 |
2.25 ± 3.41 (152) |
|
As |
308 |
90 |
107 |
91 |
109 |
92 |
158 |
127 |
93 |
150 |
132.5 ± 66.43 (50) |
|
Se |
66 |
89 |
54 |
44 |
38 |
66 |
87 |
11.2 |
77 |
67 |
59.92 ± 23.89 (40) |
|
Th |
0.14 |
0.05 |
0.13 |
0.05 |
0.05 |
0.05 |
0.3 |
0.05 |
0.05 |
0.3 |
0.12 ± 0.1 (83) |
|
Сумма элементов Э Sum of E |
2846.87 |
611.37 |
1363.86 |
1438.34 |
510.26 |
527.7 |
1220.81 |
1867.01 |
975.85 |
2908.52 |
1427 ± 879.97 (62) |
|
elements |
|||||||||||
|
Cs |
4.2 |
1 |
3.1 |
1.9 |
1.7 |
8.3 |
2.2 |
0.8 |
1.6 |
3.9 |
2.87 ± 2.22 (77) |
|
Sr |
500 |
0.05 |
400 |
0.05 |
0.05 |
19 |
170 |
120 |
0.05 |
500 |
170.92 ± 213.83 (125) |
|
Ba |
0.05 |
0.05 |
2.2 |
0.05 |
0.7 |
0.05 |
0.13 |
0.05 |
0.05 |
4.8 |
0.81 ± 1.56 (193) |
|
Y |
0.22 |
0.05 |
0.05 |
0.05 |
0.09 |
0.04 |
0.05 |
0.2 |
0.1 |
0.07 |
0.09 ± 0.06 (67) |
|
Ti |
3900 |
900 |
2100 |
600 |
500 |
160 |
2300 |
1900 |
1500 |
3000 |
1686 ± 1192.09 (71) |
|
Zr |
1.2 |
1.3 |
0.4 |
1 |
1 |
1.2 |
0.5 |
0.4 |
0.04 |
0.7 |
0.77 ± 0.43 (56) |
|
Hf |
0.15 |
0.33 |
0.04 |
0.38 |
0.05 |
0.06 |
0.02 |
0.05 |
0.08 |
0.11 |
0.13 ± 0.13 (100) |
|
V |
220 |
150 |
160 |
110 |
140 |
130 |
240 |
50 |
140 |
200 |
154 ± 55.42 (36) |
|
Cr |
100 |
7 |
70 |
70 |
19 |
17 |
180 |
19 |
50 |
90 |
62.2 ± 52.88 (85) |
|
Co |
1.2 |
0.05 |
1.5 |
0.7 |
0.05 |
0.05 |
0.05 |
0.26 |
1.4 |
0.8 |
0.61 ± 0.59 (97) |
|
Ni |
24 |
7 |
28 |
4 |
8 |
14 |
12 |
10 |
16 |
20 |
14.3 ± 7.7 (54) |
|
Cu |
31 |
7 |
9 |
8 |
3.8 |
0.05 |
10 |
4 |
0.05 |
26 |
9.89 ± 10.45 (106) |
|
Ga |
19 |
1.7 |
7 |
3 |
1.6 |
0.05 |
11 |
8 |
5 |
11 |
6.73 ± 5.79 (86) |
|
Sn |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.23 |
0.22 |
0.05 |
0.12 |
0.3 |
0.12 ± 0.1 (83) |
|
Sb |
2.5 |
4 |
2.2 |
1.7 |
2.8 |
1.7 |
2 |
2.4 |
3.1 |
4 |
2.64 ± 0.84 (32) |
|
Te |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.06 |
0.05 |
0.05 |
0.05 |
0.22 |
0.07 ± 0.05 (71) |
|
Сумма |
|||||||||||
|
элементов ФА Sum of PA |
4803.62 |
1079.63 |
2783.59 |
800.93 |
678.94 |
351.79 |
2928.22 |
2115.26 |
1717.64 |
3861.9 |
2112.15 ± 1472.58 (70) |
|
elements |
|||||||||||
|
Sc |
19 |
2.7 |
11 |
10 |
4.3 |
0.7 |
11 |
15 |
5 |
14 |
9.29 ± 5.9 (64) |
|
Nb |
0.02 |
0.05 |
.05 |
0.06 |
0.05 |
0.05 |
0.22 |
0.13 |
0.06 |
0.25 |
0.09 ± 0.08 (89) |
|
W |
0.15 |
0.004 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.12 |
0.06 ± 0.04 (67) |
|
Tl |
0.11 |
0.05 |
0.03 |
0.05 |
0.02 |
0.05 |
0.08 |
0.05 |
0.05 |
0.05 |
0.05 ± 0.03 (60) |
|
Ge |
4 |
0.05 |
0.05 |
2 |
1.4 |
1.3 |
1.9 |
2.2 |
0.49 |
1.7 |
1.51 ± 1.18 (78) |
|
La |
0.09 |
0.08 |
0.05 |
0.05 |
0.05 |
0.05 |
0.04 |
0.05 |
0.05 |
0.03 |
0.06 ± 0.02 (33) |
|
Ce |
0.05 |
0.03 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 ± 0.01 (20) |
|
Pr |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.01 |
0.05 ± 0.01 (20) |
|
Nd |
0.06 |
0.02 |
0.05 |
0.01 |
0.05 |
0.03 |
0.01 |
0.05 |
0.05 |
0.08 |
0.04 ± 0.02 (50) |
|
Sm |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.03 |
0.08 |
0.05 |
0.05 |
0.01 |
0.05 ± 0.02 (40) |
|
Gd |
0.06 |
0.05 |
0.05 |
5 |
0.16 |
0.07 |
0.2 |
0.05 |
0.05 |
0.21 |
0.59 ± 1.55 (263) |
|
Dy |
0.05 |
0.05 |
0.05 |
0.05 |
0.001 |
0.05 |
0.01 |
0.05 |
0.01 |
0.05 |
0.04 ± 0.02 (50) |
|
Er |
0.06 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 |
0.05 ± 0.004 (80) |
|
Yb |
0.05 |
0.05 |
0.05 |
0.07 |
0.13 |
0.08 |
0.05 |
0.02 |
0.05 |
0.02 |
0.06 ± 0.03 (50) |
|
Сумма |
|||||||||||
|
элементов АБ Sum of AB |
23.8 |
3.49 |
11.63 |
17.54 |
6.41 |
2.61 |
13.8 |
17.85 |
6.06 |
16.67 |
11.54 ± 7.12 (62) |
|
elements |
|||||||||||
|
Итого / Total |
7698.09 |
1697.98 |
4170.7 |
2274.35 |
1202.02 |
884.71 |
4176.63 |
4017.97 |
2705.61 |
6803.76 |
3563.18 ± 2289.49 (64) |
Таблица 16 . Содержание микроэлементов (г/л) в образцах мочи-2 пациентов с пиелонефритом (11, 12)
Table 16. Content of trace elements (g/l) in urine-2 samples of patients with pyelonephritis (11, 12)
|
Элементы / Elements |
Пациенты / Patients |
Статистика / Statistics: Х ± Sx |
|
|
11 |
12 |
||
|
Li |
0.5 |
4.17 |
0.34 ± 2.59 |
|
Be |
0.02 |
0.08 |
0.05 ± 0.04 |
|
As |
21.06 |
28.64 |
24.85 ± 5.36 |
|
Se |
0.49 |
0.16 |
0.33 ± 0.23 |
|
Rb |
6.5 |
6 |
6.25 ± 0.35 |
|
Zn |
1.63 |
3.75 |
2.69 ± 1.5 |
|
Mo |
10.5 |
13.5 |
12 ± 2.12 |
|
Ag |
1.26 |
0.45 |
0.86 ± 0.57 |
|
Cd |
8.33 |
0.83 |
4.58 ± 5.3 |
|
Pb |
0.15 |
0.05 |
0.1 ±0.07 |
|
Th |
0.009 |
0.007 |
0.008 ± 0.001 |
|
Сумма элементов Э Sum of E elements |
50.45 |
57.64 |
54.04 ±5.08 |
|
Hf |
0.04 |
0.01 |
0.025 ± 0.02 |
|
Sn |
0.01 |
0.05 |
0.03 ± 0.03 |
|
Sb |
1.38 |
1.1 |
1.24 ± 0.2 |
|
Te |
5 |
18 |
11.5 ± 9.19 |
|
Cs |
0.36 |
0.75 |
0.56 ± 0.28 |
|
Ba |
0.003 |
0.0001 |
0.002 ± 0.002 |
|
Sr |
0.53 |
0.38 |
0.46 ± 0.11 |
|
Y |
9.001 |
0.002 |
4.5 ± 0.36 |
|
Zr |
0.005 |
0.007 |
0.006 ± 0.001 |
|
Ga |
0.2 |
0.33 |
0.27 ± 0.09 |
|
Ti |
0.38 |
0.55 |
0.47 ± 0.12 |
|
V |
1.38 |
1.77 |
1.58 ± 0.28 |
|
Cr |
0.6 |
0.35 |
0.48 ± 0.18 |
|
Co |
0.05 |
0.02 |
0.04 ± 0.02 |
|
Ni |
0.14 |
0.11 |
0.13 ± 0.02 |
|
Cu |
0.19 |
0.001 |
0.1 ± 0.13 |
K 0.01—0.02 S 0—0.01 Cl l0.02—0.03 ; 5) цинковые — Zn 0.44— 0.95 Si 0.01—0.08 Al 0—0.04 Mg 0—0.42 Ca 0.01—0.03 K 0—0.02 P 0—0.12 S0—0.1; 6) цинково-медные — Cu0.55—0.74Zn0.24—0.44 Fe 0.01—0.02 ; 7) медистые — Cu 0.44 Pb 0.04 Fe 0.01 Sn 0.02 Si 0.04 Al0.04Ca0.02K0.01P0.2SS0.01Cl0.19; 8) никель-оловянные — Sn 0.53 Ni 0.13 Zn 0.1 Cu 0.04 Cl 0.2 .
Наряду с металлоорганическими соединениями в исследованных камнях обнаружены собственно металлические фазы, подразделяющиеся на четыре разновидности (в порядке снижения частоты встречаемости): оловянистые — Sn0.6—0.94Cu0.01—0.3Fe0—0.23Zn0— 0.11Ni0—0.03Cr0—0.02; железные — Fe; висмутовые — Bi0.94— 1 Ca 0—0.04 Si 0—0.02 ; железистые — Fe 0.95—0.98 Mn 0—0.04 Zn 0— 0.02Cr0—0.01(Si,Na,K)0—0.01 (табл. 7). В микроассоциации с металлическими фазами в мочевых камнях обнаружены редкие включения сульфидов , представленные пиритом (Fe = 46.13; S = 53.89 мас. %; эмпирическая формула — Fe0.98S2) и галенитом ( Pb = 86.59; S = 13.41 мас. %; PbS).
Довольно распространенным биоминералом в изученных камнях выступает магнетит , широко варьирующийся по составу (табл. 8). Его можно представить следующей эмпирической формулой: (Fe0.59—1Cu0— 0.22 Mg 0—0.16 Mn 0—0.13 Ni 0—0.0.03 Zn 0—0.02 )(Fe 0.55—2 Al 0—0.6 Cr 0— 0.81Ti0—0.04)2O4. По минальному составу этот минерал подразделяется на четыре разновидности — преобладающую магнетитовую, герцинит-магнохромит-ку-прошпинель-магнетитовую, якобсит-магнетитовую и франклинит-магнетитовую.
Широко распространены в исследованных мочевых камнях силикатные и алюмосиликатные микрофазы (табл. 9), чаще всего приуроченные к выделениям органического вещества. По составу и минералогической номенклатуре они могут быть сопоставлены (в последовательности снижения частоты встречаемости) с каолинитом, плагиоклазами, слюдами, анортоклазом, клинопироксенами, гранатами. Кроме того, в ассоциации с алюмосиликатами встречаются зерна
В образцах мочи-1 пациентов с мочекаменной болезнью выявлен 41 микроэлемент (табл. 15), что более чем в 2 раза превышает число микроэлементов в соответствующих образцах мочевых камней. К определяющим сумму в моче малым элементам относятся: Ti > Rb > Zn > Sr > V > As. В отличие от камней, моча содержит 9 лантаноидов, при этом содержание элементов иттриевой подгруппы превышает содержание элементов цериевой подгруппы в 3 раза. Проанализированная моча по сравнению с образцами камней валово обога-
щена микроэлементами в среднем в 26 раз. По суммарной их концентрации она отрицательно коррелируется с камнями (–0.73) и возрастом больных (r = –0.33). Доли (%) групп элементов органофилов в моче составляют в среднем для эссенциалов — 86.4, физиогенно-активных — 12.9, элементов-антибионтов — 0.7. То есть в составе мочи, так же как и в камнях, сильно доминируют именно органофильные микроэлементы. Согласно кларкам концентрации, степень обогащения мочи эссенциальными и физиогенно-активными микроэле-
ментами превышает таковую в базовых органических субстанциях в 10—850 раз в последовательности «бактерии < наземные растения < живое вещество < наземные животные». Относительно земной коры моча в среднем немного уступает по физиогенно-активным микроэлементам, но в 10 раз превышает по эссенциальным (рис. 13).
Таким образом, получается, что моча у пациентов с мочекаменной болезнью по валовой концентрации аномально обогащена органофильными микроэлементами как относительно камней, так и эталонных органических субстанций. При этом в ней многократно превалируют не физиогенно-активные, как в камнях, а эссенциальные элементы.
В образцах мочи-2 пациентов с пиелонефритом тоже выявлен 41 микроэлемент, к определяющим сумму элементам в этом случае относятся Ge > Sc > Te > Rb > Cd > Li. В составе 9 лантаноидов содержание элементов иттриевой подгруппы преобладает над содержанием элементов цериевой подгруппы в 9 раз (табл. 16). По валовому содержанию микроэлементов рассматриваемая моча уступает почечным камням почти в два раза, а моче пациентов с мочекаменной болезнью — в 49 раз. Доля (%) групп элементов-органофи-лов в образцах мочи-2 составляет в среднем для эссенциальных микроэлементов — 75, физиогенно-актив-ных — 23, элементов-антибионтов — 2. То есть в составе мочи пациентов с пиелонефритом, так же как и в моче пациентов с мочекаменной болезнью, абсолютно преобладают элементы-эссенциалы при ничтожной доле элементов-антибионтов. Согласно вычисленным кларкам концентрации, степень обогаще-
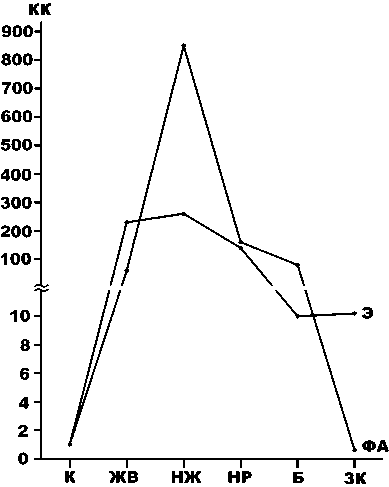
Рис. 13 . Усредненные кларки концентрации микроэлементов в образцах мочи-1 . Объекты сопоставления (по: Войткевич, Кокин, 1990): К — мочевые камни, ЖВ — живое вещество, НЖ — наземные животные, НР — наземные растения, Б — бактерии, ЗК — земная кора
Fig. 13. Averaged clark values of microelement concentrations in urine-1 samples. Objects of comparison (according to: Voitkevich, Kokin, 1990): К — urinary stones, ЖВ — living matter, НЖ — terrestrial animals, НР — terrestrial plants, Б — bacteria, ЗК — earth’s crust
Продолжение таблицы 16
Continuation of table 16
ния мочи-2 эссенциальными микроэлементами превышает кларки в большинстве органических субстанций в 18—45 раз в последовательности «наземные растения < живое вещество < наземные животные». Рассматриваемая моча почти на два порядка уступает земной коре по содержанию элементов-антибион-тов и в 5 раз — по содержанию физиогенно-активных элементов, но в 1.5 раза превосходит ее по элемен-там-эссенциалам (рис. 14 ).
KK
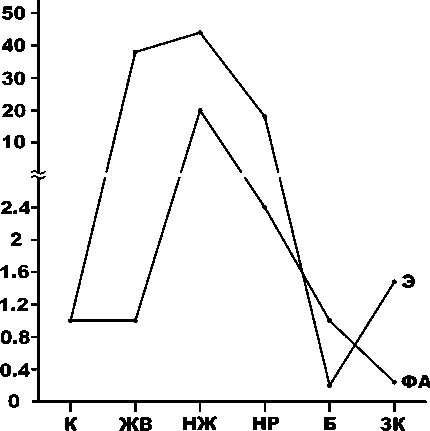
Рис. 14 . Усредненные кларки концентрации микроэлементов в образцах мочи-2 . Объекты сопоставления (по: Войткевич, Кокин, 1990): К — мочевые камни, ЖВ — живое вещество, НЖ — наземные животные, НР — наземные растения, Б — бактерии, ЗК — земная кора
Fig. 14. Averaged clark values of microelement concentrations in urine-2 samples. Objects of comparison (according to: Voitkevich, Kokin, 1990): К — urinary stones, ЖВ — living matter, НЖ — terrestrial animals, НР — terrestrial plants, Б — bacteria, ЗК — earth’s crust
Белковые аминокислоты
Важное значение в современных исследованиях органического вещества имеет анализ аминокислотного состава их белков (Амосова, Машина, 2020; Амосова, Шанина, 2018; Анищенко, Шанина, 2009, 2010; Бельская, Голованова, 2007; Изатулина, Голованова, 2007; Каткова, Симаков, 1998; Каткова, Шанина, 2019; Котельникова, 2018; Машина, Шанина, 2022; Шанина, Бушнев, 2016; Шанина, Голубев, 2022; Юшкин, 1999; Юшкин, Бушнев, 2006; Fuch, Berger, 2005; Kimura, Hamase, 2016). В рамках нашего исследования аминокислотный состав органического вещества определялся в мочевых камнях, образцах мочи-1 и мочи-2, а также непосредственно в белках мочи-1.
В мочевых камнях установлено 15 аминокислот, в том числе 7 незаменимых (табл. 17). Сумма содержаний всех кислот колеблется в пределах 13—37 мг/г, незаменимых — 4.67—14.38 мг/г. Размах колебаний групповых концентраций составляет в среднем около 15. Среднестатистический коэффициент вариации содержаний аминокислот составляет (59 ± 23) %. Доля незаменимых кислот составляет в среднем 0.85. Последовательность снижения концентрации групп аминокислот: алифатические > кислые > имино > ароматические > гидроксильные > основные > алифатические серосодержащие. Аналогичный ряд для незаменимых кислот: лейцин > метионин > лизин > фенилаланин > треонин > валин > изолейцин. В нашем случае, что храктерно для органического вещества в организме человека (Каткова, Шанина, 2019), только три аминокислоты — аланин, аспарагиновая и глутаминовая кислоты — представлены обоими энантиомерами, отношения D/L (показатель хиральности) составляют в них соответственно 0—0.013, 0.038—0.055, 0—0.011.
В образцах мочи-1 установлены те же аминокислоты (табл. 18). Сумма содержаний всех кислот варьируется в пределах 0.0552—0.4407 мг/г, а незаменимых кислот — 0.0235—0.1913 мг/г, что уступает данным для камней соответственно в 84—235 и 75—199 раз. Размах колебаний групповых концентраций аминокислот со- 35
|
Элементы / Elements |
Пациенты / Patients |
Статистика / Statistics: Х ± Sx |
|
|
11 |
12 |
||
|
Сумма элементов ФА Sum of PA elements |
19.27 |
23.43 |
21.35 ±2.94 |
|
Nb |
0.003 |
0.003 |
0.03 |
|
W |
0.03 |
0.025 |
0.027 ± 0.004 |
|
Tl |
0.07 |
0.04 |
0.055 ± 0.021 |
|
Ge |
0.2 |
0.45 |
0.325 ± 0.177 |
|
Sc |
0.21 |
0.4 |
0.305 ± 0.134 |
|
La |
0.001 |
0.001 |
0.001 |
|
Ce |
0.001 |
0.001 |
0.001 |
|
Pr |
0.01 |
0.0002 |
0.005 ± 0.007 |
|
Nd |
0.004 |
0.004 |
0.004 |
|
Sm |
0.01 |
0.008 |
0.009 ± 0.001 |
|
Gd |
0.065 |
0.023 |
0.044 ± 0.03 |
|
Dy |
0.053 |
0.011 |
0.032 ± 0.03 |
|
Er |
0.02 |
0.02 |
0.02 |
|
Yb |
0.133 |
0.016 |
0.07 ± 0.08 |
|
Сумма элементов АБ Sum of AB elements |
0.81 |
1.0 |
0.9 ± 0.14 |
|
Итого / Total |
70.53 |
82.07 |
76.29 ± 8.16 |
Таблица 17. Содержание белковых аминокислот в мочевых камнях, мг/г
Table 17. Content of protein amino acids in urinary stones, mg/g
|
Аминокислоты / Amino acids |
Объекты / Objects |
X ± S x , (V x , %) |
|||
|
2 |
4 |
6 |
7 |
||
|
Глицин / Glycine |
2.464 |
2.001 |
0.836 |
2.606 |
1.977 ± 0.803 (41) |
|
L-аланин / L-alanine |
0.677 |
3.36 |
0.987 |
1.273 |
1.574 ± 1.215 (77) |
|
D-аланин / D-alanine |
0 |
0 |
0.013 |
0.016 |
0.007 ± 0.008 (114) |
|
L-валин* / L-valine* |
0.822 |
1.456 |
0.469 |
1.107 |
0.964 ± 0.419 (43) |
|
L-лейцин* / L-leucine* |
1.46 |
4.031 |
1.247 |
2.231 |
2.242 ± 1.265 (56) |
|
L-изолейцин* / L-isoleucine* |
0.334 |
1.048 |
0.303 |
0.475 |
0.54 ± 0.347 (64) |
|
Алифатические / Aliphatic |
5.757 |
11.896 |
3.855 |
7.708 |
7.304 ± 3.442 (47) |
|
L-метионин* / L-methionine* |
0 |
1.416 |
0.306 |
0.235 |
2.086 ± 0.632 (30) |
|
Алифатические серосодержащие Aliphatic sulfur-containing |
0 |
1.416 |
0.306 |
0.235 |
0.489 ±0.632 (30) |
|
L-фенилаланин* / L-phenylalanine* |
0.764 |
2.059 |
0.725 |
1.096 |
1.161 ± 0.621 (53) |
|
L-тирозин / L-tyrosine |
0.806 |
3.72 |
1.225 |
1.462 |
1.803 ± 1.306 (72) |
|
Ароматические / Aromatic |
1.57 |
5.779 |
1.95 |
2.558 |
2.964 ± 1.92 (65) |
|
L-лизин* / L-lysine* |
0.764 |
3.593 |
1.314 |
1.946 |
1.904 ± 1.225 (64) |
|
Основные / Essential |
0.764 |
3.593 |
1.314 |
1.946 |
1.904 ± 1.225 (64) |
|
L-аспарагиновая кислота / L-aspartic acid |
1.107 |
3.201 |
1.335 |
1.665 |
1.827 ± 0.944 (52) |
|
D-аспарагиновая кислота / D-aspartic acid |
0.042 |
0.127 |
0.053 |
0.091 |
0.078 ± 0.039 (50) |
|
L-глутаминовая кислота / L-glutamic acid |
1.634 |
5.307 |
1.749 |
3.368 |
3. 14 ± 1.721 (55) |
|
D-глутаминовая кислота / D-glutamic acid |
0 |
0.046 |
0 |
0.036 |
0.021 ±0.024 (114) |
|
Кислые / Acidic |
2.783 |
8.682 |
3.137 |
0.297 |
3.725 ± 3.539 (95) |
|
L-серин / L-serine |
1.14 |
2.553 |
0.904 |
1.393 |
1.498 ±0.731 (49) |
|
L-треонин* / L-threonine* |
0.862 |
1.829 |
0.642 |
1.179 |
1.128 ± 0.517 (46) |
|
Гидроксильные / Hydroxyl |
2.002 |
4.382 |
1.546 |
2.572 |
2.625 ± 1.243 (47) |
|
L-пролин / L-proline |
0.726 |
1.282 |
0.637 |
1.048 |
0.923 ± 0.297 (32) |
|
Гидрокси-L-пролин / Hydroxy-L-proline |
0.123 |
0 |
0.077 |
0.194 |
0.098 ± 0.081 (83) |
|
Имино / Imino |
0.849 |
1.282 |
0.714 |
1.242 |
1.022 ± 0.283 (28) |
|
Сумма / Total |
13.725 |
37.029 |
12.822 |
24.558 |
22.034 ± 11.33 (51) |
Примечание. Звездочкой отмечены незаменимые кислоты, жирным шрифтом — группы аминокислот. Note. Essential acids are marked with an asterisk; amino acid groups are shown in bold.
Таблица 18. Содержание аминокислот в образцах мочи-1 , мг/г
Table 18. Amino acid content in urine-1 samples, mg/g
|
Аминокислоты Ammino acids |
Объекты / Objects |
Х ± S x (V x , %) |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
||
|
Глицин / Glycine |
0.0048 |
0.0096 |
0.0112 |
0.012 |
0.0081 |
0.021 |
0.0041 |
0.0124 |
0.0037 |
0.007 |
0.0094 ± 0.0051 (55) |
|
L-аланин L-alanine |
0.0097 |
0.0206 |
0.0115 |
0.0256 |
0.0118 |
0.0448 |
0.0106 |
0.0135 |
0.0096 |
0.0157 |
0.0173 ± 0.0109 (63) |
|
D-аланин D-alanine |
0.001 |
0.0006 |
0.0009 |
0.0014 |
0.0009 |
0.0011 |
0 |
0 |
0.0003 |
0.0009 |
0.0007 ± 0.0005 (66) |
|
L-валин* L-valine* |
0.0019 |
0.0294 |
0.0034 |
0.0104 |
0.0023 |
0.0244 |
0.0149 |
0.0033 |
0.0016 |
0.0034 |
0.0095 ± 0.0102 (185 |
|
L-лейцин* L-leucine* |
0.0043 |
0.0146 |
0.008 |
0.0215 |
0.0053 |
0.0517 |
0.006 |
0.008 |
0.0038 |
0.0094 |
0.0133 ± 0.0145 (100) |
|
L-изолейцин* L-isoleucine* |
0.0012 |
0.0053 |
0.0017 |
0.0062 |
0.001 |
0.0123 |
0.0006 |
0.0012 |
0.0008 |
0.0026 |
0.0033 ± 0.0037 (113) |
|
Алифатические Aliphatic |
0.0229 |
0.0801 |
0.0367) |
0.0771 |
0.0294 |
0.1553 |
0.0331 |
0.0364 |
0.198 |
0.039 |
0.0739 ± 0.0664 (90) |
|
L-метионин* L-methionine* |
0.0058 |
0.0137 |
0.0043 |
0.0063 |
0 |
0 |
0.0035 |
0 |
0.0086 |
0.0053 |
0.0048 ± 0.0043 (91) |
|
Алифатические серосодержащие Aliphatic sulfur-containing |
0.0058 |
0.0137 |
0.0043 |
0.0063 |
0 |
0 |
0.0035 |
0 |
0.0086 |
0.0053 |
0.0048 ± 0.0043 (91) |
|
L-фенилаланин* L-phenylalanine* |
0.003 |
0.0078 |
0.0046 |
0.0132 |
0.0032 |
0.0285 |
0.002 |
0.0057 |
0.0031 |
0.0056 |
0.0077 ± 0.0008 (104) |
|
L-тирозин L-tyrosine |
0.0019 |
0.0021 |
0.0055 |
0.013 |
0.0038 |
0.0355 |
0.0007 |
0.0075 |
0.002 |
0.0074 |
0.0079 ± 0.0104 (131 |
|
Ароматические Aromatic |
0.0049 |
0.0099 |
0.0101 |
0.0262 |
0.007 |
0.064 |
0.0027 |
0.0132 |
0.0051 |
0.013 |
0.0156 ± 0.0182 (117) |
Продолжение таблицы 18
Continuation of table 18
ставляет в среднем около 10. Среднестатистический коэффициент вариации содержаний кислот составляет (93 ± 33) %. Доля незаменимых кислот определяется в среднем как 0.93, т. е. в моче пациентов с мочекаменной болезнью доля незаменимых аминокислот выше, чем в собственно камнях. Последовательность снижения концентраций групп аминокислот: алифатические > кислые > ароматические > гидроксильные > основные > имино > алифатические серосодержащие. Этот ряд почти совпадает с аналогичным рядом для камней, отличаясь только дефицитом группы имино. Последовательность снижения концентраций незаменимых кислот имеет в рассматриваемом случае следующий вид: лизин > лейцин > валин > фенилаланин > треонин > метионин > изолейцин. То есть моча-1 отличается от камней дефицитом метионина. Так же как в камнях, в этой моче аланин, аспарагиновая и глутаминовая кислоты представлены обоими энантиомерами, отношения D/L в них составляют соответственно 0—0.103, 0—0.038, 0—0.159.
В собственно белках мочи-1 (табл. 19) сумма содержаний всех аминокислот достигает 27.74—286.43 мг/г, а незаменимых — 11.55—124.28 мг/г, что превышает данные для камней соответственно в 2—8 и 2.5—9 раз, а для мочи-1 соответственно в 533—650 и 491—650 раз. Размах колебаний групповых концентраций составля-
ет в среднем около 10. Среднестатистический коэффициент вариации содержаний аминокислот оценивается в (92 ± 27) %. Доля незаменимых кислот в проанализированных белках составляет в среднем 0.42, что гораздо ниже, чем в моче-1 и камнях. Последовательность снижения концентрации групп аминокислот в мочевых белках: алифатические > кислые > ароматические > основные > гидроксильные > имино > алифатические серосодержащие. Это практически совпадает с последовательностью в моче. Аналогичная последовательность незаменимых кислот в белках тождественна таковой в моче: лизин > лейцин > валин > фенилаланин > треонин > метионин > изолейцин. В мочевых белках, так же как в камнях и моче, аланин, аспарагиновая и глутаминовая кислоты представлены обоими энантиомерами, отношения D/L в них составляют соответственно 0—0.105, 0—0.04, 0—0.07.
В образцах мочи-2 больных хроническим пило-нефритом (табл. 20) установлен тот же набор аминокислот. Сумма содержаний всех аминокислот составляет 0.0974—0.233 мг/г, что в 1.5 раза меньше, чем в моче-1. Размах колебаний групповых концентраций достигает в среднем 19, что почти в два раза больше, чем в моче-1. Среднестатистический коэффициент вариации содержаний аминокислот определяется как 82 ± 37 %, что уступает такому показателю в моче-1. Сумма
|
Аминокислоты Ammino acids |
Объекты / Objects |
Х ± S x (V x , %) |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
||
|
L-лизин* L-lysine* |
0.0054 |
0.0128 |
0.0135 |
0.0277 |
0.0077 |
0.0482 |
0.0024 |
0.0162 |
0.0057 |
0.0154 |
0.0155 ± 0.0136 (88) |
|
Основные Essential |
0.0054 |
0.0128 |
0.0135 |
0.0277 |
0.0077 |
0.0482 |
0.0024 |
0.0162 |
0.0057 |
0.0154 |
0.0155 ± 0.0136 (88) |
|
L-аспарагиновая кислота L-aspartic acid |
0.003 |
0.011 |
0.008 |
0.0192 |
0.0057 |
0.0358 |
0.0021 |
0.0063 |
0.0033 |
0.0087 |
0.0103 ± 0.0102 (99) |
|
D-аспарагиновая кислота D-aspartic acid |
0.0001 |
0.0004 |
0.0003 |
0.0006 |
0 |
0.0009 |
0 |
0 |
0 |
0.0002 |
0.0002 ± 0.0003 (124) |
|
L-глутаминовая кислота L-glutamic acid |
0.0063 |
0.0171 |
0.0132 |
0.029 |
0.0103 |
0.0544 |
0.0057 |
0.0131 |
0.0071 |
0.0143 |
0.0171 ± 0.0148 (87) |
|
D-глутаминовая кислота D-glutamic acid |
0.0001 |
0.001 |
0.0009 |
0.0014 |
0 |
0 |
0 |
0 |
0 |
0.0011 |
0.0004 ± 0.0006 (127) |
|
Кислые / Acidic |
0.0095 |
0.0295 |
0.0224 |
0.0502 |
0.016 |
0.0911 |
0.0078 |
0.0194 |
0.0104 |
0.0243 |
0.0281 ± 0.0254 (90) |
|
L-серин / L-serine |
0.003 |
0.0075 |
0.009 |
0.0123 |
0.0068 |
0.0307 |
0.0024 |
0.0053 |
0.0035 |
0.0062 |
0.0087 ± 0.0083 (96) |
|
L-треонин* L-threonine* |
0.0019 |
0.0069 |
0.0043 |
0.0109 |
0.0022 |
0.0262 |
0.0019 |
0.003 |
0.0069 |
0.0048 |
0.0075 ± 0.0076 (102) |
|
Гидроксильные Hydroxyl |
0.0049 |
0.0144 |
0.0133 |
0.0232 |
0.009 |
0.0569 |
0.0043 |
0.0083 |
0.0104 |
0.011 |
0.0156 ± 0.0155 (99) |
|
L-пролин L-proline |
0.0026 |
0.0067 |
0.0048 |
0.0116 |
0.0029 |
0.0236 |
0.0014 |
0.0037 |
0.0024 |
0.0045 |
0.0064 ± 0.0067 (104) |
|
Гидрокси-L-пролин Hydroxy-L-proline |
0.0005 |
0.0007 |
0.0006 |
0.0015 |
0.0009 |
0.0016 |
0 |
0.0008 |
0.0007 |
0.0008 |
0.0008 ± 0.0005 (57) |
|
Имино / Imino |
0.0031 |
0.0074 |
0.0054 |
0.0131 |
0.0038 |
0.0252 |
0.0014 |
0.0045 |
0.0031 |
0.0053 |
0.0072 ± 0.0071 (98) |
|
Сумма / Total |
0.0565 |
0.1678 |
0.1057 |
0.2238 |
0.0729 |
0.4407 |
0.0552 |
0.098 |
0.2413 |
0.1133 |
0.1575 ± 0.1191 (76) |
Таблица 19. Содержание аминокислот непосредственно в белках образцов мочи-1 , мг/г
Table 19. Content of amino acids directly in proteins of urine-1 samples, mg/g
|
Аминокислоты Amino acids |
Объекты / Objects |
Х ± S x (V x , %) |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
||
|
Глицин / Glycine |
2.37 |
4.72 |
6.03 |
6.84 |
13.95 |
13.67 |
5.99 |
4.05 |
4.5 |
3.9 |
6.002 ± 4.005 (67) |
|
L-аланин / L-alanine |
4.76 |
10.14 |
6.16 |
14.59 |
20.29 |
29.12 |
15.5 |
4.41 |
11.71 |
8.81 |
12.549 ± 7.714 (61) |
|
D-аланин / D-alanine |
0.5 |
0.28 |
0.47 |
0.82 |
1.48 |
0.71 |
0 |
0 |
0.37 |
0.5 |
0.513 ± 0.431 (84) |
|
L-валин* / L-valine* |
0.92 |
14.49 |
1.83 |
5.95 |
3.88 |
15.87 |
21.77 |
1.08 |
1.91 |
1.93 |
6.963 ± 7.558 (108) |
|
L-лейцин* / L-leucine* |
2.12 |
7.21 |
4.26 |
12.26 |
9.16 |
33.61 |
4.28 |
1.96 |
4.63 |
5.3 |
8.479 ± 9.376 (111) |
|
L-изолейцин* / L-isoleucine* |
0.57 |
2.62 |
0.9 |
3.56 |
1.64 |
7.99 |
0.92 |
0.39 |
1.03 |
1.46 |
2.108 ± 2.284 (108) |
|
Алифатические Aliphatic |
11.24 |
39.46 |
19.68 |
44.02 |
50.4 |
100.97 |
48.46 |
11.89 |
24.15 |
21.9 |
37.217 ± 26.761 (72) |
|
L-метионин* / L-methionine* |
2.86 |
6.72 |
2.33 |
3.6 |
0 |
0 |
5.15 |
0 |
10.54 |
3.0 |
3.42 ± 3.356 (98) |
|
Алифатические серосодержащие Aliphatic sulfur-containing |
2.86 |
6.72 |
2.33 |
3.6 |
0 |
0 |
5.15 |
0 |
10.54 |
3.0 |
3.42 ± 3.356 (98) |
|
L-фенилаланин* L-phenylalanine* |
1.45 |
3.86 |
2.45 |
7.53 |
5.55 |
18.49 |
2.96 |
1.85 |
3.77 |
3.15 |
5.106 ± 5.033 (99) |
|
L-тирозин / L-tyrosine |
0.91 |
1.02 |
2.97 |
7.44 |
6.46 |
23.07 |
1.04 |
2.45 |
2.5 |
4.16 |
5.202 ± 6.667 (128) |
|
Ароматические / Aromatic |
2.36 |
4.88 |
5.42 |
14.97 |
12.01 |
41.56 |
4.0 |
4.3 |
6.27 |
7.31 |
10.808 ± 8.489 (108) |
|
L-лизин* / L-lysine* |
2.67 |
6.28 |
7.21 |
15.8 |
13.15 |
31.31 |
3.47 |
5.31 |
6.98 |
8.63 |
10.081 ± 8.489 (84) |
|
Основные / Essential |
2.67 |
6.28 |
7.21 |
15.8 |
13.15 |
31.31 |
3.47 |
5.31) |
6.98 |
8.63 |
10.611 ± 8.827 (83) |
|
L-аспарагиновая кислота L-aspartic acid |
1.46 |
5.43 |
4.26 |
10.92 |
9.73 |
23.24 |
3.02 |
2.04 |
3.98 |
4.89 |
6.897 ± 6.507 (94) |
|
D-аспарагиновая кислота D-aspartic acid |
0.06 |
0.17 |
0.16 |
0.36 |
0 |
0.61 |
0 |
0 |
0 |
0.1 |
0.146 ± 0.199 (136) |
|
L-глутаминовая кислота L-glutamic acid |
3.09 |
8.44 |
7.08 |
16.53 |
17.67 |
35.37 |
8.28 |
4.27 |
8.69 |
8.03 |
11.745 ± 9.515 (81) |
|
D-глутаминовая кислота D-glutamic acid |
0.06 |
0.48 |
0.46 |
0.82 |
0 |
0 |
0 |
0 |
0 |
0.61 |
0.243 ± 0.316 (130) |
|
Кислые / Acidic |
4.67 |
14.52 |
11.96 |
28.63 |
27.4 |
59.22 |
11.3 |
6.31 |
12.67 |
13.67 |
19.035 ± 16.141 (85) |
|
L-серин / L-serine |
1.48 |
3.69 |
4.83 |
7.0 |
11.67 |
19.95 |
3.53 |
1.74 |
4.32 |
3.5 |
6.171 ± 5.656 (92) |
|
L-треонин* / L-threonine* |
0.96 |
3.39 |
2.32 |
6.19 |
3.74 |
17.01 |
2.76 |
0.97 |
2.3 |
2.71 |
4.404 ± 4.984 (113) |
|
Гидроксильные Hydroxyl |
2.44 |
7.08 |
7.15 |
13.19 |
15.41 |
36.96 |
6.29 |
2.71 |
6.62 |
6.21 |
10.406 ± 10.171 (98) |
|
L-пролин / L-proline |
1.27 |
3.28 |
2.6 |
6.61 |
4.91 |
15.35 |
1.97 |
1.2 |
2.99 |
2.53 |
4.271 ± 4.227 (99) |
|
Гидрокси-L-пролин Hydroxy-L-proline |
0.23 |
0.32 |
0.35 |
0.88 |
1.54 |
1.06 |
0.25 |
0.84 |
0.45 |
0.658 ± 0.451 (68) |
|
|
Имино / Imino |
1.5 |
3.6 |
2.95 |
7.49 |
6.45 |
16.41 |
1.97 |
1.45 |
3.83 |
2.98 |
4.863 ± 4.521 (93) |
|
Сумма / Total |
27.74 |
82.54 |
56.7 |
127.7 |
124.82 |
286.43 |
80.64 |
31.97 |
71.06 |
63.66 |
95.326 ± 74.895 (78) |
|
Масса белка в исследованных образцах, г Protein mass in the studied samples, g |
0.002 |
0.002 |
0.0019 |
0.0021 |
0.0005 |
0.0013 |
0.0006 |
0.0017 |
0.0007 |
0.0022 |
0.002 ± 0.0007 |
Таблица 20. Содержание аминокислот в образцах мочи-2 , мг/г
Table 20. Amino acid content in urine-2 samples, mg/g
|
Аминокислоты / Amino acids |
Образцы / Samples |
X ± S x (V x , %) |
|
|
11 |
12 |
||
|
Глицин / Glycine |
0.006 |
0.013 |
0.0095 ± 0.0049 (52) |
|
L-аланин / L-alanine |
0.0141 |
0.037 |
0.0255 ± 0.0162 (63) |
|
D-аланин / D-alanine |
0 |
0.0015 |
0.0007 ± 0.0011 (141) |
|
L-валин* / L-valine* |
0.0122 |
0.0106 |
0.0114 ± 0.0011 (10) |
|
L-лейцин* / L-leucine* |
0.0064 |
0.0211 |
0.0137 ± 0.0104 (75) |
|
L-изолейцин* / L-isoleucine* |
0.0019 |
0.0064 |
0.0041 ± 0.0032 (77) |
|
Алифатические / Aliphatic |
0.0406 |
0.0896 |
0.0651 ± 0.0346 (53) |
|
L-метионин* / L-methionine* |
0.0012 |
0.0057 |
0.0034 ± 0.0032 (92) |
|
Алифатические серосодержащие / Aliphatic sulfur-containing |
0.0012 |
0.0057 |
0.0034 ± 0.0032 (92) |
|
L-фенилаланин* / L-phenylalanine* |
0.004 |
0.0118 |
0.079 ± 0.0055 (70) |
|
L-тирозин / L-tyrosine |
0.0004 |
0.0135 |
0.0069 ± 0.0093 (133) |
|
Ароматические / Aromatic |
0.0044 |
0.0253 |
0.0148 ± 0.0148 (99) |
Продолжение таблицы 20
Continuation of table 20
содержаний независимых кислот в моче-2 составляет 0.0384—0.1109 мг/г, что дает 0.88 общего баланса аминокислот. Это ниже, чем в моче-1. Последовательность снижения концентрации групп аминокислот: алифатические > кислые > гидроксильные > ароматические > основные > имино > алифатические серосодержащие. Здесь в сравнении c образцами мочи-1 поменялись местами гидроксильные (их стало больше) и ароматические кислоты. Последовательность незаменимых аминокислот в моче-2 специфична: треонин > лейцин > лизин > валин > фенилаланин > > изолейцин > метионин. Здесь особенность состоит в том, что в моче-2 наибольшее содержание не у алифатической, а у гидроксильной незаменимой кислоты. Кроме того, в этой моче только две аминокислоты — аланин и аспарагиновая кислота — представлены обоими энантиомерами, отношения D/L в них составляют соответственно 0—0.0415 и 0—0.032.
Обобщение полученных данных приводит к следующему выводу. Среди исследованных объектов по свойствам аминокислотности объединяются три, относящиеся к пациентам с мочекаменной болезнью и образующие более или менее упорядоченную последовательность: белки мочи-1 → мочевые камни → моча-1 . В направлении этой последовательности более или менее упорядоченно снижается сумма содержаний аминокислот (очень резко при переходе к моче), аналогичным образом падает сумма содержаний незаменимых кислот, возрастает доля незаменимых кислот в их общей сумме. Последовательности снижения концентраций групп аминокислот в белках мочи-1 и собственно моче-1 практически тождественны, а в мочевых камнях концентрация отличается аномально высоким содержанием метионина. Аналогично ведут себя величина колебаний содержаний кислот (достигает максимума в камнях) и коэффициентов их вариации (минимален в камнях). Степень хиральности в аланине, аспарагиновой и глутаминовой кислотах минимальна и примерно одинакова. Как известно, это свойство аминокислот в живых организмах и минерализациях часто объясняют старением (Huskic, Pecov, 2016; Hassan, Jaleel, 2014). Однако в нашем случае корреляции между возрастом пациентов и степенью хиральности не выявляется. Вероятной причи-
ной появления D-энантиомера в аминокислотах изученных образцов может являться участие в жизнедеятельности человека бактерий, в аминокислотах которых всегда есть D-энантиомеры (Машина, Шанина, 2022).
Остается отметить особенности аминокислотного состава образцов мочи-2 пациентов с хроническим пиелонефритом. В этом случае суммарное содержание аминокислот и содержание незаменимых кислот примерно совпадают с таковыми в образцах мочи-1, но значительно (почти в 2 раза) возрастает размах колебаний содержаний, увеличивается групповая доля гидроксильных аминокислот и особенно резко возрастает содержание треонина среди незаменимых кислот.
Изотопия
Изотопный состав углерода и азота определялся в органическом веществе мочевых камней и моче-1 пациентов с мочекаменной болезнью (табл. 21), а также моче-2 пациентов с хроническим пиелонефритом (табл. 22). Согласно полученным данным (рис. 15 ), мочевые камни характеризуются относительно изотопно-тяжелым составом углерода, но изотопно-легким составом азота. Моча- 1 более изотопно-легкая по углероду, но более изотопно-тяжелая по азоту. Моча-2 наиболее изотопно-легкая по углероду и изотопно-легкая на уровне мочевых камней по азоту. В целом исследованные нами объекты по изотопному составу весьма специфичны и отличаются как от органического вещества человеческих костей — гораздо более изотопно-тяжелые по азоту (Силаев, Белицкая, 2019), ископаемых копролитов — более изотопно-тяжелые по углероду (Силаев, Юшкин, 2019), так и от земной атмосферы (δ13СPDB = –5…–8 ‰; δ15NAIR = 5—8 ‰) и углеродного вещества в осадочных горных породах (δ13СPDB= –15 —2 ‰; δ15NAIR= от –12 до 12 ‰) (Силаев, Смолева, 2012). Как ни странно, но наиболее близкими к изученному органическому веществу по изотопным данным оказались выявленные нами в продуктах современного вулканизма абиогенные органические полимеры, в которых δ13СPDB лежит в пределах –27…–25 ‰ (Силаев, Аникин, 2018).
|
Аминокислоты / Amino acids |
Образцы / Samples |
X ± S x (V x , %) |
|
|
11 |
12 |
||
|
L-лизин* / L-lysine* |
0.0027 |
0.0217 |
0.0122 ± 0.0134 (110) |
|
Основные / Essential |
0.0027 |
0.0217 |
0.0122 ± 0.0134 (110) |
|
L-аспарагиновая кислота/ L-aspartic acid |
0.0034 |
0.0186 |
0.011 ± 0.0107 (98) |
|
D-аспарагиновая кислота / D-aspartic acid |
0 |
0.0006 |
0.0003 ± 0.0004 (140) |
|
L-глутаминовая кислота / L-glutamic acid |
0.0069 |
0.0259 |
00164 ± 0.0134 (82) |
|
D-глутаминовая кислота / D-glutamic acid |
0 |
0 |
0 |
|
Кислые / Acidic |
0.0103 |
0.0554 |
0.0328 ± 0.0319 (97) |
|
L-серин / L-serine |
0.0039 |
0.0129 |
0.0084 ± 0.0064 (76) |
|
L-треонин* / L-threonine* |
0.032 |
0.0116 |
0.0218 ± 0.0144 (66) |
|
Гидроксильные / Hydroxyl |
0.0359 |
0.0245 |
0.0302 ± 0.0081 (27) |
|
L-пролин / L-proline |
0.0023 |
0.01 |
0.0061 ± 0.005 (82) |
|
Гидрокси-L-пролин / Hydroxy-L-proline |
0 |
0.0009 |
0.0005 ± 0.0006 (142) |
|
Имино / Imino |
0.0023 |
0.0109 |
0.0066 ± 0.0061 (92) |
|
Сумма / Total |
0.0974 |
0.233 |
0.1652 ± 0.0959 (58) |
Таблица 21. Изотопный состав углерода и азота в органическом веществе мочевых камней и мочи-1 , ‰
Table 21. Isotopic composition of carbon and nitrogen in the organic matter of urinary stones and urine-1 , ‰
|
№ обр. / Sample No. |
Камни / Stones |
Моча-1 / Urine-1 |
||
|
δ 13 СPDB |
δ15N AIR |
δ13С PDB |
δ15N AIR |
|
|
1 |
–23.46 |
7.86 |
–24.59 |
6.04 |
|
2 |
–19.08 |
–1.05 |
–24.55 |
6.37 |
|
3 |
–22.32 |
4.62 |
–22.05 |
7.35 |
|
4 |
–21.89 |
н. о. |
–25.41 |
7.99 |
|
5 |
–19.72 |
–0.89 |
–22.58 |
11.47 |
|
6 |
–21.11 |
–6.8 |
–23.8 |
н. о. |
|
7 |
–19.56 |
–1.33 |
–23.16 |
2.45 |
|
8 |
–21.83 |
2.91 |
–23.78 |
3.58 |
|
9 |
–21.88 |
0.29 |
–22.71 |
10.69 |
|
10 |
–17.91 |
0.02 |
–24.38 |
4.37 |
|
Среднее / Average |
–20.88 |
2.14 |
–23.7 |
6.7 |
|
СКО / SD |
1.73 |
3.54 |
1.06 |
3.05 |
|
V, % |
8.3 |
165.4 |
4.5 |
45.5 |
|
Коэффициент корреляции |
– |
0.11 |
||
|
Correlation coefficient |
||||
Таблица 22. Изотопный состав углерода и азота в органическом веществе мочи-2 , ‰
Table 22. Isotopic composition of carbon and nitrogen in organic matter of urine-2 , ‰
|
№ обр / Sample No. |
δ 13СPDB |
δ 15NAIR |
|
11 |
–25.29 |
1.37 |
|
12 |
–26.12 |
3.93 |
|
Среднее / Average |
–25.7 |
2.65 |
|
СКО / SD |
0.58 |
1.81 |
|
V x , % |
2.3 |
68.3 |
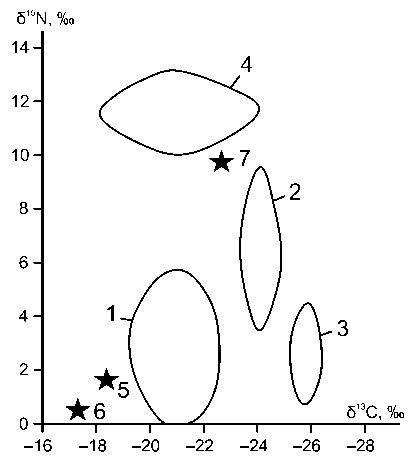
Рис. 15 , Статистика изотопного состава углерода и азота в органическом веществе мочевых камней и образцах мочи: 1 — мочевые камни; 2 — моча пациентов с мочекаменной болезнью; 3 — моча пациентов с хроническим пиелонефритом; 4 — кости человека; 5—7 — мочевые камни сульфатно-уратно-фосфатные (5), уратно-суль-фатно-фосфатные (6) и опал-фосфатные (7) (по: Силаев, Кокин, 2021)
Fig. 15. Statistics of the isotopic composition of carbon and nitrogen in the organic matter of urinary stones and urine samples: 1 — urinary stones; 2 — urine of patients with urolithiasis; 3 — urine of patients with chronic pyelonephritis; 4 — human bones; 5—7 — sulfate-urate-phosphate (5), urate-sulfate-phosphate (6) and opal-phosphate (7) urinary stones (according to: Silaev, Kokin, 2021)
Заключение
С использованием широкого комплекса минералогических и физико-химических методов изучена эталонная коллекция образцов мочевых камней мужчин и женщин в возрасте 27—83 лет и мочи пациентов с мочекаменной болезнью и хроническим пиелонефритом. Мочевые камни характеризуются преимущественно светлой окраской и округлой формой, широко варьируются по внутреннему строению. В их составе выявлено до 14 фаз: органическое вещество с урицитом и эритроцитами, водные кальциевые оксалаты, силикаты и алюмосиликаты, металлоорганические соединения, металлические фазы, гидроген-сульфаты и фосфаты, биоапатит, фосфатосульфаты бария, сульфиды, гидрокси- и гидроген-хлориды, сульфато-силикатофосфаты, магнетит, кремниевая фаза. По характеру распределения выявленных фаз исследуемые мочевые камни подразделяются на два типа: 1) многофазные (от 6 до 14), равномерно распределенные между мужчинами и женщинами в возрасте 27—83 лет; 2) ограниченно-фазные (3—5), преимущественно мужские. В целом обнаруженные в составе мочевых камней биоминералы охватывают практически всю современную номенклатуру минеральных типов. Исследованная моча состояла на 75—77 % из воды, в состав примесей входили Cl, SO3, P2O5, FeO, Na2O, K2O, CaO, MgO, NH4 — важнейшие компоненты и мочевых камней.
В мочевых камнях выявлены 18 микроэлементов, почти исключительно органофильных: 46 % — эссенциальные, 54 % физиогенно-активные. В моче-1 обнаружен 41 органофильный микроэлемент с сильным преобладанием (86 %) эссенциальных элементов. По степени суммарного обогащения микроэле- ментами моча-1 преобладает над мочевыми камнями в 26 раз. В моче-2 установлен также 41 органофильный микроэлемент с преобладанием (75 %) эссенциальных элементов. По степени суммарного обогащения микроэлементами образцы мочи-2 в два раза уступают мочевым камням и в 49 раз — образцам мочи-2.
Исследованные объекты, относящиеся к пациентам с мочекаменной болезнью, по свойствам белковых аминокислот образуют довольно упорядоченную последовательность: белки мочи-1 → мочевые камни → моча-1 . В направлении этой последовательности снижается сумма содержаний аминокислот (очень резко при переходе к моче), аналогичным образом падает сумма содержаний незаменимых кислот, но возрастает их доля в общей сумме аминокислот. Очевидно, что это обусловлено последовательностью снижения в объектах содержания белков. Последовательности снижения концентраций групп аминокислот в белках мочи-1 и собственно моче-1 практически тождественны, а в мочевых камнях аналогичная последовательность отличается только аномально высоким содержанием метионина. Аналогично ведут себя размах колебаний содержаний кислот (достигает максимума в камнях) и коэффициент их вариации (минимален в камнях). Степень хиральности в аланине, аспарагиновой и глутаминовой кислотах минимальна и примерно одинакова. Вероятной причиной появления D-энантиомера в аминокислотах изученных образцов может являться участие в жизнедеятельности человека бактерий. В целом информация об аминокислотном составе свидетельствует о высокой степени сходства мочи-1 и мочевых камней. В образцах мочи-2 пациентов с хроническим пиелонефритом суммарное содержание аминокислот и содержание незаменимых кислот примерно совпадают с таковыми в образцах мочи-1, но значительно (почти в 2 раза) возрастает размах колебаний содержаний, увеличивается групповая доля гидроксильных аминокислот и особенно резко возрастает содержание треонина среди незаменимых кислот.
Мочевые камни характеризуются относительно изотопно-тяжелым составом углерода, но изотопнолегким составом азота; моча-1 более изотопно-легкая по углероду, но более изотопно-тяжелая по азоту; моча-2 наиболее изотопно-легкая по углероду и изотопно-легкая на уровне мочевых камней по азоту. В целом исследованные объекты по изотопному составу весьма специфичны, отличаясь от органического вещества человеческих костей, ископаемых копролитов, земной атмосферы и углеродного вещества в осадочных горных породах. Но при этом они обнаруживают близость по изотопному составу углерода с абиогенными органическими полимерами в продуктах современного вулканизма. Представленные данные достаточно хорошо согласуется с современными представлениями о непрерывном процессе обмена веществом практически всех геосфер Земли (Кокин, 2024).
Результаты междисциплинарного исследования показывают следующее. Если в условиях земной коры источником энергии образования минеральных видов выступают физико-химические процессы в её геологической истории, то в организме человека биоэнергетический и биохимический потенциал выполняет ту же работу, но по синтезу металлоорганических соединений и других минералоидов. В условиях, близких к равновесному состоянию, в организме человека и земной коре не происходит существенных сдвигов, вызывающих минералообразование. В неравновесных термодинамических условиях земной коры под влиянием обменных эндогенных физико-химических и геологических процессов формируется все многообразие пород, руд и минералов. Подобное состояние наблюдается и в организме человека, но при нарушениях обменных биохимических процессов под влиянием особенностей питания, различных заболеваний, колебаний pH и Eh среды, жизнедеятельности бактерий, изменений в окружающей среде. В организме человека происходит сброс органоминеральных образований из водно-солевого раствора по всей разветвлённой сети сосудов и каналов, что приводит к возникновению мочекаменной и желчнокаменной болезней, отложению солей в кровеносных сосудах. То есть практически в организме человека возникают условия для минералообразования, имеющего принципиальное подобие с минералообразованием в геологических условиях (коэволюция минерального и биологического миров по Н. П. Юшкину). Однако концентрации органофильных элементов и соответствующих им биоминералов в организме человека могут многократно превышать таковые в геологических условиях. То есть потенциал живого для экстракции ряда химических элементов из водных растворов при образовании конкрементов может оказаться более эффективным, чем рудообразование в геологических условиях.
Все это лишний раз подтверждает известные положения о том, что «природа транслирует подобие своей организации на любом уровне вещества в рамках её фундаментальных законов» (Кокин, Кокин, 2022). Следовательно, продемонстрированные нами междисциплинарные исследования могут быть полезными не только для минералогов, биологов и медиков, но и для геологов в части изучения осадочных рудных месторождений, образовавшихся при участии живого вещества.
Исследования выполнены в рамках бюджетной темы 122040600009-2 «Фундаментальные проблемы минералогии и минералообразования, минералы как индикаторы петро- и рудогенеза, минералогия рудных районов и месторождений Тимано-Североуральского региона и арктических территорий».


