Биотрансформация бетулина с использованием актинобактерий рода Rhodococcus
Автор: Тарасова Е.В., Гришко В.В., Ившина И.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 1, 2015 года.
Бесплатный доступ
Впервые показана способность актинобактерий рода Rhodococcus к биотрансформации растительного пентациклического тритерпеноида лупанового ряда бетулина с образованием бетулона. Бетулон представляет собой продукт региоселективного окисления 3р-гидроксильной группы бетулина и является перспективным интермедиатом для получения новых биологически активных соединений. Из 104 исследованных штаммов родококков разных видов из Региональной профилированной коллекции алканотрофных микроорганизмов отобран наиболее активный штамм-биотрансформатор R. rhodochrous ИЭГМ 66. Установлено, что в присутствии 0.5 г/л бетулина растущие клетки родококков катализируют образование до 72.2% бетулона в течение 240 ч. Использование нерастущих клеток родококков позволяет существенно сократить продолжительность процесса биотрансформации бетулина, при этом уровень биоконверсии бетулина (0.5-3.0 г/л) в бетулон через 96 ч. составляет 60-75 %
Бетулин, бетулон, биотрансформация, региоселективное окисление
Короткий адрес: https://sciup.org/147204705
IDR: 147204705 | УДК: 579.66+615.322
Betulin biotransformatiom by Rhodococcus actinobacteria
The ability of Rhodococcus actinobacteria to biotransform betulin, a vegetational pentacyclic lu-pane triterpenoid, to betulone was proved and reported for the first time. Betulone, the product of regioselective oxidation of a 3p-hydroxyl group of betulin, is a useful intermediate in the synthesis of novel biologically active compounds. Of 104 rhodococcal strains tested from the Regional Specialized Collection of Alkanotrophic Microorganisms R. rhodochrous IEGM 66 was selected because it had the highest betulin-transforming ability. The growing cells of R. rhodochrous IEGM 66 were shown to transform 0.5 g/L betulin to betulone with 72.2% conversion rate within 240 h. A substantial reduction in the time of betulin biotransformation was achieved by using resting cells, wherein betulin (0.5 to 3.0 g/L) conversion to betulone was 60-75% within 96 h.
Текст научной статьи Биотрансформация бетулина с использованием актинобактерий рода Rhodococcus
Полициклические тритерпеноиды растительного происхождения представляют интерес в качестве исходных соединений в синтезе новых фармакологически активных веществ. Бетулин (луп-20(29)-ен-3,28-диол, C30H50O2, CAS: 473-98-3) – пентациклический тритерпеноид лупанового ряда, содержание которого во внешнем слое коры березы достигает 20-35%, активно используется для получения противовоспали- тельных, гепапротекторных, противоопухолевых, противовирусных, антималярийных, антибактериальных соединений [Betulin …, 2005; Pharmacological ..., 2006; Novel semisynthetic …, 2009].
Помимо химических модификаций предпринимаются попытки биологической трансформации бетулина с помощью микроорганизмов, так как биокатализ открывает возможность получать целевые продукты с высокой степенью регио- и стереоселективности в одну технологическую стадию при
обычных температурах и давлении, в неагрессивной реакции среды и экологически безопасных условиях. Примеры биотрансформации бетулина пока немногочисленны [Microbial …, 2009; Biotransformation of triterpenes, 2011] и связаны преимущественно с использованием эукариотов, в частности представителей грибов Armillaria , Aspergillus , Chaetomium , Dothideomycetes , Rhodotorula. Описаны процессы окислительного расщепления бетулина до 4,28-дигидрокси-3,4-секолуп-20(29)-ен-3-овой кислоты при участии Chaetomium longirostre IFO 9873 [Microbial …, 2002] и окисления бетулина до бетулиновой кислоты с участием Armillaria luteo-virens Sacc QH, Aspergillus foetidus Zu-G1, Aspergillus oryzae Sacc QH [The betulinic acid ..., 2009; Liu, Fu, Chen, 2010]. Недавно появились сведения о региоселективном окислении бетулина до бетулона с использованием Rhodotorula muci-laginosa F10 [Novel biotransformation …, 2012] и Dothideomycete sp. HQ 316564 [Highly …, 2013].
В качестве одного из перспективных интермедиатов в синтезе биологически активных соединений особый интерес представляет 3-оксопроизводное бетулина – бетулон [Synthesis and cytotoxicity of 2-cyano …, 2009; Synthesis and cytotoxicity of 28-carboxymethoxy …, 2009; Synthesis, proapoptotic …, 2010; Trofimov ..., 2011]. Описаны процессы химического синтеза цитотоксичных циано- и азапроизводных бетулина на основе бетулона [Synthesis and cytotoxicity of 2-cyano …, 2009; Synthesis and cytotoxicity of 28-carboxymethoxy …, 2009; Synthesis, proapoptotic …, 2010]. В отличие от трехстадийного химического синтеза бетулона использование микроорганизмов позволяет осуществлять одностадийное окисление вторичной гидроксильной группы бетулина в оксогруппу при сохранении нативной С(28) гидроксильной группы. Однако описанные процессы биотрансформации бетулина до бетулона с использованием условнопатогенных дрожжей R . mucilaginosa F10 [Novel biotransformation …, 2012] и грибов Dothideomycete sp. HQ 316564 [Highly …, 2013] имеют значительные недостатки, поскольку осуществляются в условиях использования сложных питательных сред, характеризуются высокой продолжительностью, невысоким уровнем биоконверсии субстрата при внесении низких концентраций исходного соединения. Кроме того, использование грибов в качестве биокатализаторов потенциально опасно вследствие характера их посевного материала (споры) и способности к синтезу микотоксинов, обладающих мутагенным и канцерогенным действием. В связи с этим актуальным является поиск непатогенных микроорганизмов, способных эффективно катализировать окислительные трансформации бетулина.
Одной из активно используемых групп микроорганизмов в промышленной биотехнологии являются непатогенные актинобактерии рода Rhodococcus. Не мицелиальный характер роста, политрофность и лабильность метаболических систем, синтез биосурфактантов, способность расти на минимальных средах, высокая каталитическая активность и отсутствие выраженных патогенных свойств [Ившина, Пшеничнов, Оборин, 1987; Oil desorption …, 1998; Larkin, Kulakov, Allen, 2006; Biodegradation …, 2009; Kuyukina, Ivshina, 2010] обусловливают перспективность реализации уникальных метаболических систем родококков для окислительной биотрансформации бетулина.
Цель настоящего исследования – оценка бетулинтрансформирующей активности коллекционных культур актинобактерий рода Rhodococcus и подбор оптимальных условий процесса биотрансформации.
Материалы и методы
В работе использовали 104 штамма родокок-ков, принадлежащих к видам R. erythropolis (33), ‘R. longus’ (10), R. opacus (14), R. rhodochrous (17), R. ruber (30) и поддерживаемых в Региональной профилированной коллекции алканотрофных микроорганизмов (официальный акроним коллекции ИЭГМ, номер 768 во Всемирной федерации коллекций культур, .
Условия культивирования . Бактерии выращивали в колбах Эрленмейера объемом 250 мл, в которые вносили 100 мл питательной среды. Культивирование проводили на орбитальной качалке Certomat IS (Sartorius, Германия) при 160 об/мин. и 28 ° С. В опытах по биотрансформации бетулина использовали минеральную среду следующего состава (г/л): K 2 HPO 4 – 1.0; KH 2 PO 4 – 1.0; KNO 3 – 1.0; NaCl – 1.0; MgSO 4 ∙7H 2 O – 0.2; CaCl 2 ∙2H 2 O – 0.02; FeCl 3 – 0.001 [Каталог штаммов…, 1994]. В среду добавляли 0.1% дрожжевого экстракта (Микроген, Россия) и раствор микроэлементов по Постгейту [Романенко, Кузнецов, 1974]. Исходное значение рН реакционной среды составляло 6.8-7.0 до инокуляции. В качестве субстратов роста использовали глюкозу (1.0%), глицерин (1.0%) или н -гексадекан (0.1; 1.0; 3.0 об. %). В отдельных экспериментах для культивирования родококков использовали мясопептонный бульон (МПБ) производства ГНЦ ПМБ, Оболенск, Россия следующего состава (г/л): панкреатический гидролизат рыбной муки – 8.0; пептон ферментативный – 8.0; NaCl – 4.0; рН 7.0–7.4. Бактерии, выращенные на мясопептонном агаре (МПА) в течение 48 ч., вносили в среду культивирования до конечной концентрации 6.5 x 10 6 клеток/мл. Бетулин (0.5 г/л) в культуральную среду добавляли в виде раствора в диметилсульфоксиде (1:10 мг/мкл) через 48 ч с начала культивирования родококков. В данных условиях динамику образования бетулона отслеживали с интервалом 24 ч. в течение 240 ч.
Условия иммобилизации . В качестве носителя использовали макропористый гетерофазный криогель на основе поливинилового спирта (ПВС) производства ПО «Азот», Невинномысск, Россия. Иммобилизацию клеток R. rhodochrous ИЭГМ 66, предварительно выращенных в минеральной среде с добавлением 3.0 об. % н -гексадекана, осуществляли путём внесения клеточной суспензии в раствор ПВС по методике, описанной в работе [Immobilization …, 2006]. Клеточную суспензию и раствор ПВС смешивали в соотношении 1:2 v/v. Последующие этапы гранулирования, замораживания и оттаивания осуществляли согласно указанной выше методике. Перед использованием полученный биокатализатор регидратировали в 0.5%-ном растворе NaCl в течение 24 ч. и добавляли в минеральную среду из расчета 200 гранул (5.0±0.6 х 10 6 клеток/мл) на 100 мл среды.
Подготовка суспензий нерастущих клеток . Под термином «нерастущие клетки» (resting cells) понимаем трижды отмытые от питательной среды жизнеспособные клетки стационарной фазы роста, прекратившие свое деление в силу исчерпания источников питания или в силу каких-либо иных причин [Эль-Регистан, 2005] и перенесенные из питательной среды в буферный раствор. Клетки R. rhodochrous ИЭГМ 66 предварительно выращивали в МПБ и минеральной среде в присутствии глюкозы (1.0%), глицерина (1.0%) или н -гексадекана (1.0 об. %) в течение 48-72 ч. Родо-кокки в стационарной фазе роста осаждали центрифугированием при 3000 об/мин. в течение 10 мин. и трижды промывали эквивалентным объемом фосфатного буфера (рН 7.0) с последующим центрифугированием. Для получения фосфатного буферного раствора со значением рН 6.0; 7.0; 8.0; 9.0 к 500 мл 0.1 М KH 2 PO 4 (13.6 г/л) добавляли 56, 291, 461 и 481 мл 0.1 М NaOH (4 г/л) соответственно и доводили дистиллированной водой до 1000 мл [Справочник …, 1991]. Отмытые клетки ресуспендировали в 100 мл фосфатного буфера (рН 6.0; 7.0; 8.0 или 9.0) и доводили оптическую плотность клеточных суспензий до значений OП 600 1.4; 1.6; 1.8; 2.0; 2.2; 2.4; 2.6; 2.8 с последующим пересчетом на сухой вес клеточной биомассы. Бетулин вносили в подготовленную клеточную суспензию в концентрации 0.5; 1.0; 2.0 или 3.0 г/л. Продолжительность экспериментов по биотрансформации бетулина нерастущими клетками составляла 96 ч., при оценке динамики накопления бетулона пробы отбирали каждые 24 ч. В сравнительных исследованиях бетулинтрансформирующей активности нерастущих клеток использовали подготовленные аналогичным образом клеточные суспензии родококков разных видов.
Получение клеточных фракций . Суспензию клеток R. rhodochrous ИЭГМ 66 в 100 мл фосфатном буфере (pH 7.0; OП 600 2.0) обрабатывали с помощью ультразвукового дезинтегратора Soniprep 150 (MSE, Великобритания) при амплитуде 10 мкм в течение 60 мин. Полученный гомогенат центрифугировали при охлаждении 6000 об/мин. в течение 10 мин. Для выделения мембраносвязанных ферментов осадок ресуспендировали в 100 мл 1%-ного раствора Тритона X-100 в фосфатном буфере (рН 7.0), перемешивали на орбитальном шейкере в течение 30 мин. и затем центрифунировали при 6000 об/мин. в течение 10 мин. Полученный осадок, содержащий неэкстрагируемые ферменты, ре-суспендировали в 100 мл фосфатном буфере (рН 7.0). Подготовленные клеточные фракции: (1) супернатант с внутриклеточными ферментами; (2) супернатант с мембранносвязанными ферментами, (3) ресуспендированные соникаты с ферментами, не экстрагируемыми детергентами, использовали в сравнительных исследованиях по биотрансформации бетулина (0.5 г/л) и наиболее изученных структурных аналогов бетулина - β-ситостерола (0.5 г/л) и холестерола (0.5 г/л). В качестве контроля использовали суспензию клеток R. rhodo-chrous ИЭГМ 66 (OП 600 2.0) в 100 мл фосфатном буферном растворе (pH 7.0).
Определение дыхательной активности родо-кокков проводили с помощью высокоэффективного 6-канального респирометра Micro-OxymaxR (Columbus Instruments, США) в стеклянных флаконах Micro-Oxymax вместимостью 300 мл, содержащих 100 мл бактериальной суспензии (OП 600 2.6) в фосфатном буфере и бетулин в концентрации 0.5; 1.0; 2.0 и 3.0 г/л. Постоянное перемешивание (300 об/мин.) осуществляли с помощью многоместной магнитной мешалки RT 10 (Power IKAMAG, Германия) в течение 96 ч при температуре 28±2°С. Оценивали скорость дыхания (мкл/мин-1) и количество потребляемого кислорода (мкл). В качестве контроля использовали бактериальную суспензию в фосфатном буфере (OП 600 2.6) без добавления бетулина.
Исследование продуктов биотрансформации. Для выделения продуктов биотрансформации бетулина постферментационную среду подкисляли 10%-ным водным раствором HCl до рН 3.0–4.0 и трижды экстрагировали эквивалентным объемом этилацетата. Объединенные экстракты последовательно промывали 1%-ным водным раствором Na2CO3 и дистиллированной водой (до рН 7.0). Полученный этилацетатный экстракт обезвоживали над Na2SO4. Растворитель удаляли с помощью роторного испарителя (Heidolph, Германия). Качественный состав метаболитов предварительно контролировали методом тонкослойной хроматогра- фии (ТСХ) на высокоэффективных пластинах с силикагелем ПТСХ-П-В (Sorbfil, Россия). Наличие продуктов окисления бетулина фиксировали при обработке пластин в системе растворителей этилацетат : гексан (1:4) и опрыскивании пластинок 5% H2SO4 с последующим прогреванием в течение 2-3 мин при 95–100ºС. Количественный анализ продуктов биотрансформации бетулина осуществляли методом газовой хромато-масс-спектрометрии (ГХ-МС) с использованием хроматографа Agilent 6890N/5975B (Agilent Technologies, США), оборудованного капиллярной колонкой HP-5ms (30 м х 0.25 мм, 0.25 мкм) и работавшего в режиме ионизации электронным ударом (70 эВ). В качестве газа-носителя использовали гелий (1 мл/мин.). Вводили 0.2 мкл этилацетатного экстракта с делением потока (от 1:1 до 11:1). Температура колонки программировалась от 100 до 300°С с повышением температуры со скоростью 50°С/мин. Масс-спектры регистрировали в диапазоне m/z от 40 до 460 а.е.м. В экстрактах, содержащих остаточный н-гексадекан, время начала детектирования продуктов биотрансформации выбирали через 5 мин. после выхода н-гексадекана. Полученные масс-спектры сравнивали с масс-спектрами библиотеки NIST08 MS Library. Масс-спектры считали идентифицированными при совпадении масс-спектров исследуемого вещества с библиотечным коэффициентом подобия, превышающим 90%.
Эксперименты по препаративному получению бетулона проводили в колбах Эрленмейера объемом 250 мл, содержащих 100 мл клеточной суспензии (OП 600 2.6) R. rhodochrous ИЭГМ 66 в фосфатном буфере (рН 8.0) и 0.3 г бетулина, растворенного в 3 мл ДМСО, при постоянном перемешивании (160 об/мин) и температуре 28 ° С. Через 24 ч. продукты биотрансформации трижды экстрагировали эквивалентным объемом этилацетата. Полученные продукты биотрансформации (0.28 г) разделяли с помощью колоночной хроматографии на силикагеле 60–200 μm (Merck, Германия), соотношение вещества и сорбента « 1 : 50, элюент -гексан:этилацетат (9:1). Пороговое значение температуры в точке плавления определяли на приборе OptiMelt MPA100 (Stanford Research Systems Inc., США).
Бетулон (2, луп-20(29)-ен-28-ол-3-он) - белый порошок. Т пл 120.5°C ( н -гексан–этилацетат, 5:1) (лит.: Т пл 94-96°C ( н -гексан) [Hata, Hori, Takahashi, 2002], 175-176°C [Lupane ..., 1992]. MS, m/z (отн. интенсивность): 440.4 (9.51, M+).
Статистическая обработка результатов. Математическую обработку полученных результатов осуществляли с использованием компьютерных программ Excel 2003 (Microsoft Inc., 2003), Statistica, версия 6.0 (StatSoft Inc., 2001), рассчитывая среднее арифметическое и стандартную ошибку. Достоверность различий между средними ку. Достоверность различий между средними величинами оценивали с помощью t-критерия Стьюдента [Лакин, 1990].
Результаты и их обсуждение
Бетулинтрансформирующая активность коллекционных культур родококков . По нашим данным, в присутствии глюкозы, глицерина или н -гексадекана, а также в условиях использования МПБ родококки катализируют региоселективное окисление вторичной гидроксильной группы бетулина (рис. 1, 1) с образованием бетулона (рис. 1, 2).
HO
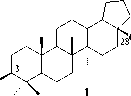
CH 2 O H
O
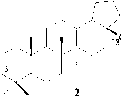
CH 2 OH
Рис. 1. Окислительная биотрансформация бетулина родококками
Как видно из табл. 1, наиболее высокий (44.9%) уровень образования бетулона достигается в присутствии 1.0 об. % н- гексадекана.
Таблица 1
Биотрансформация бетулина клетками R. rhodochrous ИЭГМ 66
|
Условия |
Содержание в сумме продуктов реакции, % |
|
|
Бетулин |
Бетулон |
|
|
Абиотический контроль |
100 |
|
|
Богатая питательная среда (МПБ) |
64.5±2.1 |
35.5±3.0 |
|
Минеральная среда с добавлением глюкозы (1.0%) |
92.5±4.2 |
7.5±0.5 |
|
Минеральная среда с добавлением глицерина (1.0%) |
74.6±3.8 |
25.4±3.2 |
|
Минеральная среда с добавлением н- гексадекана (1.0 об. %) |
48.0±4.1 |
44.9±4.7 |
При исследовании влияния концентрации н -гексадекана на интенсивность процесса биотрансформации бетулина показана прямая зависимость между уровнем образования бетулона и содержанием н- алкана в среде культивирования. Максимальный (72.2%) выход бетулона регистрируется в присутствии 3.0 об. % н- гексадекана через 240 ч. (рис. 2).
В результате сравнительного анализа бетулинтрансформирующей активности родококков разных видов в присутствии 3.0 об. % н- гексадекана выявлена гетерогенность зависимости между уровнем образования целевого продукта и видовой принадлежностью культур.
Как видно из табл. 2, высокая степень биоконверсии бетулина характерна для отдельных представителей видов R. erythropolis, ‘R. longus’, R. rhodochrous, R. ruber, при этом максимальный вы- ход бетулона достигается при использовании R. rhodochrous ИЭГМ 66. Высокая степень биоконверсии бетулина в присутствии н-гексадекана обусловлена, по-видимому, повышением уровня гидрофобности клеточной стенки родококков и синтезом биосурфактантов при росте родококков в данных условиях, что способствует взаимодействию бактериальных клеток с гидрофобным тритерпеновым субстратом. Однако, несмотря на относительно высокий (72.2%) выход целевого продукта, длительность (240 ч.) процесса биоконверсии и наличие остаточного (до 0.9 об. %) углеводорода в смеси продуктов биотрансформации (в полученных экстрактах, при проведении ГХ-МС анализа, при выделении бетулона в чистом виде) ограничивают возможность использования расту-й б
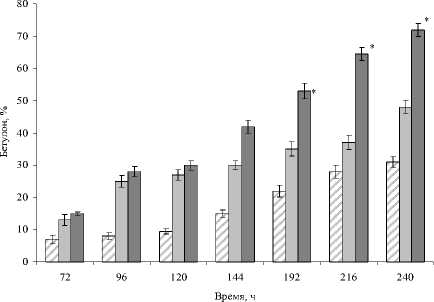
Рис. 2 . Биотрансформация бетулина (0.5 г/л) клетками R. rhodochrous ИЭГМ 66 при различном содержании н- гексадекана (об. %) в среде инкубации:
1 – 0.1; 2 – 1.0; 3 – 3.0. Бетулин вносили через 48 ч. *Данные достоверно отличаются от остальных вариантов опыта, p <0.05
Таблица 2
Биотрансформация бетулина родококками в присутствии н- гексадекана
|
Вид, штамм |
Бетулон, % |
|
Абиотический контроль |
0,0 |
|
R. erythropolis |
|
|
ИЭГМ 199 |
39.9±3.6 |
|
ИЭГМ 200 |
45.3±3.6 |
|
ИЭГМ 203 |
53.5±4.2 |
|
R. erythropolis |
|
|
ИЭГМ 199 |
10.9±3.1 |
|
ИЭГМ 200 |
34.2±2.1 |
|
ИЭГМ 203 |
38.5±3.4 |
|
‘R. longus’ |
|
|
ИЭГМ 30 |
9.8±2.0 |
|
ИЭГМ 31 |
|
|
ИЭГМ 32 |
72.2±4.8 |
|
R. opacus |
6.6±0.8 |
|
ИЭГМ 223 |
37.6±2.1 |
|
R. rhodochrous |
|
|
ИЭГМ 66 |
42.9±2.3 |
|
ИЭГМ 73 |
2.9±0.2 |
|
ИЭГМ 608 |
42.9±2.3 |
В сравнительных исследованиях каталитической активности нерастущих и иммобилизованных родококков в отношении бетулина установлено, что после иммобилизации клетки теряют бетулинтрансформирующую способность, что, очевидно, связано со снижением степени доступности тритерпенового субстрата для клеток, заключенных в матрицу ПВС.
В то время как нерастущие клетки сохраняют способность к региоселективному окислению бетулина в бетулон (рис. 3).
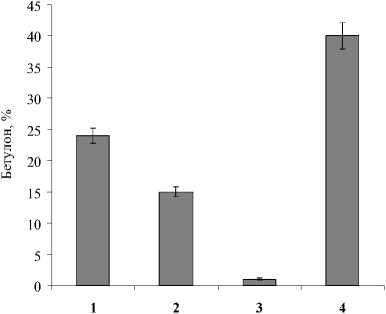
Рис. 3 . Биотрансформация бетулина (0.5 г/л) нерастущими клетками R. rhodochrous ИЭГМ 66, предварительно выращенными в минеральной среде с добавлением н -гексадекана, 1.0 об. % (1), глюкозы, 1.0 % (2), глицерина, 1.0 % (3) или в МПБ (4).
Условия процесса: OП 600 2.0; фосфатный буфер (рН 7.0), продолжительность 48 ч. *Данные достоверно отличаются от остальных вариантов опыта, p <0.05
При этом уровень образования целевого продукта определяется условиями их предварительного культивирования. Как видно из рис. 3, наибольший (24 и 40%) выход бетулона достигается при использовании клеток, предварительно выращенных в присутствии н -гексадекана или МПБ. Применение нерастущих клеток существенно сокращает продолжительность биотрансформации бетулина, а использование буферного раствора позволяет значительно упростить выделение бетуло-на из смеси продуктов биотрансформации.
Биотрансформация бетулина с использованием полученных клеточных фракций из родо-кокков . По данным отдельных авторов в реакциях микробного окисления вторичной гидроксильной группы тритерпеновых спиртов и кислот (с использованием мицелиальных грибов, бацилл или нокардий) принимают участие холестеролоксидаза [Biotransformation of betulinic …, 2007] или 3β-гидроксистероид дегидрогеназа [Biosynthesis …, 2010]. Оба фермента локализуются преимущественно в цитоплазме или связаны с клеточной мембраной и катализируют реакцию окисления 3β-гидроксильной группы стеролов (холестерола,
β-ситостерола) и стероидов с образованием соответствующих кетонов. Как видно из табл. 3, полученный супернатант с мембранносвязанными ферментами родококков катализирует реакцию окисления 3β-гидроксигруппы холестерола и β-сито-стерола с образованием 4-ен-3-оновых производных, в то время как в отношении бетулина данный супернатант не активен.
Таблица 3
Окислительная биотрансформация бетулина, холестерола и β-ситостерола с использованием клеточных фракций из R. rhodochrous ИЭГМ 66
|
Клеточная фракция |
Бетулон |
Холестенон |
Стигмаст-4-ен-3-он |
|
Целые клетки |
+++ |
+++ |
++* |
|
(1)** |
+ |
+ |
+ |
|
(2) |
+++ |
++ |
|
|
(3) |
+++ |
+ |
+ |
Незначительный (10.6%) уровень конверсии бетулина в бетулон наблюдается при использовании супернатанта с внутриклеточными ферментами родококков. Увеличение (до 22.4%) выхода бету-лона регистрируется в процессе биотрансформации бетулина ресуспендированными соникатами родо-кокков, содержащими компоненты клеточных стенок и, возможно, элементы бактериальных мембран с интегральными белками, имеющими гидрофобный якорь и связанными с мембраной за счет более прочных гидрофобных взаимодействий. Все это свидетельствует о прочной связи катализирующего окисление бетулина фермента с клеточной мембраной родококков. При этом следует особо отметить, что суммарная (33%) активность внутриклеточных ферментов и ферментов, прочно связанных с клеточной мембраной родококков, практически сопоставима с бетулинтрансформирующей активностью (40%) целых клеток.
Интенсификация процесса биотрансформации . Известно, что значительное влияние на активность ферментов оказывает уровень водородного показателя (рН среды), который определяет степень ионизации функциональных групп и конформацию каталитического центра фермента. При исследовании влияния рН буферного раствора на процесс биотрансформации бетулина (0.5 г/л) выявлено, что наиболее высокая степень образования бетулона достигается в условиях слабощелочной реакции среды. При рН 8.0 и 9.0 выход целевого продукта составляет 45%. Полученные результаты согласуются с данными X. Yang с соавт. [Rv1106c …, 2007] о максимальной активности 3β-гидроксистероид дегидрогеназы актинобактерий рода Mycobacterium при рН 8.5-9.5, в то время как холестеролоксидаза актинобактерий рода Rhodococcus проявляет наибольшую активность при рН 7.0-7.5 [Purification …, 2008; Extracellular
…, 2010], что может свидетельствовать об участии дегидрогеназы в окислении бетулина.
Нами установлена зависимость между количеством биомассы нерастущих клеток и выходом целевого продукта. Как видно из рис. 4, максимальный (65%) выход бетулона регистрируется при использовании 10 г/л (ОП 600 2.6) клеточной биомассы. Дальнейшее повышение (до 25 г/л) количества биомассы приводит к резкому снижению степени биоконверсии бетулина. Наблюдаемый эффект, по-видимому, обусловлен ограничениями процессов массопереноса при увеличении (более 10 г/л) клеточной биомассы.
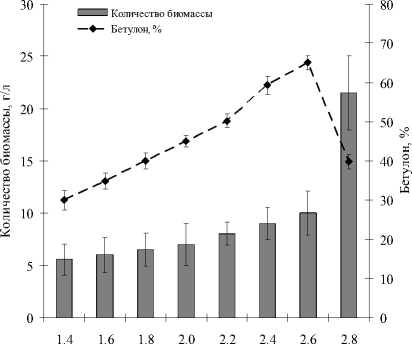
Оптическая плотность клеточной суспензии, ОП 600
Рис. 4 . Влияние количества биомассы R. rhodochrous ИЭГМ 66 на процесс биотрансформации бетулина (0.5 г/л).
Условия процесса: фосфатный буфер (рН 8.0), продолжительность 48 ч.
Серия дальнейших экспериментов посвящена изучению возможности биотрансформации бетулина в условиях повышенных (в 2–6 раз) концентраций нерастущими клетками R. rhodochrous ИЭГМ 66. В процессе исследования респираторной активности родококков установлено, что бетулин в концентрации от 0.5 до 3.0 г/л не оказывает ингибирующего влияния на дыхание бактериальных клеток. При этом скорость потребления О 2 практически не зависит от концентрации вносимого бетулина и достигает максимальных значений в течение первых 24 ч. эксперимента, что совпадает с периодом наибольшей каталитической активности родококков в отношении 0.5, 1.0, 2.0, 3.0 г/л бетулина с образованием 60, 56.8, 51.7 и 40% бетулона соответственно. На рис. 5 представлена характерная зависимость уровня образования бетулона от скорости потребления О 2 .
Сравнительно высокий уровень метаболической активности нерастущих родококков на начальном этапе процесса биотрансформации бетулина, по-видимому, может быть связан с запуском адаптационных механизмов при переносе жизне- способных клеток в среду без источников питания [Эль-Регистан, 2005; Мулюкин, 2010]. В последующие часы наблюдается постепенное снижение и стабилизация интенсивности дыхания и каталитической активности родококков. Как видно из рис. 6, повышение концентрации вносимого бетулина приводит к незначительному снижению каталитической активности родококков, при этом выход целевого продукта через 96 ч. составляет 60-75%
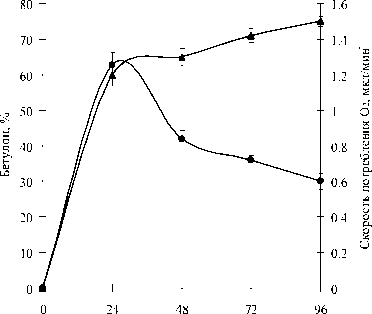
Время, ч
Рис. 5 . Динамика образования бетулона (1) и респираторная активность (2) нерастущих клеток R. rhodoсhrous ИЭГМ 66 в процессе биотрансформации бетулина (0.5 г/л).
Условия процесса: фосфатный буфер (рН 8.0), OП 600 2.6
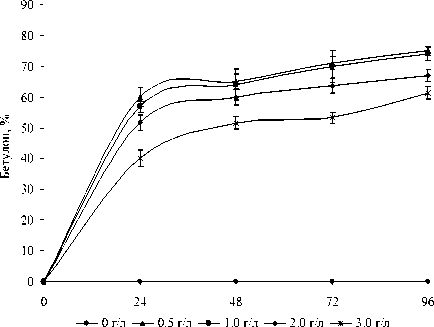
Рис. 6 . Динамика образования бетулона в процессе биотрансформации бетулина (0.5-3.0 г/л) клетками R. rhodochrous ИЭГМ 66.
Условия процесса: фосфатный буфер (рН 8.0); OП 600 2.6, продолжительность 24 ч.
Следует отметить, что в процессах биотрансформации бетулина в бетулон с применением растущих клеток грибов Dothideomycete [Highly …, 2013] и дрожжей Rhodotorula [Novel biotransformation …, 2012] биоконверсия бетулина не превышала 43.4 и 52.6% соответственно при использовании значительно меньших концентраций субстрата.
Заключение
В результате проведенных исследований проведена оценка возможности биотрансформации растительного пентациклического тритерпеноида бетулина с использованием актинобактерий рода Rhodococcus. При сравнении бетулинтрансформирующей активности 104 коллекционных культур родококков разных видов отобран штамм R. rhodochrous ИЭГМ 66, эффективно катализирующий образование бетулона - ключевого интермедиата в синтезе биологически активных соединений. Максимальный (свыше 70%) уровень биоконверсии бетулина (0.5 г/л) регистрируется в присутствии 3.0 об. % н -гексадекана в течение 240 ч. Существенное сокращение (до 24 ч) длительности процесса биотрансформации бетулина достигается при использовании нерастущих клеток. Оптимальными условиями трансформации бетулина нерастущими клетками являются предварительное выращивание родококков в богатой питательной среде (МПБ), слабощелочная реакция среды (рН 8.0-9.0) и использование клеточной биомассы в количестве 10 г/л. В экспериментах с использованием различных клеточных фракций родококков подтверждена прочная связь ферментов, катализирующих региоселективное окисление бетулина, с клеточной мембраной родококков. Использование бетулона в качестве ключевого интермедиата в химическом синтезе функционализированных производных (А-секопроизводных и гетероциклических, в частности) бетулина позволит расширить спектр новых тритерпеновых соединений с ценной биологической активностью.
Исследования выполнены в рамках Государственного задания 6.1194.2014/K Минобрнауки России и поддержаны грантом №14-04-96017-р_урал_а РФФИ и Министерства образования и науки Пермского края.
Список литературы Биотрансформация бетулина с использованием актинобактерий рода Rhodococcus
- Ившина И.Б., Пшеничнов Р.А., Оборин А. А. Пропанокисляющие родококки. Свердловск, 1987. 128 с
- Каталог штаммов Региональной профилированной коллекции алканотрофных микроорганизмов/под ред. И.Б. Ившиной. М.: Наука, 1994. 163 с
- Лакин Г.Ф. Биометрия: учеб. пособие для вузов. М.: Высшая школа, 1990. 352 c
- Романенко В.И., Кузнецов С.И. Экология микроорганизмов пресных вод. Лабораторное руководство. М.: Наука, 1974. 194 с
- Справочник биохимика: пер. с англ./Р. Досон, Д. Эллиот, У. Эллиот, К. Джонс. М.: Мир, 1991. 544 с
- Эль-Регистан Г.И. Покой как форма адаптации микроорганизмов//Механизмы выживания бактерий/отв. ред. В.И. Покровский. М.: Медицина, 2005. С. 11-129.
- Betulin and its derivatives. Chemistry and biological activity/G.A. Tolstikov et al.//Chemistry for Sustainable Development. 2005. Vol. 13. P. 1-29
- Biodegradation potential of the genus Rhodococcus/L. Martinkova et al.//Environment International. 2009. Vol. 35, № 5. P. 162-177
- Biosynthesis of ursolic acid derivatives by microbial metabolism of ursolic acid with Nocardia sp. strains -Proposal of new biosynthetic pathways/D. Leipold et al.//Process Biochemistry. 2010. Vol. 45, № 7. P. 1043-1051
- Biotransformation of betulinic and betulonic acids by fungi/D. Bastos et al.//Phytochemistry. 2007. Vol. 68, № 6. P. 834-839
- Biotransformation of triterpenes/K. Muffler et al.//Process Biochemistry. 2011. Vol. 46, № 7. P. 1-15
- Extracellular cholesterol oxidase from Rhodococcus sp.: isolation and molecular characterization/H. Lashkarian et al.//Iranian Biomedical Journal. 2010. Vol. 14, № 1-2. P. 49-57
- Hata K., Hori K., Takahashi S. Differentiation-and apoptosis-inducing activities by pentacyclic triter-penes on a mouse melanoma cell line//Journal of Natural Products. 2002. Vol. 65, № 5. P. 645-648
- Highly regioselective synthesis of betulone from betulin by growing cultures of marine fungus Do-thideomycete sp. HQ 316564/H. Liu et al.//Journal of Molecular Catalysis B: Enzymatic 2013. Vol. 88. P. 32-35
- Immobilization of hydrocarbon-oxidizing bacteria in poly(vinyl alcohol) cryogels hydrophobized using a biosurfactant/M.S. Kuyukina et al.//Journal of Microbiological Methods. 2006. Vol. 65, № 3. P. 596-603
- Kuyukina M.S., Ivshina I.B. Rhodococcus biosurfac-tants: biosynthesis, properties and potential applications//Biology of Rhodococcus. Microbiology Monography/Alvarez HM (editor). Berlin: Springer; 2010. Vol. 16. P. 291-313
- Larkin M.J., Kulakov LA., Allen C.R. Biodegradation by members of the genus Rhodococcus: biochemistry, physiology and genetic adaptation//Advances in Applied Microbiology. 2006. Vol. 59. P. 1-29
- Liu J., Fu M.L., Chen Q.H. Biotransformation optimization of betulin into betulinic acid production catalysed by cultured Armilaria luteo-virens Sacc ZJUQH100-6 cells//Journal of Applied Microbiology. 2010. Vol. 110. P. 1-8
- Lupane triterpenoids of Salacia cordata/W.F. Tinto et al.//Journal of Natural Products. 1992. Vol. 55, № 3. P. 395-398
- Microbial transformation of triterpenoids/A. Parra et al.//Mini-Reviews in Organic Chemistry. 2009. Vol. 6, № 4. P. 307-320
- Microbial transformations of two lupane-type triter-penes and anti-tumor-promoting effects of the transformation products/T. Akihisa et al.//Journal of Natural Products. 2002. Vol. 65, № 3. P. 278-282.
- Novel biotransformation of betulin to produce betu-lone by Rhodotorula mucilaginosa/D-B. Mao et al.//Journal of the Taiwan Institute of Chemical Engineers. 2012. Vol. 43, № 6. P. 825-829
- Novel semisynthetic derivatives of betulin and betulinic acid with cytotoxic activity/R.C. Santos et al.//Bioorganic & Medicinal Chemistry. 2009. Vol. 17, № 17. P. 6241-6250
- Oil desorption from mineral and organic materials using biosurfactant complexes produced by Rhodococcus species/I.B. Ivshina et al.//World Journal of Microbiology and Biotechnology. 1998. Vol. 14, № 5. P. 711-717
- Pharmacological properties of the ubiquitous natural product betulin/S. Alakurtti et al.//European Journal of Pharmaceutical Sciences. 2006. Vol. 29, № 1. P. 1-13
- Purification and characterization of extra-cellular cholesterol oxidase from Rhodococcus sp. PTCC 1633/M.T. Yazdi et al.//Biotechnology. 2008. Vol. 7, № 4. P. 751-756
- Rv1106c from Mycobacterium tuberculosis is a 3beta-hydroxysteroid dehydrogenase/X. Yang et al.//Biochemistry. 2007. Vol. 46, № 31. P. 9058-9067
- Synthesis and cytotoxicity of 28-carboxymethoxy lu-pane triterpenoids. Preference of 28-O-acylation over 28-O-alkylation of betulin by ethyl bromoace-tate/A.A. Mar et al.//Chinese Chemical Letters. 2009. Vol. 20, № 10. P. 1141-1144
- Synthesis and cytotoxicity of 2-cyano-28-hydroxy-lup-1-en-3-ones/A. Koohang et al.//Bioorganic & Medicinal Chemistry Letters. 2009. Vol. 19, № 8. P. 2168-2171
- Synthesis, proapoptotic screening, and structure-activity relationships of novel aza-lupane triterpe-noids/A.A. Mar et al.//Bioorganic & Medicinal Chemistry Letters. 2010. Vol. 20, № 18. P. 5389-5393
- The betulinic acid production from betulin through biotransformation by fungi/Q-H. Chen et al.//Enzyme and Microbial Technology. 2009. Vol. 45, № 3. P. 175-80
- Trofimov synthesis of betulin derivatives with 2,3-annelated pyrrole/A.V. Orlov et al.//Chemistry of Natural Compounds. 2011. Vol. 46, № 6. P. 906-909
- Мулюкин А.Л. Покоящиеся формы неспорообразующих бактерий: дис.. д-ра биол. наук: 03.02.03. М., 2010. 349 с


